Como bien se ha expresado a lo largo de este documento, la diabetes mellitus es una epidemia en salud pública, la cual se ha relacionado con complicaciones macrovasculares y microvasculares que llevan a una alta morbilidad y mortalidad cardiovascular. A partir del 2008, la Administración de Drogas y Alimentos (FDA, su sigla en inglés por Food and Drug Administration), ente regulatorio en los Estados Unidos, determinó la evaluación de la seguridad cardiovascular para todas las moléculas antidiabéticas. Esto ha generado gran número de nuevos estudios con nuevos medicamentos que buscan demostrar protección cardiovascular más allá del control glicémico. Este artículo describe los principales estudios que se están realizando con los inhibidores del cotransportador de sodio-glucosa tipo 2 (i-SGLT2) en pacientes con insuficiencia cardiaca con y sin diabetes.
As has been shown throughout this article, diabetes mellitus is a public health epidemic. It has been associated with macrovascular and microvascular complications that have a high cardiovascular morbidity and mortality. Since 2008, the American Food and Drug Administration (FDA) evaluated the cardiovascular safety of all the anti-diabetic drugs. This has led to a large number of studies with new drugs that seek to demonstrate cardiovascular protection beyond that of glycaemic control. A description is presented of the principal studies that are being carried out with sodium-glucose cotransporter-2 (SGLT2) inhibitors in patients with heart failure and with and without diabetes.
La evaluación de la seguridad de los tratamientos para la diabetes mellitus ha sido una exigencia desde el 20081 debido a la alerta generada por la mayor tasa de infarto cardiaco que se presentó con la rosiglitazona2,3. Entre estos nuevos medicamentos desarrollados recientemente están los inhibidores de la dipeptidil peptidasa 4 (iDPP-4) y los inhibidores del cotransportador de sodio-glucosa tipo 2 (i-SGLT2)4. Los estudios con i-SGLT2 en pacientes con diabetes mellitus han demostrado disminución de muerte cardiovascular (32%)5 y de las hospitalizaciones por falla cardíaca (35%)6. Adicionalmente, este beneficio ha sido demostrado en pacientes con falla cardiaca, independiente de la presencia de diabetes7. Por esta razón, y dada la creciente epidemia de enfermedades cardiovasculares y de diabetes mellitus, han venido estudiándose nuevos beneficios de las indicaciones de los i-SGLT2 en pacientes con falla cardiaca, con y sin diagnóstico de diabetes mellitus.
Para identificar los estudios más relevantes en la actualidad se realizó una búsqueda de la literatura que incluyó hombres o mujeres mayores de 18 años y experimentos clínicos aleatorizados en fase 3 con intervención activa, que permitieran conocer nuevos tratamientos o nuevas indicaciones de tratamiento comparado con la terapia estándar. Se realizó la búsqueda en la base de datos de clinical trials, central e ICTRP portal, mediante los siguientes términos: [“Heart Failure” AND “Diabetes” AND “Antidiabetics”] y [“Heart Failure” AND “Antidiabetics”]. Se complementó la búsqueda por grupo farmacológico (biguanidas, tiazolinedionas, sulfonilureas, análogos GLP-1, inhibidores de la DPP-4, iSLGT-2 y meglitinidas) de manera que coincidieran con los resultados obtenidos con los criterios de búsqueda planteados. Se incluyeron estudios que en su condición de “reclutamiento” se encontraban en reclutamiento activo, activo pero no reclutando (en seguimiento), terminado (se completó tempranamente el reclutamiento y el seguimiento) o completado (no está reclutando y ya se completó el último seguimiento). Se encontraron 3 estudios en pacientes diabéticos con falla cardíaca y 7 estudios en pacientes con falla cardíaca (con o sin diabetes mellitus) en quienes se evalúan diferentes intervenciones (antidiabéticos orales). Más de la mitad de estos estudios se realizan en pacientes con fracción de eyección preservada.
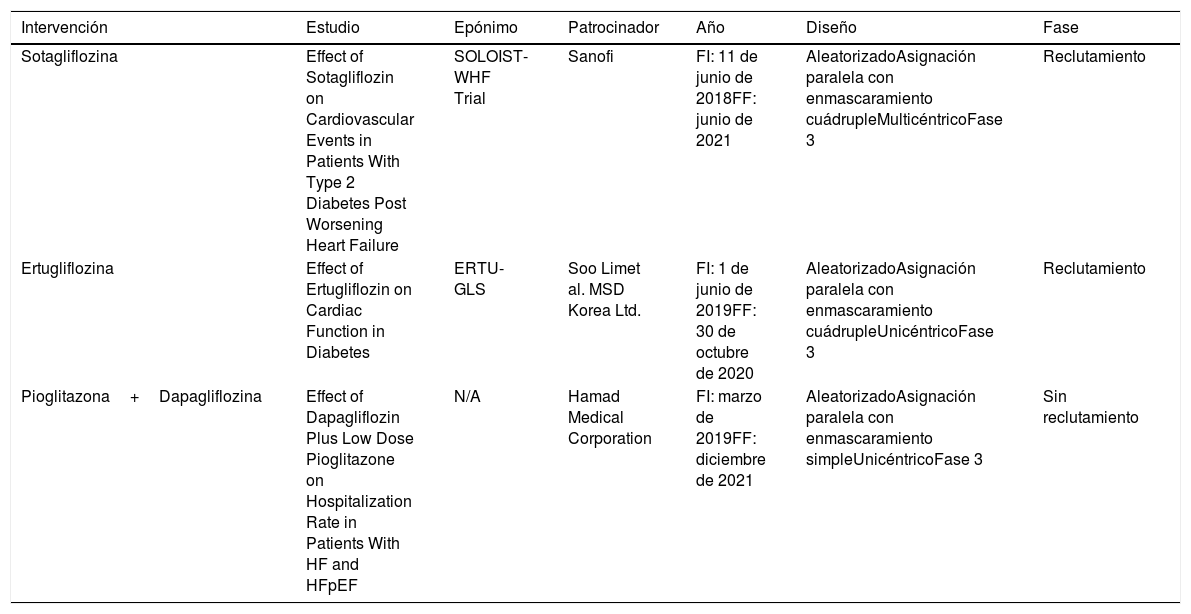
Metodología de los estudios incluidos (tablas 1 y 2)
Pacientes con diabetes mellitus y falla cardiaca que reciben antidiabéticos
| Intervención | Estudio | Epónimo | Patrocinador | Año | Diseño | Fase |
|---|---|---|---|---|---|---|
| Sotagliflozina | Effect of Sotagliflozin on Cardiovascular Events in Patients With Type 2 Diabetes Post Worsening Heart Failure | SOLOIST-WHF Trial | Sanofi | FI: 11 de junio de 2018FF: junio de 2021 | AleatorizadoAsignación paralela con enmascaramiento cuádrupleMulticéntricoFase 3 | Reclutamiento |
| Ertugliflozina | Effect of Ertugliflozin on Cardiac Function in Diabetes | ERTU-GLS | Soo Limet al. MSD Korea Ltd. | FI: 1 de junio de 2019FF: 30 de octubre de 2020 | AleatorizadoAsignación paralela con enmascaramiento cuádrupleUnicéntricoFase 3 | Reclutamiento |
| Pioglitazona+Dapagliflozina | Effect of Dapagliflozin Plus Low Dose Pioglitazone on Hospitalization Rate in Patients With HF and HFpEF | N/A | Hamad Medical Corporation | FI: marzo de 2019FF: diciembre de 2021 | AleatorizadoAsignación paralela con enmascaramiento simpleUnicéntricoFase 3 | Sin reclutamiento |
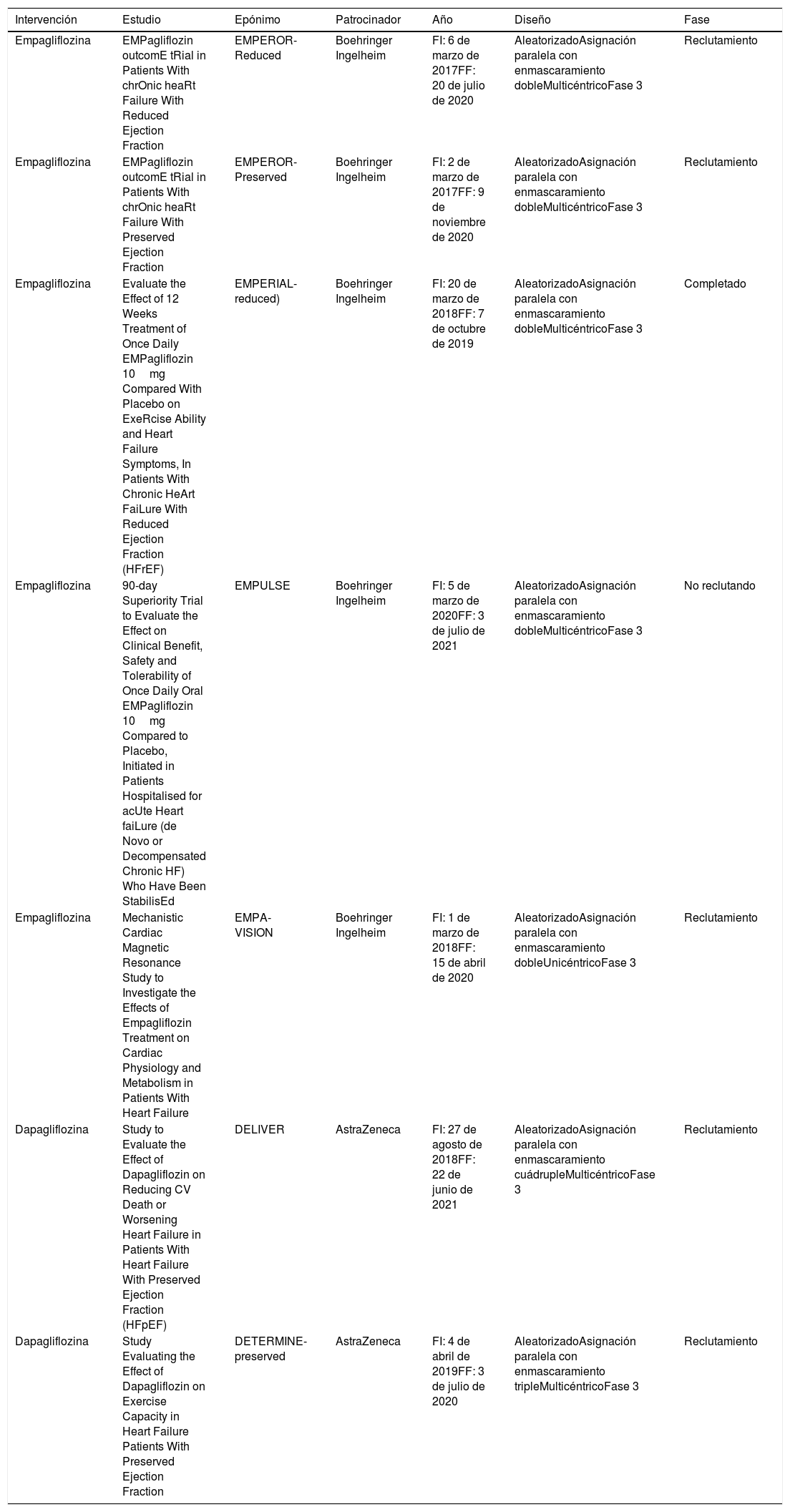
Pacientes con falla cardíaca (con o sin diabetes mellitus) que reciben antidiabéticos
| Intervención | Estudio | Epónimo | Patrocinador | Año | Diseño | Fase |
|---|---|---|---|---|---|---|
| Empagliflozina | EMPagliflozin outcomE tRial in Patients With chrOnic heaRt Failure With Reduced Ejection Fraction | EMPEROR-Reduced | Boehringer Ingelheim | FI: 6 de marzo de 2017FF: 20 de julio de 2020 | AleatorizadoAsignación paralela con enmascaramiento dobleMulticéntricoFase 3 | Reclutamiento |
| Empagliflozina | EMPagliflozin outcomE tRial in Patients With chrOnic heaRt Failure With Preserved Ejection Fraction | EMPEROR-Preserved | Boehringer Ingelheim | FI: 2 de marzo de 2017FF: 9 de noviembre de 2020 | AleatorizadoAsignación paralela con enmascaramiento dobleMulticéntricoFase 3 | Reclutamiento |
| Empagliflozina | Evaluate the Effect of 12 Weeks Treatment of Once Daily EMPagliflozin 10mg Compared With Placebo on ExeRcise Ability and Heart Failure Symptoms, In Patients With Chronic HeArt FaiLure With Reduced Ejection Fraction (HFrEF) | EMPERIAL-reduced) | Boehringer Ingelheim | FI: 20 de marzo de 2018FF: 7 de octubre de 2019 | AleatorizadoAsignación paralela con enmascaramiento dobleMulticéntricoFase 3 | Completado |
| Empagliflozina | 90-day Superiority Trial to Evaluate the Effect on Clinical Benefit, Safety and Tolerability of Once Daily Oral EMPagliflozin 10mg Compared to Placebo, Initiated in Patients Hospitalised for acUte Heart faiLure (de Novo or Decompensated Chronic HF) Who Have Been StabilisEd | EMPULSE | Boehringer Ingelheim | FI: 5 de marzo de 2020FF: 3 de julio de 2021 | AleatorizadoAsignación paralela con enmascaramiento dobleMulticéntricoFase 3 | No reclutando |
| Empagliflozina | Mechanistic Cardiac Magnetic Resonance Study to Investigate the Effects of Empagliflozin Treatment on Cardiac Physiology and Metabolism in Patients With Heart Failure | EMPA-VISION | Boehringer Ingelheim | FI: 1 de marzo de 2018FF: 15 de abril de 2020 | AleatorizadoAsignación paralela con enmascaramiento dobleUnicéntricoFase 3 | Reclutamiento |
| Dapagliflozina | Study to Evaluate the Effect of Dapagliflozin on Reducing CV Death or Worsening Heart Failure in Patients With Heart Failure With Preserved Ejection Fraction (HFpEF) | DELIVER | AstraZeneca | FI: 27 de agosto de 2018FF: 22 de junio de 2021 | AleatorizadoAsignación paralela con enmascaramiento cuádrupleMulticéntricoFase 3 | Reclutamiento |
| Dapagliflozina | Study Evaluating the Effect of Dapagliflozin on Exercise Capacity in Heart Failure Patients With Preserved Ejection Fraction | DETERMINE-preserved | AstraZeneca | FI: 4 de abril de 2019FF: 3 de julio de 2020 | AleatorizadoAsignación paralela con enmascaramiento tripleMulticéntricoFase 3 | Reclutamiento |
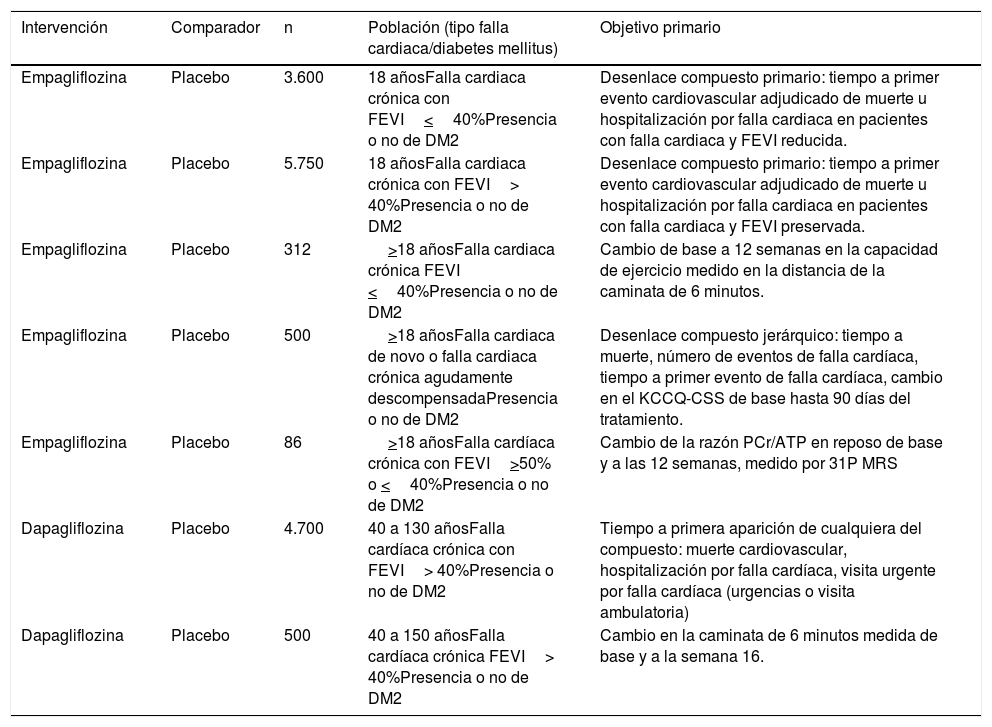
Características de la población y objetivo primario (tablas 3 y 4)
Pacientes con diabetes mellitus y falla cardiaca que reciben antidiabéticos
| Intervención | Comparador | n | Población (tipo falla cardiaca/diabetes mellitus) | Objetivo primario |
|---|---|---|---|---|
| Sotagliflozina | Placebo | 4.000 | 18 a 85 añosFalla cardiaca crónica agudamente descompensadaDM2 | Reducción de mortalidad cardiovascular y morbilidad (compuesto de muerte cardiovascular u hospitalización por falla cardiaca) en pacientes hemodinámicamente estables |
| Ertugliflozina | Placebo | 120 | 20 a 75 añosFalla cardiaca estadio BDM2 | Cambio en strain longitudinal global (medición: base, 12 semanas y 24 semanas) |
| Pioglitazona+Dapagliflozina | Placebo | 648 | 18 a 80 añosFalla cardiaca con FEVI >50%DM2 | Tiempo a primera hospitalización (> 24 horas de infusión intravenosa de diurético) por falla cardíaca posterior al inicio de la intervención. |
Pacientes con falla cardíaca (con o sin diabetes mellitus) que reciben antidiabéticos
| Intervención | Comparador | n | Población (tipo falla cardiaca/diabetes mellitus) | Objetivo primario |
|---|---|---|---|---|
| Empagliflozina | Placebo | 3.600 | 18 añosFalla cardiaca crónica con FEVI<40%Presencia o no de DM2 | Desenlace compuesto primario: tiempo a primer evento cardiovascular adjudicado de muerte u hospitalización por falla cardiaca en pacientes con falla cardiaca y FEVI reducida. |
| Empagliflozina | Placebo | 5.750 | 18 añosFalla cardiaca crónica con FEVI> 40%Presencia o no de DM2 | Desenlace compuesto primario: tiempo a primer evento cardiovascular adjudicado de muerte u hospitalización por falla cardiaca en pacientes con falla cardiaca y FEVI preservada. |
| Empagliflozina | Placebo | 312 | >18 añosFalla cardiaca crónica FEVI <40%Presencia o no de DM2 | Cambio de base a 12 semanas en la capacidad de ejercicio medido en la distancia de la caminata de 6 minutos. |
| Empagliflozina | Placebo | 500 | >18 añosFalla cardiaca de novo o falla cardiaca crónica agudamente descompensadaPresencia o no de DM2 | Desenlace compuesto jerárquico: tiempo a muerte, número de eventos de falla cardíaca, tiempo a primer evento de falla cardíaca, cambio en el KCCQ-CSS de base hasta 90 días del tratamiento. |
| Empagliflozina | Placebo | 86 | >18 añosFalla cardíaca crónica con FEVI>50% o <40%Presencia o no de DM2 | Cambio de la razón PCr/ATP en reposo de base y a las 12 semanas, medido por 31P MRS |
| Dapagliflozina | Placebo | 4.700 | 40 a 130 añosFalla cardíaca crónica con FEVI> 40%Presencia o no de DM2 | Tiempo a primera aparición de cualquiera del compuesto: muerte cardiovascular, hospitalización por falla cardíaca, visita urgente por falla cardíaca (urgencias o visita ambulatoria) |
| Dapagliflozina | Placebo | 500 | 40 a 150 añosFalla cardíaca crónica FEVI> 40%Presencia o no de DM2 | Cambio en la caminata de 6 minutos medida de base y a la semana 16. |
KCCQ-CSS: cuestionario de calidad de vida de miocardiopatías de Kansas: PCR: fosfocreatina. ATP: adenosín trifosfato. 31 P MRS: resonancia magnética por espectroscopia 31 P.
En la actualidad se realizan varios estudios con i-SGLT2 que buscan demostrar su beneficio en la reducción de eventos cardiovasculares en pacientes con insuficiencia cardiaca con función reducida y preservada, independiente de la presencia de diabetes mellitus tipo 2. También se llevan a cabo estudios a nivel fisiológico (fase 2) para entender otros mecanismos por los cuales este grupo farmacológico ha contribuido a la disminución de la morbilidad. No se encontraron estudios de fase 3 que incluyeran grupos farmacológicos diferentes a los i-SGLT2, excepto con pioglitazona (tiazolidinediona) en combinación con dapagliflozina en pacientes con falla cardiaca y fracción de eyección preservada.
Conflicto de interesesNinguno.