La hiponatremia es un factor de mal pronóstico en pacientes con insuficiencia cardiaca. Nuestro objetivo fue valorar el impacto de la hiponatremia en la evolución de los pacientes sometidos a implante de desfibrilador en prevención primaria.
MétodoSe trata de un estudio observacional retrospectivo multicéntrico en el que se valoró la natremia periimplante y los eventos adversos (la mortalidad de cualquier causa y la cardiovascular, el primer ingreso por insuficiencia cardiaca, la primera terapia apropiada e inapropiada del desfibrilador), en una cohorte española sometida a implante de desfibrilador en la prevención primaria. Se comparó la hiponatremia ligera (Na≤135mEq/l) y la moderada-severa (Na≤131mEq/l) respecto a la ausencia de la hiponatremia.
ResultadosUn total de 725 pacientes, con un valor medio de sodio en la sangre periimplante de 139±3,6mEq/l y un tiempo medio de seguimiento de 34,1±18,5meses. En los pacientes con Na≤135mEq/l (n=105) se observó una mayor incidencia de primer ingreso por insuficiencia cardiaca (odds ratio: 1,701; p=0,031). En los pacientes con hiponatremia moderada-severa (n=18) se observó mayor mortalidad total (hazard ratio; 3,552; p=0,002) y mayor mortalidad cardiovascular (hazard ratio: 4,24; p=0,003). Ninguno de los grados de la hiponatremia estudiados se asoció con mayor incidencia de terapias apropiadas o inapropiadas.
ConclusionesLa hiponatremia ligera en el momento del implante de un desfibrilador se asocia a una mayor incidencia de ingreso por insuficiencia cardiaca en el seguimiento, mientras que en el caso de una hiponatremia moderada-severa, se asocia a un riesgo de muerte 4 veces mayor.
Hyponatremia is a prognostic factor in patients with heart failure. Our objective was to assess the impact of hyponatremia in the evolution of patients undergoing cardioverter implantation in primary prevention.
MethodThis is a multicenter retrospective observational study in which serum sodium periimplant and adverse events (all-cause and cardiovascular mortality, first admission for heart failure, first appropriate and inappropriate therapy) were assessed in a Spanish cohort receiving cardioverter in primary prevention. Patients with mild hyponatremia (Na≤135mEq/L) and those with moderate to severe hyponatremia (Na≤131mEq/L) were compared to those without hyponatremia.
Results725 patients, with a mean value of sodium in blood peri-implant of 139±3.6mEq/L and a mean follow-up was 34.1±18.5months. In patients with Na≤135mEq/L (n=105), an increased incidence of first admission for heart failure was observed (Odds Ratio: 1.701; P=.031). In patients with moderate to severe hyponatremia (n=18), higher total mortality (Hazard Ratio: 3.552; P=.002) and increased cardiovascular mortality (Hazard Ratio: 4.24; P=.003) were observed. None of those values of hyponatremia were associated with increased incidence of appropriate or inappropriate therapies
ConclusionsMild hyponatremia at the time of cardioverter implantation is related with a higher incidence of hospitalization for heart failure during follow-up, while moderate to severe hyponatremia increases the risk of death during follow-up
La natremia es un factor pronóstico en cuanto a mortalidad y reingresos en pacientes con insuficiencia cardiaca crónica1, así como en los pacientes que ingresan por descompensación aguda, tanto en los estudios aleatorizados y los controlados2, como en los registros realizados con la población no seleccionada3. La prevalencia de la hiponatremia (definida como un valor de Na<135mEq/l) entre pacientes ingresados por insuficiencia cardiaca se encuentra alrededor del 20%2–4. Por otra parte, la disminución de la mortalidad en los pacientes con disfunción ventricular a los que se les coloca desfibrilador automático implantable (DAI) se atribuye principalmente a una disminución de la muerte súbita cardiaca por eventos arrítmicos5,6. Su impacto sobre la mortalidad secundaria a insuficiencia cardiaca o a causas no cardiovasculares prácticamente no se ve modificado. El pronóstico de los pacientes con disfunción ventricular es muy heterogéneo, y de ahí la importancia de realizar una adecuada selección de aquellos que van a recibir un DAI. No obstante, las guías de práctica clínica sobre implante de dispositivos de estimulación cardiaca se basan casi exclusivamente en la fracción de eyección ventricular izquierda (FEVI) y en la clase funcional del paciente como indicadores a la hora de realizar el implante de un DAI. Los propios autores reconocen las amplias limitaciones en la estratificación de riesgo de estos pacientes con la utilización de pruebas no invasivas7,8.
En esta línea, recientemente se ha demostrado el impacto del valor de la natremia preimplante en la evolución de los pacientes portadores de DAI tanto en la prevención primaria como en la prevención secundaria9.
El objetivo de nuestro estudio fue valorar la relación de la hiponatremia sobre la mortalidad, los ingresos por insuficiencia cardiaca y las terapias del dispositivo (las apropiadas y las inapropiadas), en una cohorte española de pacientes con disfunción ventricular (FEVI≤35%) sometidos a implante de DAI en prevención primaria en varios centros nacionales.
Material y métodosPoblación de estudioSe trata de un estudio multicéntrico retrospectivo y observacional realizado en 15 centros hospitalarios españoles que disponen de la Unidad de Electrofisiología. El centro coordinador fue el Hospital Clínico de Santiago de Compostela. Pese a que el diseño del estudio fue retrospectivo, el cardiólogo o electrofisiólogo responsable recogió los datos de cada paciente de modo prospectivo. Los datos demográficos, los clínicos, del procedimiento y de la evolución se recogieron por parte de cada hospital en formularios Access estandarizados.
Con el fin de evitar sesgos, se decidió incluir a todos los pacientes consecutivos con la miocardiopatía dilatada isquémica y no isquémica y FEVI≤35% remitidos para implante de DAI en prevención primaria entre el 1 de enero de 2010 y el 31 de diciembre de 2011, aunque en 3 centros se incluyeron los pacientes remitidos a implante de DAI desde el 1 de enero de 2008.
Criterios de exclusión:
- 1.
Pacientes sometidos a implante de DAI por canalopatías, disfunción ventricular en el contexto de cardiopatía congénita, displasia arritmogénica del ventrículo derecho o miocardiopatía hipertrófica.
- 2.
Pacientes sometidos a revascularización percutánea o quirúrgica en los 3meses previos al implante del DAI.
- 3.
Pacientes que hubieran padecido infarto agudo de miocardio en los 40días previos al implante del DAI.
- 4.
Pacientes que no dispusieran de seguimiento en el centro en el que se había llevado a cabo el implante.
- 5.
Pacientes que no dispusieran de una determinación analítica que incluyera la natremia en las 24horas previas o posteriores al implante del DAI.
La determinación analítica del sodio tuvo lugar en las 24horas previas o posteriores al implante del DAI y se expresa en mEq/litro (mEq/l). En primer lugar, con el objetivo de valorar si cualquier grado de la hiponatremia se relacionaba con eventos en el seguimiento, se dividió la muestra en:
- -
Paciente con hiponatremia de cualquier grado (Na≤135mEq/l). Grupo A.
- -
Pacientes con sodio normal (Na>135mEq/l). Grupo B.
En segundo lugar, con el objetivo de valorar si la hiponatremia moderada-severa se relacionaba con eventos en el seguimiento, se dividió la muestra en:
- -
Pacientes con hiponatremia moderada-severa (Na≤131mEq/). Grupo C.
- -
Pacientes sin hiponatremia moderada-severa (Na>131mEq/). Grupo D.
El objetivo principal del estudio fue valorar la mortalidad durante el seguimiento. El tiempo de seguimiento se consideró desde el momento del implante hasta la fecha del fallecimiento (incluyendo la muerte o el trasplante cardiaco), o hasta el último control evolutivo disponible. La información sobre el estado clínico del paciente se obtuvo de la historia clínica hospitalaria y de la atención primaria disponible en cada centro y mediante el contacto telefónico con el paciente.
Se recogió la causa específica de la muerte, clasificándola en cardiovascular y no cardiovascular. Se consideraron las causas cardiacas: la muerte súbita (MS), la insuficiencia cardiaca refractaria (IC) o el infarto agudo de miocardio (IAM). La muerte súbita fue definida como muerte inesperada de un paciente que hasta ese momento se consideraba estable. La MS podía ser presenciada (con o sin documentación de arritmias) o no presenciada (en este caso el paciente debería haber sido visto en las 24horas previas al fallecimiento), sin haber mostrado clínica de la insuficiencia cardiaca (IC). Se definió como muerte por descompensación de IC la que no responde al tratamiento, en ausencia de otra causa de muerte. El IAM se consideró como causa de muerte en el caso en que se produjeran complicaciones mecánicas y/o eléctricas que provocaran la muerte precoz del paciente. Se consideraron causas de mortalidad vascular no cardiacas las debidas a un accidente cerebrovascular, a enfermedades vasculorrenales (fallo renal en ausencia de glomerulopatías u otras alteraciones parenquimatosas), o a rotura de aneurismas. El resto se consideraron muertes de causa no cardiovascular. Por otro lado, se recogió el primer ingreso por insuficiencia cardiaca en el seguimiento y las terapias administradas por el desfibrilador durante el seguimiento, tanto apropiadas como inapropiadas.
Análisis estadísticoSe obtuvieron análisis estadísticos descriptivos de las variables continuas estudiadas (media±desviación típica) y las variables categóricas (porcentaje±desviación típica). Las variables continuas se compararon mediante test t de Student, mientras que las categóricas se compararon mediante test de Chi cuadrado.
Se realizaron modelos de regresión de Cox para determinar los factores predictores de la mortalidad total y la mortalidad de causa cardiovascular, y los modelos de regresión logística para determinar los factores predictores de primer ingreso por insuficiencia cardiaca en el seguimiento. Todos los modelos incluyeron potenciales variables de confusión, como edad, función renal, fracción de eyección al implante (FEVI), clase funcional al implante (NYHA), ritmo al implante, implante de TRC y tipo de cardiopatía (isquémica o no isquémica).
El análisis estadístico se realizó con el programa IBM SPSS Statistics 18W (SPSS Inc.; Chicago, Estados Unidos). Se consideraron estadísticamente significativos valores de p<0,05.
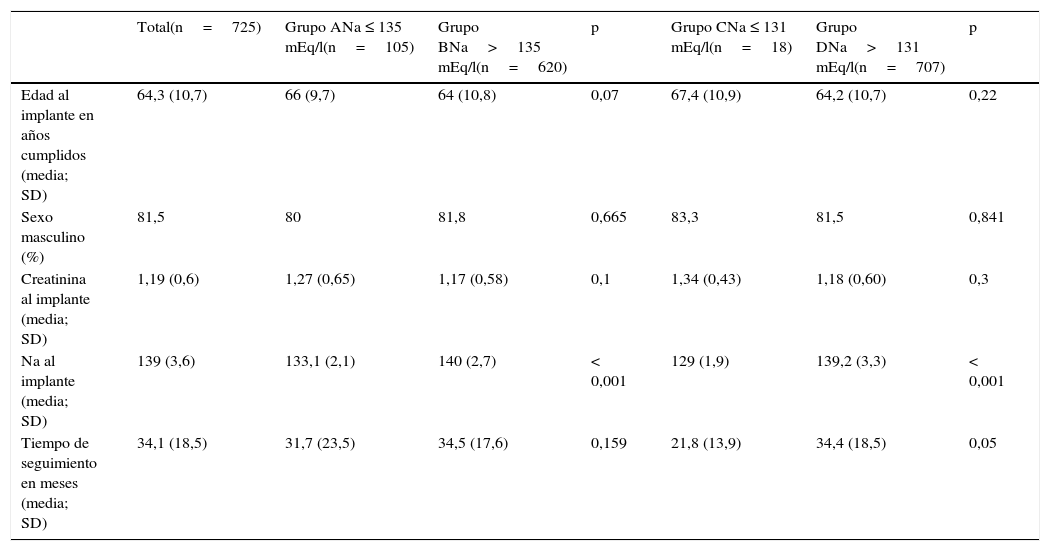
ResultadosDe los 1.176 pacientes que cumplían los criterios clínicos de inclusión en el estudio, se seleccionaron 725 pacientes en los que se disponía del valor del sodio en la sangre periimplante. Las características basales y el tratamiento de la población general y de los grupos de estudio se recogen en las tablas 1–4. En la muestra global, el 81,5% de los pacientes eran varones, con una edad media de 64,3±10,7años y un valor medio de sodio en sangre periimplante de 139±3,6mEq/l (figs. 1–3).
Características basales de la muestra total y de los 4 grupos de estudio
| Total(n=725) | Grupo ANa ≤ 135 mEq/l(n=105) | Grupo BNa>135 mEq/l(n=620) | p | Grupo CNa ≤ 131 mEq/l(n=18) | Grupo DNa>131 mEq/l(n=707) | p | |
|---|---|---|---|---|---|---|---|
| Edad al implante en años cumplidos (media; SD) | 64,3 (10,7) | 66 (9,7) | 64 (10,8) | 0,07 | 67,4 (10,9) | 64,2 (10,7) | 0,22 |
| Sexo masculino (%) | 81,5 | 80 | 81,8 | 0,665 | 83,3 | 81,5 | 0,841 |
| Creatinina al implante (media; SD) | 1,19 (0,6) | 1,27 (0,65) | 1,17 (0,58) | 0,1 | 1,34 (0,43) | 1,18 (0,60) | 0,3 |
| Na al implante (media; SD) | 139 (3,6) | 133,1 (2,1) | 140 (2,7) | < 0,001 | 129 (1,9) | 139,2 (3,3) | < 0,001 |
| Tiempo de seguimiento en meses (media; SD) | 34,1 (18,5) | 31,7 (23,5) | 34,5 (17,6) | 0,159 | 21,8 (13,9) | 34,4 (18,5) | 0,05 |
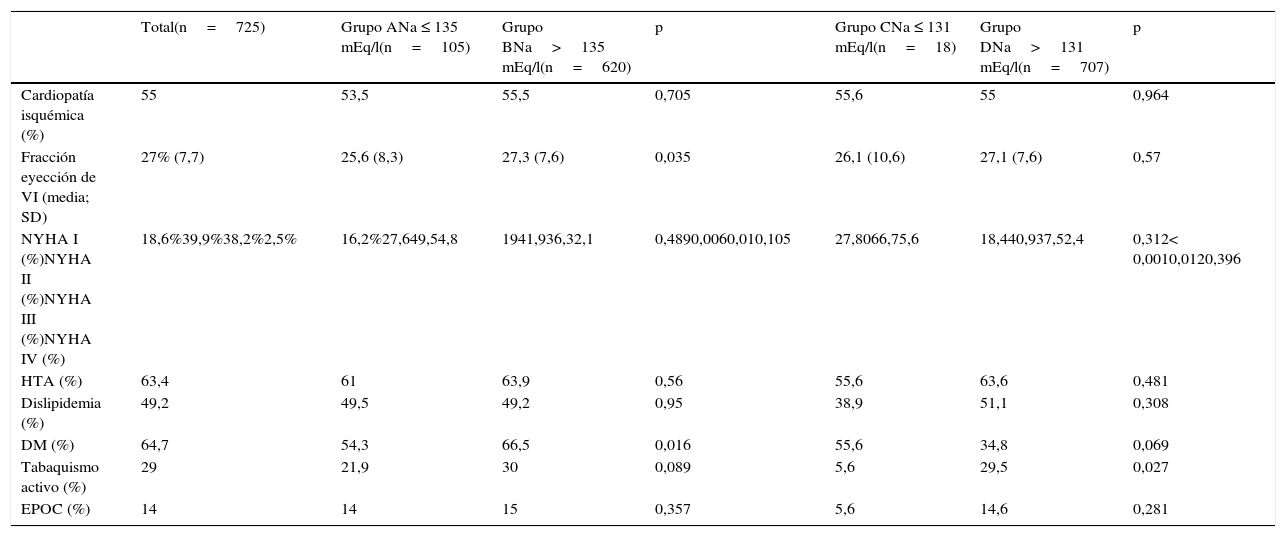
Tipo de cardiopatía y factores de riesgo cardiovascular
| Total(n=725) | Grupo ANa ≤ 135 mEq/l(n=105) | Grupo BNa>135 mEq/l(n=620) | p | Grupo CNa ≤ 131 mEq/l(n=18) | Grupo DNa>131 mEq/l(n=707) | p | |
|---|---|---|---|---|---|---|---|
| Cardiopatía isquémica (%) | 55 | 53,5 | 55,5 | 0,705 | 55,6 | 55 | 0,964 |
| Fracción eyección de VI (media; SD) | 27% (7,7) | 25,6 (8,3) | 27,3 (7,6) | 0,035 | 26,1 (10,6) | 27,1 (7,6) | 0,57 |
| NYHA I (%)NYHA II (%)NYHA III (%)NYHA IV (%) | 18,6%39,9%38,2%2,5% | 16,2%27,649,54,8 | 1941,936,32,1 | 0,4890,0060,010,105 | 27,8066,75,6 | 18,440,937,52,4 | 0,312< 0,0010,0120,396 |
| HTA (%) | 63,4 | 61 | 63,9 | 0,56 | 55,6 | 63,6 | 0,481 |
| Dislipidemia (%) | 49,2 | 49,5 | 49,2 | 0,95 | 38,9 | 51,1 | 0,308 |
| DM (%) | 64,7 | 54,3 | 66,5 | 0,016 | 55,6 | 34,8 | 0,069 |
| Tabaquismo activo (%) | 29 | 21,9 | 30 | 0,089 | 5,6 | 29,5 | 0,027 |
| EPOC (%) | 14 | 14 | 15 | 0,357 | 5,6 | 14,6 | 0,281 |
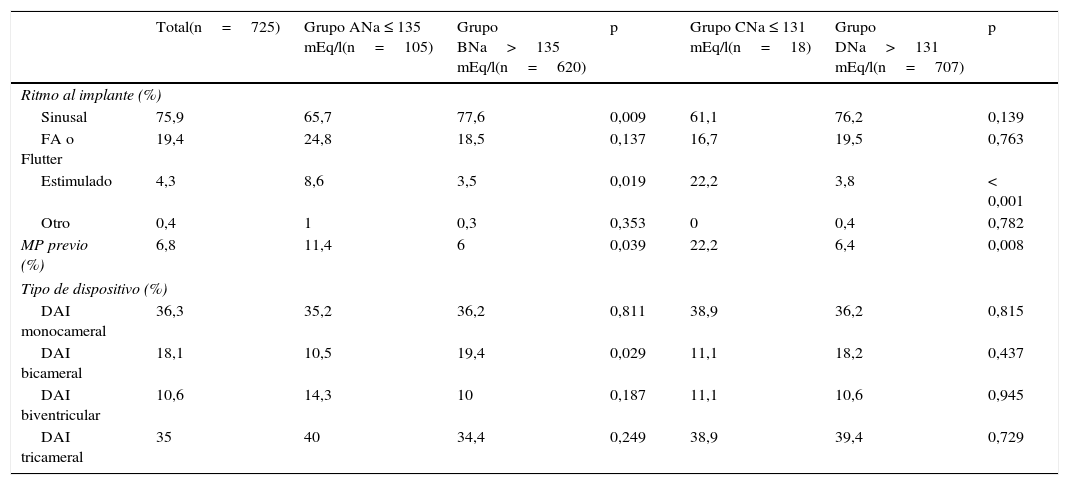
Ritmo al implante y tipo de dispositivo implantado
| Total(n=725) | Grupo ANa ≤ 135 mEq/l(n=105) | Grupo BNa>135 mEq/l(n=620) | p | Grupo CNa ≤ 131 mEq/l(n=18) | Grupo DNa>131 mEq/l(n=707) | p | |
|---|---|---|---|---|---|---|---|
| Ritmo al implante (%) | |||||||
| Sinusal | 75,9 | 65,7 | 77,6 | 0,009 | 61,1 | 76,2 | 0,139 |
| FA o Flutter | 19,4 | 24,8 | 18,5 | 0,137 | 16,7 | 19,5 | 0,763 |
| Estimulado | 4,3 | 8,6 | 3,5 | 0,019 | 22,2 | 3,8 | < 0,001 |
| Otro | 0,4 | 1 | 0,3 | 0,353 | 0 | 0,4 | 0,782 |
| MP previo (%) | 6,8 | 11,4 | 6 | 0,039 | 22,2 | 6,4 | 0,008 |
| Tipo de dispositivo (%) | |||||||
| DAI monocameral | 36,3 | 35,2 | 36,2 | 0,811 | 38,9 | 36,2 | 0,815 |
| DAI bicameral | 18,1 | 10,5 | 19,4 | 0,029 | 11,1 | 18,2 | 0,437 |
| DAI biventricular | 10,6 | 14,3 | 10 | 0,187 | 11,1 | 10,6 | 0,945 |
| DAI tricameral | 35 | 40 | 34,4 | 0,249 | 38,9 | 39,4 | 0,729 |
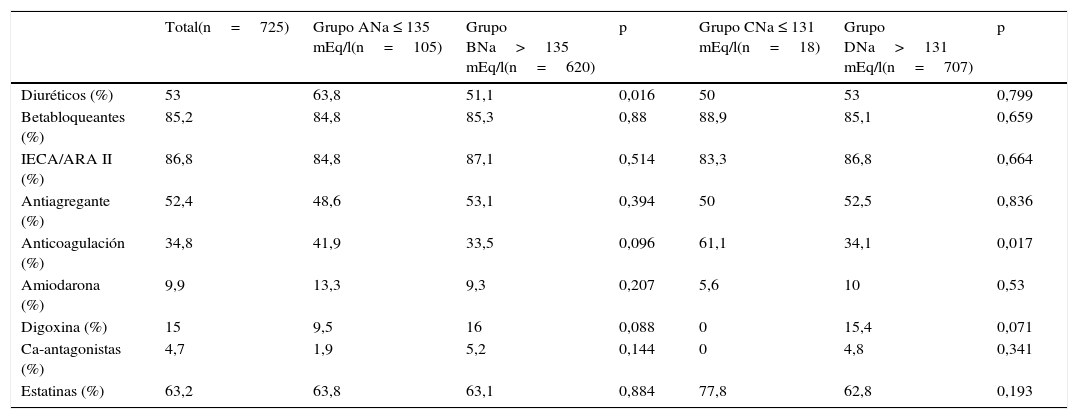
Tratamiento en el momento del implante
| Total(n=725) | Grupo ANa ≤ 135 mEq/l(n=105) | Grupo BNa>135 mEq/l(n=620) | p | Grupo CNa ≤ 131 mEq/l(n=18) | Grupo DNa>131 mEq/l(n=707) | p | |
|---|---|---|---|---|---|---|---|
| Diuréticos (%) | 53 | 63,8 | 51,1 | 0,016 | 50 | 53 | 0,799 |
| Betabloqueantes (%) | 85,2 | 84,8 | 85,3 | 0,88 | 88,9 | 85,1 | 0,659 |
| IECA/ARA II (%) | 86,8 | 84,8 | 87,1 | 0,514 | 83,3 | 86,8 | 0,664 |
| Antiagregante (%) | 52,4 | 48,6 | 53,1 | 0,394 | 50 | 52,5 | 0,836 |
| Anticoagulación (%) | 34,8 | 41,9 | 33,5 | 0,096 | 61,1 | 34,1 | 0,017 |
| Amiodarona (%) | 9,9 | 13,3 | 9,3 | 0,207 | 5,6 | 10 | 0,53 |
| Digoxina (%) | 15 | 9,5 | 16 | 0,088 | 0 | 15,4 | 0,071 |
| Ca-antagonistas (%) | 4,7 | 1,9 | 5,2 | 0,144 | 0 | 4,8 | 0,341 |
| Estatinas (%) | 63,2 | 63,8 | 63,1 | 0,884 | 77,8 | 62,8 | 0,193 |
El tiempo medio de seguimiento fue de 34,1±18,5meses.
El tipo de dispositivo implantado con más frecuencia fue el DAI monocameral (36,3% de la muestra global). El porcentaje de pacientes que recibió un DAI bicameral ascendió al 18,1%. En el 45% de los pacientes se implantó también una sonda para estimulación del ventrículo izquierdo, incluyendo en un 35% de los mismos también la sonda auricular.
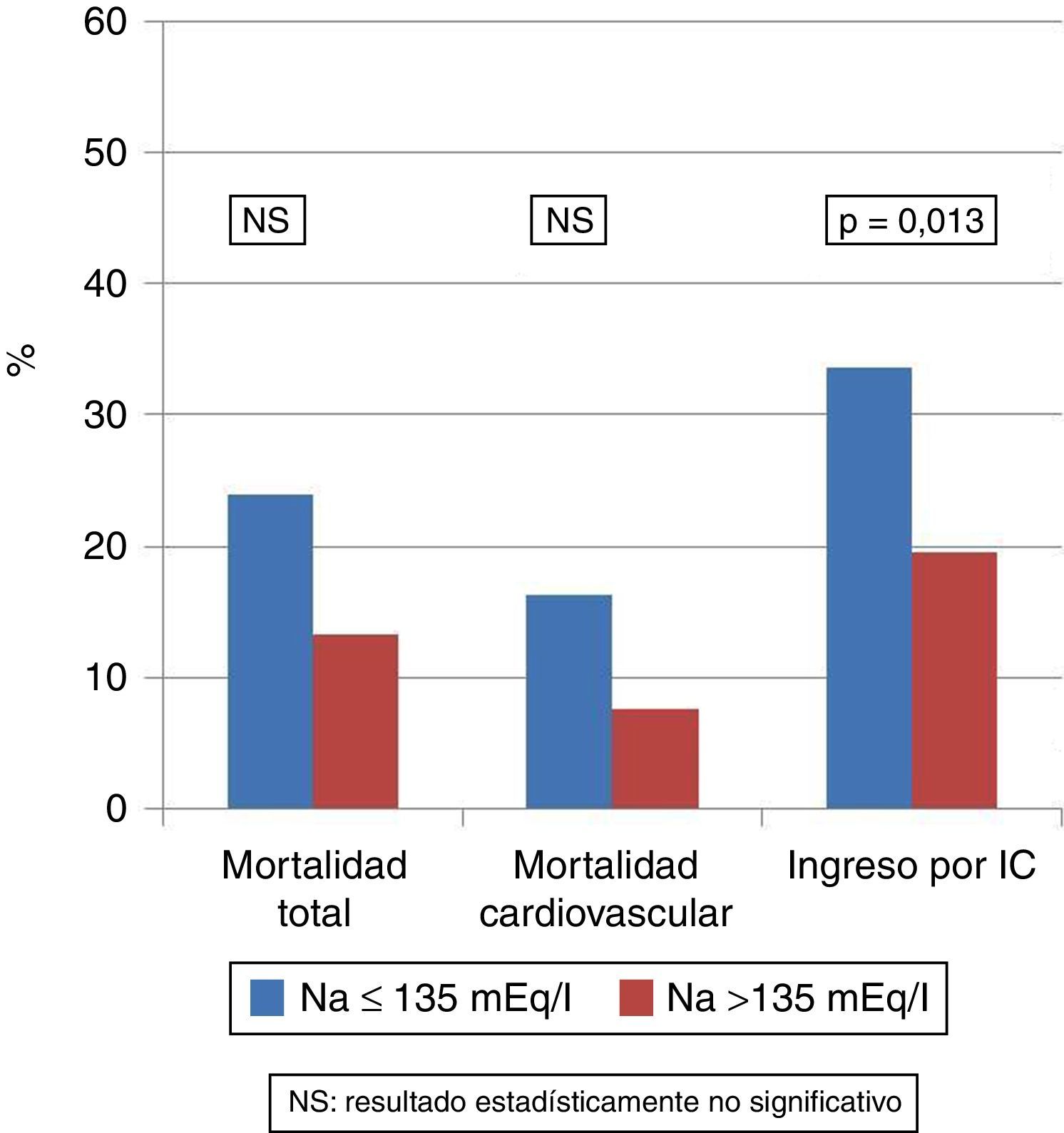
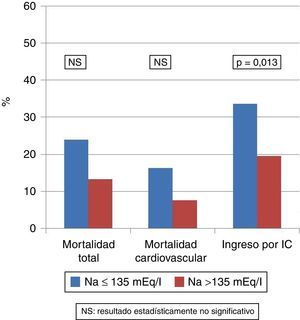
Estudio del efecto de cualquier grado de la hiponatremiaLa mortalidad total en el grupo con Na>135mEq/l (n=620) fue de 13,29%, mientras que en el grupo con Na≤135mEq/l (n=104) fue del 24% (p=0,011). La mortalidad cardiovascular en el grupo Na>135mEq/l (n=620) fue del 7,59%, mientras que en el grupo con Na≤135mEq/l (n=104) fue del 16,34% (p=0,013). La incidencia de primer ingreso por insuficiencia cardiaca en el grupo Na>135mEq/l (n=620) fue del 19,6%, mientras que en el grupo con Na≤135mEq/l (n=104) fue del 33,6% (p=0,001).
En el modelo multivariado, la hiponatremia no se mostró independientemente asociada a la mortalidad total (HR: 1,508; IC95%: 0,942-2,413; p=0,086) ni a mortalidad cardiovascular (HR: 1,76; IC95%: 0,989-3,132; p=0,054).
Los pacientes con cualquier grado de hiponatremia mostraron mayor incidencia de ingreso hospitalario por insuficiencia cardiaca en el seguimiento, manteniendo la significación estadística en el modelo multivariado (OR 1,701; IC95%: 1,05-2,756; p=0,031). Las variables creatinina al implante, mayor edad y menor FEVI también se mostraron como factores predictores de la mortalidad.
Terapias apropiadas e inapropiadas: se comparó la incidencia de la primera terapia apropiada y la inapropiada en los grupos con Na mayor (n=620) y menor de 136 (n=104), mediante análisis de Chi cuadrado, y no se obtuvieron diferencias estadísticamente significativas (16,7% vs. 17,5%, p=0,553, y 8,6% vs. 7,6%, p=0,708, respectivamente).
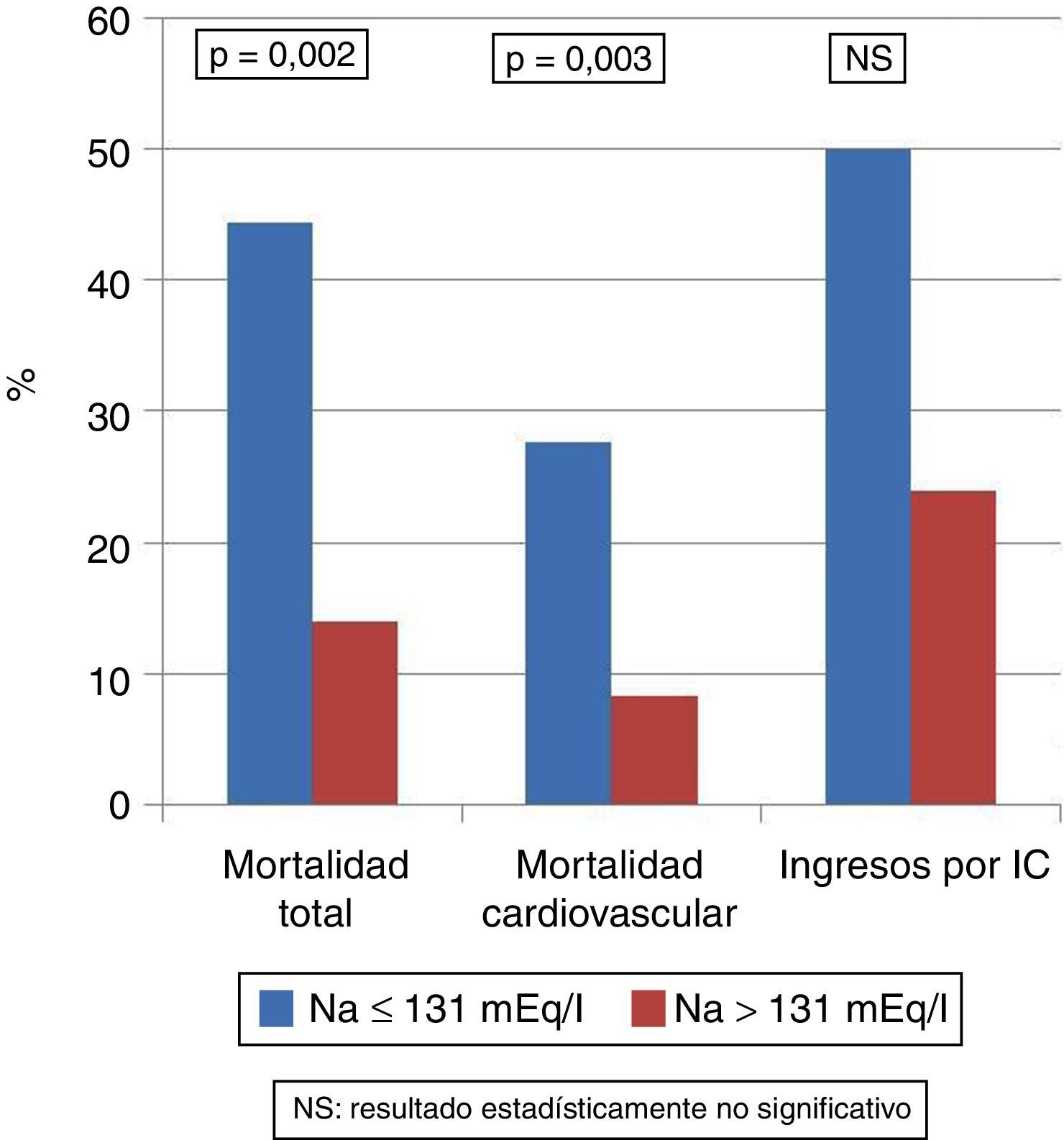
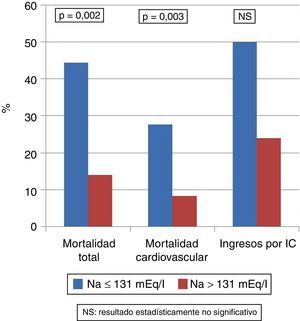
Estudio del efecto de la hiponatremia severa-moderadaLa mortalidad total en el grupo con Na>131mEq/l (n=707) fue del 14%, mientras que en el grupo con Na≤131mEq/l (n=18) fue del 44,4% (p=0,001). La mortalidad cardiovascular en el grupo Na>131mEq/l (n=707) fue del 8,3%, mientras que en el grupo con Na≤131mEq/l (n=18) fue del 27,7% (p=0,015). La incidencia de primer ingreso por insuficiencia cardiaca en el grupo Na>131mEq/l (n=707) fue del 24%, mientras que en el grupo con Na≤131mEq/l (n=18) fue del 50% (p=0,015).
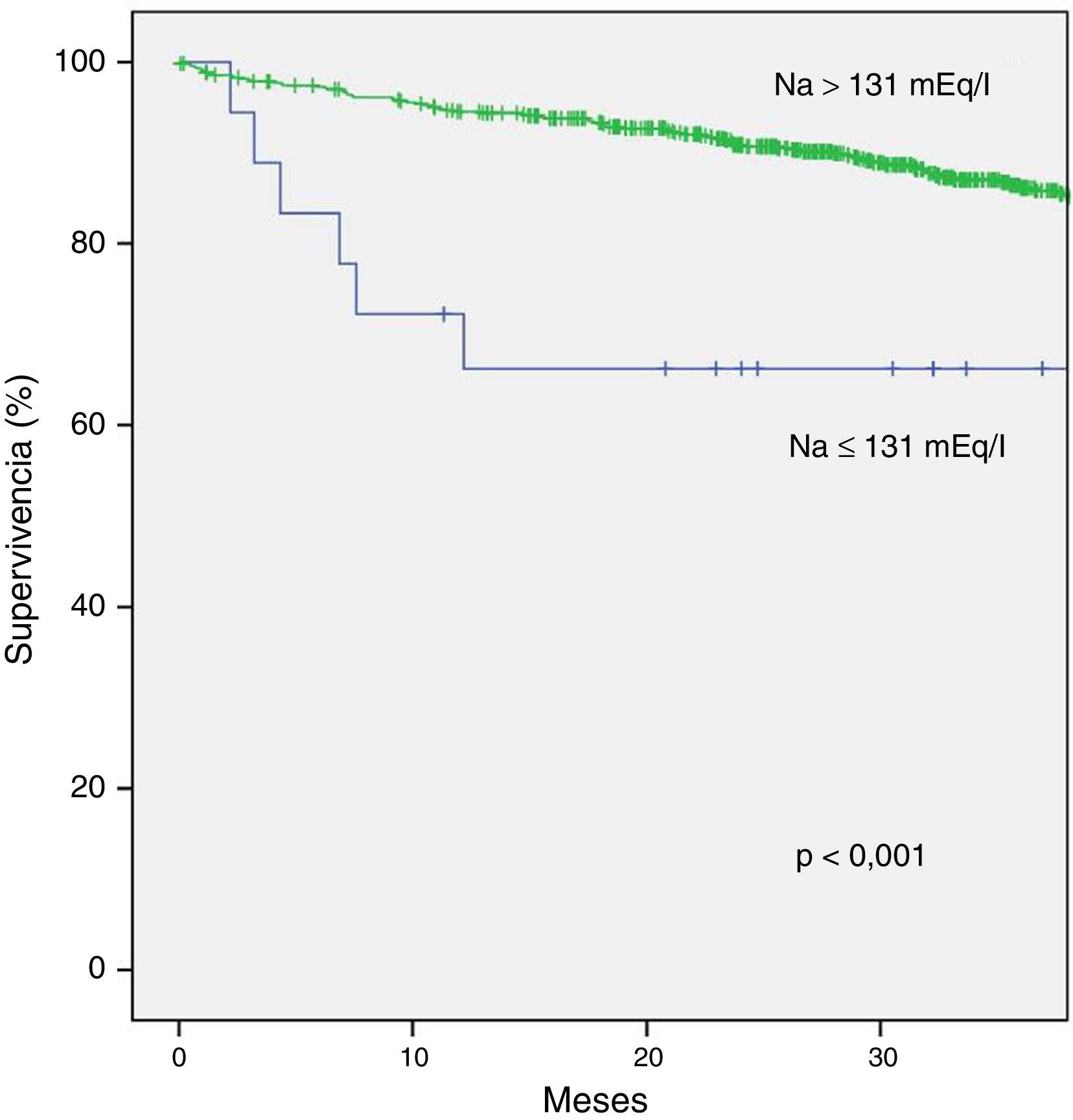
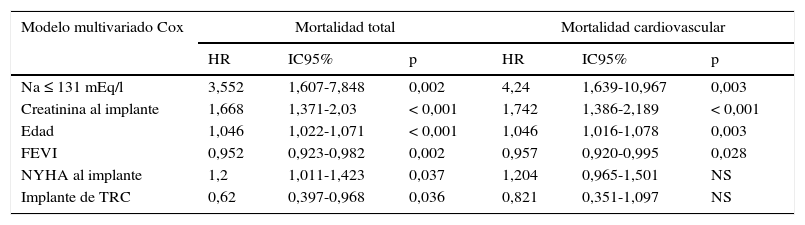
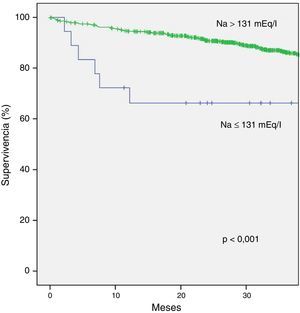
Mortalidad de cualquier causa: los pacientes con hiponatremia moderada-severa mostraron mayor mortalidad por cualquier causa que los pacientes sin dicho grado de la hiponatremia, manteniendo la significación estadística en el modelo multivariado (HR: 3,552; IC95%: 1,607-7,848; p=0,002). Las variables creatinina al implante, mayor edad, mayor NYHA al implante, ausencia de TRC y menor FEVI también se mostraron como factores predictores de mortalidad en este modelo. La media de supervivencia en meses difirió de forma significativa en ambos grupos: en el grupo con Na>131mEq/l fue de 100,46meses (IC95%: 90,37-110,55), mientras que en el grupo con Na≤131mEq/l fue de 31,19meses (IC95%; 22,24-40,15), (p<0,001) (tabla 5).
Modelo multivariado Cox: predictores de muerte total y muerte cardiovascular
| Modelo multivariado Cox | Mortalidad total | Mortalidad cardiovascular | ||||
|---|---|---|---|---|---|---|
| HR | IC95% | p | HR | IC95% | p | |
| Na ≤ 131 mEq/l | 3,552 | 1,607-7,848 | 0,002 | 4,24 | 1,639-10,967 | 0,003 |
| Creatinina al implante | 1,668 | 1,371-2,03 | < 0,001 | 1,742 | 1,386-2,189 | < 0,001 |
| Edad | 1,046 | 1,022-1,071 | < 0,001 | 1,046 | 1,016-1,078 | 0,003 |
| FEVI | 0,952 | 0,923-0,982 | 0,002 | 0,957 | 0,920-0,995 | 0,028 |
| NYHA al implante | 1,2 | 1,011-1,423 | 0,037 | 1,204 | 0,965-1,501 | NS |
| Implante de TRC | 0,62 | 0,397-0,968 | 0,036 | 0,821 | 0,351-1,097 | NS |
Mortalidad de origen cardiovascular: los pacientes con hiponatremia moderada-severa mostraron mayor mortalidad por cualquier causa que los pacientes sin dicho grado de la hiponatremia, manteniendo la significación estadística en el modelo multivariado (HR: 4,24; IC95%: 1,639-10,967; p=0,003). Las variables creatinina al implante, mayor edad y menor FEVI también se mostraron como factores predictores de mortalidad.
En el modelo multivariado, la hiponatremia moderada-severa no se asoció de manera independiente a un aumento de ingresos por insuficiencia cardiaca en el seguimiento (OR: 2,001; IC95%: 0,694-5,765; p=0,199). Las variables creatinina al implante, mayor edad y menor FEVI sí se mostraron como factores predictores de primer ingreso por la insuficiencia cardiaca.
Terapias apropiadas e inapropiadas: se comparó la incidencia de la primera terapia apropiada y la inapropiada en los grupos con el Na mayor (n=707) y menor de 131 (n=18), mediante análisis de Chi cuadrado, y no se obtuvieron diferencias estadísticamente significativas (15,2 vs. 17,9, p=0,936, y 5,6 vs. 7,8, p=0,727, respectivamente).
DiscusiónLos resultados de nuestro estudio ponen de manifiesto que valores bajos de sodio sérico periimplante (Na≤131mEq/l) se relacionan con un aumento de la mortalidad durante el seguimiento en los pacientes a quienes se implanta un DAI por prevención primaria en nuestro país.
En los pacientes con insuficiencia cardiaca tiene lugar una regulación al alza del sistema simpático, lo que supone una activación neurohormonal que afecta tanto al sistema renina-angiotensina-aldosterona como a la liberación de arginina-vasopresina. Estas alteraciones hormonales, junto al uso de diuréticos, son los condicionantes fundamentales de la hiponatremia en pacientes con insuficiencia cardiaca10-13.
La hiponatremia puede ayudar a identificar a un grupo de pacientes con insuficiencia cardiaca que presentan un peor pronóstico. Existen varios estudios que apoyan esta afirmación. En el año 2002, el grupo de Kearney et al.1, con el objetivo de buscar marcadores pronósticos no invasivos en la insuficiencia cardiaca, obtuvieron que el descenso en los niveles de sodio sérico se relacionaba con un aumento significativo de la mortalidad entre pacientes con insuficiencia cardiaca crónica estable. Posteriormente se ha relacionado la hiponatremia con estancias hospitalarias más prolongadas2 y con mayor mortalidad hospitalaria y precoz tras el alta2,3.
En los pacientes portadores de desfibriladores, la evidencia científica al respecto es menor, aunque existen varias publicaciones recientes en las que la hiponatremia también supone un aumento de los eventos adversos en el seguimiento. Recientemente, el estudio de Bhavnani et al.8 puso de manifiesto que la hiponatremia preimplante moderada (Na 131-133mmol/l) o severa (Na≤130mmol/l) suponía un aumento del riesgo de muerte, multiplicándolo por 2 o por 3, respectivamente. Además, el grupo con hiponatremia severa presentaba mayor probabilidad de ingreso por insuficiencia cardiaca en el seguimiento y menor incidencia de descargas apropiadas del dispositivo. No obstante, los autores no pueden afirmar que ello conlleve que estos pacientes presenten menor riesgo arrítmico, y en nuestra opinión dicho hallazgo podría estar en el contexto del menor tiempo de seguimiento debido a mortalidad temprana en este subgrupo, aunque el estudio no ofrece datos al respecto que permitan confirmarlo.
La utilidad de la hiponatremia como factor pronóstico también se ha establecido en los pacientes que se someten a un implante de dispositivos de resincronización. Un nivel de sodio preimplante <135mEq/l ha demostrado asociarse a mayor probabilidad de ocurrencia del endpoint combinado de muerte de cualquier causa, trasplante cardiaco, necesidad de dispositivo de asistencia ventricular o ingreso por insuficiencia cardiaca en el seguimiento, en un grupo de más de 400 pacientes sometidos a terapia de resincronización14, de forma que el 57,9% de los pacientes con dicho grado de hiponatremia presentaron al menos alguno de los eventos en la evolución, respecto al 40,7% de los pacientes sin hiponatremia. Resulta llamativo que los pacientes que normalizaban la natremia tras el implante presentaban menor incidencia del evento primario que los que partían de unas cifras de sodio normales y desarrollaban posteriormente hiponatremia. Datos congruentes se observan en otro trabajo similar, aunque de menor tamaño muestral15.
Los hallazgos de nuestro estudio demuestran que la hiponatremia en el momento del implante de un DAI por prevención primaria en los pacientes con FEVI≤35% es relativamente común, siendo en nuestra muestra del 14,5%. Esta prevalencia es similar a la reportada en el trabajo de Arévalo-Lorido et al.16 y ligeramente inferior a la obtenida en otros estudios, donde la hiponatremia aparece en el 20-25% de los pacientes2,3,9. La causa probablemente se deba a que en nuestro trabajo y en el de Arévalo-Lorido et al. los pacientes en la clase funcionali-ii representan el 56-58% de la muestra, mientras que en otros trabajos el porcentaje de pacientes en clase funcionali-ii solo asciende al 25%, aproximadamente.
Los pacientes incluidos en nuestro estudio presentan ciertas particularidades respecto a otros trabajos publicados. En primer lugar se trata del primer trabajo realizado con el objetivo de valorar la hiponatremia como factor pronóstico únicamente en pacientes con indicación de prevención primaria para el implante del desfibrilador. La indicación, en el estudio de Bhavnani et al.8, incluía tanto la prevención primaria como la secundaria, mientras que en los estudios realizados exclusivamente con terapia de resincronización, el principal objetivo del dispositivo era la mejoría de la clase funcional en pacientes con grados más avanzados de insuficiencia cardiaca. En segundo lugar, se trata del primer estudio que valora el poder pronóstico de la hiponatremia en el momento del implante en una cohorte española.
A pesar de las diferencias en la población de estudio, los resultados obtenidos en nuestro trabajo refuerzan los referidos en las publicaciones previas. Estudiamos 725 pacientes, con un seguimiento medio de casi 3años desde el implante. En más del 50% la causa de su cardiopatía era isquémica. En primer lugar se observa una mayor mortalidad total y mortalidad cardiovascular en el grupo con cualquier grado de la hiponatremia, que incluye la hiponatremia ligera (Na≤135mEq/l), con respecto a los pacientes normonatrémicos, aunque la significación estadística se pierde al incluirla en el modelo multivariado. Además, el hecho de presentar cualquier grado de hiponatremia se asocia a un riesgo 1,7 veces mayor de presentar un primer ingreso por IC en el seguimiento. Los resultados en cuanto a mortalidad son más evidentes en el grupo con hiponatremia moderada-severa, en el que la relación de la natremia se mantiene significativa al ajustar por potenciales variables de confusión como la FEVI, la función renal, el tipo de cardiopatía, la clase funcional, el implante de TRC y el ritmo al implante. Un valor de Na≤131mEq/l se asocia a un riesgo 4 veces mayor de muerte total (HR: 3,79; p=0,001) y cardiovascular (HR: 4,5; p=0,002). Llama la atención que la asociación entre la hiponatremia moderada-severa e ingresos por insuficiencia cardiaca pierda la significación estadística en el análisis multivariado. En nuestra opinión, este hecho se debe a que se trata de un grupo que incluye pocos pacientes y en el que la incidencia de muerte en el seguimiento es muy elevada, ascendiendo a más del 44%. Se trata de pacientes con múltiples comorbilidades, por lo que la causa de muerte es de origen no cardiovascular en el 17% de los pacientes, y en el 27,7% en el que el fallecimiento sí tiene un origen cardiovascular, este no se debe únicamente a descompensación de insuficiencia cardiaca, sino que también incluye la muerte súbita, los eventos coronarios y la muerte de origen vascular. Todo ello supone que el tiempo de seguimiento de los pacientes fallecidos por causa no relacionada con insuficiencia cardiaca se vea reducido y por tanto, también, se limite la posibilidad de presentar un ingreso por insuficiencia cardiaca. De hecho, se objetiva que la supervivencia media estimada en los pacientes con hiponatremia moderada-severa es significativamente menor, lo que obliga a pensar en la posible menor utilidad del DAI en prevención primaria en los pacientes con dicho grado de hiponatremia.
En nuestro trabajo, también se valoró la incidencia de la primera terapia apropiada e inapropiada del dispositivo, sin encontrar diferencias significativas en los pacientes con hiponatremia ligera ni tampoco en aquellos con hiponatremia moderada-severa, al compararlos con los que presentaban el sodio normal. Estos datos difieren de los ya comentados del estudio de Bhavnani et al.8. En dicha publicación, la incidencia de terapias apropiadas en ambos grupos era superior a la de nuestro estudio, de modo que los pacientes sin hiponatremia presentaban una tasa de terapias apropiadas del 37%, siendo del 29% en el grupo con hiponatremia moderada-severa, mientras que nuestra tasa de terapias en ambos grupos se encuentra en torno al 17%. Lo más probable es que esta diferencia se deba a que nuestro estudio incluye únicamente a los pacientes a los que se les implanta un DAI por prevención primaria, mientras que en el estudio de Bhavnani et al. encontramos pacientes con implantes tanto en prevención primaria como secundaria.
La decisión de implantar un DAI en prevención primaria sigue siendo controvertida. Las indicaciones actuales se basan en la presencia de disfunción ventricular y en la clase funcional principalmente, aunque hacen hincapié en la necesidad de realizar una valoración individualizada en cada paciente y en que se sopesen tanto el riesgo-beneficio como el coste-efectividad de este tipo de procedimiento6,7. Ciertas comorbilidades y características que se reconocen como limitantes para el implante de un DAI en la prevención primaria incluyen: esperanza de vida<1año, edad ≥90años, consumo de drogas o ausencia de adherencia al tratamiento prescrito, patología psiquiátrica grave, insuficiencia renal terminal e infección sistémica activa. Actualmente no están correctamente identificados otros factores que, como la hiponatremia, podrían establecer una población que realmente no se beneficiará del implante de un desfibrilador en cuanto a que estos dispositivos no modifiquen su pronóstico, aumentando, no obstante, el riesgo de complicaciones y efectos adversos derivados de la utilización del DAI.
LimitacionesSe trata de un estudio observacional retrospectivo, por lo que, pese a realizar un análisis multivariado para controlar las posibles variables de confusión, no podemos asegurar que no existan otras variables que difieran en los grupos comparados y que no se hayan tenido en cuenta. Por otro lado, se ha valorado la influencia del nivel de sodio en el momento del implante, sin que se hayan registrado las variaciones a lo largo del seguimiento que podrían repercutir en la incidencia de eventos. En cuanto a las terapias, el hecho de utilizar varias de ellas y una programación basada en el criterio clínico y probablemente heterogénea, limitan las conclusiones que puedan extraerse de la incidencia de terapias apropiadas e inapropiadas.
ConclusionesUn valor de sodio ≤135mEq/l en el momento del implante de un desfibrilador en prevención primaria se asocia a una mayor incidencia de ingreso por insuficiencia cardiaca en el seguimiento, mientras que la hiponatremia moderada-severa se asocia a un riesgo de muerte en la evolución 4 veces mayor, todo ello sin que existan diferencias en la incidencia de terapias apropiadas o inapropiadas.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesEn el presente documento declaramos que no existe potencial conflicto de intereses por parte de ninguno de los autores ni de sus instituciones.
Emad Abu-Assi (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario Santiago de Compostela, Santiago de Compostela, La Coruña), Larraitz Gaztañaga (Unidad de Arritmias, Servicio de Cardiología, Hospital de Basurto, Bilbao), Pilar Cabanas-Grandío (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario de Vigo, Vigo, Pontevedra), María Teresa Barrio-López (Unidad de Arritmias, Servicio de Cardiología, Hospital Virgen de Las Nieves, Granada), Cristina González-Cambeiro (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario Santiago de Compostela, Santiago de Compostela, La Coruña), Vicente Bertomeu-González (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario San Juan, Alicante), Álvaro Arce-León (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario Virgen del Rocío, Sevilla), Hugo Arguedas-Jiménez (Unidad de Arritmias, Servicio de Cardiología, Clínica Universidad de Navarra, Pamplona), José Antonio Iglesias-Bravo (Unidad de Arritmias, Servicio de Cardiología, Hospital Fundación Jiménez Díaz, Madrid), Juan Fernández-Armenta (Unidad de Arritmias, Servicio de Cardiología, Hospital Puerta del Mar, Cádiz), Luis Martínez-Sande (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario Santiago de Compostela, Santiago de Compostela, La Coruña), Joaquín Osca Asensi (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario La Fe, Valencia), José Moreno-Arribas (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario San Juan, Alicante), Agustín Fernández-Cisnal (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario Virgen del Rocío, Sevilla),Óscar Cano (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario La Fe, Valencia), Juan Benezet-Mazuecos (Unidad de Arritmias, Servicio de Cardiología, Hospital Fundación Jiménez Díaz, Madrid), Ignacio García-Bolao (Unidad de Arritmias, Servicio de Cardiología, Clínica Universidad de Navarra, Pamplona), Oscar Salvador (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario La Paz, Madrid), Rafael Peinado (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario La Paz, Madrid), Ernesto Díaz-Infante (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario Virgen Macarena, Sevilla), Juan José Olalla Antolín (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario Marqués de Valdecilla, Santander), Jose Ormaetxe (Unidad de Arritmias, Servicio de Cardiología, Clínica Universidad de Navarra, Pamplona), Enrique García (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario de Vigo, Vigo, Pontevedra), José Olagüe de Ros (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario La Fe, Valencia), Luis Tercedor-Sánchez (Unidad de Arritmias, Servicio de Cardiología, Hospital Virgen de Las Nieves, Granada), Alonso Pedrote-Martínez (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario Virgen del Rocío, Sevilla), José Ramón González-Juanatey (Unidad de Arritmias, Servicio de Cardiología, Hospital Universitario Santiago de Compostela, Santiago de Compostela, La Coruña).