Las guías internacionales recientes proponen el uso de estatinas como piedra angular del manejo de la dislipidemia en adultos. Sin embargo, no se ha definido con claridad el tratamiento de los pacientes con intolerancia o efectos adversos asociados con estas. Las resinas secuestradoras de ácidos biliares son una alternativa interesante, pese a que la evidencia que avala su uso no ha sido evaluada cuidadosamente.
MétodosSe realizó una búsqueda de la literatura en MEDLINE, Embase y en la Biblioteca Cochrane hasta junio de 2013, acerca de artículos publicados en inglés y español, identificando experimentos clínicos aleatorizados y estudios de cohortes que evaluaran el impacto de las resinas secuestradoras de ácidos biliares en mortalidad, eventos cardiovasculares, niveles de lípidos séricos y efectos adversos. Se presenta la información de forma descriptiva.
ResultadosSe identificaron cuatro experimentos clínicos aleatorizados y un estudio de cohortes, que incluían 6.833 pacientes. Solo uno de los estudios evaluó el impacto en la mortalidad cardiovascular, evidenciando que no hay diferencia estadísticamente significativa en comparación con placebo (RR de 0,76; IC 95% 0,5:1,15), aunque se observó una reducción del 16% en la incidencia de infarto agudo de miocardio (RR 0,84; IC 95% 0,67:1,00). Tres estudios evaluaron cambios en las fracciones lipídicas, los cuales mostraron disminución moderada en los niveles de colesterol LDL, sin percibir diferencias clínicamente significativas en los niveles de colesterol HDL y triglicéridos.
ConclusiónLa evidencia que respalda el uso de resinas secuestradoras de ácidos biliares es limitada y no avala su empleo como terapia de primera línea en pacientes con dislipidemia; no obstante, son una alternativa en pacientes con efectos adversos o intolerancia al manejo con estatinas.
Recent international guidelines have proposed statins as the corner stone of dyslipidemia management in adults. However it is not clear if they are best option for patients with statin related intolerance or what their adverse effects are. The bile acid sequestrants are an interesting alternative, however its evidence has not been carefully evaluated.
MethodsA search was conducted on MEDLINE, Embase and Cochrane library databases for articles published up to June 2013, limited to Spanish and English language. Randomized clinical trials (RCT) and cohort studies evaluating the impact of bile acid sequestrants on mortality, cardiovascular outcomes, seric lipids and adverse effects were selected. Information was presented in a descriptive way.
ResultsFour RCT and one cohort study with aggregate data on 6833 people were included. Just one study evaluated cardiovascular mortality showing no statistically significant difference when compared with placebo, (RR 0.76; 95% CI 0.5:1.15), however there was a 16% reduction on acute myocardial infarction incidence. (RR 0.84; 95% IC 0.67: 1.00). Three studies evaluated seric lipids changes showing a moderate reduction in LDL levels without clinical significant differences on HDL and triglyceride levels.
ConclusionsThe evidence supporting bile acid sequestrants use is lacking and not conclusive to recommend its use as first-line therapy in dyslipidemic patients; however, these are an alternative option for patients with statin-related intolerance or adverse effects.
De acuerdo con el boletín epidemiológico del Instituto Nacional de Salud publicado en 2013, la enfermedad cardiovascular es la principal causa de muerte en Colombia, y ha venido en continuo crecimiento durante la última década1, realidad compartida tanto con países desarrollados como con otros en vía de desarrollo2. Como parte de las estrategias de control se han intensificado y aunado esfuerzos para controlar los principales factores de riesgo cardiovascular, como hipertensión arterial, tabaquismo, diabetes mellitus, dislipidemia y obesidad3.
Recientemente, la Asociación Americana del Corazón y el Colegio Americano de Cardiología (AHA/ACC) publicaron las Guías para el tratamiento del colesterol sanguíneo con miras a reducir el riesgo aterosclerótico cardiovascular en adultos4, en las que propusieron a las estatinas como el pilar fundamental del tratamiento farmacológico de las dislipidemias en la población adulta. Sin embargo, algunos grupos de pacientes presentan intolerancia o efectos secundarios que obligan a suspender dicha terapia o hay quienes no logran reducciones significativas en las fracciones lipídicas, de modo tal que se impacta de manera negativa el riesgo de presentar desenlaces cardiovasculares o cerebrovasculares.
Una de las opciones terapéuticas con la que se cuenta en este escenario clínico son las resinas secuestradoras de ácidos biliares (RSAB), que incluyen colestiramina, colestipol y colesevelam. Su mecanismo de acción estriba en la formación de un compuesto inabsorbible que termina siendo excretado por la materia fecal, lo que disminuye la circulación enterohepática de ácidos biliares, propiciando a su vez una cadena de retroalimentación positiva para la producción de nuevos ácidos biliares a partir de colesterol LDL. El hepatocito depletado de colesterol LDL, termina por expresar receptores para capturar LDL, proceso que finalmente conlleva la reducción de LDL plasmático5–10.
A pesar de que durante varias décadas las RSAB han estado disponibles como parte de las opciones terapéuticas para el manejo de la dislipidemia, la evidencia que avala su uso nunca ha sido sintetizada y evaluada de forma sistemática. Esta publicación constituye la primera revisión sistemática de la literatura que evalúa el impacto de las RSAB en los desenlaces cardiovasculares y en los niveles séricos de lípidos.
El estudio fue desarrollado inicialmente como parte de la «Guía colombiana para la prevención, detección temprana, diagnóstico, tratamiento y seguimiento de la dislipidemia en pacientes colombianos mayores de 18 años»11. Conocer esta evidencia es fundamental a la hora de definir el papel real de estos medicamentos en el manejo de la dislipidemia en pacientes adultos, tanto en prevención primaria como secundaria.
Materiales y métodosBúsqueda de la literaturaSe llevó a cabo una búsqueda sistemática de la literatura con el fin de hallar artículos relevantes, incluyendo las bases de datos MEDLINE (Pubmed), EMBASE, y la base de datos de la colaboración Cochrane (Cochrane Central Register of Controlled trials), desde la iniciación hasta junio de 2013. Los términos de búsqueda incluyeron: hiperlipidemia, dislipidemia, hipercolesterolemia, colesevelam, colestipol y colestiramina, tanto en texto libre como en términos MeSH. Se restringió la búsqueda a publicaciones en inglés o español, y adicionalmente se realizó una búsqueda manual de las referencias bibliográficas de los artículos identificados.
Selección de los estudiosLos artículos hallados se incluían en la revisión sistemática de la literatura si cumplían los siguientes criterios: pacientes mayores de 18 años que cursaran con dislipidemia, con o sin enfermedad cardiovascular incluyendo ataque cerebrovascular, infarto agudo de miocardio, angina inestable o enfermedad arterial periférica; que recibieran alguna de las resinas secuestradoras de ácidos biliares (colestiramina, colestipol o colesevelam) por lo menos durante un periodo de 24 semanas, comparando su uso contra placebo o dieta. Se incluyeron tanto estudios de cohortes como experimentos clínicos aleatorizados. Los experimentos clínicos debían contar con un mínimo de 50 pacientes en cada brazo de tratamiento y evaluar al menos uno de los desenlaces del estudio. Los desenlaces primarios fueron mortalidad de causa cardiovascular e incidencia de infarto agudo de miocardio o ataque cerebrovascular; también se incluyeron cambios en las fracciones lipídicas, adherencia a la terapia e incidencia de efectos adversos.
Se descartaron estudios que incluyeran pacientes con dislipidemias familiares, VIH u otras inmunodeficiencias, y pacientes con enfermedad renal crónica en cualesquiera de sus estadios. La selección de los estudios se hizo de forma pareada y estuvo a cargo de dos investigadores (AH y NC); las discrepancias fueron resueltas por consenso, contando con la opinión de un tercer investigador (OM).
Extracción de los datos y evaluación de calidadComo se expresó, los datos fueron extraídos independientemente por dos investigadores (NC y AH), utilizando un formato estandarizado. Las discrepancias fueron resueltas por consenso, con la intervención de un tercer investigador (OM). Los investigadores recolectaron los siguientes datos para cada estudio: diseño del estudio, tamaño de la muestra, características basales de la población, medicamento utilizado y dosis, duración del seguimiento, resultados en los desenlaces. Cuando se trató de un experimento clínico el estimativo de resumen utilizado fue el riesgo relativo (RR), y para los estudios de cohorte se utilizó la razón de disparidad (OR). En los casos en que se disponía de más de un estudio publicado sobre la misma población se seleccionó el más reciente; a pesar de ello, se revisaron los artículos complementarios en busca de datos adicionales.
La evaluación del riesgo de sesgo de los estudios incluidos se hizo a través de los cuestionarios propuestos por el Scottish Intercollegiate Guidelines Network (SIGN 50)12, mediante formatos diferenciales según el diseño (estudios de cohorte o experimentos clínicos aleatorizados). Lo anterior estuvo de acuerdo con las recomendaciones de la «Guía metodológica para la elaboración de guías de práctica clínica y evaluación económica en el Sistema General de Seguridad Social colombiano»13. Los resultados de esta evaluación permitieron clasificar los estudios en alto, moderado o bajo riesgo de sesgo.
Análisis estadísticoSe planeó la recolección de los RR o las OR (para los estudios de cohorte) y de la reducción absoluta de riesgo, reportados en cada estudio para los desenlaces primarios, y la diferencia de medias para los cambios en el perfil lipídico, con sus respectivos intervalos de confianza del 95%. Adicionalmente, se planeó la evaluación de la heterogeneidad usando el estadístico I2. Con estos datos se planeó resumir la información contenida en los experimentos clínicos aleatorios, mediante un modelo de efectos aleatorios, considerando la evaluación de múltiples moléculas que podrían conferir heterogeneidad a los datos. Estos, a su vez, se procesaron con el programa estadístico RevMan versión 5.3.5, sugerido por la Colaboración Cochrane.
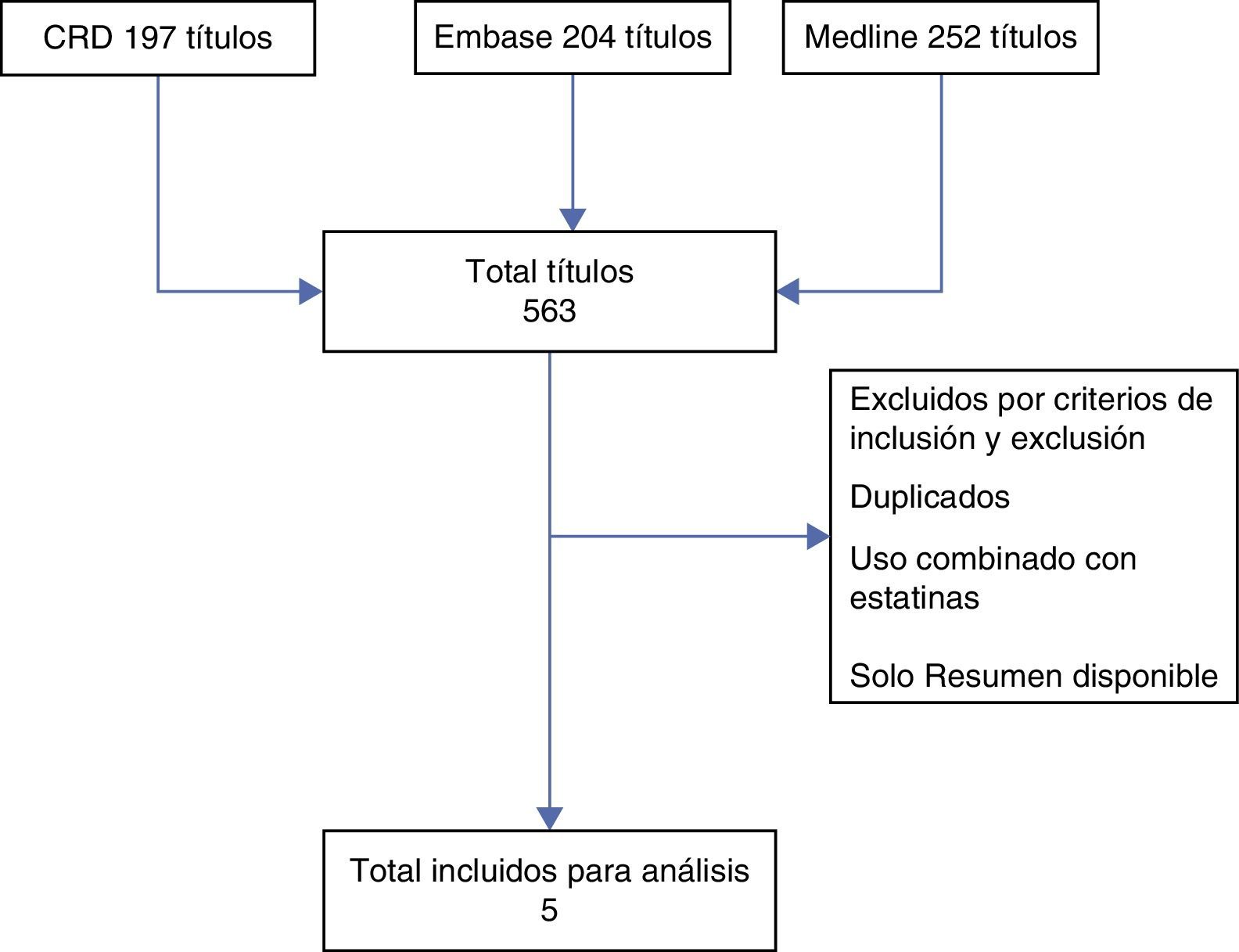
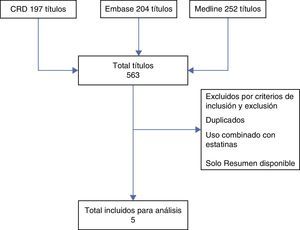
ResultadosDe los 563 títulos identificados se seleccionaron 514–18 que incluían 6.833 pacientes. Cuatro de estos estudios correspondieron a experimentos clínicos controlados14–18 y uno a un estudio de cohortes19 (fig. 1). Dos de los estudios correspondían a una misma población en la que usaron como intervención colestiramina14,15, en dos se utilizó colesevelam16,17 y en uno colestipol18.
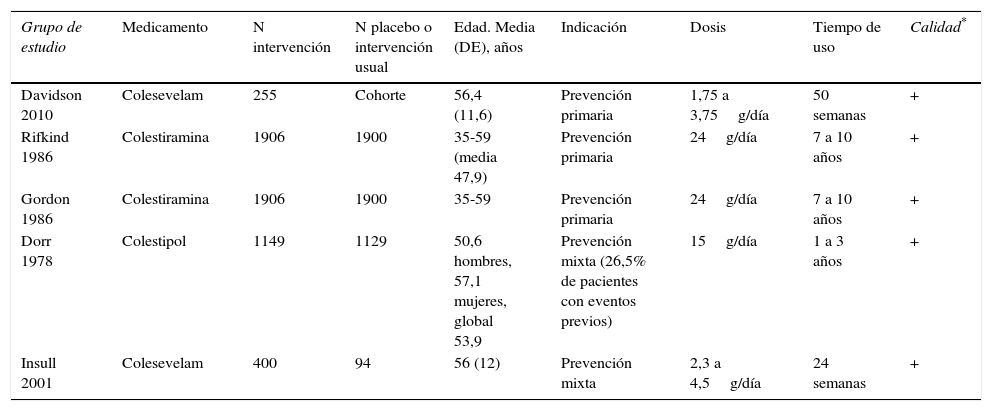
Las características de los estudios se muestran en la tabla 1. Los estudios más grandes14,15 fueron publicados antes de 1990, fecha en la que aún no estaban disponibles las estatinas. Todos ellos incluyeron población de prevención primaria y dos incluyeron adicionalmente una proporción de pacientes con eventos previos17,18. El tiempo de seguimiento estuvo en el rango entre 24 semanas y 10 años.
Características de los estudios incluidos para el análisis del uso de resinas secuestradoras de ácidos biliares vs. placebo
| Grupo de estudio | Medicamento | N intervención | N placebo o intervención usual | Edad. Media (DE), años | Indicación | Dosis | Tiempo de uso | Calidad* |
|---|---|---|---|---|---|---|---|---|
| Davidson 2010 | Colesevelam | 255 | Cohorte | 56,4 (11,6) | Prevención primaria | 1,75 a 3,75g/día | 50 semanas | + |
| Rifkind 1986 | Colestiramina | 1906 | 1900 | 35-59 (media 47,9) | Prevención primaria | 24g/día | 7 a 10 años | + |
| Gordon 1986 | Colestiramina | 1906 | 1900 | 35-59 | Prevención primaria | 24g/día | 7 a 10 años | + |
| Dorr 1978 | Colestipol | 1149 | 1129 | 50,6 hombres, 57,1 mujeres, global 53,9 | Prevención mixta (26,5% de pacientes con eventos previos) | 15g/día | 1 a 3 años | + |
| Insull 2001 | Colesevelam | 400 | 94 | 56 (12) | Prevención mixta | 2,3 a 4,5g/día | 24 semanas | + |
La evaluación de calidad se presenta de acuerdo con la propuesta de SIGN, con base en una evaluación sistemática de la capacidad de los estudios para minimizar los sesgos: ++ se refiere a estudios de buena calidad con características que minimizan adecuadamente la posibilidad de sesgos;+implica calidad intermedia con control parcial del potencial de sesgos.
Todos los estudios tuvieron riesgo moderado de sesgo de acuerdo con la evaluación efectuada con los cuestionarios propuestos por SIGN. Las principales limitaciones detectadas fueron falta de cegamiento a los evaluadores16,17 y alta tasa de pérdidas al seguimiento14,15,17.
Eventos cardiovasculares y cerebrovascularesLos desenlaces primarios evaluados fueron el impacto en la mortalidad y en las frecuencias de infarto agudo de miocardio y accidente cerebrovascular. El estudio de Dorr18 fue el único que evaluó cambios en la mortalidad, mostrando una disminución no estadísticamente significativa (RR de 0,76; IC 95% 0,5:1,15). El impacto de la colestiramina en la incidencia de infarto agudo de miocardio fue evaluado en el estudio de Rifkind14, The Lipids Research Clinics Coronary Primary Prevention Trial, el más grande realizado con RSAB. Fue publicado en 1986 e incluyó 1.906 pacientes que recibieron colestiramina y 1.900 a quienes se les suministró placebo, en un seguimiento entre 7 y 10 años. Se demostró una reducción en la incidencia de infarto agudo de miocardio del 16% (RR 0,84; IC 95% 0,67: 1,00) (tabla 2). Ningún estudio publicado ha evaluado el impacto de las RSAB en la incidencia de accidente cerebrovascular.
Impacto de las RSAB en mortalidad cardiovascular e infarto agudo de miocardio
| Referencia/tipo de estudio | Intervención | Desenlace | Número de participantes en grupo intervención/control | Eventos en grupo intervención/control n (%) | Tamaño del efecto RR |
|---|---|---|---|---|---|
| Rifkind1986ECA | Colestiramina | IAM | 1906/1900 | 155 (8,3%)/187(9,8%) | 0,84 IC 95% (0,67; 1,00) |
| Dorr1978ECA | Colestipol | Muerte cardiovascular | 1149/1129 | 37 (3,2%)/48 (4,2%) | 0,76 IC 95% (0,5; 1,15) |
ECA: experimento clínico aleatorizado; RR: riesgo relativo.
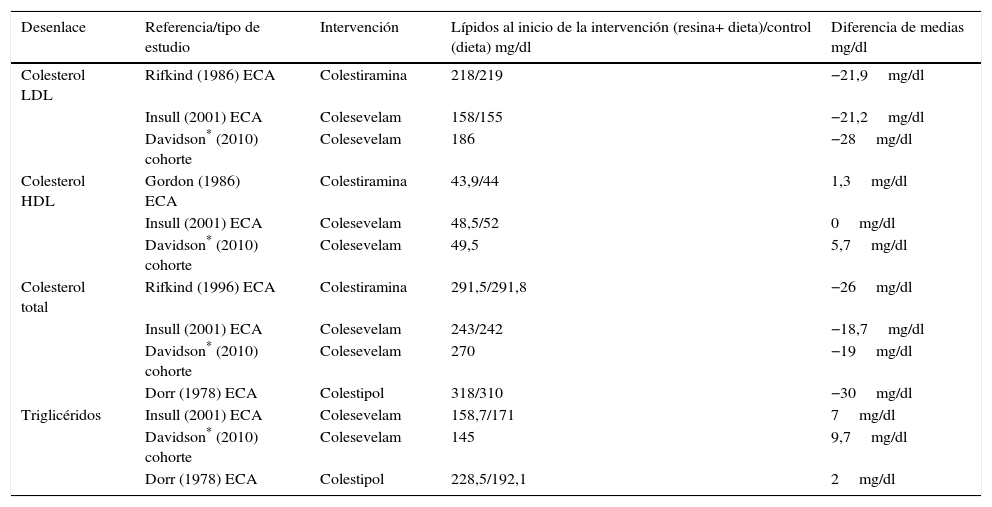
Tres estudios reportaron cambios en los niveles de colesterol LDL14,16,17. Todos detectaron disminución en los niveles de colesterol LDL con la intervención, en el rango entre 21 y 28mg/dl. En cuanto a los niveles de colesterol HDL, los resultados también tuvieron tendencias similares, ya que los tres estudios15–17 determinaron que no hubo variaciones clínicamente significativas, con un aumento máximo de 5,7mg/dl reportado en el estudio de Davidson. Por último, tres estudios más16–18 presentan la información sobre el cambio en los niveles de triglicéridos y todos demuestran un aumento clínicamente no significativo en rangos entre 2 y 9,7mg/dl. Cabe resaltar que no fue posible hacer un metaanálisis de la información puesto que los estudios originales no reportaron los intervalos de confianza. En la tabla 3 se presenta la información contenida en los estudios acerca de los cambios en las fracciones de perfil lipídico.
Impacto de las RSAB en las fracciones lipídicas
| Desenlace | Referencia/tipo de estudio | Intervención | Lípidos al inicio de la intervención (resina+ dieta)/control (dieta) mg/dl | Diferencia de medias mg/dl |
|---|---|---|---|---|
| Colesterol LDL | Rifkind (1986) ECA | Colestiramina | 218/219 | −21,9mg/dl |
| Insull (2001) ECA | Colesevelam | 158/155 | −21,2mg/dl | |
| Davidson* (2010) cohorte | Colesevelam | 186 | −28mg/dl | |
| Colesterol HDL | Gordon (1986) ECA | Colestiramina | 43,9/44 | 1,3mg/dl |
| Insull (2001) ECA | Colesevelam | 48,5/52 | 0mg/dl | |
| Davidson* (2010) cohorte | Colesevelam | 49,5 | 5,7mg/dl | |
| Colesterol total | Rifkind (1996) ECA | Colestiramina | 291,5/291,8 | −26mg/dl |
| Insull (2001) ECA | Colesevelam | 243/242 | −18,7mg/dl | |
| Davidson* (2010) cohorte | Colesevelam | 270 | −19mg/dl | |
| Dorr (1978) ECA | Colestipol | 318/310 | −30mg/dl | |
| Triglicéridos | Insull (2001) ECA | Colesevelam | 158,7/171 | 7mg/dl |
| Davidson* (2010) cohorte | Colesevelam | 145 | 9,7mg/dl | |
| Dorr (1978) ECA | Colestipol | 228,5/192,1 | 2mg/dl |
ECA: experimento clínico aleatorizado.
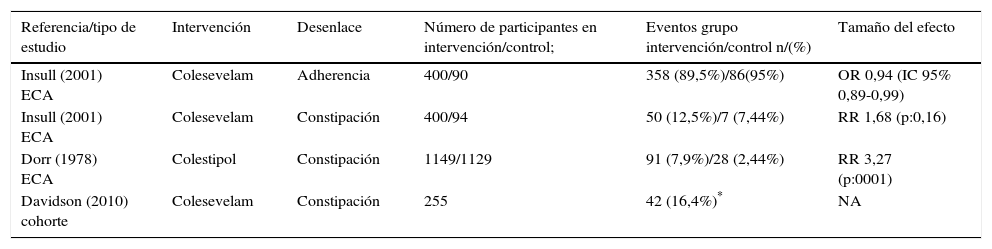
En cuanto a efectos adversos, tres estudios17–19 evaluaron este desenlace y reportaron constipación como el efecto adverso más frecuente (tabla 4). La adherencia al medicamento solo se evaluó en un estudio de cohorte17, en el que se mostró que el uso de este medicamento era bien tolerado, con una adherencia muy similar a la reportada para el placebo (OR 0,94; IC 95% 0,89-0,99) (tabla 4).
Adherencia y efectos adversos asociados al uso de RSAB
| Referencia/tipo de estudio | Intervención | Desenlace | Número de participantes en intervención/control; | Eventos grupo intervención/control n/(%) | Tamaño del efecto |
|---|---|---|---|---|---|
| Insull (2001) ECA | Colesevelam | Adherencia | 400/90 | 358 (89,5%)/86(95%) | OR 0,94 (IC 95% 0,89-0,99) |
| Insull (2001) ECA | Colesevelam | Constipación | 400/94 | 50 (12,5%)/7 (7,44%) | RR 1,68 (p:0,16) |
| Dorr (1978) ECA | Colestipol | Constipación | 1149/1129 | 91 (7,9%)/28 (2,44%) | RR 3,27 (p:0001) |
| Davidson (2010) cohorte | Colesevelam | Constipación | 255 | 42 (16,4%)* | NA |
ECA: experimento clínico aleatorizado; NA: no aplica; OR: razón de disparidad; RR: riesgo relativo.
De acuerdo con la evidencia disponible en la actualidad y con las guías internacionales recientes4,6, resulta claro que las estatinas son los medicamentos de primera línea en el tratamiento de la dislipidemia en adultos. Las guías de la ACC/AHA4 proponen considerar el uso de las RSAB al mismo nivel que otros grupos de medicamentos hipolipemiantes, como ezetimibe, ácido nicotínico y fibratos, dejando al clínico la decisión de cuál usar en caso de contraindicación o intolerancia a las estatinas.
La actual es la primera revisión sistemática de la literatura que evalúa de forma rigurosa la evidencia disponible en cuanto a los efectos del uso de las RSAB, denotando las serias deficiencias de la evidencia que avala su uso. El primer inconveniente radica en la antigüedad de los estudios clínicos disponibles, que se asocia con limitaciones importantes en la aplicabilidad de los datos. Un ejemplo es el estudio publicado por Rifkind en 198614, que es adicionalmente el más grande y significativo de los estudios que han evaluado las RSAB en el manejo de la dislipidemia. Este dio un giro histórico a la enfermedad cardiovascular al mostrar que la disminución en los niveles de las fracciones lipídicas sanguíneas atenuaba la probabilidad de eventos cardiovasculares de origen aterotrombótico (específicamente de infarto agudo de miocardio). Sin embargo, es difícil evaluar sus resultados a la luz de los conocimientos actuales dado que ahora se dispone de múltiples intervenciones adicionales no existentes previamente, como estatinas y medicamentos antitrombóticos y antiplaquetarios. En esa población sin esos nuevos medicamentos era más sencillo demostrar cambios significativos, ya que les faltaban intervenciones que ahora son rutinarias.
Otra limitación de la evidencia disponible está dada por el pobre reporte de estos estudios, que no presentan los resultados en profundidad, lo que impide hacer un metaanálisis de la información y, por tanto fortalecer los estimativos del tamaño del efecto en las fracciones lipídicas.
Es importante resaltar que si bien la actividad hipolipemiante de las RSAB es modesta, son medicamentos con perfil de seguridad apropiado y altas tasas de adherencia. En vista de que no pasan a la circulación sistémica, los principales efectos adversos de las RSAB son gastrointestinales, entre los cuales sobresale el estreñimiento20. Su perfil de seguridad se ha comprobado en pacientes embarazadas21, en quienes no solo se usan como hipolipemiantes, sino como depuradoras de medicamentos fetotóxicos como metotrexate y leflunomida22.
Teniendo en cuenta la información presentada, el grupo desarrollador de la «Guía Colombiana para la prevención, detección temprana, diagnóstico, tratamiento y seguimiento de la dislipidemia en pacientes colombianos mayores de 18 años»11, concluyó que la evidencia actual no apoya el uso de las RSAB como medicamentos de primera línea en el tratamiento de la dislipidemia, mientras que se propone su uso solamente cuando se han presentado efectos adversos serios que limiten la terapia con estatinas o cuando haya verdadera intolerancia a las mismas. Adicionalmente, son una alternativa interesante en mujeres embarazadas que requieran tratamiento.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónEste trabajo fue financiado por el Ministerio de la Protección Social y COLCIENCIAS.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.