¿Cuál es la situación actual técnica y productiva de los cuatro bancos que están certificados en buenas prácticas para tejido cardiovascular en Colombia si se comparan con estándares internacionales?
ObjetivoCaracterizar la capacidad técnica y la actividad de los bancos certificados del país para tejido cardiovascular durante el periodo de tiempo 2014 a 2016.
MetodologíaMediante una encuesta realizada por vía teleconferencia a cada banco, se evaluaron ítems de donación, extracción, procesamiento, almacenamiento, distribución y capacidad de producción de los tejidos cardiovasculares. La información referida por las instituciones fue complementada con actas de certificación de buenas prácticas del INVIMA y la suministrada por el INS de las estadísticas reportadas por los mismos bancos durante el periodo 2014 a 2016.
ResultadosEl tejido cardiovascular procesado por los bancos colombianos procede principalmente de donantes con muerte encefálica y es extraído directamente en el quirófano; la edad de los donantes va desde recién nacidos hasta los 60 años. Cuando se requiere, el antibiótico de elección es la vancomicina. El almacenamiento más usado es la criopreservación y su distribución se hace principalmente a grupos quirúrgicos preestablecidos e intrainstitucionales.
ConclusionesEl desarrollo del banqueo de este tipo de tejido está muy rezagado en Colombia respecto a otros países, debido a las dificultades de donación, extracción y utilización por grupos con alta experticia; adicionalmente, la normativa utilizada para evaluar estas instituciones está muy desactualizada.
A study is performed to determine if the current technical and productive situation of the four cardiovascular tissue banks that have Good Practice Certificates in Colombia compare with international standards.
ObjectiveTo determine the technical capacity and activity of the banks certified by the country for cardiovascular tissue during the period from 2014 to 2016.
MethodologyThe items analysed using a questionnaire completed by teleconference to each bank were, donation, extraction, processing, storage, distribution, and production capacity of the cardiovascular tissues. The information provided by the institutions was complemented with the Minutes of Good Practice Certification of the Colombia National Food and Drug Surveillance Institute (INVIMA) as well as the statistics reported by the banks themselves and provided by the National Health Institute (INS) during the period 2014 to 2016.
ResultsThe cardiovascular tissue processed by Colombian tissue banks mainly comes from donors with brain death, and is extracted directly in the operating theatre. The age of the donors go from newborn up to 60 years-old. When used, the antibiotic of choice is vancomycin. The most used storage method is cryopreservation, and is mainly distributed to established and institutional surgical groups.
ConclusionsThe development of this type of tissue bank is lagging behind in Colombia compared to other countries. This is due to the difficulties in donation, extraction, and use by groups with high expertise. Furthermore, the guidelines used to evaluate these institutions are very out of date.
El injerto cardiovascular es un tejido implicado en funciones vitales que tienen consideraciones especiales. El estado de asepsia es una de las condiciones sine qua non en este injerto, debido a que su contacto directo con componente hematopoyético en la fase postimplante, hace que las implicaciones de una falla tengan un riesgo alto que compromete la salud del receptor. Otra situación relevante, es la funcionalidad total que deben poseer las válvulas y vasos trasplantados, por ello el control de calidad que se realiza en las fases de procesamiento del tejido. Por último, su característica inmunológica hace que aún no sea un tejido perenne cuando es implantado en el cuerpo humano; no obstante, procesos específicos y el avance tecnológico puede hacer que esa situación cambie en los próximos años, de modo que la caracterización técnica del procesamiento se encuentra en constante evolución1.
La calidad de vida alcanzada por parte de los pacientes sujetos a trasplante de homoinjertos de válvulas cardiacas, en algunos casos es superior a la alcanzada con bioprótesis y prótesis mecánicas, sin contar que en niños la indicación de un injerto que pueda crecer junto con el corazón es absoluta y en este sentido los homoinjertos son los adecuados para prevenir reintervenciones frecuentes1.
Los homoinjertos valvulares cardiacos son el sustituto de elección en endocarditis valvulares aórticas, pacientes con contraindicación para la anticoagulación, reconstrucción del tracto de salida de ventrículo derecho, sustitución valvular aórtica en niños o adultos jóvenes (mediante la intervención de Ross) y sustitución valvular aórtica junto con la aorta ascendente, en pacientes con edad superior a 60 años. En homoinjertos con sustitutos arteriales se pueden beneficiar los pacientes con infección vascular, inmunodeprimidos o pacientes complejos cuya técnica durante la intervención puede requerir un homoinjerto2.
En las últimas décadas se ha precisado un aumento de procesamiento y demanda en la cantidad de tejido cardiovascular en el mundo, datos internacionales indican que la principal actividad de obtención y procesamiento se encuentra liderada por organizaciones de Norte América y Europa3. Actualmente, según la Organización nacional de trasplante, en España, con una población cercana a los 49 millones de habitantes, están autorizados 23 bancos de tejidos cardiovasculares, mientras que en Colombia solo existen cuatro bancos para una población de aproximadamente 50 millones de habitantes.
Sin desconocer la importancia del nuevo escenario normativo (Decreto 2493 de 2004, la Resolución 5108 de 2005 Manual de Buenas Prácticas para Bancos de Tejidos, y la Ley 1805 de 2016 referente a la donación), que derivó en cambio de las prácticas de obtención de órganos y tejidos en Colombia durante la última década, se requiere comenzar a evaluar todas las variables que puedan ser causa fáctica de la actividad actual del banqueo de tejido cardiovascular en nuestro país, por lo cual es necesario conocer las condiciones técnicas de los bancos colombianos, sus procesos, así como la actividad realizada y evidenciar en qué se diferencian de sus homólogos internacionales.
Por consiguiente, el objetivo de este trabajo es caracterizar la actividad de los bancos de tejidos certificados en Colombia en buenas prácticas para tejido cardiovascular, a través de la descripción de las principales características de operación de estas instituciones, el análisis de la información suministrada y la estimación de la capacidad productiva en forma grupal de los tejidos procesados por estos.
Materiales y métodosEstudio descriptivo de tipo trasversal de la muestra completa de bancos de tejidos cardiovascular, certificados en buenas prácticas en Colombia por parte del INVIMA a marzo de 2017, con evaluación de las estadísticas globales de actividad de 2014 hasta 2016.
Se diseñó una encuesta para evaluar las actividades de los bancos sobre donación, extracción, procesamiento, almacenamiento, distribución y capacidad de producción de los tejidos cardiovasculares, que actualmente se encuentran amparados por la regulación colombiana de buenas prácticas para bancos de tejidos humanos y médula ósea.
Las encuestas se hicieron vía teleconferencia a cada uno de los bancos de tejidos en forma individual y concertada previamente.
Adicionalmente, la información referida por las instituciones se complementó con datos de las últimas actas de certificación de buenas prácticas, que son encontradas en los expedientes del INVIMA e información completa suministrada durante los años 2014, 2015 y 2016 por el INS, de las estadísticas reportadas por los mismos bancos a las secretarías regionales correspondientes y que posteriormente son consolidadas por esta institución gubernamental.
La información recibida en las encuestas se codificó y se ingresó a una base de datos para ser analizada posteriormente.
Se hizo un análisis descriptivo y de frecuencias de los diferentes ítems evaluados; debido a la pequeña cantidad de establecimientos, en Colombia no se utilizan análisis complejos de la información cuantitativa. Se utilizó la hoja de cálculo de Microsoft Excel 2010 con sus complementos para el análisis de la información.
ResultadosDesde 2014 hasta 2016 fueron reconocidos por todos los bancos de tejidos del país y por otras instituciones coadyuvantes un total de 5.561 donantes potenciales, cifra que, que después de ser sometidos a evaluación, se redujo a 126 donantes efectivos para tejido cardiovascular (en promedio 42 por año) que corresponden al 2,3% de los evaluados. De estos donantes se obtuvieron 247 tejidos (en promedio 82 tejidos por año; 2 tejidos por donante efectivo durante el periodo) entre válvulas cardiacas, pericardio y vasos sanguíneos. Finalmente, se distribuyeron 165 tejidos en los tres años (en promedio 55 tejidos por año).
En promedio, por donante se obtuvieron 5.2 tejidos, lo que, en concreto, se da principalmente debido a la extracción de vasos sanguíneos más que de válvulas cardiacas.
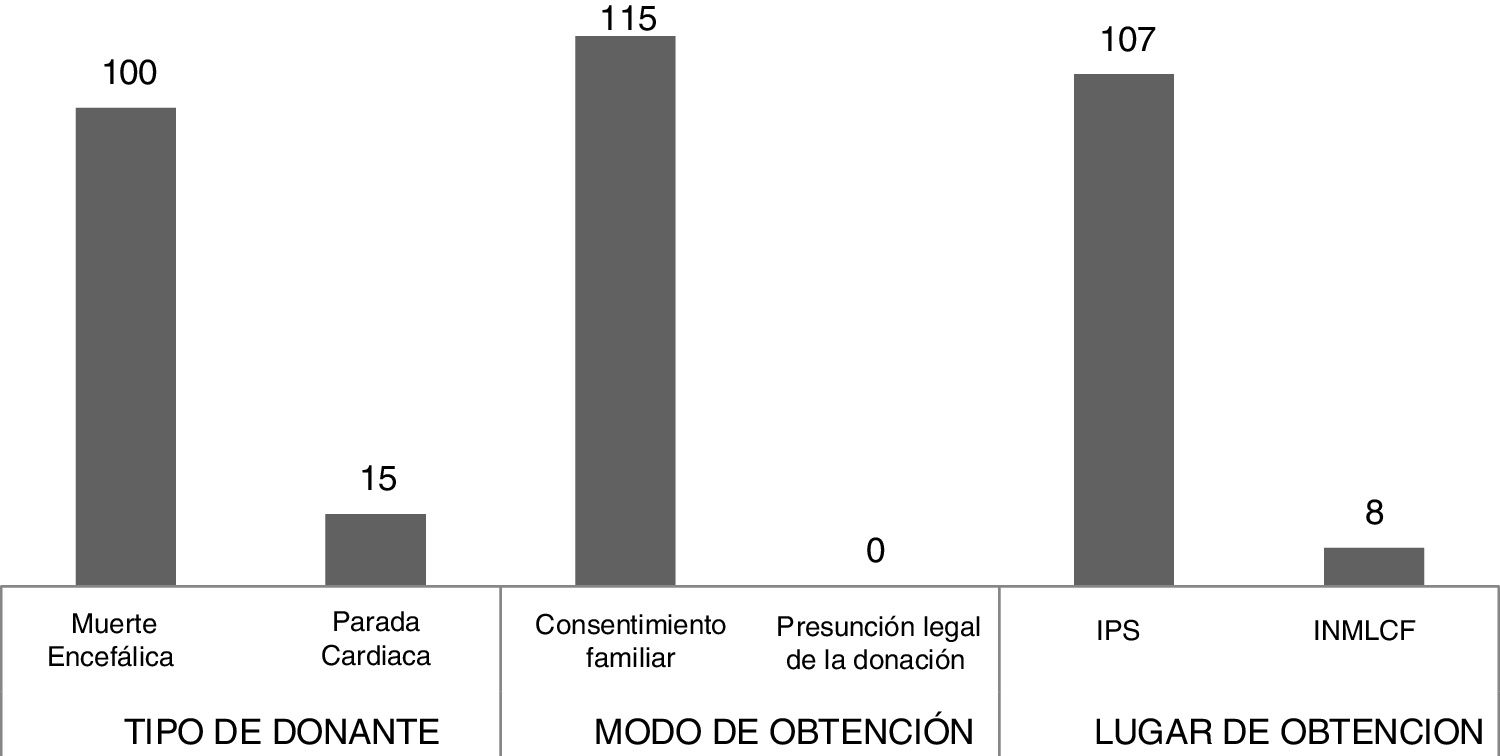
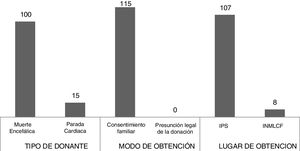
DonaciónLas cuatro fundaciones captan el tejido de donantes procedentes de muerte encefálica. Adicionalmente, una de ellas al mismo tiempo puede hacerlo de donantes vivos que van a ser intervenidos para trasplante cardiaco (corazón dominó) y otra lo realiza con pacientes en paro cardiorrespiratorio. (figuras 1 y 2)
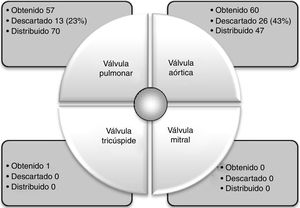
Ruta crítica del tejido cardiovascular 2014-2016 en Colombia
Lo tejidos cardiacos distribuidos no necesariamente son los mismos que se extrajeron y procesaron, debido a los amplios periodos de almacenamiento que estos presentan en criopreservación. Se descartaron 52 tejidos, por lo que se almacenaron para distribución 195 durante este periodo.
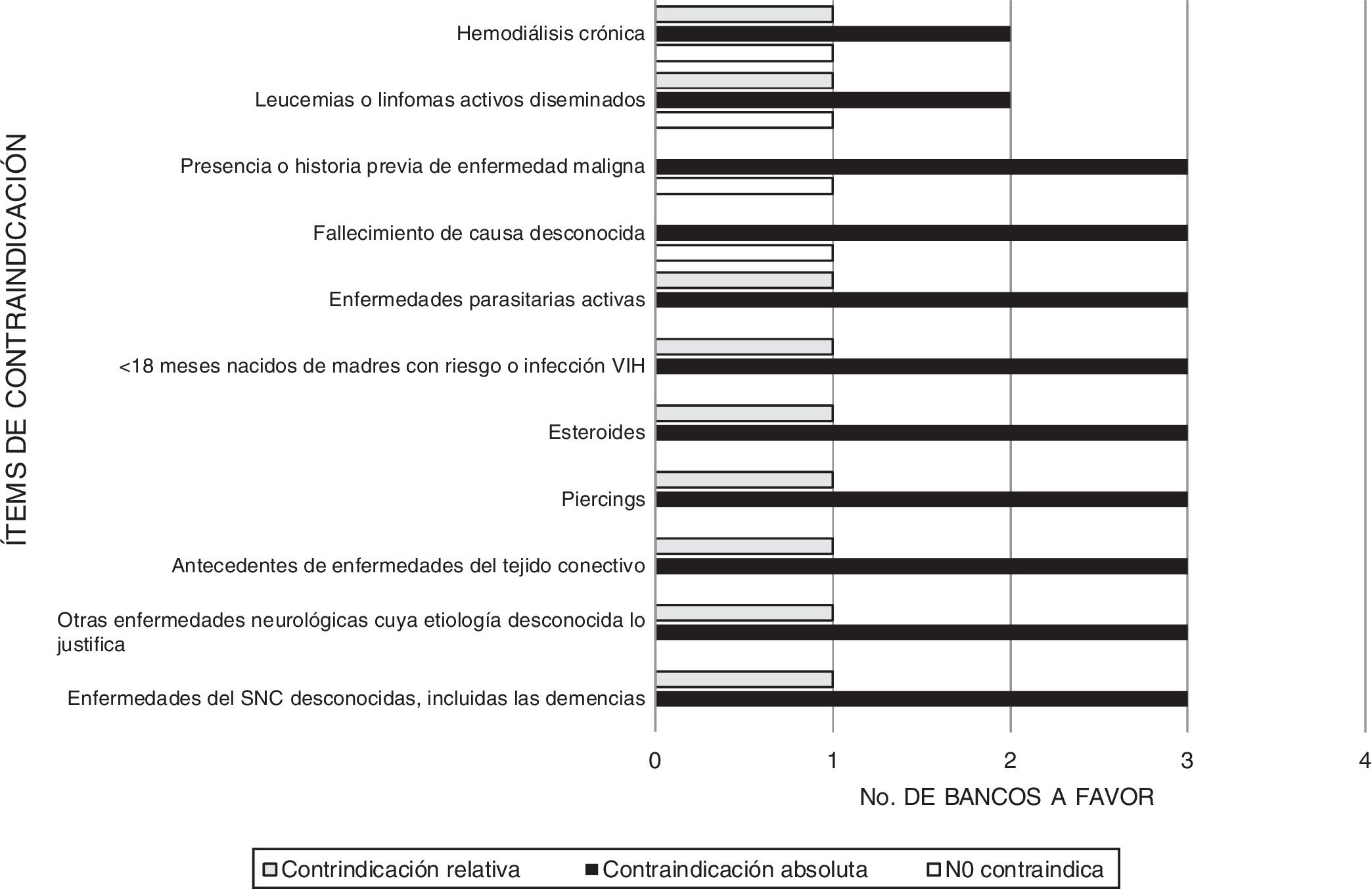
Coincide el hecho de contraindicar absolutamente la donación de tejido cardiovascular en personas con antecedentes de enfermedades infecciosas del sistema nervioso central, septicemia activa, evidencia sugerente de infección por VIH o sífilis, evidencia de infección por VHB, VHC o hepatitis viral activa, endocarditis bacteriana o fúngica activa, prácticas de riesgo, tratamientos prolongados con esteroides o sustancias de toxicidad conocida, historia de enfermedades autoinmunes, irradiación previa de la zona del tejido a extraer e imposibilidad de realizar estudio serológico.
En la figura 3 se halla la relación de contraindicaciones en que no hay coincidencia, referida por los bancos. Otras contraindicaciones importantes que no fueron evaluadas por la encuesta, pero que los Bancos consideran importantes son:
- •
Más de 5 días en UCI con monitorización intensiva
- •
Donante con peso menor a 2,7kg.
- •
Fiebre en las últimas 24 horas.
- •
Herida cardíaca no documentada.
- •
Fiebre reumática y otras enfermedades valvulares del corazón.
- •
Trauma de tórax, particularmente trauma penetrante (incluyendo inyección intracardiaca).
- •
Cirugía cardíaca previa de la válvula.
- •
Hipertensión.
- •
Miocarditis.
- •
Mayores de 40 años en cirugía por ateromatosis.
- •
Malaria de importancia en vigilancia salud pública.
- •
Receptores de hormonas derivadas de la pituitaria y receptores de duramadre.
- •
Antecedente de viruela.
- •
Enfermedades infecciosas cardiacas en donación de válvulas y
- •
Cirugías cardiacas previas.
El límite superior de edad en el que se contraindica la donación por los bancos colombianos, está entre los 30 y 60 años. A su vez, el límite inferior de donación lo consideran desde recién nacido hasta los 4 años (fig. 4).
Las pruebas infecciosas realizadas a los donantes son: grupo sanguíneo, Rh, sífilis, Anti-VHC, HBsAg, Anti-HBc, HTLV 1 y 2, VIH 1 y 2, Chagas y anticuerpos CMV. Adicionalmente, dos instituciones realizan examen de toxoplasmosis y Epstein-Barr por considerarlas necesarias por su nexo epidemiológico en las regiones en donde son captados los donantes. No se refirieron pruebas de ácidos nucleicos en ninguno de los bancos (NAT).
ExtracciónTodas las instituciones pueden obtener sus tejidos en el quirófano; solamente en un caso se tiene adicionalmente validada la extracción en una unidad forense. En cuanto al personal que realiza la extracción, usualmente el cirujano cardiovascular es el encargado; éste puede estar asociado a un grupo quirúrgico que efectuá el procedimiento rutinariamente y en otros es contactado previo a la intervención.
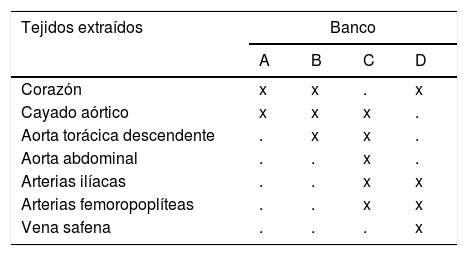
ProcesamientoLas instalaciones de los bancos (áreas para el procesamiento de los tejidos), tienen calificaciones de ambientes para recuentos de partículas ISO 5 o ISO 7; adicionalmente, se utilizan cámaras de flujo laminar y biológicas con diferentes calificaciones técnicas (tablas 1 y 2).
Coctel de antibióticos usados para desinfección del tejido cardiovascular por los cuatro bancos de tejidos
| Tejidos extraídos | Banco | |||
|---|---|---|---|---|
| A | B | C | D | |
| Corazón | x | x | . | x |
| Cayado aórtico | x | x | x | . |
| Aorta torácica descendente | . | x | x | . |
| Aorta abdominal | . | . | x | . |
| Arterias ilíacas | . | . | x | x |
| Arterias femoropoplíteas | . | . | x | x |
| Vena safena | . | . | . | x |
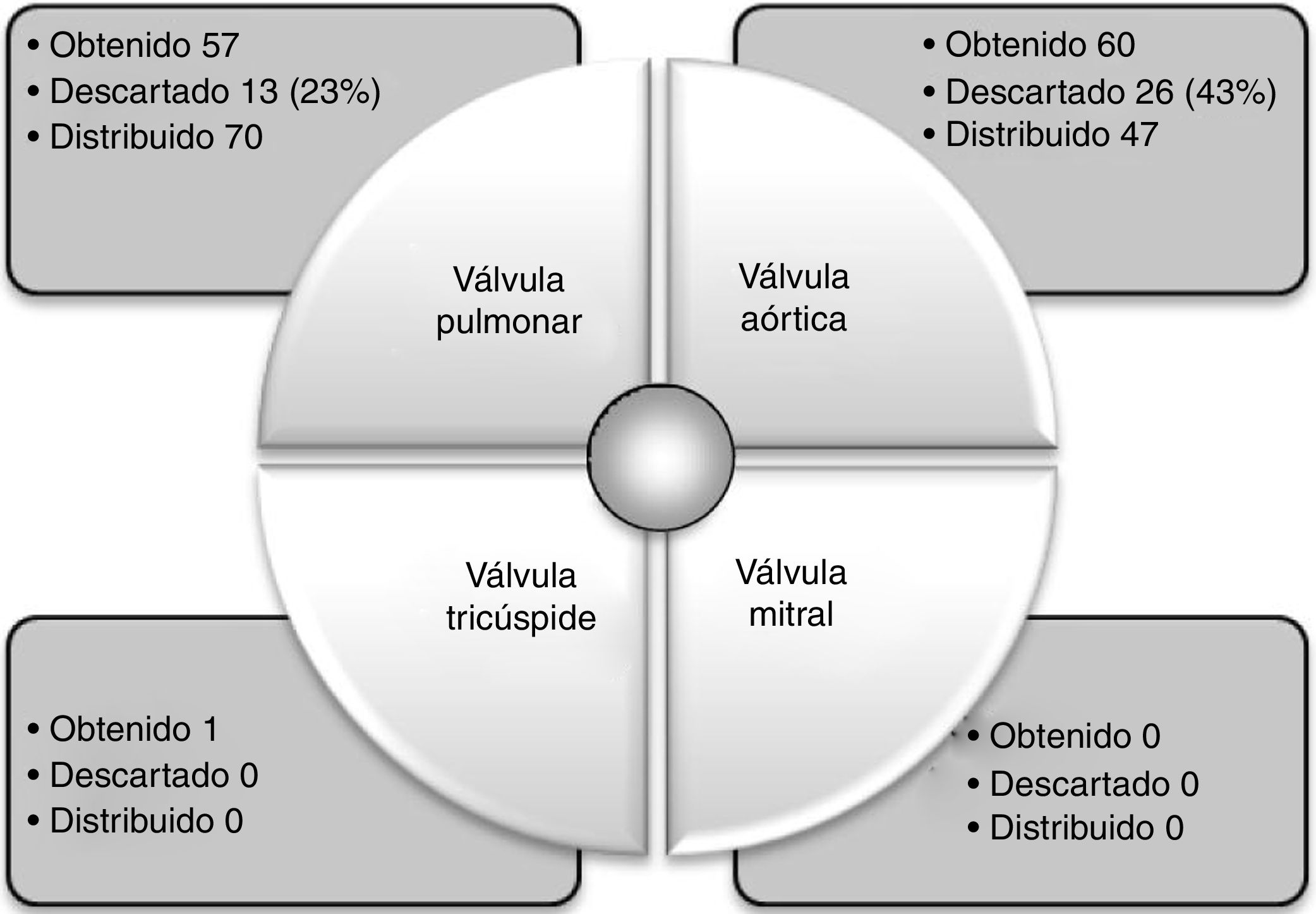
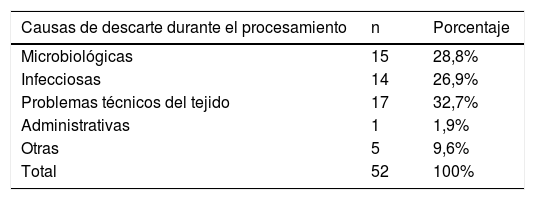
Al discriminar los motivos del descarte de 2014 a 2016 (tabla 3), se observa que los tejidos que fueron rechazados por estas causas fueron válvulas aórticas en un 50%, seguidas de válvulas pulmonares en un 25% y de vasos sanguíneos y pericardio con 25%.
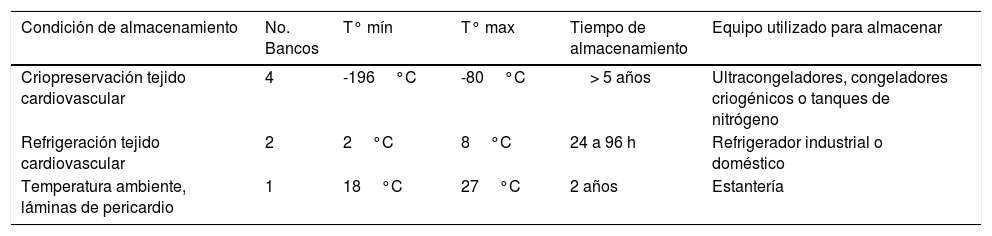
AlmacenamientoLa relación de las condiciones de almacenamiento encontradas en los bancos colombianos se resume en la tabla 4. En relación con el pericardio, este se procesa con formaldehído y se almacena a temperatura ambiente durante máximo dos años.
Condiciones de almacenamiento referidas por los bancos de tejido osteomuscular en la encuesta
| Condición de almacenamiento | No. Bancos | T° mín | T° max | Tiempo de almacenamiento | Equipo utilizado para almacenar |
|---|---|---|---|---|---|
| Criopreservación tejido cardiovascular | 4 | -196°C | -80°C | > 5 años | Ultracongeladores, congeladores criogénicos o tanques de nitrógeno |
| Refrigeración tejido cardiovascular | 2 | 2°C | 8°C | 24 a 96 h | Refrigerador industrial o doméstico |
| Temperatura ambiente, láminas de pericardio | 1 | 18°C | 27°C | 2 años | Estantería |
La indicación de cirugía que utiliza este tipo de componentes anatómicos siempre es electiva; sin embargo, en ocasiones al realizar la evaluación intraquirúrgica del insumo valvular, se puede decidir por una nueva, la cual debe conseguirse con urgencia.
Tres bancos tienen distribución intrainstitucional debido a los trabajos conjuntos con grupos quirúrgicos preestablecidos.
En el primer trimestre de 2017 se reportaron 31 parches de pericardio almacenado. En este sentido solo dos instituciones las producen en la actualidad y no procesan el resto de tejido cardiovascular. En el momento de la encuesta se tenían 4 válvulas en criopreservación.
Las principales indicaciones de los tejidos distribuidos referidas por los bancos fueron:
- •
Cardiopatía congénita (ej., atresia valvular).
- •
Infecciones de válvula nativa.
- •
Prótesis valvulares preimplantadas que se infectaron o dañaron.
- •
Parafugas valvulares.
- •
Isquemias de miembros inferiores.
- •
Pie diabético sin vaso donante para uso autólogo.
En los últimos tres años, las válvulas pulmonares fueron las más suministradas con un 42%, la aórtica en un 28%, las láminas de pericardio en un 21% y los vasos sanguíneos con un 8% del total distribuido.
Finalmente, en relación con la biovigilancia, se indica que se realiza seguimiento en la mayoría de receptores en distintos tiempos desde el trasplante, lo que usualmente es coordinado con los bancos de tejidos, pero no se ha generado ningún reporte de incidente hasta el momento.
DiscusiónLa producción de tejido cardiovascular en Colombia es mínima comparada con otros países. Para evidenciar el panorama colombiano frente a este contexto, en España se tiene registro anual de procesamiento de válvulas cardiacas cercano a las 3003, comparado con las casi 40 válvulas, en promedio anual, que se produjeron en Colombia durante el periodo de tiempo evaluado.
El promedio de descarte también tiene una diferencia evidente; el porcentaje de este en España es aproximadamente del 25% por cuestiones de calidad. La principal estructura descartada es la válvula pulmonar, y la mayoría de veces se debe a problemas en la disección (morfológicos y anatómicos) y a la contaminación durante el procesamiento3. En el ambiente local este porcentaje es mayor al 33% para válvulas cardiacas y en todo el tejido cardiovascular del 21%; sin embargo, las causas son las mismas.
Una condición particular que se presenta en el mundo, pero en Colombia no es usual, es el hecho de la procedencia de los homoinjertos vasculares de donantes vivos, es decir los denominados “corazones dominó” (pacientes que van a un transplante cardiaco y donan el órgano reemplazado), que representan el 60% de los donantes en los Estados Unidos, el 40% en Europa2 y el 3,6% en Brasil4. En Colombia sólo uno de los cuatro bancos refirió que tiene esta opción de obtención y según los datos recopilados no se tiene reporte de que se haya realizado en el periodo evaluado.
En contraste con lo anterior, en Colombia los donantes con muerte encefálica representaron el 86,9% de los donantes totales durante el periodo 2014-2016, comparándolos con Brasil, en donde representa aproximadamente un 92,3%4,5. En donación de vasos sanguíneos la principal fuente es Europa (95%)6, no así en válvulas cardiacas, en la cual y como en el resto del mundo los donantes que proceden de paro cardiovascular, son la principal fuente de homoinjertos cardiovasculares4,5.
La posible razón de no preferir captar en personas fallecidas es que con las disposiciones legales colombianas para custodia de elementos probatorios y de las indicaciones para la obtención de componentes anatómicos para fines de trasplantes (Decreto 0786 de 1990), es muy complicado lograr un donante cadavérico adecuado, porque al aumentar las horas desde el rescate, se incrementa el riesgo de contaminación. Adicional a esto, con la nueva Ley 1805 de 2016, en la cual los potenciales donantes deben ser evaluados para encontrar si esa persona durante su vida ha ejercido el derecho a oponerse a la donación, en muchas oportunidades el banco enfrentado a esta búsqueda de información, que repercute en demora y gasto de tiempo, opta por no querer extraer de este tipo de fuente.
En consecuencia, el riesgo de infección siempre es más alto en los donantes cadavéricos que en el resto de las posibles fuentes, hecho que fue evidenciado en un banco de Singapur con un 50% de contaminación posextracción, respecto a los donantes multiórganos (37,5%) y a los trasplantados en cirugía (12,5%)7.
Al ser tan importante la condición de asepsia de los tejidos cardiovasculares, algunos bancos internacionales realizan múltiples evaluaciones de la esterilidad valvular en varios de los estadios del proceso (prelavado, lavado con soluciones estériles, solución de desinfección en diferentes tiempos)4. En los bancos colombianos, la segunda proporción más elevada de descarte durante el periodo se debió precisamente a análisis microbiológico alterado.
De otra parte, no se tiene registro de los gérmenes encontrados en los reportes colombianos, pero para hacerse a una idea de la gran variedad de estos, en trabajos publicados, los gérmenes gramnegativos más comúnmente aislados en un banco de la India fueron Klebsiella, enterobacterias y Aeromonas, y en cuanto a los grampositivos los enterococos, especies de Candida y Aspergillus8, En un estudio similar de Brasil se encontraron con más frecuencia cepas de Staphylococcus sp, Serratia sp y Escherichia coli4 pudiendo descontaminar el tejido en dos terceras partes posteriormente con cocteles de antibióticos. En Singapur los Staphylococcus coagulasa positivo fueron los mayormente aislados junto con los Propionibacterium acnes y Candida sp., gérmenes que se lograron descontaminar casi en su totalidad luego del tratamiento antibiótico7.
Debido a esta gran variabilidad de gérmenes, por lo general, la descontaminación se realiza con un coctel previamente validado según los microorganismos y el diagnóstico epidemiológico local, con el objetivo de eliminar bacterias aerobias, anaerobias y hongos; usualmente contiene antibiótico y antifúngico (ej.: estreptomicina, cefotaxime, anfotericina B) a 4°C durante 24h. Existe también referenciación de incubación a 37°C con buena efectividad de descontaminación posterior2,9. La validación periódica, es por lo tanto, una actividad importante para evidenciar cambios en la sensibilidad de los gérmenes locales, sin encontrar un coctel de antibióticos estándar para un Banco, estos por lo tanto deberán variar según los cambios de la microflora que sean encontrados en los tejidos censados periódicamente.
Para evitar el hecho de que se aumente la toxicidad del tejido al descontaminarlo con concentraciones de antibióticos cada vez mayores o de grupos especiales, se ha optado por no aplicar antifúngicos en algunos protocolos6, o no suministrar antibióticos que puedan dañar las fibras de colágeno del injerto10. En Colombia se utilizan, según los datos obtenidos, cocteles que pueden contener polimixina B, sin embargo, equiparar la microflora local en los bancos colombianos con la internacional no sería posible, como ya se mencionó.
Estas condiciones de contaminación generaron en Colombia la segunda causa de descarte, sin embargo es de resaltar que contrario a lo que se pensaría, cuando en alguna institución se mejoran los procesos y la tecnología, se rechazan más tejidos debido al aumento de los controles y exigencias de calidad del tejido cardiovascular. Comparado con el 33% de descarte de válvulas en Colombia, en un banco brasileño fue del 27%4, mientras en uno Belga descartaron el 41% de las válvulas6.
El otro motivo principal de descarte en Colombia es el de la calidad mecánica y funcional de las válvulas, lo cual dependerá de las características del donante. Cuando se realizan pruebas de función a las válvulas7,11, durante el procesamiento, el tejido se descarta por tener alteraciones morfológicas, depósitos de calcio y ateromas8. La edad madura del donante y las enfermedades crónicas concomitantes serán por lo tanto y según las necesidades de tejido locales, características variables en los criterios de cada banco.
Otro caso particular que redundaría en la calidad del tejido, son los límites de edad para donar. Se debe tener en cuenta que a más edad, mayor probabilidad de rechazo del tejido por alteraciones estructurales, siendo esto más crítico en la válvula aórtica cuando el donante está por encima de los 50 años4; sin embargo este aspecto dependerá de las condiciones de salud locales, por lo que la comparación de Colombia con otros países no sería posible.
El almacenamiento del tejido cardiovascular se realiza en Colombia, principalmente con la técnica de criopreservación. Se ha cuestionado si la viabilidad del endotelio valvular y los fibroblastos originales del donador, son conservados adecuadamente con esta técnica. La importancia radica en que existen estudios que en teoría explican que entre mayor viabilidad de estas células, mayor durabilidad pos implante, aunado a la preservación de la matriz de colágeno, factor clave en la sobrevida del injerto12. En los vasos sanguíneos, la criopreservación reduce la falla del injerto (rompimiento, aneurisma, infección, etc.) y mantiene una reserva constante para disposición en cirugías de urgencia6.
Se han llevado a cabo estudios de preservación por más de 5 años en nitrógeno líquido, en los que se observa adecuada viabilidad celular y mínimo daño estructural13, sin embargo, las curvas de supervivencia del homoinjerto se aproximan al final de la segunda década2, lo cual está más que acorde con los 5 años promedio de preservación que refieren los bancos colombianos.
Actualmente, se emplean técnicas de descelularización de los homoinjertos y están siendo promovidas para mejorar el pronóstico de sobrevida de estas válvulas cardiacas y los injertos vasculares, pues existe evidencia de que pueden generar una respuesta inmunitaria en el receptor14, por lo que no necesita tomarse el apareamiento HLA e incluso está siendo revalidado el uso de medios de preservación y replicación celular, en el procesamiento de estos tejidos15–20.
Adicionalmente, debido al delicado proceso de descongelamiento en la criopreservación, es recomendable que el trasporte corra por cuenta de personal calificado. Es así que la tendencia tanto mundial como local, es formar grupos quirúrgicos, hecho que ocasionará menor probabilidad de fallas y el descarte del ya poco tejido existente.
Finalmente, en Colombia no pareciera ser utilizado este tejido de forma amplia, pudiera ser por la facilidad de manejo de bioprótesis del mercado, por desconocimiento de las ventajas o por falta de grupos de cirugía que estén entrenados de manera adecuada en los procedimientos requeridos para estos injertos en todas las regiones del país (los bancos están ubicados en Medellín y Bucaramanga).
ConclusionesLos bancos de tejido cardiovascular colombianos tienen problemas en cuanto a la donación; es una carga muy alta de infraestructura, personal y tiempo para la consecución de apenas una fracción de tejidos. Aunque el donante de muerte encefálica es el más idóneo, la tendencia mundial muestra que el paciente de paro cardiorrespiratorio, manejado de forma correcta para evitar la contaminación, es una alternativa más costoefectiva dentro de las demás opciones.
Al continuar con algunos de los actuales requerimientos normativos, se estaría complicando y desalentando el banqueo de tejidos en nuestro país, desconociendo los avances científicos realizados en la última década.
En cuanto a las condiciones técnicas de los bancos de tejidos cardiovascular, la mayoría de ellas son equiparables a los estándares internacionales, sin embargo, el uso de pruebas de ácidos nucleicos (NAT) ya es obligatoria en otros países, pero en Colombia la norma no lo indica y los costos acarreados para los bancos serían altos.
Se debería continuar con este ejercicio periódicamente en otros trabajos similares, para evaluar la evolución de los bancos de tejidos en Colombia, con reportes discriminados de causas de rechazo de donantes, descarte de tejido procesado y reportes postimplante a fin de evaluar alternativas técnicas que aumenten la donación de tejido, disminuyan el descarte de tejido procesado y consideren cambios en las metodologías regionales de procesamiento para disminuir el riesgo inherente del producto.
Responsabilidades éticasLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales. No se indica información susceptible de confidencialidad en el presente trabajo. Adicionalmente, tampoco se requiere consentimiento informado, por cuanto no se utilizaron pacientes.
FinanciaciónINVIMA participó en la decisión de enviar el artículo para su publicación y los gastos propios de la contratación de los autores.
Conflictos de interésNinguno.