el modelo Seis Sigma es una herramienta de gestión de la calidad que se basa en la medida de la variabilidad de un proceso, en términos de desviación típica o de fallos por millón. Implica haber definido previamente una especificación de la calidad para el proceso que se investiga.
Material y métodoeste trabajo estudia los datos obtenidos en los programas de garantía externa de la calidad de la Sociedad Española de Bioquímica Clínica y Patología Molecular (SEQC), con el propósito de deducir consecuencias prácticas que aseguren el diagnóstico y el seguimiento correctos del paciente, mediante el informe aportado por el laboratorio. Se incluyen magnitudes biológicas con especificaciones de la calidad definidas para situaciones clínicas concretas (colesterol, glucosa, glucohemoglobina y antígeno prostático específico total) y con valores de variación biológica bajos (ión sodio, albúmina), intermedios (colesterol, creatinina, glucosa) y altos (hierro, triglicéridos). El valor sigma se calcula mediante el cociente entre el límite de tolerancia establecido y la variabilidad del proceso.
Resultadoslos valores sigma obtenidos son adecuados (⩾3) si se toman especificaciones muy permisivas, mientras que no lo son cuando se desea cumplir la especificación derivada de la variación biológica. Ello indica que los instrumentos y métodos analíticos disponibles en nuestro mercado requieren un procedimiento de control de la calidad muy cuidadoso (procesamiento de varias muestras control, necesidad de realizar repeticiones, etc.).
Conclusionesen ningún caso se debe confundir el objetivo de alcanzar la calidad necesaria para el adecuado uso clínico del informe analítico con el de conseguir un laboratorio industrialmente productivo; ambos forman parte del concepto de calidad total.
The Six Sigma model is a management tool based on measuring process variability, in terms of standard deviation or defects per million. It involves defining the specifications of the quality desired for the process investigated.
Material and methodThis work uses data obtained by the laboratories participating in the external surveys organized by the Spanish Society of Clinical Biochemistry and Molecular Pathology (SEQC), with the aim of promoting practical recommendations for assuring satisfactory patient diagnosis or monitoring through the laboratory report. The analytes included have quality specifications defined for specific clinical situations (cholesterol, glucose, HbA1C, total PSA) and have narrow (albumin, sodium), medium (cholesterol, creatinine, glucose) and wide (iron, triglyceride) biological variations. Results from control materials with the relevant concentrations to make clinical decisions have been used in this study. Sigma matrix is calculated from the ratio between quality specification and process coefficient of variation.
ResultsResults obtained show that sigma values are good (⩾3) when using permissive quality specifications, whereas they are poor if quality specifications are derived from biological variation. This finding indicates that instruments and methods available in our field require a strict quality control procedure (several control samples per run, repeated tests, etc.).
ConclusionsThe objective of obtaining the quality required for adequate clinical use, must not be confused with that of achieving an economically productive laboratory; both are part of the concept of total quality management.
El modelo Seis Sigma es una herramienta de gestión de la calidad que introduce el concepto «mejora» en el clásico ciclo de Deming PDCA (plan, do, check, act) para gestionar un proceso. Se basa en la medida de la variabilidad de un proceso, en términos de desviación típica o de fallos (defectos) por millón.
Implica haber definido previamente una especificación de la calidad, también denominado límite de tolerancia, límite de aceptabilidad o requisito de la calidad, para el proceso que se investiga. Éste, en el proceso analítico del laboratorio clínico, puede estar basado en cualquiera de los criterios aceptados en el acuerdo de Estocolmo, 19991.
El valor Seis Sigma ideal implica que la variabilidad de un proceso debe caber 6 veces dentro del límite aceptable preestablecido, para considerar que el proceso funciona perfectamente. Un valor sigma de 3 es considerado como indicativo de calidad mínima aceptable para un producto o proceso2.
El valor sigma permite comparar la calidad de procesos muy dispares, por ejemplo, la seguridad de una línea aérea, la seguridad de un neumático, la pérdida de equipajes en un aeropuerto, la variabilidad de resultados entre laboratorios usuarios de un mismo método e instrumento, etc. Los valores sigma ideales para estos ejemplos son 6, 5, 4 y 3, respectivamente2. Gras y Philippe3 realizaron una revisión muy completa sobre la aplicación del modelo Seis Sigma en el laboratorio clínico.
Con el objeto de determinar el valor sigma de las prestaciones analíticas en nuestro país, este trabajo estudia los datos obtenidos en los programas de garantía externa de la calidad de la Sociedad Española de Bioquímica Clínica y Patología Molecular (SEQC). El propósito final es deducir consecuencias prácticas que aseguren el diagnóstico y el seguimiento correctos del paciente, mediante el informe aportado por el laboratorio.
Material y métodoSe utilizan los datos obtenidos en el programa de garantía externa de la calidad de la SEQC de bioquímica en suero, del año 20064.
Las magnitudes estudiadas son: albúmina, antígeno prostático específico (PSA) total, colesterol, creatinina, glucosa, glucohemoglobina (HbA1C), hierro, ión potasio, ión sodio y triglicérido. Para cada magnitud se han tomado los resultados obtenidos para los lotes control de concentración próxima a los valores de decisión clínica. Estos datos se encuentran disponibles para los usuarios del programa en la página web (http://www.contcal.org/k3/).
El valor sigma se calcula mediante el cociente entre el límite de tolerancia establecido y la variabilidad del proceso. Sobre la base de los resultados obtenidos en los programas de garantía externa de la calidad, se calculan los siguientes parámetros:
- –
Calidad global de una prueba (CG), que tiene en cuenta la variabilidad de los resultados obtenidos por todos los laboratorios para una prueba (p. ej., determinación de glucosa en sangre).
- –
Calidad de un instrumento (CI), que es consecuencia de la variabilidad de los resultados producidos por los usuarios de un mismo instrumento y método analítico.
Se define la especificación de la calidad para el error total (ETT) como la desviación de una determinación única de un material control respecto al valor teórico de dicho material5. Para ello se utilizan cuatro de los criterios aceptados internacionalmente en Estocolmo1 que, en orden decreciente en cuanto a utilidad médica, son:
- –
Satisfacción de las necesidades médicas en una situación clínica concreta.
- –
Variabilidad biológica.
- –
Criterios de expertos y encuestas a especialistas.
- –
Especificación mínima consensuada entre las sociedades científicas españolas SEQC, AEFA y AEBM6.
Las fórmulas utilizadas para calcular los dos parámetros mencionados son:
donde CVglobal es el coeficiente de variación obtenido con los resultados de todos los participantes para una magnitud concreta, y CVinstrumento, el coeficiente de variación obtenido con los resultados de los laboratorios que emplean el mismo instrumento.ResultadosPara cada magnitud estudiada se han revisado datos de hasta 870 laboratorios, con 12 valores anuales cada uno, por lo que se ha trabajado con un total de 10.440 resultados.
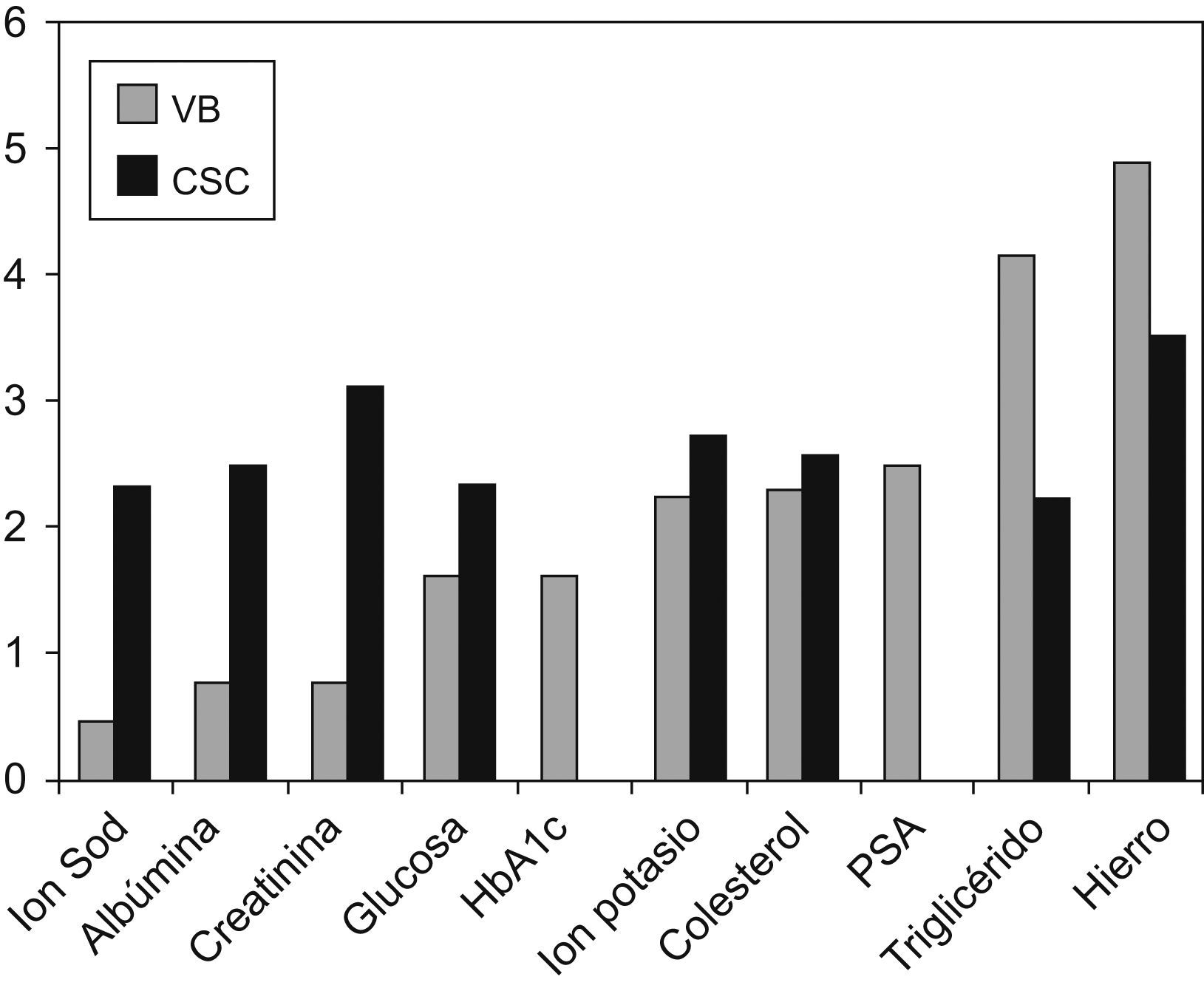
En la figura 1 se muestran los valores sigma indicativos de la calidad global de las magnitudes incluidas en este estudio, calculados teniendo en cuenta las especificaciones derivadas de la variación biológica (VB) y del Consenso de Sociedades Científicas (CSC) y en orden creciente respecto al valor derivado de la variación biológica. El valor sigma calculado con las especificaciones de consenso es bastante uniforme entre las diversas magnitudes estudiadas (de 2,2 a 3,5). En cambio, cuando la especificación se basa en la variación biológica, el valor sigma varía más (entre 0,4 y 4,9), y es menor para las magnitudes con fuerte regulación homeostática (ión sodio, albúmina y creatinina).
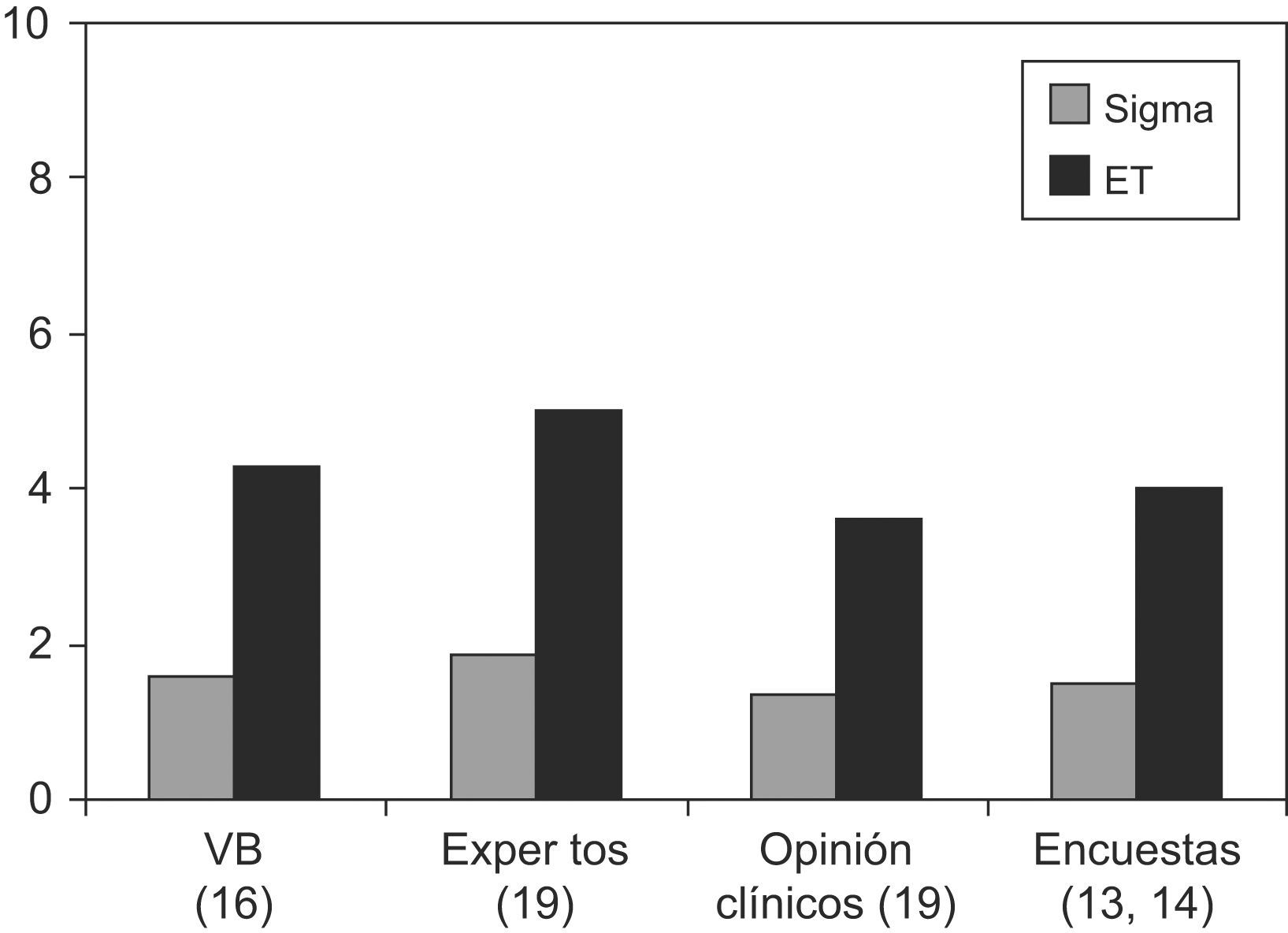
En la figura 2 se muestra el error total tolerable según los cuatro tipos de especificaciones de la calidad descritos en el apartado «Material y método», para la determinación de HbA1C, así como los valores sigma resultantes. En todos los casos el valor sigma es<3.
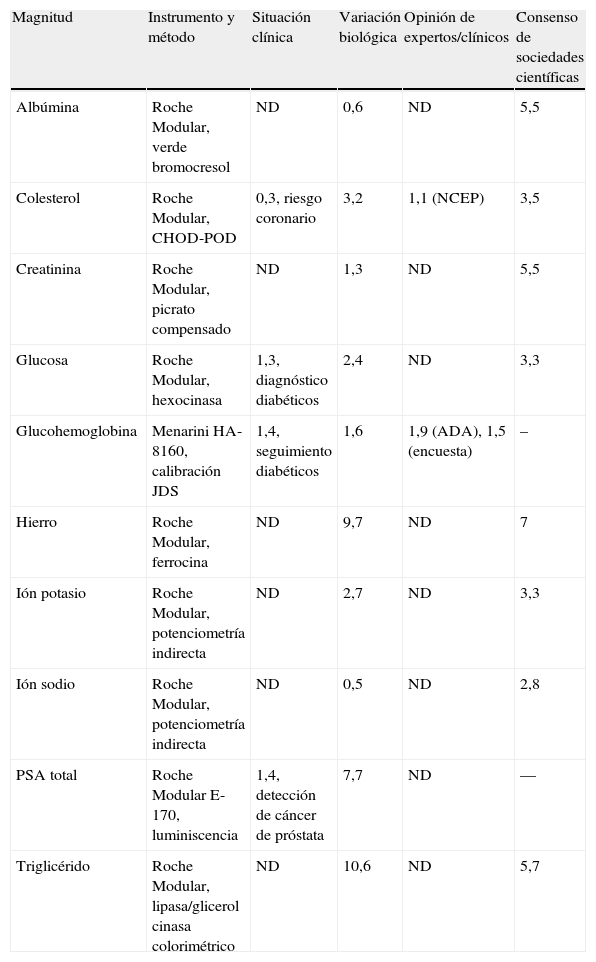
En la tabla 1 se muestran los valores sigma obtenidos con el instrumento más utilizado en los programas de garantía externa examinados, calculados sobre la base de los cuatro tipos de especificaciones mencionados anteriormente. Para las magnitudes estudiadas, todos los valores sigma son >3 (excepto ión sodio, con muy fuerte regulación homeostática) si se consideran las especificaciones mínimas consensuadas entre sociedades científicas. Por el contrario, sólo lo son en algunos casos en que se definen a partir de la variación biológica, y en ningún caso cuando se hace a partir de las opiniones de expertos o de los clínicos.
Valores sigma obtenidos con el instrumento más utilizado sobre la base de especificaciones mínimas o deseables
| Magnitud | Instrumento y método | Situación clínica | Variación biológica | Opinión de expertos/clínicos | Consenso de sociedades científicas |
| Albúmina | Roche Modular, verde bromocresol | ND | 0,6 | ND | 5,5 |
| Colesterol | Roche Modular, CHOD-POD | 0,3, riesgo coronario | 3,2 | 1,1 (NCEP) | 3,5 |
| Creatinina | Roche Modular, picrato compensado | ND | 1,3 | ND | 5,5 |
| Glucosa | Roche Modular, hexocinasa | 1,3, diagnóstico diabéticos | 2,4 | ND | 3,3 |
| Glucohemoglobina | Menarini HA-8160, calibración JDS | 1,4, seguimiento diabéticos | 1,6 | 1,9 (ADA), 1,5 (encuesta) | – |
| Hierro | Roche Modular, ferrocina | ND | 9,7 | ND | 7 |
| Ión potasio | Roche Modular, potenciometría indirecta | ND | 2,7 | ND | 3,3 |
| Ión sodio | Roche Modular, potenciometría indirecta | ND | 0,5 | ND | 2,8 |
| PSA total | Roche Modular E-170, luminiscencia | 1,4, detección de cáncer de próstata | 7,7 | ND | — |
| Triglicérido | Roche Modular, lipasa/glicerol cinasa colorimétrico | ND | 10,6 | ND | 5,7 |
ND: no disponible; PSA: antígeno prostático específico.
Las magnitudes biológicas incluidas en el estudio cumplen alguna de las siguientes condiciones: tener especificaciones de la calidad definidas para situaciones clínicas concretas (colesterol, glucosa, HbA1C y PSA total), así como valores de variación biológica bajos (ión sodio, albúmina), intermedios (colesterol, creatinina, glucosa) y altos (hierro, triglicéridos).
Para cada magnitud evaluada se eligieron los resultados del control de concentración relevante para tomar decisiones clínicas. Éstas son: albúmina para decidir tratamiento con nutrición parenteral7, colesterol para determinar el riesgo de enfermedad coronaria8, creatinina como expresión del filtrado glomerular alterado9,10, glucosa para el diagnóstico de la diabetes mellitus11; para HbA1C, hierro, ión potasio, ión sodio, triglicéridos y PSA total se tomaron los valores correspondientes al límite superior del intervalo de referencia poblacional.
El valor sigma resultante depende de la especificación de la calidad predeterminada. Si se toman especificaciones muy permisivas, como las consensuadas entre sociedades científicas españolas6, el valor sigma obtenido para la mayoría de las magnitudes estudiadas es aceptable. Por ejemplo, para creatinina el valor sigma del instrumento más utilizado (Roche Modular) es de 5,5 (aceptable) frente a la especificación mínima consensuada por sociedades científicas españolas, mientras que es de 1,3 (inaceptable) si se calcula frente a la especificación derivada de la variación biológica.
Las especificaciones consenso (SEQC/AEFA/AEBM) delimitan la calidad mínima, por debajo de la cual una prestación no se puede considerar profesionalmente aceptable6. El valor sigma uniforme obtenido en las magnitudes estudiadas es consecuencia del razonamiento utilizado para definir el consenso, que se basa en la prestación obtenida por el 95% de los 1.806 laboratorios participantes en los programas de garantía externa de la calidad organizados por estas sociedades, una vez excluidos los valores extremos.
Si se asume que un laboratorio alcanza las especificaciones de la calidad basadas en las necesidades médicas para resolver situaciones clínicas concretas, el valor sigma obtenido es en general ⩽3. Ejemplos para situaciones clínicas específicas son:
- –
En el diagnóstico de diabetes mellitus se acepta un coeficiente de variación analítico menor del 4% y error sistemático nulo en la determinación de glucosa en sangre12. Aplicando este concepto al coeficiente de variación del instrumento más utilizado en el programa externo de la SEQC (Roche Modular con método Hexoquinasa) (CV=3,2%), el valor sigma resultante es 1,3.
- –
La encuesta internacional sobre seguimiento del paciente diabético mediante la determinación de HbA1C indica que el coeficiente de variación deber estar comprendido entre el 3 y el 4%13,14. En el programa de la SEQC, el CV del método más frecuente (HPLC calibración JDS) es del 2,6%, y su valor sigma es 1,4.
- –
En la evaluación del riesgo de enfermedad cardíaca el error sistemático para la determinación de colesterol debe ser menor del 1%15. En el programa externo de la SEQC, el valor sigma para el método más frecuente (colesterol oxidasa-estearasa-peroxidada en Roche Modular) es 0,3.
- –
En la evaluación del riesgo de cáncer de próstata el error sistemático para la determinación de PSA total debe ser menor del 6%15. En el programa de la SEQC el método con mayor participación es la luminiscencia con el instrumento Roche Modular E-170, que obtiene un CV del 4,4%. El valor sigma es 1,4.
En cuanto a las especificaciones derivadas de la variación biológica, si un laboratorio las cumple para imprecisión y sesgo (considerando que las dos fuentes de variabilidad se encuentran en el proceso analítico sistemático), los valores sigma obtenidos para las magnitudes biológicas incluidas en este trabajo resultan, en general, menores que 1,6.
Mediante revisión realizada por los autores de este trabajo, lo mismo sucede para las 300 magnitudes descritas en la página web de la SEQC16. Si se consiguiera anular el error sistemático, entonces los valores sigma estarían situados alrededor de 3 con lo que se conseguiría una prestación satisfactoria.
Los resultados de este trabajo indican que si la especificación de la calidad analítica exigida es amplia, el valor sigma es ⩾3. Mientras que si la especificación es más exigente, el valor sigma no es satisfactorio. Cuando esto sucede en todos los laboratorios usuarios de un mismo sistema analítico (instrumento y método), hay que pedir a los fabricantes que dediquen un mayor esfuerzo para producir equipos y reactivos con menor variabilidad.
El valor sigma sólo es mayor que 3 cuando las especificaciones a cumplir se corresponden con una exigencia de calidad mínima. ¿Es suficiente esta calidad analítica para el cuidado de la salud? La respuesta es no, porque el sistema de salud actual, basado en guías de práctica clínica, requiere que los resultados del laboratorio sean indiscutiblemente seguros. Como aboga Westgard2, no es suficiente cumplir los requisitos mínimos de la calidad, como los del CLIA17 o el acuerdo SEQC/AEFA/AEBM6, sino que hay que alcanzar las especificaciones de satisfacción médica. Además, ya se ha visto que si se definen especificaciones que satisfagan las situaciones clínicas específicas, la variación biológica y las opiniones de expertos, el valor sigma es inadecuado. Indiscutiblemente, no se puede bajar la guardia y se debe alcanzar la calidad necesaria para fines médicos.
Obtener un valor sigma mayor que 3 significa que el sistema analítico es productivo desde el punto de vista industrial; requiere poco control, pocas repeticiones y resultará poco costoso18. Como se ha visto, esto sólo sucede para las magnitudes biológicas con poca regulación homeostática o bien si se renuncia a alcanzar el estándar de calidad requerido para satisfacer las necesidades médicas. Cuanto menor es el valor sigma obtenido, mejor y más estricto debe ser el control de la calidad, con el propósito de conseguir la máxima potencia de detección de errores (aumentar el número de muestras control, estrechar la regla operativa, implementar otros diseños que aseguren la calidad, utilizar medias de pacientes, etc.).
Todo lo expuesto hasta aquí se refiere a resultados entre laboratorios. En un laboratorio individual se supone que hay menos fuentes de variación que entre distintos laboratorios y sus valores sigma serían ligeramente mejores. No obstante, los razonamientos planteados en este trabajo son igualmente válidos.
Por último, aunque se ha postulado que la aplicación del concepto Seis Sigma para reducir los errores es costosa para el laboratorio3, no lo es en absoluto si se utiliza como herramienta de mejora en un laboratorio que tenga implantado un sistema de gestión de la calidad, ya que los datos necesarios son elementos básicos de dicha gestión y suelen ser fácilmente accesibles. Además, conocer el valor sigma facilita la definición de las reglas operativas para el control interno del proceso analítico2 mediante programas informáticos de control de la calidad analítica disponibles en nuestro mercado (Unity Real Time de Bio-Rad Laboratories, S.A. e Inter QC de Vitro, S.A.).
ConclusionesEn general, los instrumentos y métodos disponibles en nuestro mercado no son «industrialmente productivos» si se desea cumplir los objetivos de calidad apropiados para el cuidado de la salud.
Nuestros sistemas analíticos requieren un procedimiento de control de la calidad del proceso analítico muy cuidadoso, al que hay que dedicar esfuerzo y recursos para conseguir prestaciones adecuadas (procesamiento de varias muestras control, necesidad de realizar repeticiones, etc.).
En ningún caso se debe confundir el objetivo de alcanzar la calidad necesaria para el adecuado uso clínico del informe analítico con el de conseguir un laboratorio industrialmente productivo; ambos forman parte del concepto de calidad total.