La medición exacta y precisa de bilirrubina es fundamental en el diagnóstico y tratamiento de la ictericia neonatal.
ObjetivosEvaluar la medición de bilirrubina total en el módulo de cooximetría del analizador Gem® Premier™ 4000 (Instrumentation Laboratory) con el propósito de utilizarlo de forma rutinaria en nuestro hospital.
Material y métodoSe han estudiado muestras de suero (n=113) y de sangre (n=90) procedentes de recién nacidos y 111 muestras de suero y 64 de sangre de adultos con bilirrubina total entre 2–20 y 1,5–42mg/dL respectivamente y se han comparado los resultados con el método de 2,5-diclorofenildiazonio en el analizador Cobas® 711 (Roche Diagnostics). La comparación de procedimientos se realizó con el análisis de regresión lineal según Passing-Bablok y la concordancia de resultados se analizó con las gráficas de Bland-Altman.
ResultadosLa imprecisión obtenida (CV) es menor a 4%. En el estudio de muestras de adultos no encontramos diferencias significativas. En las muestras de recién nacidos las pendientes de las rectas de regresión son 1,076 (1,035-1,097) en muestras de suero y 1,093 (1,028-1,148) en muestras de sangre. Las diferencias absolutas entre los métodos son de 0,6 (-1,3 a 2,6) mg/dL en suero y 0,3 (-1,3 a 1,9) mg/dL en sangre
ConclusionesLas diferencias encontradas entre los procedimientos evaluados no son significativas en muestras de adultos. En muestras de sangre de RN se observa un error proporcional del 9,3% con diferencias de > 2 mg/dL respecto al método habitual en el 3,3% de ellas. El analizador GEM® Premier™ 4000 puede ser una alternativa adecuada para la medición de bilirrubina total en muestras de sangre de recién nacidos en las unidades de neonatología y en los laboratorios clínicos.
The exact and precise measurement of bilirubin is fundamental in the diagnosis and treatment of neonatal jaundice.
ObjectiveTo evaluate the measurement of total bilirubin on the co-oximetry module of the Gem® Premier™ 4000 analyser (Instrumentation Laboratory), in order to use it in our hospital. A total of 113 samples of serum and 90 of blood from new-borns (NB), and 111 serum and 64 blood samples from adults, with a range of total bilirubin between 2–20 and 1.5–42 mgldL respectively, were measured. The results were compared with the 2,5-dichlorophenyldiazonium method on the Cobas® 711 analyser (Roche Diagnostics). Comparisons of procedures were calculated with linear regression analysis according to the Passing-Bablok equation and the assessment agreement of methods was analyzed with the Bland-Altman plots.
ResultsThe total imprecision (CV) was less than 4%. No significant differences were found in the study of the adult samplesIn samples of newborns the slopes of the regression lines were 1.076 (1.035 to 1.097) in the newborn serum samples and 1.093 (1.028 to 1.148) in blood samples. The absolute difference between the methods was 0.6 (-1.3 to 2.6) mg/dL in serum and 0.3 (-1.3 to 1.9) mg/dL in blood.
ConclusionsThere were no significant differences between the procedures evaluated in adult samples. In NB whole blood samples the proportional error was 9,3%, with discrepancies > 2 mg/dL compared to the routine method in 3,3% of them. The GEM® Premier™ 4000 analyzer could be a suitable alternative for the quantification of bilirubin in blood samples from new-borns in the neonatal units and clinical laboratories.
La hiperbilirrubinemia neonatal es una situación fisiológica transitoria en los RN que se observa en aproximadamente el 60% de los neonatos, teniendo en la mayoría de los casos un curso benigno. La causa es el aumento de la bilirrubina no conjugada en sangre hasta 5-6mg/dL (86-103μmol/L, factor de conversión 17,1) en los recién nacidos (RN) a término en los 3-5 primeros días de vida. Se resuelve normalmente en unas dos semanas cuando el hígado madura y la concentración de bilirrubina en sangre llega a los concentraciones dentro el intervalo de referencia del adulto (<1mg/dL)1.
Cuando la concentración en sangre de bilirrubina no conjugada aumenta por encima de 7-20mg/dL (119-342μmol/L) se acumula en piel, tejidos y cerebro causando daño neurológico (kernicterus). Los factores de riesgo de desarrollar esta hiperbilirrubinemia severa son la prematuridad (gestación<38 semanas), la lactancia materna, antecedentes familiares de ictericia, incompatibilidad Rh/ABO, o deficiencia de glucosa-6-fosfato deshidrogenasa2. El tratamiento se realiza con fototerapia o, en casos más graves, con transfusión sanguínea. Su objetivo evitar la encefalopatía producida por la neurotoxicidad de la bilirrubina.
La bilirrubina es un pigmento de color amarillo anaranjado producido en el catabolismo de las proteínas con grupo hemo, fundamentalmente la hemoglobina. En sangre la bilirrubina esta presente en diversas formas e isómeros, siendo biotransformada mayoritariamente en el hígado, y excretada en bilis y orina3.
En todos los RN, según las guías clínicas actuales, se realiza control de la hiperbilirrubinemia4,5 con la evaluación de factores de riesgo clínico y con la medida de la concentración de bilirrubina total (BT) en sangre (según la edad en días) y aplicando nomogramas como el de Bhutani et al.6. Antes del alta hospitalaria y para evitar las complicaciones neurológicas se realizan pruebas de seguimiento de bilirrubina en aquellos RN con mayor riesgo1. Por tanto, la determinación de la bilirrubina total en el RN es un parámetro clave para realizar el diagnóstico y el seguimiento de la ictericia neonatal y por ello, es conveniente disponer de métodos precisos y exactos, además de rápidos y poco invasivos. Los métodos utilizados habitualmente son métodos estandarizados en los analizadores del laboratorio clínico que utilizan muestras de suero y/o plasma. Tienen el inconveniente de necesitar un volumen de muestra alto, y que el tiempo invertido en el proceso es relativamente elevado. También se han empleado bilirrubinómetros transcutáneos que tienen la ventaja de no ser invasivos y ser muy rápidos. Sin embargo las evaluaciones realizadas hasta el momento no han sido siempre satisfactorias y han dado lugar a cierta controversia sobre su utilidad7–9. Esto ha llevado a desarrollar en el módulo de cooximetría de los analizadores de gases y electrolitos de pruebas en el lugar de atención al paciente métodos de determinación de BT en sangre que podría facilitar esta medida, debido principalmente a cuestiones de practicabilidad: el volumen de muestra requerido, la facilidad y la rapidez del análisis.
El objetivo de este estudio ha sido evaluar la medición de BT en el analizador Gem® Premier™ 4000 y comparar los resultados con el método utilizado habitualmente en el laboratorio, para valorar su utilización de forma rutinaria en la evaluación de la ictericia en el RN en nuestro hospital.
Material y métodosPacientesSe analizaron especímenes de RN (90 muestras de sangre y 113 de suero) procedentes de las Unidades de Neonatología y Maternidad del hospital, a los que les solicitaba la determinación de BT, durante un periodo de 6 meses. Las muestras se obtuvieron por punción venosa o a través de vía en tubos sin anticoagulante y con separador (BD Vacutainer®) para los análisis en suero y en tubos con EDTA (Sarstedt Monovette®) para los análisis en sangre. Se recogieron también 111 muestras de suero y 64 de sangre de pacientes adultos. Los tubos de sangre sin anticoagulante se dejaron coagular y se centrifugaron a 1.500xg durante 15 minutos a temperatura ambiente antes de ser procesados de la forma habitual en el laboratorio. En ningún caso el tiempo transcurrido en el procesamiento de las muestras por los diferentes métodos superó 1h.
Para este estudio se utilizó sangre y/o suero residual de la realización de las peticiones solicitadas de forma habitual, los resultados obtenidos han sido siempre anónimos y no se han utilizado con ningún fin asistencial.
MétodosAnalizador GEM®Premier™ 4000 (Instrumentation Laboratory): las muestras de suero y sangre se procesaron siguiendo en todo momento las recomendaciones del fabricante. El analizador se calibra automáticamente utilizando patrones de referencia internos y se verifica con soluciones externas, GEM CVP1 y GEM CVP2, suministradas por Instrumentation Laboratory, que contienen los analitos y colorantes necesarios, con trazabilidad a materiales de referencia del National Institute of Standars and Technology (NIST). La medición de la BT se realiza en el módulo de cooximetría utilizando medidas de longitud de onda entre 480-650nm y fórmulas de regresión multivariante a 37°C después de lisis química. El analizador lleva incorporado un programa de control interno Intelligent Quality Management (iQM®) que monitoriza la precisión del sistema de forma automática (máximo CV% permitido 10%). El intervalo de medida declarado por el fabricante es entre 0,3 y 40mg/dL.
Analizador Cobas®711 (Roche Diagnostics): la determinación de BT se realizó con el método del 2,5-diclorofenildiazonio (DPD)10, siguiendo las recomendaciones del fabricante, con reactivos del mismo proveedor (Ref.03146022 122). Las muestras séricas con índice de hemólisis mayor de 50 eliminaron por su interferencia con este método, como se hace habitualmente. Los controles utilizados son Liquid Unassayed Multiqual (BioRad®). El calibrador utilizado (Calibrator for automated systems; Ref.10759350) con trazabilidad con el SRM 916a11. El intervalo de medición fue de 0,1-34mg/dL y hasta 40mg/dL con programación de volumen de muestra disminuido.
Imprecisión: se analizaron 3 soluciones control: (Bilirrubin Control Pediatric (Quantimetrix®), Liquid Unassayed Multiqual level 3 (BioRad®)) y Liquid QC Bilirrubin Control (Clinica®) por duplicado 2 veces al día durante 20 días siguiendo el protocolo de CLSI EP5-A2.
Linealidad: se verificó realizando diluciones seriadas de 2 muestras de suero con concentración de BT elevada (30mg/dL) y calculando la recuperación (%) del valor inicial, según las recomendaciones del College of American Pathologists.
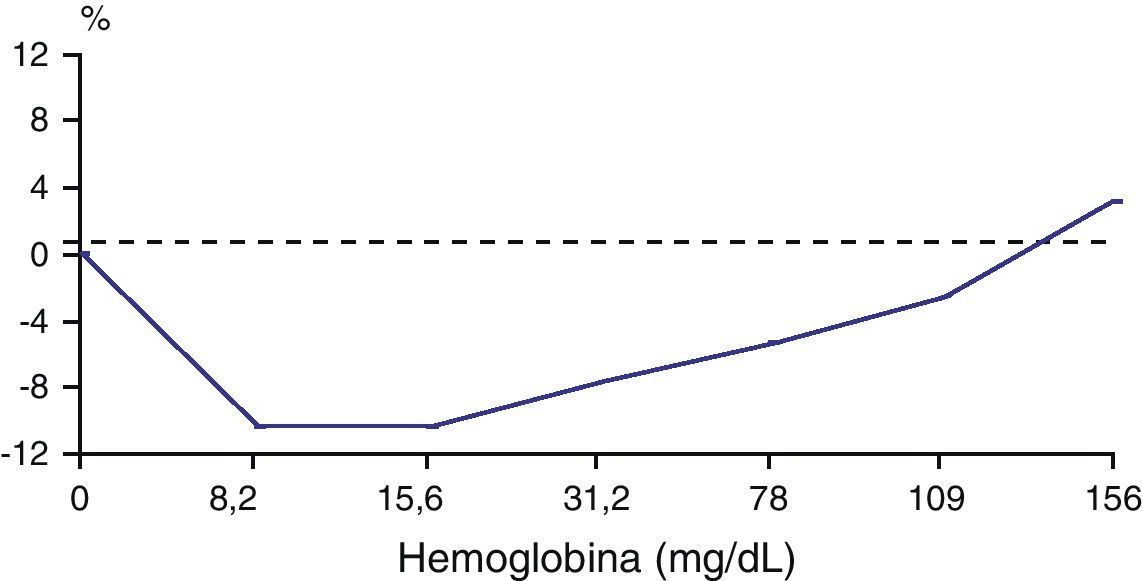
Interferencia por hemoglobina: se estudió siguiendo el protocolo de Glick12 en dos mezclas de suero con concentraciones de bilirrubina de 13 y 8mg/dL a las que se añadió hemoglobina hasta una concentración de 160mg/dL y se calculó el porcentaje de recuperación frente al valor inicial.
Estudio estadísticoLa comparación de las medias obtenidas en los grupos se realizó con la prueba de t de Student y la U de Mann-Whitney. Para el estudio de normalidad se utilizó el test de Kolmogorov-Smirnov. El estudio de comparación de los procedimientos de medida se realizó mediante el análisis de regresión lineal con el método no paramétrico de Passing-Bablok13. El análisis de las diferencias de los resultados se realizó con las graficas de Bland-Altman14. Los coeficientes de correlación fueron calculados según Pearson y Spearman. Se utilizó el programa estadístico MedCalc (v 9.5.2.0).
ResultadosImprecisiónDurante el tiempo del estudio, el chequeo interno de precisión que realiza el GEM® Premier™ 4000 de forma automática (iQM®) fue correcto, habiéndose utilizado 4 lotes de reactivos. La imprecisión total en términos de coeficiente de variación (CV) en las soluciones control fue de 2,5 a 3,6% (tabla 1). En el analizador Cobas® 711 los CV en el periodo del estudio fueron de 6,5%, 3,8% y 2,8% a concentraciones de 8,2, 4,2 y 2,5mg/dL, respectivamente. El error sistemático fue < 10%, valorado a través de la participación en el programa externo de intercomparación de la SEQC.
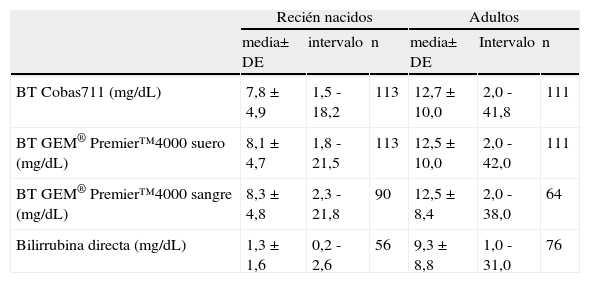
Estudio de comparación de métodosLos resultados descriptivos de las muestras estudiadas de RN y de adultos en el GEM® Premier™ 4000 y en el Cobas® 711 están resumidos en la tabla 2. No existen diferencias significativas entre las medias de BT obtenidas por ambos métodos (p>0,05), tanto en muestras de RN como de adultos. En adultos la BT es fundamentalmente conjugada o directa y en RN es no conjugada o indirecta.
Estudio descriptivo de las muestras de recién nacidos y adultos procesadas en el GEM® Premier™ 4000 y en el Cobas® 711
| Recién nacidos | Adultos | |||||
| media± DE | intervalo | n | media± DE | Intervalo | n | |
| BT Cobas711 (mg/dL) | 7,8±4,9 | 1,5 - 18,2 | 113 | 12,7±10,0 | 2,0 - 41,8 | 111 |
| BT GEM® Premier™4000 suero (mg/dL) | 8,1±4,7 | 1,8 - 21,5 | 113 | 12,5±10,0 | 2,0 - 42,0 | 111 |
| BT GEM® Premier™4000 sangre (mg/dL) | 8,3±4,8 | 2,3 - 21,8 | 90 | 12,5±8,4 | 2,0 - 38,0 | 64 |
| Bilirrubina directa (mg/dL) | 1,3±1,6 | 0,2 - 2,6 | 56 | 9,3±8,8 | 1,0 - 31,0 | 76 |
DE: desviación estándar.
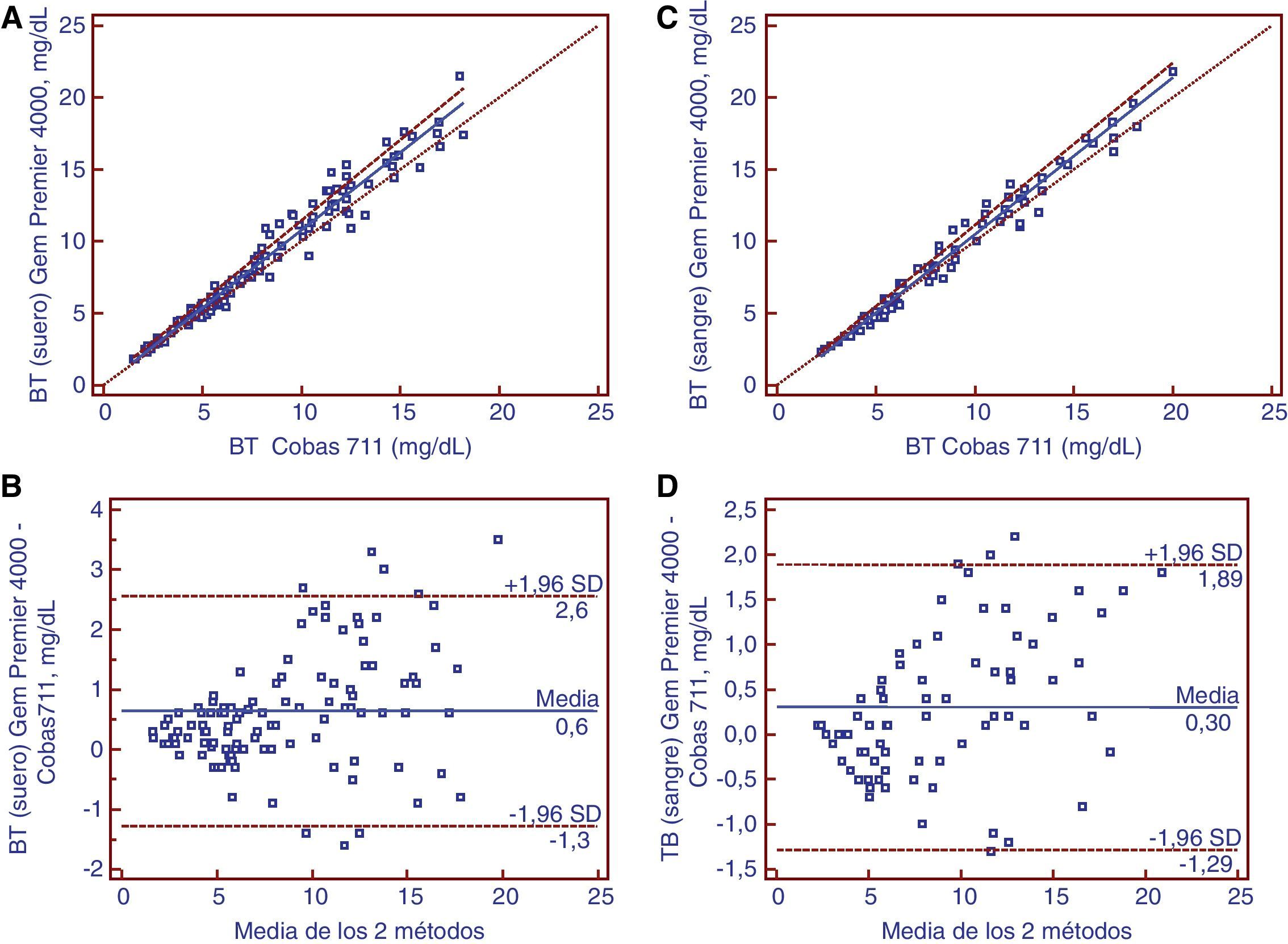
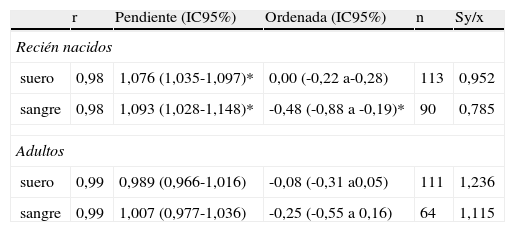
En la tabla 3 están reflejados los resultados del análisis de comparación de métodos según Passing-Bablok en especímenes de adultos y RN. En la tabla 4 las diferencias porcentuales y absolutas de la concentración de BT en el GEM® Premier™ 4000 respecto al Cobas® 711 para ambos grupos. En la figura 1 están representados los resultados de la comparación entre métodos en muestras de RN: sangre (derecha) y suero (izquierda), en la parte superior las gráficas de regresión lineal y en la parte inferior las gráficas de Bland-Altman.
Resultados del análisis de comparación de métodos de bilirrubina según Passing-Bablok en el GEM® Premier™ 4000 frente al Cobas® 711 en muestras de suero y sangre
| r | Pendiente (IC95%) | Ordenada (IC95%) | n | Sy/x | |
| Recién nacidos | |||||
| suero | 0,98 | 1,076 (1,035-1,097)* | 0,00 (-0,22 a-0,28) | 113 | 0,952 |
| sangre | 0,98 | 1,093 (1,028-1,148)* | -0,48 (-0,88 a -0,19)* | 90 | 0,785 |
| Adultos | |||||
| suero | 0,99 | 0,989 (0,966-1,016) | -0,08 (-0,31 a0,05) | 111 | 1,236 |
| sangre | 0,99 | 1,007 (0,977-1,036) | -0,25 (-0,55 a 0,16) | 64 | 1,115 |
IC95%: Intervalo de confianza del 95%; r: Coeficiente de correlación; S y/x: Error estándar de la estima. * p<0,05
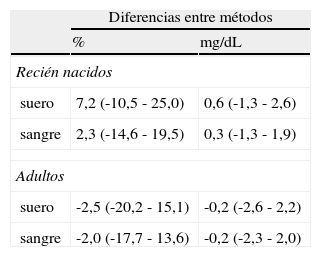
Diferencias medias de la concentración de bilirrubina en el GEM® Premier™ 4000 respecto al Cobas® 711 en muestras de suero y sangre de recién nacidos y adultos
| Diferencias entre métodos | ||
| % | mg/dL | |
| Recién nacidos | ||
| suero | 7,2 (-10,5 - 25,0) | 0,6 (-1,3 - 2,6) |
| sangre | 2,3 (-14,6 - 19,5) | 0,3 (-1,3 - 1,9) |
| Adultos | ||
| suero | -2,5 (-20,2 - 15,1) | -0,2 (-2,6 - 2,2) |
| sangre | -2,0 (-17,7 - 13,6) | -0,2 (-2,3 - 2,0) |
En muestras procedentes de RN el análisis de regresión lineal demuestra que la ordenada en el origen es igual a cero. Sin embargo, las pendientes de dichas rectas de regresión son diferentes a 1, indicando un error sistemático proporcional de 7,6% en muestras de suero y 9,3% en muestras de sangre, en el intervalo de medida estudiado de 2-22mg/dL. En las muestras de adultos las pendientes y las ordenadas no son diferentes de 1 y de 0 respectivamente en muestras de suero y sangre, indicando que no hay error sistemático proporcional ni constante en el intervalo de 1,5 a 40mg/dL estudiado.
En las gráficas de Bland-Altman la media de las diferencias incluye el 0 para ambos tipos de muestras en RN y adultos. Por tanto, la variación entre métodos es baja, siendo el límite de concordancia (definido como 1,96xSD de las diferencias) de 2,0mg/dL en suero y 1,6mg/dL en sangre. En el grupo de RN, en 3 muestras de sangre de 90 (3,3%) y en 14 de suero de 113 (12,4%) la diferencia entre métodos fue >2 mg/dL. En el grupo de adultos hubo un 11,7% de muestras de suero y un 6,2% de muestras de sangre con diferencias > 2 mg/dL.
En ambas poblaciones los coeficientes de correlación (r) obtenidos fueron de 0,98 y 0,99, con bajos errores de la estima (S y/x) (tabla 3).
LinealidadLa recuperación en el intervalo estudiado (2,5 a 30mg/dL) es del 97-107% (5%).
Interferencia por hemoglobinaEn el estudio de la interferencia por hemólisis (fig. 2) en muestras de suero observamos una interferencia negativa (-11%) a concentraciones bajas de hemoglobina, que no se observa a concentraciones mas altas (> 80mg/dL)
ConclusionesEn este trabajo se presentan los resultados de la evaluación de la determinación de BT en el analizador GEM® Premier™ 4000 y la comparación de los resultados con los obtenidos por el método habitual del laboratorio en el analizador Cobas® 711. Los resultados en especímenes de RN y adultos demuestran que la determinación de BT en el GEM® Premier™ 4000 es fiable y reproducible y los valores correlacionan y son intercambiable con el método de comparación. Este método puede utilizarse en las muestras de RN para la valoración de la ictericia neonatal.
La imprecisión total de la medición de BT en el GEM® Premier™ 4000 fue inferior a 4% durante el período del estudio, en el que se utilizaron 4 lotes de reactivos y 3 materiales de control comerciales. De acuerdo con la bibliografía, la variabilidad biológica de la bilirrubina es del 23,8% y por tanto cumple las especificaciones deseables (CV<11,9%) y óptimas (CV<6%) de calidad analítica de esta magnitud biológica según recomendaciones del Comité de Garantía de la Calidad y Acreditación de Laboratorios de la SEQC15. Estos resultados son similares a los descritos por Borgard JP et al.16 en un estudio multicéntrico francés con el analizador ABL 735 (Radiometer Medical). En el analizador RapidLab® 1265 (Siemens) en el estudio realizado por Mielsch et al.17 describen una imprecisión más alta, desde 23% a valores bajos (5mg/dL) hasta 5,6% a valores altos (20mg/dL).
Los análisis del estudio de comparación de métodos indican que en especimenes de adultos los resultados del método espectrofotométrico en el GEM® Premier™ 4000 son comparables e intercambiables con el método DPD en el Cobas® 711 en todo el intervalo de concentración estudiado (1,5 - 40mg/dL). No existen diferencias significativas entre los métodos. La media de las diferencias entre métodos en muestras de suero es -0,2mg/dL y en muestras de sangre -0,2mg/dL.
En especímenes de RN el comportamiento es ligeramente diferente. En el intervalo de concentración estudiado de 2 a 22mg/dL se observa un error proporcional de 9,3% en las muestras de sangre y 7,6% en muestras de suero. El límite de concordancia es ±2mg/dL, semejante al obtenido (±2,5mg/dL) por Mielsch et al.17 para el RapidLab® 1265 al compararlo con el Vitros® 350. No hay grandes discrepancias entre pares de resultados, ya que solo un 2,2% de las muestras de sangre de RN tienen una diferencia >±2mg/dL. En las muestras de suero de RN en un 12% las diferencias son > 2mg/dL. Este hecho pude estar relacionado con la manipulación de la muestra, o con el hecho de que la calibración del GEM® Premier™ 4000 está diseñada para muestras de sangre total, que es el tipo recomendado por el fabricante y utilizado en la práctica diaria en estos analizadores. La interferencia de la hemoglobina a bajas concentraciones en muestras de suero, también puede estar relacionada con estas diferencias.
El error proporcional en los especimenes de RN, que no se observa en adultos, puede ser debido a las diferencias en las isoformas de bilirrubina presentes en ambas poblaciones16. En adultos la mayor parte de la bilirrubina circula en forma conjugada, mientras que en RN lo hace en la forma libre (tabla 2). Otra causa del diferente comportamiento de las muestras de adulto y RN puede ser la presencia en estos últimos de hemoglobina fetal en proporción superior a las muestras de adultos y su posible interferencia con el espectro de absorción.
El GEM® Premier™ 4000 es un analizador de gases y electrolitos que puede utilizarse a la cabecera del paciente y en el propio laboratorio de análisis clínicos. La manipulación y mantenimiento es fácil y mínima. La medición de BT se ha incorporado recientemente en el modulo de cooximetría y recibió la aprobación de la FDA en 2010 y a continuación en el mercado europeo. Se necesitan 100μL de sangre o suero para determinación de BT y el tiempo de respuesta de 95 segundos. El sistema incorpora un sistema automático de control de calidad que hace comprobaciones constantes para detectar problemas y resolverlos. El fabricante advierte de interferencias que producen sustancias como la cianometahemoglobina, la sulfohemoglobina y o el exceso de turbidez con la determinación de BT en el módulo de cooximetría. En estos casos el aparato no calcula los resultados e informa con una alarma.
En nuestro conocimiento, este es el primer estudio de evaluación de la medición de BT en el analizador GEM® Premier™ 4000 en muestras de suero y sangre de RN. Hay pocos estudios disponibles relacionados con la medición de BT con analizadores de gases, siendo el más detallado el realizado por Mielsch et al.17 en el RapidLab® 1265. El grupo de Bénéteau-Burnat B. et al.18 evalúa el GEM® Premier™ 4000 en 2 laboratorios comparándolo a su vez con otros tres analizadores de gases (ABL 835 y 725, Radiometer; OMNI S, Roche Diagnostics) pero sin incluir la prueba de BT. Concluyen que los aspectos de practicabilidad como facilidad de manejo, volumen requerido y robustez del aparato son muy positivos.
En resumen, el analizador de gases GEM® Premier™ 4000 se presenta como una alternativa adecuada para la medición de BT en muestras de sangre de RN, tanto en las unidades de neonatología como en los laboratorios clínicos. Para la valoración de hiperbilirrubinemia en el neonato con el GEM® Premier™ 4000 la muestras utilizadas preferentemente son de sangre, y los resultados obtenidos en ellas podemos considerarlos adecuados para su uso en la clínica habitual. En casos dudosos sería necesaria la comprobación por el método habitual del laboratorio. La concentración de bilirrubina es, junto con los factores de riesgo clínicos, una magnitud biológica clave para valorar la probabilidad de desarrollar hiperbilirrubinemia severa en el recién nacido y determinar la conducta y el tratamiento a seguir para evitar la morbilidad y mortalidad asociada a esta patología.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.