La sección de Vía Aérea de la Sociedad Española De Anestesiología, Reanimación y Terapéutica del Dolor (SEDAR), la Sociedad Española de Medicina de Urgencias y Emergencias (SEMES) y la Sociedad Española de Otorrinolaringología y Cirugía de Cabeza y Cuello (SEORL-CCC) presentan la Guía para el manejo integral de la vía aérea difícil en el paciente adulto. Sus principios están focalizados en el factor humano, los procesos cognitivos para la toma de decisiones en situaciones críticas y la optimización en la progresión de la aplicación de estrategias para preservar una adecuada oxigenación alveolar con el objeto de mejorar la seguridad y la calidad asistencial. El documento proporciona recomendaciones basadas en la evidencia científica actual, herramientas teórico/educativas y herramientas de implementación, fundamentalmente ayudas cognitivas, aplicables al tratamiento de la vía aérea en el campo de la anestesiología, cuidados críticos, urgencias y medicina prehospitalaria. Para ello se realizó una amplia búsqueda bibliográfica según las directrices PRISMA-R y se analizó utilizando la metodología GRADE. Las recomendaciones se formularon de acuerdo con esta metodología. Las recomendaciones de aquellas secciones con evidencia de baja calidad se basaron en la opinión de expertos mediante consenso alcanzado a través de un cuestionario Delphi.
The Airway Management section of the Spanish Society of Anesthesiology, Resuscitation, and Pain Therapy (SEDAR), the Spanish Society of Emergency Medicine (SEMES), and the Spanish Society of Otorhinolaryngology and Head and Neck Surgery (SEORL-CCC) present the Guide for the comprehensive management of difficult airway in adult patients. Its principles are focused on the human factor, cognitive processes for decision-making in critical situations, and optimization in the progression of strategies application to preserve adequate alveolar oxygenation in order to enhance safety and the quality of care. The document provides evidence-based recommendations, theoretical-educational tools, and implementation tools, mainly cognitive aids, applicable to airway management in the fields of anesthesiology, critical care, emergencies, and prehospital medicine. For this purpose, an extensive literature search was conducted following PRISMA-R guidelines and was analyzed using the GRADE methodology. Recommendations were formulated according to the GRADE methodology. Recommendations for sections with low-quality evidence were based on expert opinion through consensus reached via a Delphi questionnaire.
El tratamiento de la vía aérea (VA) es una piedra angular de múltiples procedimientos asistenciales en medicina1. Series recientes indican que la incidencia de la vía aérea difícil (VAD) y fallida ha descendido hasta situarse en 1,6 y 0,06 por 1.000 casos, respectivamente2, aunque sigue siendo una causa importante de morbimortalidad3,4.
Una gran proporción de complicaciones derivadas de la asistencia clínica son evitables5. El análisis de incidentes en registros nacionales, así como de datos médico/legales juega un papel relevante para la detección de fallos en la práctica clínica y la implementación de nuevas estrategias para paliarlos5–7. España no dispone de registro de eventos adversos asociados a la VA. Sin embargo, los datos mundiales podrían ser extrapolables a nuestra área de influencia. Especial trascendencia tiene el 4th National Audit Project (NAP4), del Reino Unido8,9. Las 168 recomendaciones derivadas permitieron optimizar la seguridad10. Desde entonces, sociedades de diferentes especialidades han elaborado nuevas guías, algoritmos11–16 y ayudas cognitivas17, para proporcionar estrategias actualizadas. Pese a ello, casi una década después, muchas de las deficiencias detectadas persisten4,18, como evidencian recientes estudios que arrojan datos prácticamente superponibles3,7,19–21. Todos han objetivado errores recurrentes: evaluación y planificación inadecuadas, falta de anticipación ante una VAD, preparación y disponibilidad de equipo específico insuficiente, perseverancia en una estrategia fallida, omisión del uso de un dispositivo extraglótico (DEG) ante dificultad en la ventilación, y la no progresión oportuna a una VA quirúrgica5,18. Así, los factores humanos (FFHH) y ergonómicos juegan un papel contribuyente clave22,23. Dichos hallazgos respaldan la importancia de la anticipación, la preparación y el seguimiento de las guías, y enfatizan la necesidad de redoblar esfuerzos y proseguir la implementación de mejoras4,24.
Las estrategias de abordaje de la VAD están condicionadas por el entorno, los medios tecnológicos y la experiencia de los profesionales implicados. Por ello, es recomendable la implementación de guías adaptadas al entorno asistencial nacional e institucional4,18,25, como indica la Declaración de Helsinki sobre la seguridad del paciente en anestesiología26. Las herramientas actuales para la toma de decisiones no son del todo satisfactorias ya que omiten la influencia de los FFHH y de la especificidad contextual, dando lugar a intervenciones que pueden ser ineficaces e inducir a errores23,27. La mayoría de algoritmos presuponen invariablemente la intubación traqueal (IT) como objetivo inicial28. Sus diseños son más efectivos para la educación y la capacitación en un contexto teórico que para su ejecución en situaciones clínicas reales dinámicas y estresantes23,24,29,30. Algunos estudios han demostrado, incluso, un efecto negativo en la toma de decisiones31,32. Asimismo, presentan una implementación irregular y una adherencia generalmente limitada18,30,33. La razón de estos hallazgos ha sido atribuida a sus diseños complejos e inflexibles, siendo en ocasiones percibidos como una barrera para el flujo de trabajo más que como una ayuda en situaciones emergentes34. Por ello, se precisan ayudas cognitivas eficaces que simplifiquen la transición de una técnica a otra35, dando continuidad al tratamiento de la VA.
El objetivo del presente documento es aportar al profesional un conjunto de recomendaciones basadas en la evidencia, así como herramientas racionales y de implementación para la toma de decisiones en el manejo de la VAD.
ObjetivosProporcionar recomendaciones de la Sociedad Española de Anestesiología, Reanimación y Terapéutica del Dolor (SEDAR), la Sociedad Española de Medicina de Urgencias y Emergencias (SEMES) y la Sociedad Española de Otorrinolaringología y Cirugía de Cabeza y Cuello (SEORL-CCC) basadas en la evidencia científica para el manejo integral de la VAD en el paciente adulto.
Proporcionar herramientas racionales y de implementación, fundamentalmente ayudas cognitivas con un diseño basado en los FFHH y ergonómicos, contexto específicas, enfocadas en los procesos cognitivos en situaciones críticas relacionadas con la VAD. Las mismas pueden facilitar la toma de decisiones y optimizar la progresión en la aplicación de estrategias para preservar una adecuada oxigenación durante todo el procedimiento y reducir la incidencia de complicaciones, contribuyendo así a la mejora de la seguridad y la calidad asistencial.
Los postulados descritos en ningún caso deben ser considerados estándares de obligado cumplimiento y, dada la diversidad y complejidad contextual, su aplicación no garantiza el éxito ante cualquier situación. Las recomendaciones tienen un carácter flexible, prevaleciendo siempre el buen juicio clínico del profesional tras el pertinente análisis del balance riesgo beneficio en cada caso específico.
Validez y aplicabilidadLos contenidos de esta guía son recomendaciones generales basadas en la evidencia actual. Por ello, podrían ser aplicables a cualquier circunstancia y procedimiento que requiere el control de la VA, bien sea ventilación con mascarilla facial (VMF), ventilación con dispositivo extraglótico (VDEG) o IT, y por cualquier profesional responsable del tratamiento de la VA.
Dado el constante incremento del conocimiento y del desarrollo tecnológico, las recomendaciones serán sometidas a revisión periódica desde el momento de su publicación.
MetodologíaEl proceso de desarrollo de la presente guía se adhirió a las directrices Appraisal of Guidelines, Research and Evaluation II (AGREE II)36. Para garantizar el respaldo de las recomendaciones por la evidencia, se realizó una revisión sistemática rápida siguiendo las recomendaciones PRISMA Rapid reviews (PRISMA-R).
Un comité director conformado por 27 expertos en VA seleccionó las secciones a tratar y constituyó el «Grupo español de manejo de la vía aérea», grupo conformado por facultativos de toda España, miembros de la SEDAR, SEMES y SEORL-CCC con experiencia en docencia e investigación en la materia y que desarrollan su actividad asistencial en anestesia, cuidados críticos y urgencias hospitalarias.
La búsqueda bibliográfica se realizó en MEDLINE, Embase, Scopus, Web of Science, PubMed, Science Citation Index y The Cochrane Library en el periodo comprendido entre el 1 de junio de 2000 y el 1 de diciembre de 2022. Las palabras clave empleadas fueron «airway», «airway management», «difficult airway», «tracheal intubation», «guideline», «algorithm», «cognitive aid», «checklist», «awake tracheal intubation», «fiberoptic intubation», «videolaryngoscopy», «supraglottic airway», «face mask», «oxygenation», «preoxygenation», «apneic oxygenation», «ventilation failure», «rapid sequence induction», «can’t intubate can’t ventilate», «airway complications», «emergency airway», «front of neck access», «cricothyrotomy», «extubation», «teaching», «training» y «competence». La búsqueda se limitó a literatura publicada en inglés y español en los últimos 22 años, y versada exclusivamente en el paciente adulto. Los términos de búsqueda se usaron de forma individual y en combinación. Se incluyeron ensayos clínicos controlados aleatorizados, series de casos, encuestas, artículos de revisión y editoriales.
El análisis de la literatura y las recomendaciones fue realizado siguiendo la metodología Grading of Recommendations Assessment, Development, and Evaluation (GRADE)37. Un revisor (MAGR) realizó una preselección de títulos y resúmenes desduplicados utilizando el software Rayyan, seguida de una revisión completa del texto realizada por 3 revisores (JAS, TL y AAG) de forma independiente, documentando las razones de exclusión. Se consideró la literatura citada dentro de los artículos identificados, así como publicaciones relevantes posteriores. Los diferentes estudios fueron incorporados a una tabla de resumen de hallazgos con una evaluación de la calidad de la evidencia para cada resultado37. Los datos obtenidos fueron editados y sintetizados para la formulación de recomendaciones y nivel de evidencia.
Las recomendaciones se formularon y clasificaron según el sistema GRADE. Las recomendaciones y las justificaciones fueron redactadas inicialmente y revisadas críticamente por 4 autores. Posteriormente fueron revisadas por el comité antes del proceso de consenso. Los autores participaron en conferencias de consenso virtuales en febrero y marzo de 2023. Durante las cuales se confirmó la formulación y la clasificación de cada recomendación.
Las secciones con evidencia de baja calidad o literatura prácticamente inexistente, fueron destinadas para la elaboración de un cuestionario Delphi (material suplementario) del que se extrajo una declaración de expertos en aquellas cuestiones en las que se alcanzó el consenso suficiente.
El texto final fue enviado a todos los integrantes del grupo y a consultores externos para su revisión. Aquellas apreciaciones enriquecedoras fueron incorporadas en el documento.
Todo el proceso fue íntegramente independiente de la industria y de cualquier tipo de financiación.
El material suplementario 1 muestra las escalas de evidencia GRADE.
DefinicionesLa literatura actual no aporta definiciones estándar en VAD al no existir un consenso universal al respecto38,39. El uso de una terminología clara, concisa y precisa es clave para mejorar la consciencia situacional de equipo y la comunicación, el desarrollo de procesos cognitivos y un modelo mental compartido. Esto permite generar acciones coordinadas, la progresión adecuada en un algoritmo de estrategias, evitar errores y uniformizar criterios para la investigación y la documentación en el campo de la VA38,40–42. El material suplementario 2 incluye los factores de riesgo para las diferentes entidades.
Vía aérea difícilSituación clínica en la que un operador con capacitación convencional tiene dificultad para la VMF, para la VDEG o para realizar una IT pudiendo resultar en una oxigenación alveolar inadecuada.
Ventilación difícil con mascarilla facial (VDMF) o dispositivo extraglótico (VDDEG)Situación en la que no puede ser aportada una ventilación adecuada a pesar de haber establecido un bloqueo neuromuscular (BNM) intenso con la presencia de uno o más de los siguientes problemas: ausencia de dióxido de carbono exhalado o ausencia de las fases II y/o III de la onda de capnografía, disminución de la saturación de oxígeno o saturación inadecuada, ausencia o inadecuación de las medidas espirométricas del flujo de gas espirado, sellado incorrecto, fuga o resistencia excesivas durante la entrada o salida de gas. Los signos de ventilación inadecuada incluyen (pero no se limitan a): ausencia de movimiento o movimiento inadecuado del tórax, ausencia o inadecuación de la auscultación de ruidos respiratorios, signos de obstrucción grave, cianosis, dilatación gástrica y cambios hemodinámicos asociados a hipoxemia e hipercapnia (p. ej., hipertensión, taquicardia, arritmias).
Laringoscopia difícilLa amplia difusión de la videolaringoscopia hace apropiado diferenciar entre43,44:
Laringoscopia directa o convencional difícilSituación en la que no es posible visualizar las estructuras glóticas con la mejor exposición laringoscópica posible y con las condiciones óptimas (posición del paciente, pala adecuada, BNM completo, manipulación laríngea externa o BURP), y es definida por un Cormack-Lehane (C-L) grado 3 o 4.
Videolaringoscopia o laringoscopia indirecta difícilSituación en la que mediante videolaringoscopia no es posible obtener porcentaje alguno de visualización glótica con la mejor exposición videolaringoscópica posible y con las condiciones óptimas (posición del paciente, pala adecuada, BNM completo, manipulación laríngea externa o BURP), y es definida por un Percentage Of Glottis Opening (POGO) al 0%, equivalente a un C-L grados 3 o 4 con laringoscopia directa (LD)45.
Intubación traqueal difícilAquella que precisa múltiples intentos, operador/es adicional/es, dispositivos y/o técnicas o maniobras adyuvantes para avanzar el tubo a nivel endotraqueal.
Para cuantificar y documentar la dificultad se puede considerar como sistema de puntuación la Escala de dificultad de intubación (IDS) propuesta por Adnet et al.46, o la escala de Fremantle45,47 que incluye el grado de visión laríngea, la facilidad de paso del tubo endotraqueal (TET), el tipo de dispositivo empleado y cualquier adyuvante.
Intubación traqueal fallidaImposibilidad para avanzar un tubo a nivel endotraqueal a pesar de varios intentos, con uno o varios dispositivos y adyuvantes.
Situación no intubable-no oxigenable (NINO)Imposibilidad de alcanzar una oxigenación alveolar mediante métodos no invasivos de oxigenación (IT, VMF o VDEG) dada la imposibilidad de mantener permeable la VA superior. La restauración de la oxigenación alveolar requiere un acceso infraglótico invasivo (AII) a la VA.
Acceso infraglótico invasivo difícil (AIID)Dificultad para identificar las estructuras anatómicas cervicales (membrana cricotiroidea, MCT) o para lograr un AII a la VA.
Vía aérea de difícil acceso y controlSituación clínica en la que, un operador capacitado, no es capaz de realizar VMF, VDEG o IT debido a una compleja interacción entre paciente, patología, entorno, operador, equipos, experiencia y circunstancias.
Intento fallidoPrueba dentro de un plan específico de tratamiento de la VA que no resulta exitosa.
Plan fallidoAquel que no alcanza el éxito tras 3 intentos.
Extubación traqueal difícilExtracción del TET de un paciente con una VAD conocida o prevista.
Extubación traqueal fallidaPérdida de la permeabilidad de la VA y de la ventilación adecuada tras la extracción del TET.
Tolerancia reducida al periodo de apneaEstado fisiopatológico, habitualmente causado por shunt, desajuste ventilación/perfusión o capacidad residual funcional (CRF) reducida, que determina la presencia de hipoxemia, escasa o nula eficacia de las técnicas de oxigenación periprocedimiento y/o un tiempo de apnea seguro (período comprendido desde el cese de la ventilación hasta una saturación de oxihemoglobina arterial ≤90%) acortado.
Factores humanos y ergonómicosEl entorno clínico es un sistema sociotécnico complejo y dinámico, donde múltiples factores interactúan dando como resultado una variabilidad en los procesos operativos y, en consecuencia, en el rendimiento de los mismos23. Los FFHH hacen referencia a factores individuales, grupales, ambientales y organizacionales que afectan tanto a la toma de decisiones como al desempeño general del sistema34. La disciplina que los estudia trata de comprender su influencia para optimizar las interacciones entre los humanos y con otros elementos del sistema con el objeto de aumentar la contribución humana al éxito (eficiencia), así como limitarla al error (seguridad)48.
El papel de los FFHH en la aparición de eventos adversos en VA tiene tanta trascendencia como las limitaciones técnicas49. El NAP4 concluyó que contribuyeron al 40% de las complicaciones importantes, con un promedio de 4 FFHH contribuyentes por caso50. Los accidentes ocurren habitualmente por un «error de acción», como la omisión de una tarea crítica, y se deben fundamentalmente a la falta de consciencia de la situación50. Una urgencia como la situación NINO exige una inmediata respuesta coordinada de equipo23. Sin embargo, el exceso de información y la presión genera una sobrecarga cognitiva y sensorial30, así como cambios en los procesos mentales y conductuales secundarios a la respuesta de estrés que anulan el pensamiento sistemático, fomentan los sesgos cognitivos y aumentan el riesgo de errores22,23,51,52. La multiplicidad de algoritmos y su escasa aplicabilidad en una crisis, paralizan el flujo de trabajo. Factores como la fatiga, causada, por ejemplo, por turnos prolongados, entorpecen aún más el rendimiento22. Así, los errores no están causados por una deficiencia en las competencias individuales, sino por la propia naturaleza de los procesos cognitivos y su articulación en situaciones desafiantes52. Hasta el 93% de las IT difíciles son inesperadas53. Por lo tanto, son necesarias herramientas eficaces, que no causen mayor saturación perceptiva, y que faciliten procesos complejos tales como planificación, consciencia situacional, toma de decisiones, coordinación del equipo o gestión de tareas48,54. El abordaje algorítmico lineal de crisis no se corresponde con los procesos cognitivos flexibles e intuitivos que se activan para la resolución de situaciones dinámicas estresantes29,55,56.
Por las razones expuestas, esta guía proporciona una ayuda cognitiva aplicable a cualquier situación de urgencia asociada a una VAD, la estandarización del carro de VAD como extensión de esta, un checklist preprocedimiento, así como principios de ergonomía. El material suplementario 3 detalla el objeto de cada elemento según los principios de los FFHH.
Ayuda cognitivaSe recomienda disponer de ayudas cognitivas visuales para el manejo de las crisis emergentes (declaración de expertos [D.E.] 97,1%).
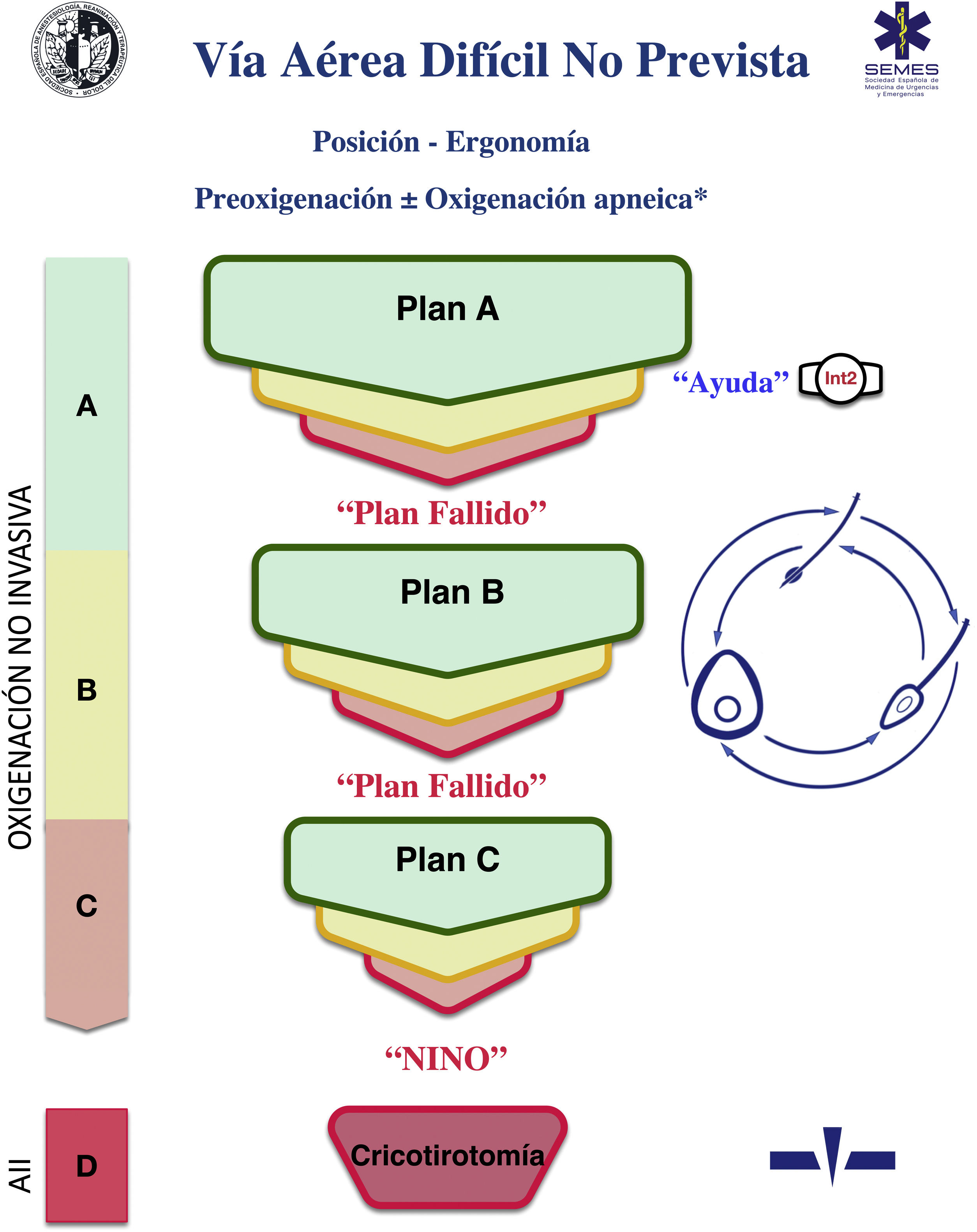
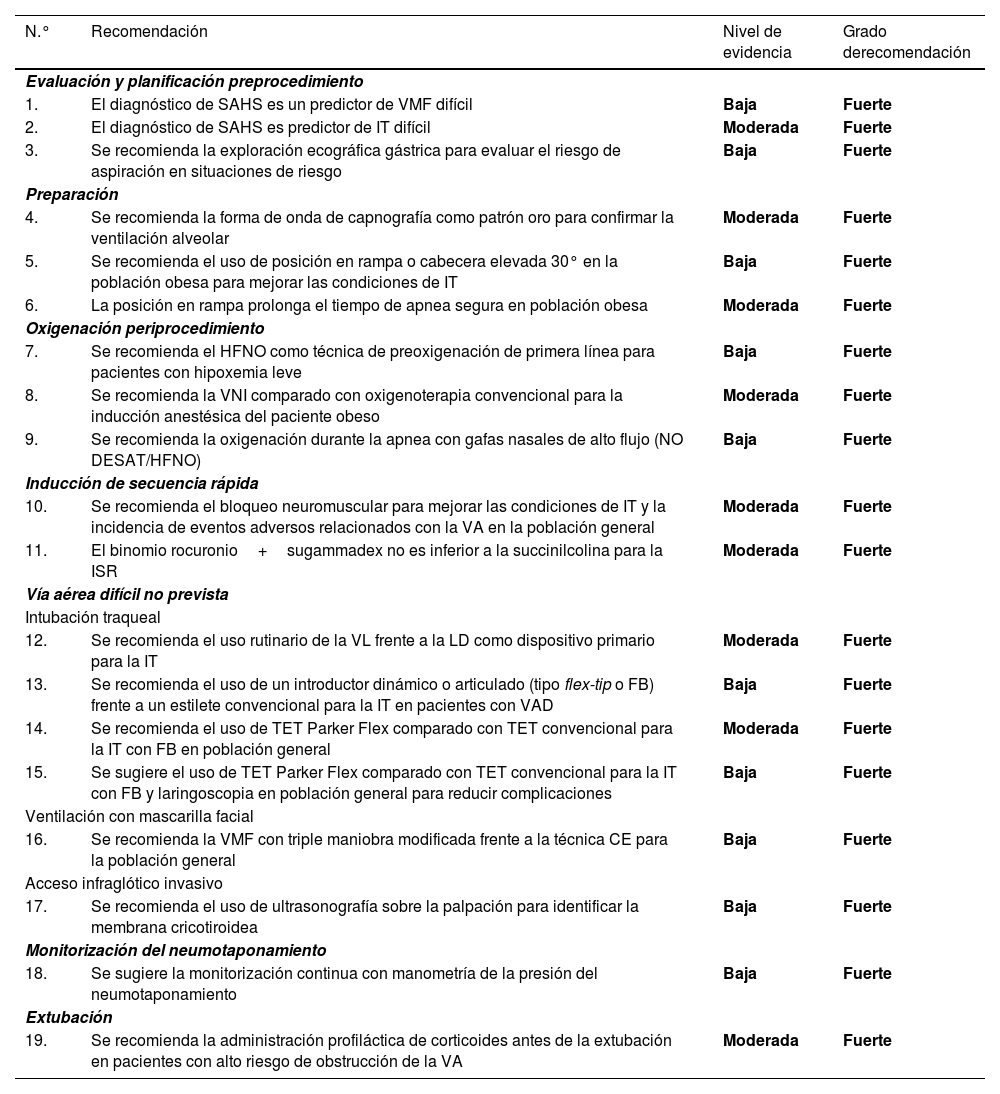
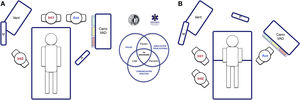
Una ayuda cognitiva es una herramienta dirigida a perfeccionar el funcionamiento cognitivo (memoria, percepción, atención, concentración, lenguaje) para mejorar las funciones ejecutivas como solución de problemas, planificación, razonamiento y control48. La figura 1 muestra la ayuda propuesta por la SEDAR, la SEMES y la SEORL-CCC para tratar una VAD no prevista. Su objeto principal es reducir la instrumentalización de la VA usando el menor número posible de intentos. Su diseño es contexto/específico y centrado en la toma de decisiones y los FFHH para manejar una crisis emergente. Consiste en una representación visual sencilla acorde con la evidencia disponible de la secuencia de pasos a seguir para asegurar la oxigenación alveolar de un paciente con una VAD no prevista.
La ayuda sigue la filosofía Vortex propuesta por Chrimes17 a la que se añade la simbología universal de los colores del semáforo.
Existen 4 categorías de técnicas para conservar o restituir la oxigenación alveolar. Tres no invasivas: IT, VMF y VDEG; y una invasiva: AII, necesaria cuando fracasan las tres estrategias no invasivas.
El número de intentos de cada plan de tratamiento no invasivo debe limitarse a 3 (D.E. 88,6%). El primer intento debe realizarse ya en condiciones óptimas para maximizar las posibilidades de éxito57–59. Cada nuevo intento exige el uso de un nuevo dispositivo o de nuevos métodos o adyuvantes que permitan optimizar la técnica previa. De no alcanzar el éxito en ninguno de ellos debe ser declarado verbalmente el «Fracaso del Plan» e iniciar un nuevo Plan. De fracasar los tres planes de técnicas no invasivas debe declararse sin demora la «situación NINO» y realizar un AII, último recurso para salvaguardar la oxigenación alveolar. Para garantizar una transición rápida, es recomendable abrir el equipo AII tras un primer intento fallido de VMF o VDEG.
El abordaje de una VA puede iniciarse seleccionando cualquiera de las 3 estrategias de oxigenación no invasiva. La selección de la técnica de primera línea, así como las técnicas de respaldo es sensible al contexto (condición del paciente, habilidad del operador, disponibilidad de asistencia cualificada, ubicación y equipo disponible, u hora del día). La seleccionada como primaria será denominada «Plan A». El fallo del primer intento exige declarar una «Vía Aérea Difícil No Prevista» y solicitar ayuda inmediata. De no alcanzar el éxito tras los 3 intentos del «Plan A» debe progresarse al «Plan B» y de fracasar al «Plan C» haciendo uso del esquema circular de técnicas no invasivas siguiendo un giro horario o antihorario desde el plan primario. La alternancia de planes sin agotar los intentos de cada uno es opcional.
Las alertas o signos centinela que fuerzan la transición entre técnicas son la ventilación deficiente o ausente, desaturación sensible al tiempo y/o signos clínicos de hipoxemia, así como el fracaso de un plan tras tres intentos fallidos.
La forma de onda de capnografía es el patrón oro para confirmar la ventilación alveolar. Debe estar disponible en todas las localizaciones donde se pueda efectuar un tratamiento de la VA para testar el éxito de cualquiera de los 4 planes empleados60. Para tal fin, recomendamos el uso de la clasificación propuesta por la Sociedad Japonesa de Anestesiólogos para evaluar la eficacia de la ventilación61. La figura 2 muestra una adaptación de la misma. Dicha clasificación permite diagnosticar de forma precisa y casi instantánea el estado de ventilación, que todos los integrantes del equipo compartan un modelo mental, una transición oportuna entre técnicas o planes y evitar errores de fijación. Los patrones de onda de capnografía son aplicables en cada ciclo respiratorio a pacientes en ventilación espontánea o mecánica a través de MF, DEG, TET o cánula infraglótica y permiten predecir una hipoxemia e hipercapnia severas. Una ventilación grado 2 o 3 obliga a cambiar de técnica o iniciar un nuevo plan más efectivo para mantener la oxigenación. La SEDAR, la SEMES y la SEORL-CCC recomiendan la declaración de capnografía «ausente» o «presente» para promover la consciencia situacional del equipo y generar acciones coordinadas.
Grados de ventilación según la forma de onda de la capnografía y su interpretación clínica. Vt: volume tidal.
Fuente: adaptada de Japanese Society of Anesthesiologists. JSA airway management guideline 2014: To improve the safety of induction of anesthesia. J Anesth. 2014;28:482-493.
Signos clínicos como la inspección de los movimientos torácicos o la auscultación pueden evaluarse de forma conjunta, aunque son menos fiables. Las mediciones del volumen corriente pueden ser más precisas y objetivas, aunque no se dispone de su monitorización en todas las localizaciones.
Los cambios en la saturación periférica de oxígeno (SpO2) proporcionan un feedback más tardío porque existe un período «silente» relativamente prolongado hasta la desaturación.
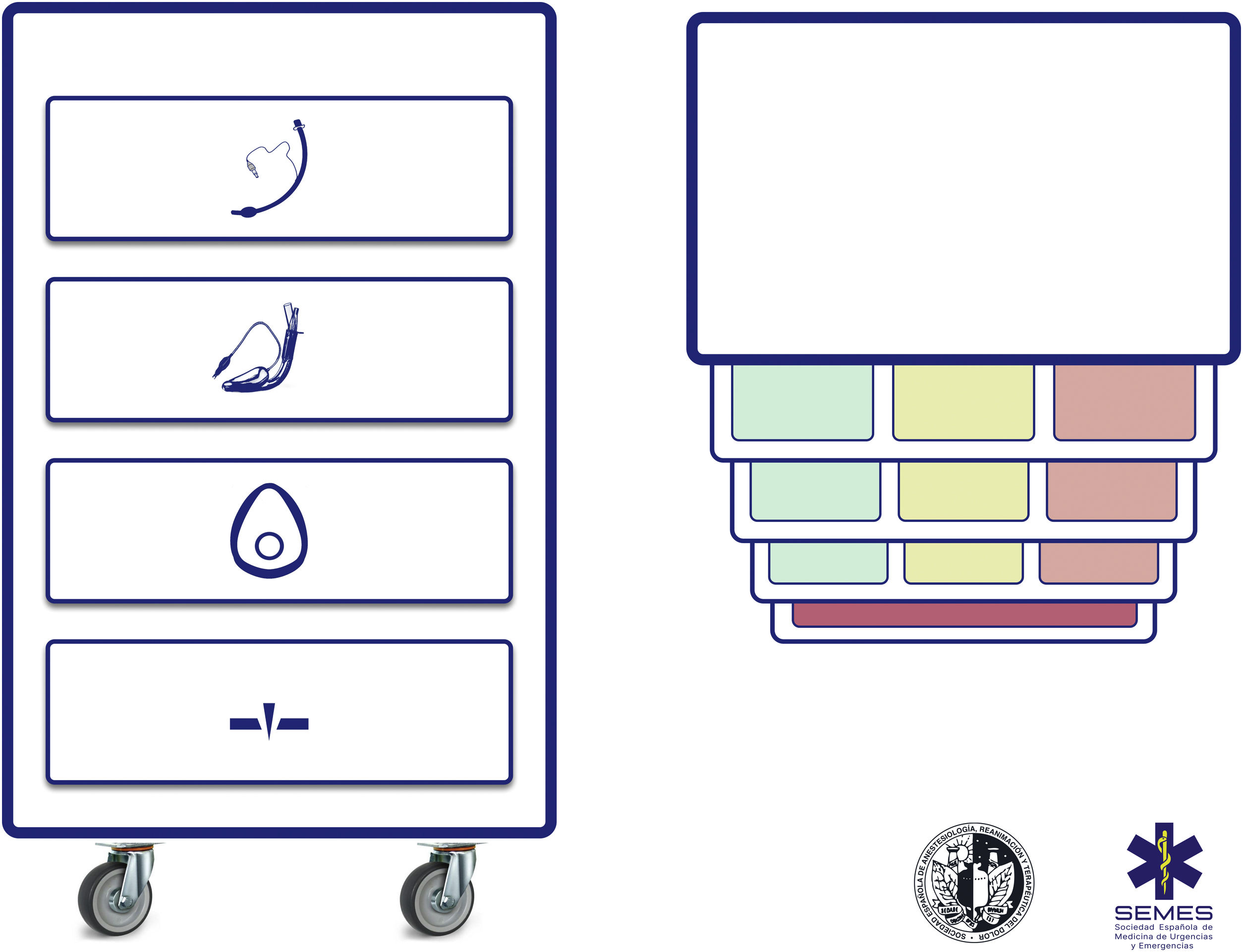
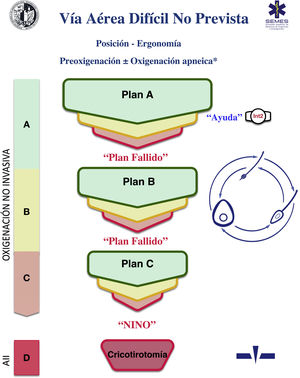
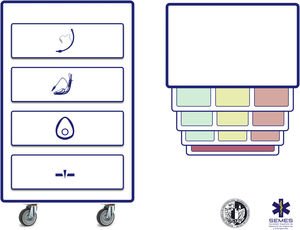
Carro de vía aérea difícilSe recomienda disponer de un carro de VAD estandarizado en las áreas donde se trata la VA (D.E. 100%). La figura 3 muestra el carro de VAD propuesto para complementar la ayuda cognitiva.
El NAP4 describió múltiples incidentes causados por la ausencia de material elemental para tratar la VA8,9. La rápida disponibilidad y presentación de los dispositivos necesarios para ejecutar los diferentes planes es un componente contextual clave62. Dichos dispositivos a menudo se incluyen en unidades portátiles fácilmente transportables63. Su estandarización ayuda a la adherencia a los algoritmos, promueve la consciencia situacional y la progresión secuencial a través del mismo, reducen el riesgo de retraso en la decisión y la sobrecarga cognitiva63.
La disposición del carro propuesto con la ayuda cognitiva integrada consta de 4 compartimentos etiquetados con pictogramas fácilmente reconocibles. Cada uno de los tres primeros alberga una categoría de técnicas de oxigenación alveolar no invasiva de las tres posibles. Cada compartimento, a su vez, se subdivide en 3 subcompartimentos (verde, ámbar y rojo) destinados a albergar los diferentes dispositivos y técnicas alternativas para cada categoría, así como estrategias de optimización, ordenados según si son primera (verde), segunda (ámbar) y tercera opción (rojo), categorizadas por color al igual que la ayuda cognitiva. Los carros basados en ayudas cognitivas integradas pueden mejorar la eficiencia en el tratamiento de la VAD64. La selección de la prioridad de cada alternativa dentro de una categoría puede estandarizarse en cada institución según los dispositivos existentes. Si la planificación para tratar una VAD prevista específica hace recomendable cambiar el orden de prioridad de la técnica dentro de cada categoría, el cambio se efectuará antes de iniciar el procedimiento, restituyendo el orden estándar tras finalizar el caso. El cuarto compartimento está reservado para albergar los sets de AII para rescatar una situación NINO.
Esta disposición del material de VA permite que la enfermería desarrolle de una forma más efectiva su papel crucial como asistente para preparar equipos alternativos cuando el operador todavía está ejecutando la opción precedente y ofrecerlos de inmediato en caso de fallo. Esto permite la anticipación, la transición sin demora entre técnicas y la prevención de la fijación de una técnica determinada64.
Idealmente, debe tenerse acceso al carro en menos de 1min desde cualquier ubicación en la que se trata la VA ante una posible crisis60,62. Además del acceso inmediato al equipo es crucial que todos los profesionales dispongan de la capacitación necesaria para el uso de cada uno de los dispositivos incluidos60,63. Se recomienda una inspección al menos semanal de contenido siguiendo una lista de verificación adjunta permanentemente al carro, y una adicional después de cada uso60.
Checklist preprocedimientoSe recomienda usar listados de verificación (checklist) para reducir la incidencia del error humano, mejorar el tiempo de ejecución de tarea y reforzar la cultura de seguridad en el manejo de la VA (D.E. 100%).
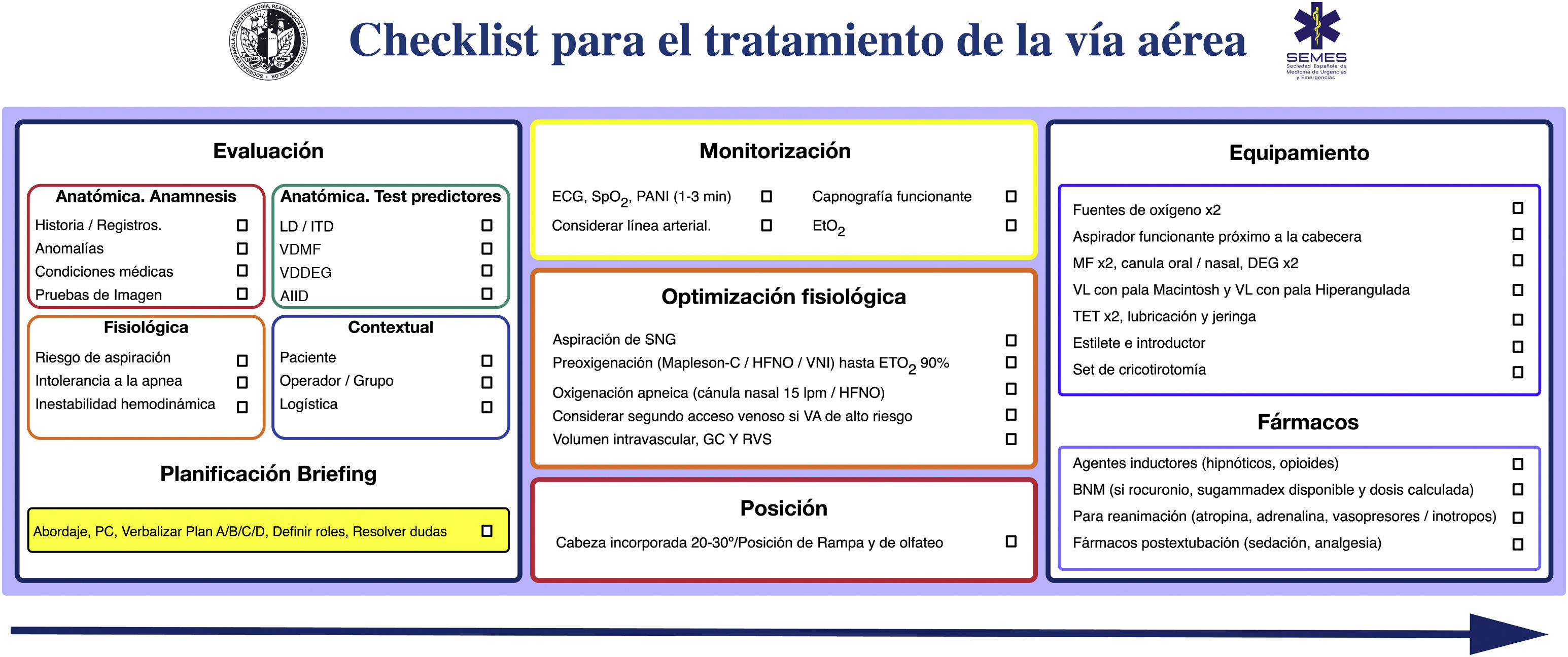
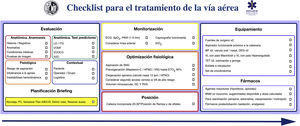
La seguridad del paciente es a menudo producto de una buena comunicación, el trabajo en equipo y la anticipación; la verificación es el eje que vincula estos factores65,66. Los listados de verificación permiten reducir la incidencia del error humano, mejorar el tiempo en el que se ejecutan las tareas y refuerzan una cultura de seguridad y «control»22,29,48,67. Son especialmente útiles en situaciones exigentes de gran carga de trabajo, en las que es probable desarrollar una «visión de túnel» (errores de fijación) y la omisión de pasos cruciales, así como en tareas rutinarias y repetitivas cuando la poca atención puede fomentar la complacencia y las desviaciones de los protocolos estándar65. Las revisiones sistemáticas de su uso en quirófano demuestran una reducción de las complicaciones y de la morbimortalidad, pero solo cuando los equipos participan y cuando el cumplimiento de los elementos es alto68,69. Asimismo, optimiza la anticipación, el debate proactivo, el trabajo en equipo y la comunicación eficaz65, mecanismos que podrían justificar la mejora de resultados70. Aunque el uso de un checklist para la IT no parece mejorar de forma consistente algunos resultados clínicos71,72, existe evidencia de su asociación con un menor número de eventos hipóxicos71. Se necesita mayor evidencia para definir su beneficio71. Pese a ello, se recomiendan ampliamente para el manejo de la VA73,74 como una herramienta cognitiva vital dentro de un programa de seguridad integral65. La figura 4 muestra el checklist «leer y hacer» pretratamiento de la VA propuesto por la SEDAR, la SEMES y la SEORL-CCC.
Checklist pretratamiento de la vía aérea de la SEDAR y la SEMES.
AIID: acceso infraglótico invasivo difícil; BNM: bloqueo neuromuscular; DEG: dispositivo extraglótico; ECG: electrocardiograma; EtO2: concentración de O2 al final de la espiración; HFNO: oxigenoterapia nasal de alto flujo; ITD: intubación traqueal difícil; LD: laringoscopia difícil; MF: mascarilla facial; PANI: presión arterial no invasiva; PC: presión cricoidea; SpO2: saturación periférica de oxígeno; TET: tubo endotraqueal; VDDEG: ventilación difícil con dispositivo extraglótico; VDMF: ventilación difícil con mascarilla facial; VL: videolaringoscopio; VNI: ventilación no invasiva.
Se recomienda el uso de modelos ergonómicos y de comunicación (D.E. 91,4%).
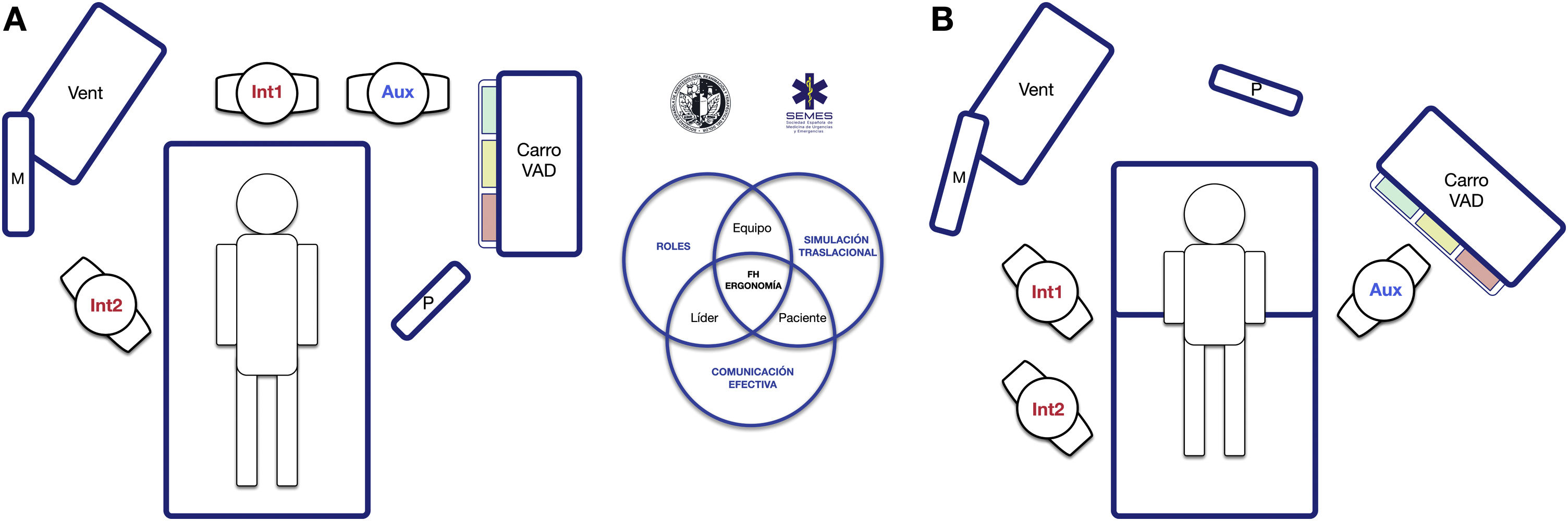
El entorno sociotécnico tiene un impacto significativo en la eficacia, la seguridad y la calidad asistencial75. Sistemas con diseños inapropiados han sido vinculados a errores, atención inadecuada y pérdida operacional76. Por ello, la planificación preintervención del espacio y la disposición de los recursos humanos y materiales es esencial para potenciar la consciencia situacional, la amplitud de movimientos y la respuesta rápida77. La figura 5 presenta 2 opciones ergonómicas para tratar la VAD que optimizan estos aspectos.
Ergonomía de la intubación traqueal hospitalaria (A) en una VAD no prevista tras la inducción anestésica (decúbito supino) y (B) en una VAD conocida o prevista en paciente despierto (posición sentada). En una intubación rutinaria suelen establecerse dos roles, operador (Int1) y ayudante (Aux). Ambos deben estar en línea para que la comunicación y la colaboración sea efectiva, así como con la pantalla (P) de los dispositivos empleados, la monitorización del paciente (M) y el respirador (Vent). En el caso de una VAD no prevista (A) se debe solicitar ayuda de inmediato, siendo recomendable que acuda un experto en VAD para que asuma el rol de segundo operador (Int2), y aproximar el carro de VAD al ayudante para que este pueda proporcionar los dispositivos necesarios al operador. El rol de líder podrá intercambiarse entre ambos. En el caso de una VAD prevista o conocida, el paciente despierto se dispondrá preferentemente en posición sentada (beneficio del efecto gravedad sobre la VA) con un segundo operador ya presente al inicio. El panel B muestra la disposición sugerida para una IT con FB. La asignación anticipada de los roles del equipo mejora la atención y la comunicación efectiva entre los integrantes, lo que permite optimizar los resultados de la intervención. El posterior debriefing y análisis del caso permitirá aplicar conceptos de simulación que mejorarán la siguiente atención realizada por el equipo.
El trabajo en equipo mejora los resultados y potencia una cultura de seguridad78–80. Los profesionales deben funcionar como unidad mediante la articulación eficaz de acciones individuales para alcanzar un objetivo común81. La figura del líder es clave para cohesionar los elementos25,80. Para ello, previamente debe informar al equipo sobre lo que se espera que suceda y sobre los planes seleccionados, asignar roles para simplificar el flujo de trabajo, y dirigir clara y explícitamente todo el procedimiento con la creación de modelos mentales compartidos22,80,82. Una comunicación eficaz y dinámica es esencial22,83. Debe basarse en la claridad, brevedad y empatía, reforzar la comunicación no verbal84 y permitir la participación y el feedback80,85, evitando ruido e información innecesaria ya que, de lo contrario, causa distracción y errores22,86.
Un evento crítico debe ser tratado por un operador cualificado y experto en el manejo de estas situaciones, no necesariamente el especialista más senior, sino aquel con amplio conocimiento en un determinado procedimiento avanzado. Debe ser avisado con la mayor antelación posible, y siempre tras el primer fallo del plan primario. A su llegada, tras ser informado sucintamente de la situación y de los planes ejecutados, debe ser resolutivo para evitar retrasos.
La disponibilidad del equipo y su ubicación estratégica es uno de los principales facilitadores para el éxito34. Los dispositivos con pantalla permiten compartir la evolución del procedimiento con todo el equipo, por lo que son recomendables para facilitar el trabajo coordinado y prestar apoyo dirigido anticipando las necesidades del operador87.
La ergonomía es altamente sensible al contexto. La pandemia COVID-19 ha evidenciado la importancia del trabajo en equipo, la comunicación y la adaptación de guías ante la irrupción de nuevas barreras88–90 como los equipos de protección individual (EPI) o las «cajas de intubación»91,92.
La herramienta nemotécnica ARACHNID simplifica todos los componentes de la ergonomía (Algoritmo, Resiliencia —adaptación y prevención del incidente crítico—, Ayudas cognitivas, Checklist, Herramientas técnicas, ayudas No técnicas, comunicación de Incidentes y Diseño del quirófano)93.
Evaluación y planificación preprocedimientoEvaluación generalSe recomienda la evaluación prepocedimiento en todo paciente que requiere un tratamiento de la VA (D.E. 100%).
La anticipación y la planificación son principios fundamentales en el manejo de una crisis. Así, la evaluación de la VA preprocedimiento constituye una práctica clínica habitual39. Los test de predicción de VAD actuales tienen un valor diagnóstico limitado e inconsistente39,94–100 ya que la gran mayoría están orientados a predecir exclusivamente la LD difícil99,101, y todos ellos tienen baja sensibilidad y bajo valor predictivo negativo, por lo que ninguno es adecuado para detectar una VAD no prevista39,96. El test de mordida es el que tiene mayor sensibilidad 0,67 (IC 95%: 0,45-0,83) para predecir la LD difícil, mientras que para la IT difícil es el Mallampati modificado (0,51 [0,40-0,61])39,96,98. La combinación de la puntuación de Mallampati y la distancia tiromentoniana proporciona la mayor precisión para predecir una IT difícil94. La mayoría de los estudios se han centrado en test individuales, a diferencia de la práctica clínica en la que se utilizan combinados97. Los modelos multivariantes podrían tener una mayor capacidad de predicción (D.E. 97,1%)44,102–108, pero han sido poco investigados, siendo el test de Wilson el más analizado98. El test MACOCHA106 que combina anatomía, fisiología y las características del operador es el único validado para el paciente crítico. Con todo, hasta el 93% de las IT difíciles son inesperadas53 y causan hasta el 17% de eventos adversos relacionados con el tratamiento de la VA109. Pese a ello, se recomienda la valoración rutinaria de la VA como estándar de atención, incluso en las situaciones emergentes51,96,110. Su importancia radica en que: 1) permite estratificar el riesgo y realizar una planificación ajustada39, con transiciones eficientes y el uso racional de recursos96,110, y 2) fomenta una cultura de seguridad al forzar el proceso cognitivo que exige la preparación ante una posible VAD no prevista97,99,110. Los estudios de morbilidad en VA indican los peligros de omitir la evaluación o ignorar sus hallazgos7–9. La falta de una evaluación documentada ha sido calificada en casos médico/legales como inferior al estándar de atención3.
La evaluación preprocedimiento de la VA debe ser multifactorial, estructurada y orientada a la detección de una VAD anatómica, fisiológica y contextual (D.E. 97,1%)25,97,111.
En lo posible, se recomienda realizar una historia clínica y un examen físico preprocedimiento51. Una anamnesis completa comienza con una revisión de registros de IT previas y la presencia de factores que pueden alterar la anatomía cervical o de la VA como radioterapia, cirugías o afecciones médicas previas112. El diagnóstico de SAHS es un predictor de VMF difícil (1C) e IT difícil (1B). Una historia de IT difícil es el factor de riesgo con mayor valor predictivo para una nueva IT difícil98,113. Se recomienda revisar cualquier prueba de imagen (TC, RNM); en caso de estenosis u obstrucción, proporciona información valiosa sobre su nivel y gravedad51,97,114. Ante una enfermedad obstructiva glótica o supraglótica conocida o sospechada, la exploración preoperatoria de la VA mediante fibronasolaringoscopia o videonasolaringoscopia flexible (FNL) por un otorrinolaringólogo es especialmente útil para la toma de decisiones115–117.
La exploración de la VA puede comenzar por la detección de predictores de dificultad o fallo para el plan primario y posteriormente para los 3 planes alternativos (D.E. 97,1%)97,118,119. Algunos expertos abogan por evaluar una posible AII difícil solo en caso de VAD51,97,120,121. En dicho supuesto, debe identificarse de forma preventiva la MCT mediante palpación120,122 y ecografía51,121; esta última permite realizar cricotirotomías con tasas de éxito superiores y menos complicaciones123.
La ecografía tiene un papel prometedor para la detección rápida de VAD124, con una precisión diagnóstica de IT difícil comparable a la TC y la radiografía, y muy superior a la del test de Mallampati modificado125,126. Es particularmente útil en la evaluación del riesgo de aspiración121,127–130 y de la VAD en pacientes inconscientes o que no cooperan99.
La existencia de una VAD fisiológica (VADF) o «fisiológicamente difícil»1,111,131,132 por la presencia de cambios fisiopatológicos que incrementan el riesgo de complicaciones durante la IT como tolerancia reducida al periodo de apnea, inestabilidad hemodinámica, acidosis metabólica severa o estómago lleno, así como una VAD contextual debido a un bajo grado de cooperación del paciente, situaciones de urgencia, experiencia y/o habilidades limitadas del operador, o la ausencia de asistencia cualificada o del dispositivo más indicado, pueden modificar el abordaje, por lo que deben ser tenidos en cuenta en la planificación1,25,97.
El resultado final de la evaluación debe ser el establecimiento de un plan definido de abordaje de la VA, que debe ser discutido y compartido con todo el equipo antes de iniciar el procedimiento. El mismo, debe incluir la preparación para tratar una VAD no prevista para todo paciente, aun en ausencia de predictores de dificultad97.
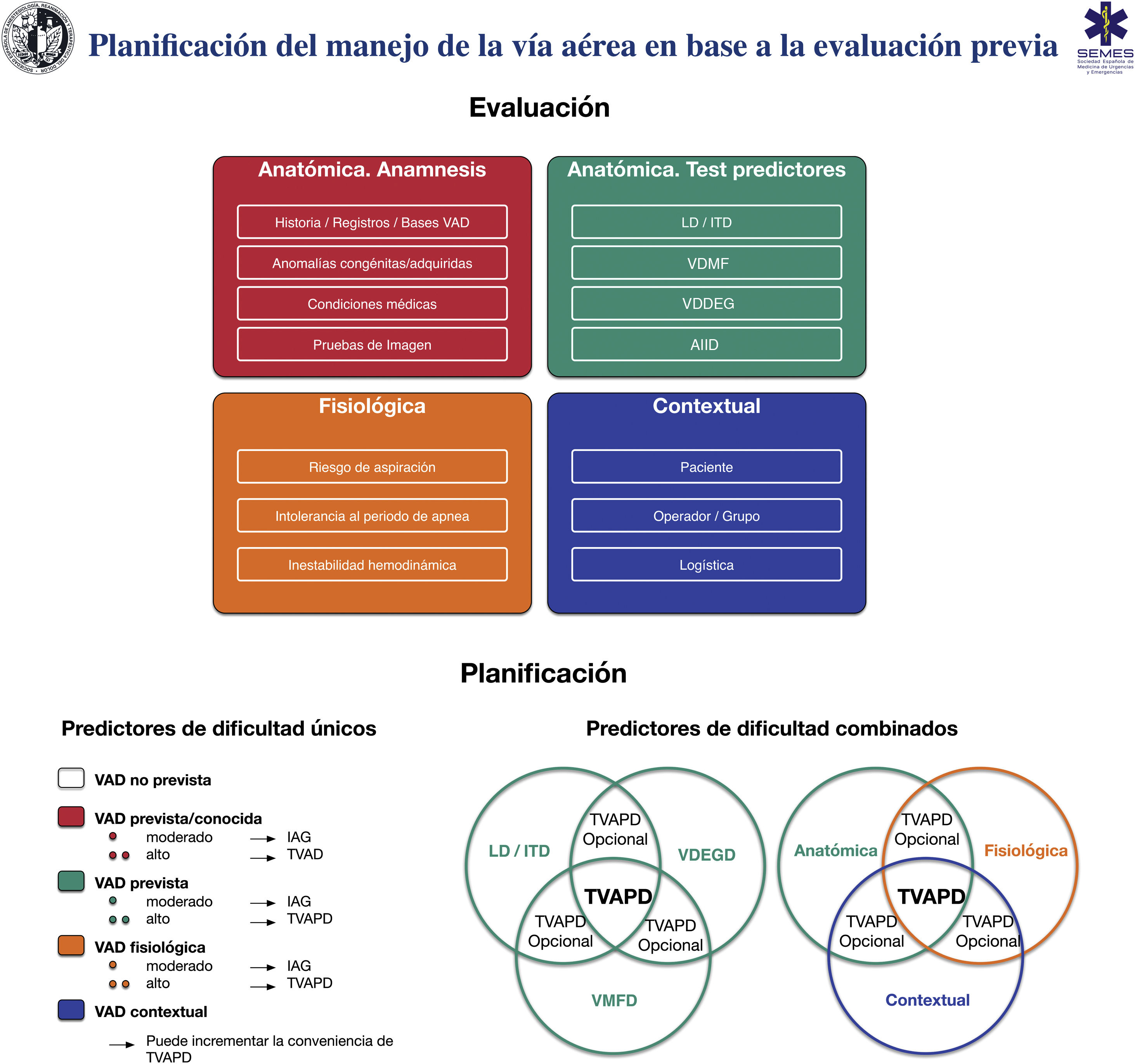
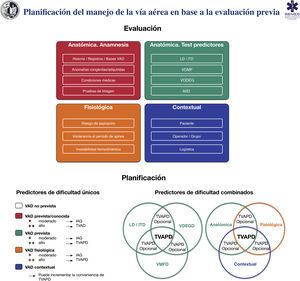
La figura 6 muestra una herramienta de implementación para la evaluación de la VA y la planificación de su manejo en base a la misma.
Herramienta de implementación para la evaluación de la vía aérea y planificación de su manejo. AIID: acceso infraglótico invasivo difícil; IAG: inducción anestesia general; ITD: intubación traqueal difícil; LD: laringoscopia difícil; TVAPD: tratamiento vía aérea con paciente despierto; VAD: vía aérea difícil; VDDEG: ventilación difícil con dispositivo extraglótico; VDMF: ventilación difícil con mascarilla facial.
Fuente: imágenes esféricas de la parte inferior de la figura adaptadas de Law JA, Heidegger T. Structured Planning of Airway Management, Core Topics in Airway Management, 3.ª edition. Edited by Cook T, Kristensen MS. Cambridge, Cambridge University Press, 2020, pp 38-49.
La toma de decisiones debe ser individualizada según paciente, operador, contexto y tiempo (D.E. 97,1%)119,133.
RecomendaciónEvaluación del riesgo de aspiraciónLa aspiración es la principal causa de mortalidad en VA134,135; causa hasta el 50% de las muertes8, por lo que su prevención constituye una piedra angular. La evaluación del riesgo y la planificación deficientes son la causa fundamental de estos eventos8. La adherencia a guías y ayudas cognitivas podría evitar la mayor parte de los casos136. El estómago lleno es el factor de riesgo principal135,137. Para evitarlo es necesaria la restricción de la ingesta de alimentos y líquidos siguiendo las pautas de ayuno preoperatorio (D.E. 97,1%)138; sin embargo, estas tienen una fiabilidad limitada en ciertas situaciones entre las que se encuentran134,137,139–141: 1) incumplimiento de las pautas de ayuno o estado prandial incierto (p. ej., urgencia, barrera lingüística, disfunción cognitiva); 2) enfermedades causantes de retraso del vaciado gástrico sintomático (p. ej., diabetes mellitus, disfunción hepática o renal avanzada, enfermedad de Parkinson, paciente crítico, activación simpática, dolor, administración crónica de opioides), y 3) aumento de la presión intraabdominal (obesidad mórbida de predominio troncular, ascitis, masas, obstrucción). Por ello, es recomendable completar estas pautas con una herramienta objetiva para aumentar el margen de seguridad141,142. La ecografía gástrica permite estratificar el riesgo individual con mayor precisión al constatar el carácter y volumen del contenido gástrico de forma simple139,141, no invasiva e inmediata, con una alta sensibilidad (1,0) y especificidad (0,975)139,143–145.
Pese a la limitada evidencia de su coste/efectividad, la ecografía gástrica ha demostrado que conduce a cambios en la toma de decisiones135,146. La ausencia de estómago lleno y de otros factores de riesgo indica que no se requieren precauciones especiales. Por el contrario, la presencia de estómago lleno con o sin factores de riesgo adicionales indica que la VA debe protegerse con una IT (D.E. 88,6%). El contexto clínico individual y el resto de factores de riesgo específicos para la aspiración deben ser tenidos en cuenta en la toma de decisiones119,147. La SEDAR, la SEMES y la SEORL-CCC recomiendan la exploración ecográfica gástrica para evaluar el riesgo de aspiración en situaciones de riesgo (1C)
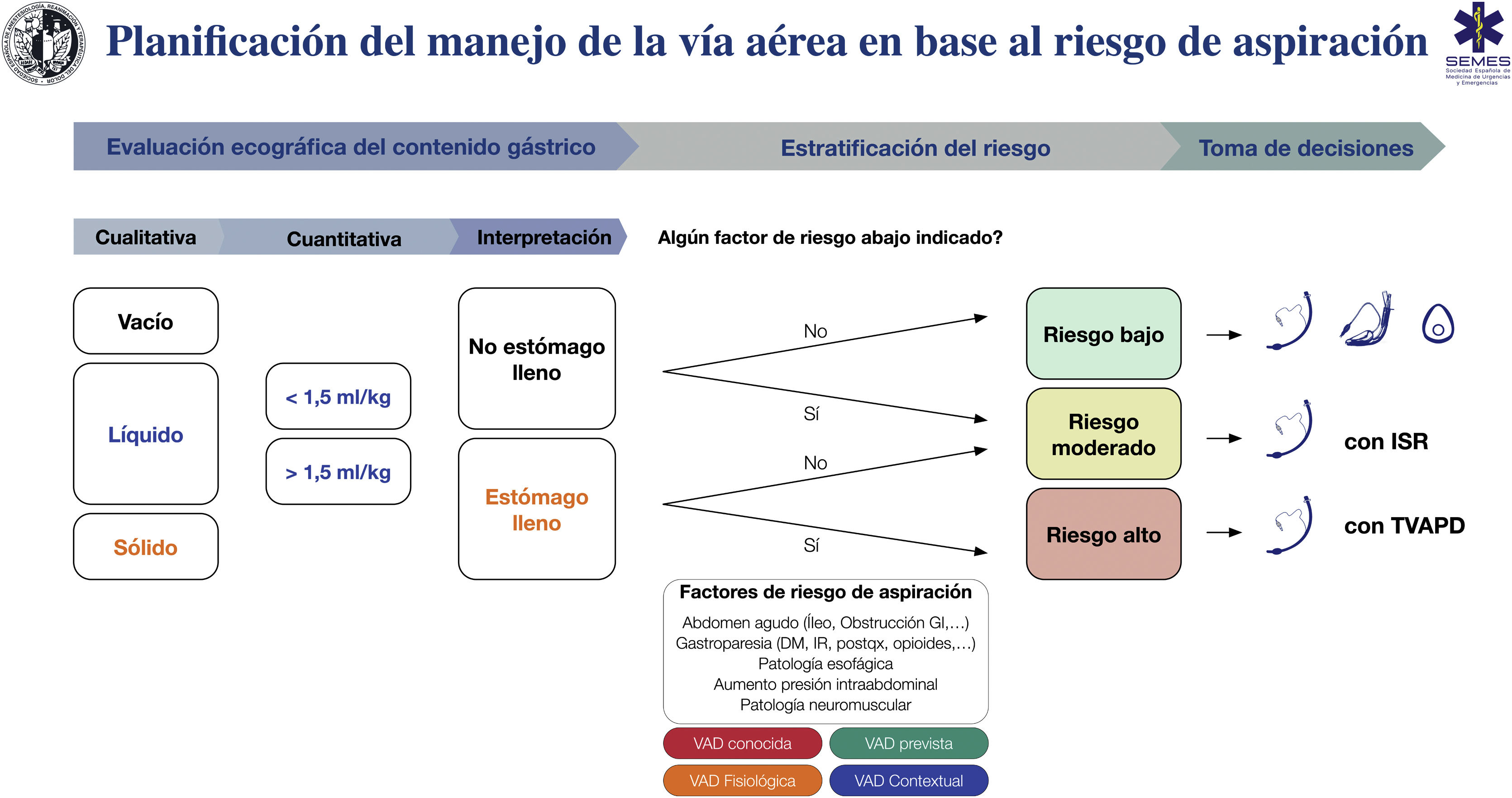
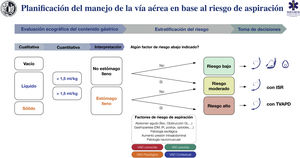
La figura 7 muestra una ayuda cognitiva para el tratamiento de la VA en base al riesgo de aspiración.
Ayuda cognitiva para la planificación, estratificación del riesgo y toma de decisiones para el manejo de la VA en base al riesgo de aspiración. DM: diabetes mellitus; GI: gastrointestinal; IR: insuficiencia renal; ISR: inducción de secuencia rápida; postqx: postoperatorio; TVAPD: tratamiento de la vía aérea con paciente despierto; VAD: vía aérea difícil.
El tratamiento de la VA conlleva riesgos6,148,149. La mayoría de las técnicas implican la supresión de la ventilación espontánea y la protección frente a la aspiración134,137. Las lesiones laríngeas ocurren con frecuencia tras instrumentaciones sencillas, en pacientes sanos de bajo riesgo, y tras procedimientos electivos3,19,150,151. Por lo tanto, antes de cada procedimiento debe evaluarse la pertinencia del tratamiento y realizar un análisis del balance riesgo beneficio (D.E. 97,1%). Confirmada la indicación, debe decidirse cuál es el mejor abordaje para garantizar los principios fundamentales de tratamiento: mantener la oxigenación alveolar, mantener la permeabilidad de la VA y minimizar el riesgo de aspiración. La preferencia del paciente y la habilidad del operador, deben ser considerados en esta decisión. Entre las opciones se encuentran110:
| Opción | Requisitos | Ventajas | Inconvenientes | Indicaciones | |
|---|---|---|---|---|---|
| Tratamiento con paciente despierto (TVAPD) | Adecuada anestesia tópica oral, orofaríngea, laríngea y traquealoBloqueos nerviosos±sedación consciente. | Preserva la ventilación espontánea, la permeabilidad de la VA y la protección frente a la aspiración.Facilita la identificación de las estructuras anatómicas.Impide que la laringe adopte una posición más anterior. | Requiere la colaboración y la tolerancia del paciente. | Técnica de elección para tratar la VAD prevista.Predictores de alta dificultad o imposibilidad de IT con laringoscopia y/o VMF, predictores de dificultad combinados o VAD fisiológica y contextual. | |
| InducciónAG | Preservación VE | Anestesia inhalatoria con sevoflurano a una CAM del 4,5%oMonoterapia con ketamina iv dosis disociativas. | Preserva el intercambio alveolar espontáneo de gases y los reflejos laríngeos. | No garantiza un Vm adecuado, la permeabilidad de la VA, o la protección frente a la aspiración.Mayor colapsabilidad de la VA. La aplicación de PEEP o CPAP ayuda a evitar el colapso. Importante morbilidad en VA críticamente obstruídas pudiendo conducir a una IT fallida y obstrucción completa.Educción lenta.Posibilidad de apnea, laringoespasmo, paroxismos de tos o regurgitación. | Cuando las características de la VA hacen recomendable un TVAPD, pero la AG es inevitable por falta de cooperación o la urgencia de la situación y no presenta predictores fisiológicos ni contextuales de dificultad.Se recomienda preparar un AII en paralelo (localización de la MCT, con equipo y personal capacitado preparado). |
| Abolición VE | Habitualmente consiste en una inducción intravenosa con BNM. | Condiciones óptimas para el manejo de la VA. | Durante el periodo de apnea y hasta asegurar la VA el operador debe mantener el intercambio de gases y la permeabilidad de la VA. | Cuando no se predice dificultad alguna o existe sospecha de dificultad moderada para laringoscopia, pero no presenta predictores de dificultad para el resto de planes ni VAD fisiológica ni contextual. | |
| Aplazamiento | Cuando el beneficio del aplazamiento supera el riesgo del tratamiento. | En un procedimiento anestésico, la anestesia regional o local puede ser una alternativa, manteniendo disponibles los planes de rescate de la VA en el caso de fracasar la técnica anestésica primaria. | Imposibilidad ante un procedimiento urgente. | Aplicable a una VAD fisiológica (enfermedad subyacente que requiere optimización) o contextual. | |
Se recomienda un tratamiento con paciente despierto cuando existe un grado alto de dificultad o imposibilidad de IT, predictores de dificultad combinados o alteraciones fisiológicas y condiciones contextuales negativas (D.E. 82,9%).
Se sugiere la inducción de anestesia general con preservación de la ventilación espontánea en aquellas situaciones que hacen recomendable un tratamiento con paciente despierto, pero la anestesia general es inevitable por falta de cooperación o urgencia, y no presenta predictores fisiológicos ni contextuales de dificultad ni patología obstructiva (D.E. 91,4%).
Cuando existan predictores de dificultad de VA fisiológicos o contextuales se podrá valorar el beneficio del aplazamiento si supera el riesgo de proceder al tratamiento, o valorar la posibilidad de establecer estrategias anestésicas alternativas (D.E. 85,7%).
PreparaciónConsentimiento informadoEl consentimiento informado es un presupuesto esencial de la lex artis ad hoc. Por regla general, se recaba por escrito en procedimientos invasivos y, en general, en aquellos que supongan riesgos para la salud, como los empleados para tratar la VA. Sin embargo, procedimientos como la IT forman parte de otro procedimiento como la anestesia general o de un protocolo de cuidados críticos de consentimiento informado152,153. Por lo tanto, no será necesario un documento específico, aunque sí la constancia documental de todos los elementos de la discusión y del proceso de consentimiento informado; en especial para procedimientos «no rutinarios», como el tratamiento de la VA con paciente despierto154.
En caso de exención para recabar el consentimiento informado153 se dejará constancia razonada de las circunstancias en la historia clínica y se comunicará la decisión a familiares o personas allegadas155. A menudo es posible tener una discusión abreviada.
MonitorizaciónPara el tratamiento de la VA, son aplicables los estándares de monitorización para un procedimiento anestésico156,157.
La forma de onda de capnografía debe estar disponible en todas las localizaciones donde se trata la VA para testar el éxito de cualquiera de los 4 planes empleados (D.E. 97,1%) para proporcionar una oxigenación alveolar158 y detectar de forma precoz el desplazamiento de cualquier VA artificial, así como una hiper o hipoventilación inadvertida1,6,9,159. También se recomienda su uso durante la sedación moderada o profunda para TVAPD.
La monitorización de la concentración de oxígeno al final de la espiración (EtO2) es el patrón oro para evaluar la eficacia de la preoxigenación160.
Se recomienda la monitorización neuromuscular si se administra un relajante neuromuscular para determinar condiciones óptimas para la IT, la recuperación del BNM y la necesidad de reversión durante la educción161,162.
La monitorización de la concentración de agentes anestésicos volátiles al final de la espiración es útil para realizar una inducción inhalatoria.
La monitorización hemodinámica invasiva avanzada puede ser necesaria para realizar una optimización guiada por objetivos preprocedimiento en caso de inestabilidad hemodinámica111,163.
PosiciónAsegurar el mejor posicionamiento antes de cualquier intervención permite optimizar las condiciones anatómicas y fisiológicas164. Así, una posición correcta maximiza las posibilidades de laringoscopia e IT, mejora la permeabilidad de la VA superior, optimizando la preoxigenación, la oxigenación apneica y la VMF165,166, el acceso a la misma (p. ej., acceso a la MCT) o la mecánica respiratoria. Se recomienda el uso de posición en rampa o cabecera elevada 30° en la población obesa para mejorar las condiciones de IT (1C). La posición en rampa prolonga el tiempo de apnea segura en esta población (1B).
La posición sentada o semisentada (de Fowler) o la cabeza incorporada 25-30° o posición de Trendelenburg inversa a 30°, es deseable en pacientes con un alto riesgo de desaturación o aspiración si el estado hemodinámico lo permite1,159,167,168, ya que incrementa la CRF, reduce la formación de atelectasias169,170, reduce el riesgo de aspiración159 y podría asociarse a mejor exposición laríngea171, mejores tasas de IT al primer intento172 y menos complicaciones173. La posición sentada o semisentada es óptima para el TVAPD al proporcionar ventajas anatómicas y fisiológicas174,175.
El conducto auditivo externo debe estar alineado con la horquilla supraesternal en el eje horizontal para facilitar el tratamiento de la VA1,176. En el caso del paciente obeso, para ello, es necesaria la posición «en rampa» usando una pila de sábanas o una cuña en la parte superior del torso y la cabeza40,177. La posición de «olfateo» (flexión cervical inferior y extensión cervical superior), es la óptima para la LD1,178,179. La IT con ambas posiciones no muestra diferencias180,181, aunque la exposición laríngea podría ser superior con la posición «en rampa» en la población quirúrgica181. La cabeza en hiperextensión podría ser la posición más apropiada para la IOT con FB con paciente despierto al asociarse a una mejor visión glótica182.
RecomendaciónSe recomienda el uso de posición en rampa o cabecera elevada 30° en la población obesa para mejorar las condiciones de intubación traqueal.
Recomendación fuerte; nivel de evidencia baja (⊕⊕⊝⊝),
La posición en rampa prolonga el tiempo de apnea segura en población obesa.
Recomendación fuerte; nivel de evidencia moderada (⊕⊕⊕⊝)
Dada la potencial dificultad para tratar la VA, la oxigenación periprocedimiento debe ser universal183 para incrementar la reserva pulmonar de oxígeno fundamentalmente a través de la CRF, y extender el tiempo de apnea sin desaturación184,185. Para ello es necesario elegir la técnica más adecuada en función de la fisiología, la cooperación y la situación clínica del paciente184.
PreoxigenaciónLa preoxigenación es un estándar de atención ya que amplía el tiempo de apnea seguro (período comprendido desde el cese de la ventilación hasta una saturación de oxihemoglobina arterial ≤90%)186. Por lo tanto, debe aplicarse a todos los pacientes; y de forma especialmente meticulosa en la VA con predictores de dificultad, pacientes con alto riesgo de hipoxemia o si la ventilación manual está contraindicada187. Así, es un componente esencial de la inducción de secuencia rápida (ISR)184.
El objetivo es alcanzar un EtO2>90% antes de iniciar la inducción anestésica184.
El método de preoxigenación convencional consiste en la ventilación espontánea con MF y oxígeno al 100% e incluye básicamente 2 técnicas: volumen corriente (VC) durante 3min y 8 capacidades vitales (8CV) durante 1min para IT de urgencia160,188. El flujo de oxígeno debe ser el apropiado para eliminar la reinhalación; 5l/min durante 3 a 5min para VC, y 10l/min durante 1min para 8CV 188. La presencia de fugas bajo la MF y la reinhalación de gases exhalados disminuye la eficacia al no alcanzarse una FiO2 de 1,0. La presencia de un trazo de capnografía normal (grado 1 de ventilación), una medida clara de los valores de CO2 inspiratorio y espiratorio (EtCO2), y el movimiento correcto de la bolsa reservorio son indicativos de un sellado apropiado184. En presencia de fuga, se recomienda agregar una cánula nasal con un flujo superior a 10l/min189,190.
Oxigenación apneicaLa oxigenoterapia nasal durante los esfuerzos para asegurar un TET (NO DESAT), la insuflación de oxígeno faríngeo y la oxigenoterapia nasal de alto flujo (HFNO) 40-70l/m186 pueden prolongar el tiempo de apnea hasta 100min, pero no previenen la acidosis respiratoria progresiva debido a la hipercapnia160,186,191,192. Las cánulas nasales estándar a 10-15l/min permiten una oxigenación apneica bien tolerada, de bajo coste y riesgo193.
La oxigenación apneica ha demostrado ser útil para reducir las desaturaciones en IT de urgencia160,194–198.
Se recomienda la oxigenación apneica con gafas nasales de alto flujo (NO DESAT/HFNO) (1C).
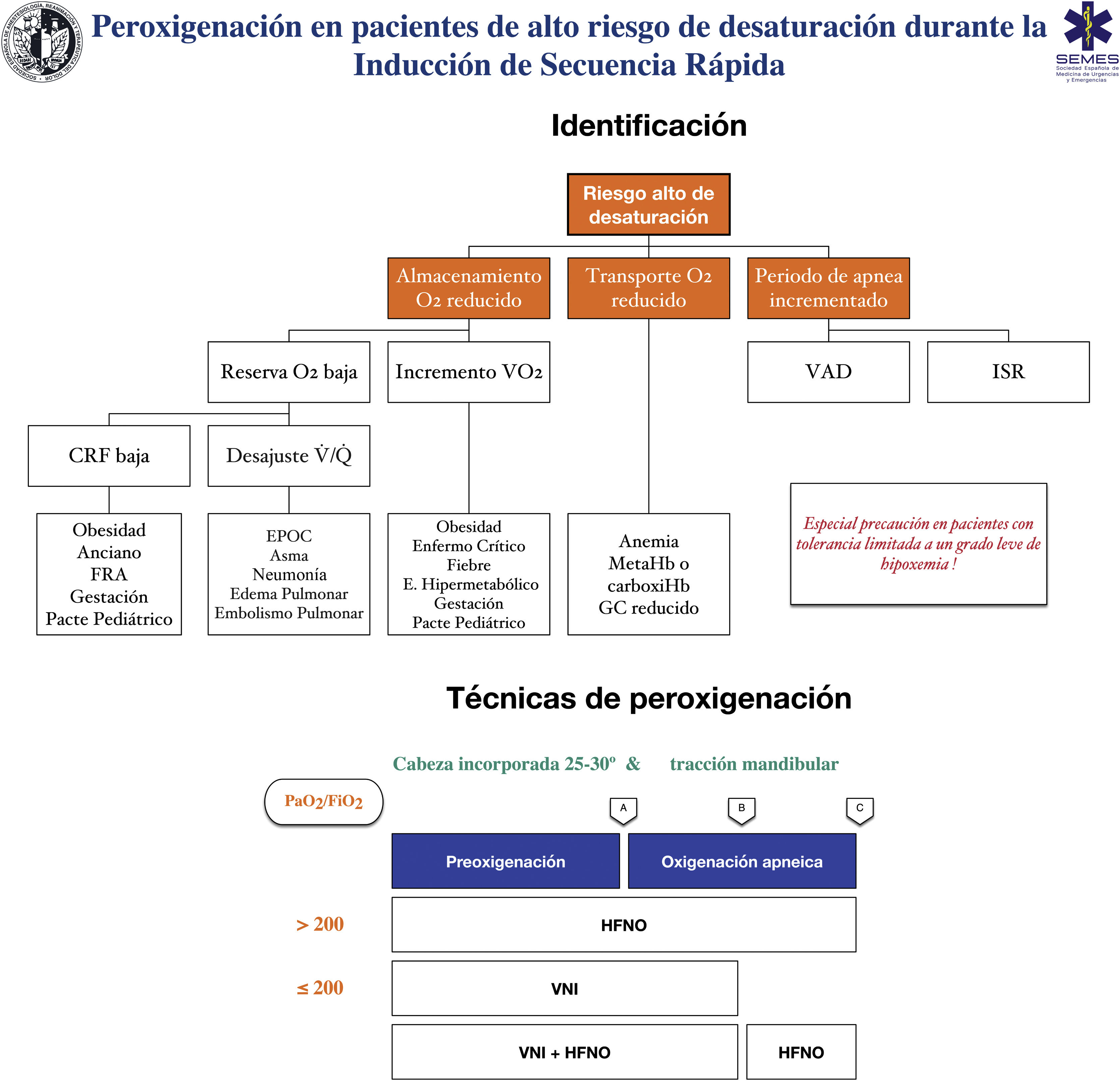
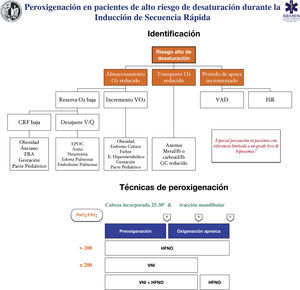
RecomendaciónTécnicas para pacientes con alto riesgo o escasa tolerancia a la hipoxemiaLa eficacia de las técnicas convencionales es limitada en pacientes con alto riesgo de hipoxemia (debido al shunt, el desajuste V/Q, baja CRF o al consumo de oxígeno incrementado que presentan) y tolerancia reducida a la misma (p. ej., enfermedad cerebrovascular, epilepsia o coronariopatía)199. Intentar compensar esta deficiencia aumentando el tiempo de preoxigenación puede incluso empeorar la hipoxemia, probablemente por atelectasias de reabsorción200. Asimismo, la ISR se asocia a desaturaciones en un 10-30% de los casos. Para planificar la preoxigenación es recomendable plantear las siguientes preguntas antes de iniciar el tratamiento201: ¿Es probable que haya dificultades con la ventilación y/o la IT? ¿Con qué rapidez se producirá la desaturación? ¿Cuál es el nivel seguro de desaturación? La figura 8 muestran las principales entidades asociadas a un alto riesgo de desaturación y las técnicas de oxigenación periprocedimiento recomendadas para esta población.
Herramienta teórico/educativa para la detección de pacientes con alto riesgo de desaturación y técnicas de preoxigenación y oxigenación apneica recomendadas durante la inducción de secuencia rápida. A: inducción anestésica; B: laringoscopia; C: intubación traqueal; CRF: capacidad residual funcional; Desajuste V /Q : desajuste ventilación/perfusión; EPOC: enfermedad pulmonar obstructiva crónica; GC: gasto cardíaco; FRA: fallo respiratorio agudo; HFNO: oxigenoterapia nasal de alto flujo; ISR: inducción de secuencia rápida; VNI: ventilación no invasiva; VO2: consumo de oxígeno.
Esta figura ilustra los 2 métodos utilizados para aumentar las reservas pulmonares de oxígeno: preoxigenación y oxigenación apneica. La preoxigenación se refiere al oxígeno aplicado antes de la inducción anestésica, mientras que la oxigenación apneica se refiere al suministro de oxígeno después de perder la ventilación espontánea.
Fuente: adaptada de Gómez-Ríos MA, Úbeda-Iglesias A, Esquinas AM. Anesthesiology Pre-intubation and upper airways procedure. Respiratory care in non invasive mechanical ventilatory support. principles and practice. Esquinas AM, AlAhmari MD. Nova Science Publishers. New York. 2021.
Cuanto mayor es el riesgo de desaturación, más opciones deben combinarse202. El uso de adyuvantes preapnea como la posición incorporada de la cabeza, la tracción mandibular, la PEEP y la oxigenación apneica permiten optimizar el reservorio de seguridad de O2160,167. La HFNO, la VNI o una combinación de ambas son más eficaces que los métodos convencionales203, ya que reducen el shunt y mejoran el desajuste V/Q mediente el reclutamiento alveolar. Se recomienda el HFNO como técnica de preoxigenación de primera línea para pacientes con hipoxemia leve (PaO2/FiO2>200mmHg) (1C). La VNI sería la técnica de elección en aquellos con hipoxemia severa (PaO2/FiO2≤200mmHg) (D.E. 87,15%)204–209 ya que genera mayor PEEP y permite aplicar presión soporte para aumentar la CRF210,211.
Oxígenoterapia nasal de alto flujo (HFNO)La preoxigenación con HFNO mostró resultados mixtos212–214. Un metaanálisis reciente demostró que en adultos con hipoxemia redujo el riesgo de complicaciones relacionadas con la IT en comparación con la oxigenoterapia convencional215. Así, la HFNO podría ser superior a esta216–220, pero inferior a la VNI215,221, aunque es una buena alternativa cuando la última no es bien tolerada168.
Para la preoxigenación, los pacientes deben realizar respiraciones nasales de VC a un flujo de O2 inicial de 30l/min y FiO2 100%, con la boca cerrada herméticamente durante 3min y con la cánula bien ajustada a las fosas nasales para evitar la contaminación. Tras la inducción, el flujo se incrementa a 70l/min y se mantiene hasta la IT. La permeabilidad de la VA debe mantenerse mediante tracción mandibular160,189.
La HFNO permite una oxigenación apneica eficaz durante la laringoscopia. Este podría ser su principal mecanismo de reducción de la desaturación194,222,223.
El HFNO dificulta la monitorización del EtO2192, podría empeorar las condiciones de IT224 y potencialmente causar una insuflación gástrica225. Investigaciones recientes contradicen esta última posibilidad226,227, aunque es incierto si estos datos son extrapolables a pacientes con estómago lleno225.
RecomendaciónLa VNI es especialmente beneficiosa en pacientes con CRF reducida212,228. Así, maximiza la preoxigenación en pacientes obesos y/o críticamente enfermos160,186,202. El efecto beneficioso sobre la PaO2 todavía se observa 30min tras la IT debido al reclutamiento alveolar y el aumento del volumen pulmonar229. Se recomienda la VNI comparado con oxigenoterapia convencional para la inducción anestésica del paciente obeso (1B).
Una CPAP (5 a 10cmH2O) con respiraciones asistidas (VC 7-10ml/kg) ha demostrado una mejor oxigenación en la clínica230. La VNI debe interrumpirse durante la laringoscopia228, por lo que puede ser superior al HFNO durante la fase de ventilación espontánea207, y el HFNO puede ser más beneficioso durante la oxigenación apneica204,205,210. La preoxigenación con VNI más HFNO y la oxigenación apneica con HFNO deben ser una opción prioritaria para los pacientes críticamente enfermos (D.E. 85,7%) al asociarse con una desaturación significativamente menor214,231,232.
Para pacientes que no toleren la interfase o con delirium se puede considerar la analgosedación con dexmedetomidina o la inducción de un estado disociativo con ketamina (bolos de 10-20mg iv) para facilitar la preoxigenación («intubación de secuencia retardada»)111,168,211,233.
Se recomienda considerar la VNI antes y después de la anestesia general (AG) en pacientes obesos199,234.
Presiones >20cmH2O pueden provocar distensión gástrica, por lo que exige un análisis riesgo beneficio en pacientes con riesgo de aspiración. Asimismo, es deseable otro método de preoxigenación en pacientes con fracturas faciales, tras una cirugía laríngea, esofágica o gástrica, y aquellos con inestabilidad hemodinámica, hipertensión arterial pulmonar, embolismo pulmonar o fallo ventricular derecho209.
RecomendaciónVía aérea difícil fisiológicaLas consideraciones de esta sección hacen referencia al paciente con VADF previamente definida o al paciente crítico235. El tratamiento de la VA urgente es un procedimiento de alto riesgo1,131,167,235–237. La incidencia de VAD en este contexto es hasta 20 veces mayor en comparación con las IT electivas238 y los eventos que causan muerte o daño cerebral son aproximadamente entre 30 y 60 veces más frecuentes10,239. Los trastornos fisiopatológicos subyacentes como la hipoxemia y la inestabilidad hemodinámica son los responsables de las descompensaciones periintubación que causan colapso cardiovascular hasta en el 30% de los pacientes críticos240,241 debido a la depresión miocárdica causada por hipoxia o baja perfusión241–243. Así, hasta el 50% de los pacientes críticos pueden sufrir un evento adverso importante periintubación243. Este riesgo se exacerba cuando la IT requiere más de un intento111,243,244. La IT difícil es un predictor independiente de muerte. Así, las tasas de complicaciones se multiplican por 5 después del segundo intento de IT245,246, por lo que el objetivo de asegurar la VA al primer intento es especialmente trascendente en el paciente crítico58,111,243,247,248.
La desaturación periintubación es el mayor factor de riesgo de parada cardiorrespiratoria y se produce en el 19-70% de las IT en paciente crítico 168. Se trata de la razón más importante para abordar la IT al primer intento168. La preoxigenación y la oxigenación apneica son las intervenciones más importantes para prevenirla248,249, por lo que deben efectuarse en todos los pacientes en posición incorporada168,235.
La inestabilidad hemodinámica es un predictor independiente de mortalidad tras IT235,250,251. La hipotensión periintubación168 afecta hasta el 46% de los casos de VADF252,253 y se asocia con estancias en la UCI más prolongadas, lesión de órganos diana y mayor mortalidad hospitalaria241,252,254. Entre los factores de riesgo preintubación se incluyen una PAM≤65mmHg y un índice de shock (IS, frecuencia cardíaca/presión arterial sistólica) >0,7168,235. Durante la IT del paciente crítico, el riesgo de colapso cardiovascular aumenta debido a la hipovolemia, la resistencia vascular sistémica alterada, vasodilatación y depresión miocárdica por agentes anestésicos, la estimulación simpática por hipoxia y/o hipercapnia, y la reducción del retorno venoso por la conversión a ventilación con presión positiva (VPP)167,240,242,255.
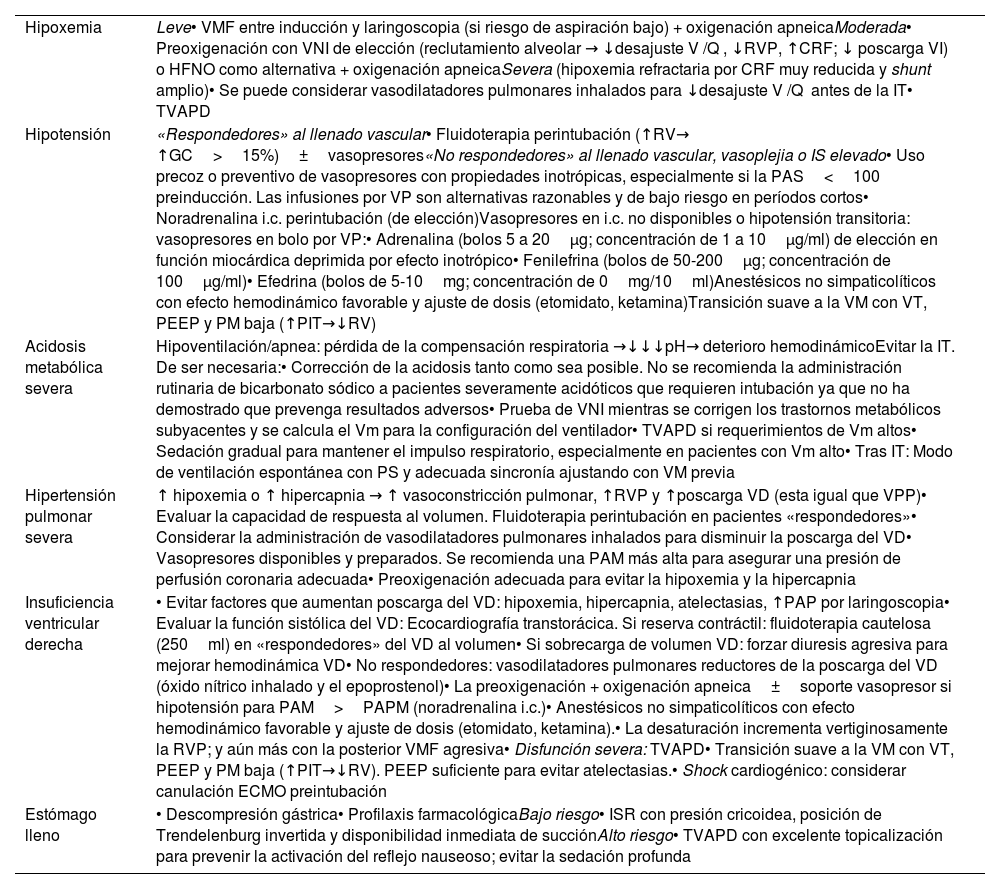
Las amenazas fisiológicas son, por lo tanto, tan peligrosas como las dificultades técnicas, por lo que exigen, de igual forma, anticipación, planificación y una optimización fisiológica preinstrumentalización si la situación específica lo permite1,256. La evidencia de las intervenciones destinadas a lograr la estabilidad fisiológica antes de la IT es limitada167,236,243, por lo que parece prudente planificar una terapia individualizada236. Si el tiempo lo permite, una exploración ecográfica en el punto de atención puede ser útil para realizar una optimización dirigida257. La tabla 1 muestra los principales factores predictores de una VADF y los métodos propuestos para reducir las complicaciones periintubación1,111,131,159,167,168,236,248,258.
Principales factores predictores de vía aérea difícil fisiológica y métodos propuestos para reducir las complicaciones periintubación derivadas
| Hipoxemia | Leve• VMF entre inducción y laringoscopia (si riesgo de aspiración bajo) + oxigenación apneicaModerada• Preoxigenación con VNI de elección (reclutamiento alveolar → ↓desajuste V /Q , ↓RVP, ↑CRF; ↓ poscarga VI) o HFNO como alternativa + oxigenación apneicaSevera (hipoxemia refractaria por CRF muy reducida y shunt amplio)• Se puede considerar vasodilatadores pulmonares inhalados para ↓desajuste V /Q antes de la IT• TVAPD |
| Hipotensión | «Respondedores» al llenado vascular• Fluidoterapia perintubación (↑RV→ ↑GC>15%)±vasopresores«No respondedores» al llenado vascular, vasoplejia o IS elevado• Uso precoz o preventivo de vasopresores con propiedades inotrópicas, especialmente si la PAS<100 preinducción. Las infusiones por VP son alternativas razonables y de bajo riesgo en períodos cortos• Noradrenalina i.c. perintubación (de elección)Vasopresores en i.c. no disponibles o hipotensión transitoria: vasopresores en bolo por VP:• Adrenalina (bolos 5 a 20μg; concentración de 1 a 10μg/ml) de elección en función miocárdica deprimida por efecto inotrópico• Fenilefrina (bolos de 50-200μg; concentración de 100μg/ml)• Efedrina (bolos de 5-10mg; concentración de 0mg/10ml)Anestésicos no simpaticolíticos con efecto hemodinámico favorable y ajuste de dosis (etomidato, ketamina)Transición suave a la VM con VT, PEEP y PM baja (↑PIT→↓RV) |
| Acidosis metabólica severa | Hipoventilación/apnea: pérdida de la compensación respiratoria →↓↓↓pH→ deterioro hemodinámicoEvitar la IT. De ser necesaria:• Corrección de la acidosis tanto como sea posible. No se recomienda la administración rutinaria de bicarbonato sódico a pacientes severamente acidóticos que requieren intubación ya que no ha demostrado que prevenga resultados adversos• Prueba de VNI mientras se corrigen los trastornos metabólicos subyacentes y se calcula el Vm para la configuración del ventilador• TVAPD si requerimientos de Vm altos• Sedación gradual para mantener el impulso respiratorio, especialmente en pacientes con Vm alto• Tras IT: Modo de ventilación espontánea con PS y adecuada sincronía ajustando con VM previa |
| Hipertensión pulmonar severa | ↑ hipoxemia o ↑ hipercapnia → ↑ vasoconstricción pulmonar, ↑RVP y ↑poscarga VD (esta igual que VPP)• Evaluar la capacidad de respuesta al volumen. Fluidoterapia perintubación en pacientes «respondedores»• Considerar la administración de vasodilatadores pulmonares inhalados para disminuir la poscarga del VD• Vasopresores disponibles y preparados. Se recomienda una PAM más alta para asegurar una presión de perfusión coronaria adecuada• Preoxigenación adecuada para evitar la hipoxemia y la hipercapnia |
| Insuficiencia ventricular derecha | • Evitar factores que aumentan poscarga del VD: hipoxemia, hipercapnia, atelectasias, ↑PAP por laringoscopia• Evaluar la función sistólica del VD: Ecocardiografía transtorácica. Si reserva contráctil: fluidoterapia cautelosa (250ml) en «respondedores» del VD al volumen• Si sobrecarga de volumen VD: forzar diuresis agresiva para mejorar hemodinámica VD• No respondedores: vasodilatadores pulmonares reductores de la poscarga del VD (óxido nítrico inhalado y el epoprostenol)• La preoxigenación + oxigenación apneica±soporte vasopresor si hipotensión para PAM>PAPM (noradrenalina i.c.)• Anestésicos no simpaticolíticos con efecto hemodinámico favorable y ajuste de dosis (etomidato, ketamina).• La desaturación incrementa vertiginosamente la RVP; y aún más con la posterior VMF agresiva• Disfunción severa: TVAPD• Transición suave a la VM con VT, PEEP y PM baja (↑PIT→↓RV). PEEP suficiente para evitar atelectasias.• Shock cardiogénico: considerar canulación ECMO preintubación |
| Estómago lleno | • Descompresión gástrica• Profilaxis farmacológicaBajo riesgo• ISR con presión cricoidea, posición de Trendelenburg invertida y disponibilidad inmediata de succiónAlto riesgo• TVAPD con excelente topicalización para prevenir la activación del reflejo nauseoso; evitar la sedación profunda |
CRF: capacidad residual funcional; Desajuste V /Q : desajuste ventilación/perfusión; ECMO: oxigenación por membrana extracorpórea; GC: gasto cardiaco; HFNO: oxigenoterapia nasal de alto flujo; i.c.: infusión continua; IS: índice de shock; IT: intubación traqueal; PAM: presión arterial media; PAP: presión arterial pulmonar; PAPM: presión arterial pulmonar media; PAS: presión arterial sistólica; PEEP: presión positiva al final de la espiración; PIT: presión intratorácica; PM: presión media; PS: presión soporte; RV: retorno venoso; RVP: resistencias vasculares pulmonares; TVAPD: tratamiento de la vía aérea con paciente despierto; VD: ventrículo derecho; VI: ventrículo izquierdo; VM: ventilación mecánica; Vm: volumen minuto; VMF: ventilación con mascarilla facial; VNI: ventilación no invasiva; VP: vía venosa periférica; VPP: ventilación con presión positiva; VT: volumen tidal.
La fluidoterapia en forma de bolo preintubación tiene un beneficio mínimo240,259, aunque administrado como parte de un paquete de medidas para la IT, entre ellas preoxigenación con VNI, administración preinducción de 500ml de cristaloides isotónicos en pacientes sin edema pulmonar cardiogénico e inicio temprano de noradrenalina en caso de presión arterial diastólica <35mmHg tras la IT, se asoció a reducción relativa del 50% de colapso cardiovascular e hipoxemia grave260, por lo que podría prevenir la hipotensión periprocedimiento. Sin embargo, podría no estar justificado la administración rutinaria de un bolo de cristaloides preinducción en pacientes que no reciben VPP ya que solo mostró beneficio en el subgrupo de pacientes que recibieron VNI para la preoxigenación o VMF entre la inducción y la laringoscopia, mientras que podría ser perjudicial en el resto de la población no respondedora al volumen240. La implementación de un protocolo de IT podría reducir estas complicaciones260–262.
Aunque su eficacia para evitar la hipotensión periintubación todavía no ha sido establecida248,255, se sugiere la administración preventiva o el inicio precoz de vasopresores211 y que un operador experto se encargue de tratar la VA mientras que otro miembro del equipo lidere el manejo del estado hemodinámico1,168,243. La infusión de noradrenalina seria la terapia vasoactiva de primera línea168,235. La administración inicial a través de cánulas venosas periféricas es segura263,264, por lo que el inicio de vasopresores no requiere un acceso venoso central235.
Inducción de secuencia rápidaLa IT es el patrón oro para asegurar la VA y la ISR es la técnica recomendada cuando existe un riesgo considerable de aspiración en una VA sin predictores de dificultad (D.E. 97,1%)265,266. Sus componentes (descompresión gástrica, preparación previa, posición adecuada, oxigenación periprocedimiento, inducción anestésica y presión cricoidea en casos seleccionados) están diseñados para223,267–269: 1) acortar el intervalo de tiempo entre la pérdida de los reflejos protectores y el sellado traqueal mediante el neumotaponamiento del TET; 2) lograr condiciones óptimas para una IT exitosa al primer intento con una profundidad anestésica y un BNM adecuado para evitar tos, vómitos activos o aumento de la presión intraabdominal265, y 3) minimizar los riesgos secundarios a su uso, fundamentalmente hipoxia, hipotensión e IT difícil. Su práctica está sustentada en escasa evidencia266,268,270–273 y puede asociarse a resultados nocivos266,274,275, por lo que debe estar justificado con indicaciones claras22,268. El punto clave es identificar a los pacientes con riesgo de aspiración (fig. 7). En caso de duda o de no ser factible una ecografía gástrica debe asumirse el riesgo más alto268. Asimismo, se recomienda usar ISR con o sin maniobra de Sellick en todas las IT de urgencia (D.E. 84,4%) dado el característico vaciado gástrico deficiente y el alto riesgo de aspiración en el paciente crítico frágil223,268,276.
Para la preparación segura de la ISR se sugiere el uso de checklist (D.E. 97,1%). El uso de checklist (fig. 4) podría reducir la tasa de complicaciones71,277–279 al minimizar la carga cognitiva y los errores, y mejorar la seguridad mediante un enfoque estandarizado223,235,266,280.
Para los pacientes con alto riesgo se sugiere la premedicación con un antiácido no particulado (p. ej., citrato de sodio) inmediatamente antes de la inducción y un antagonista del receptor H2 o un inhibidor de la bomba de protones 40-60min antes para aumentar el pH y reducir el volumen del contenido gástrico (D.E. 82,9%)265,281.
El tratamiento con sonda nasogástrica debe ser individualizado (D.E. 88,6%) ya que no existe base científica265,282. Se suele insertar si el volumen gástrico residual esperado o evaluado ecográficamente excede los 200-300ml265,268. El vaciado gástrico con sonda de doble luz tipo Salem es obligatorio durante el tratamiento preoperatorio de pacientes con íleo u obstrucción intestinal265,283,284. La descompresión gástrica debe iniciarse lo antes posible en la planta quirúrgica y proseguir en el periodo preinducción y preeducción267,284. La sonda debe mantenerse en aspiración continua durante la ISR265,284,285.
La preparación para la ISR incluye la evaluación de los posibles desafíos anatómicos, fisiológicos o situacionales, desarrollar un plan primario y de rescate con instrucciones claras y reunir el personal, el equipo y los fármacos necesarios para realizar una IT de urgencia223,266,286. Ante una posible regurgitación debe garantizarse la disponibilidad de dispositivos de succión de alta eficiencia con sondas de gran calibre multiorificio (D.E. 100%) tipo Yankauer o DuCanto223,287.
Se recomienda una posición con cabeza elevada 20-30° (posición sentada o semisentada o Trendelenburg inverso) para prevenir la regurgitación pasiva y, en caso de producirse, la posición de Trendelenburg, girar la cabeza hacia un lado y aspirar la orofaringe y la tráquea antes de iniciar la VPP (D.E. 94,3%)267,288.
Es esencial que una preoxigenación y oxigenación apneica óptimas, así como una optimización hemodinámica individualizada precedan a la inducción223,286. La selección del anestésico hipnótico ha sido descrita como el único factor asociado de forma independiente con la inestabilidad y/o el colapso cardiovascular289, por lo que tiene especial trascendencia255. La elección del agente hipnótico, así como la dosis y la velocidad de administración debe ser individualizada (D.E. 91,4%), según el perfil de comorbilidad, estado hemodinámico del paciente y la rapidez con que se precise asegurar la VA223,266. El propofol (2-3mg.kg-1) es el agente de elección en el paciente euvolémico hemodinámicamente estable ya que posibilita las mejores condiciones de intubación265,274,276. En el paciente inestable puede aumentar las complicaciones hemodinámicas y el riesgo de muerte243, y ha sido identificado como factor de riesgo independiente para colapso hemodinámico perintubación289. Estos datos sugieren que debería ser evitado en el paciente crítico con inestabilidad hemodinámica potencial255. El etomidato (0,2-0,3mgkg-1) y la ketamina (1-2mgkg-1 iv) son alternativas ante inestabilidad hemodinámica275,286. La ketamina puede producir un colapso hemodinámico en el paciente con reserva simpática agotada (p. ej., shock hipovolémico severo) como resultado de su efecto depresor miocárdico directo leve290. Debe evitarse en enfermos con isquemia miocárdica aguda223,291. El uso de etomidato puede estar asociado con un menor riesgo de hipotensión postinducción en comparación con la ketamina290. En enfermos agitados y no colaboradores puede realizarse una inducción de secuencia retardada, que consiste en la administración de ketamina en bolos de 0,25-0,5mg.kg-1 hasta un estado disociativo, tras lo cual se procede a la preoxigenación y la posterior administración del relajante neuromuscular233,292–294.
Aunque la ISR clásica no incluía la administración de un opioide, actualmente el uso de alfentanilo (15-40μg.kg-1), remifentanilo (1μg.kg-1) y fentanilo (2-5μg.kg-1) es práctica común ya que disminuye la dosis necesaria del hipnótico, promueve la estabilidad hemodinámica al atenuar la respuesta cardiovascular a la laringoscopia y mejora las condiciones de intubación265,271,283,285, sin ocasionar excesiva hipotensión y bradicardia275,283,295.
La administración de un relajante neuromuscular constituye la piedra angular286, ya que mejora las condiciones de IT, suprime la tos y el laringoespasmo, disminuye las complicaciones y optimiza la distensibilidad de la pared torácica296,297. Se recomienda el bloqueo neuromuscular para mejorar las condiciones de IT y reducir la incidencia de eventos adversos relacionados con la VA en la población general (1B).
El rocuronio 1,0-1,2mg.kg-1 es comparable con la succinilcolina 1,0-1,5mg.kg-1 para la ISR269,298–300, tiene un perfil clínico más seguro, ofrece un bloqueo más duradero266, y puede ser revertido más rápidamente que la succinilcolina con el sugammadex (16mg.kg-1)301; la dosis de rescate debe ser precalculada y estar inmediatamente disponible para una reversión de urgencia266,302. La succinilcolina puede causar hipertermia maligna, hiperpotasemia y las fasciculaciones musculares ocasionadas incrementan la presión intragástrica y acortan el tiempo de apnea303,304. En conjunto, el uso de rocuronio se ve cada vez más favorecido235,303–305. El binomio rocuronio+sugammadex no es inferior a la succinilcolina para la ISR (1B). No se recomienda la técnica de precurización o priming, por su eficacia y seguridad cuestionables dado el riesgo de pérdida de reflejos protectores265,306.
El uso de la presión cricoidea es objeto de controversia265,268,295. La maniobra no ha demostrado evitar la aspiración307–309, es biomecánicamente imposible mantener la presión recomendada310 y su empleo produce una reducción del tono del esfínter esofágico inferior311. Igualmente puede contribuir a la obstrucción de la VA270, dificultar la laringoscopia y la IT309, la VMF312, la inserción, la ventilación e IT a través de un DEG313 y dificultar la visualización de la glotis con FB314, pudiendo prolongar los tiempos de IT309,315. Por todo ello, no se puede recomendar el uso rutinario de la presión cricoidea (D.E. 81,3%)223,260,286,316,317, debe planificarse de forma individualizada y ser aplicada cuando es necesaria la VMF durante el periodo de apnea286, ya que previene la insuflación gástrica318. En los casos indicados debe: 1) aplicarse correctamente: 1kg (10N) hasta la pérdida de la consciencia y posteriormente 3kg (30N) hasta la instauración del neumotaponamiento del TET265,317 y 2) liberarse en caso de dificultar la laringoscopia, la IT o la ventilación, antes de insertar un DEG o en caso de vómito activo.
La oxigenación apneica se asocia a menor prevalencia de desaturación y un mayor éxito de IT al primer intento196,319–321. Se puede aplicar una «ISR modificada» en pacientes con alto riesgo de hipoxia no candidatos a un TVAPD (D.E. 85,7%)322 consistente en la VMF bimanual o mecánicamente con una presión inspiratoria limitada (<15cmH2O sin presión cricoidea o a <20cmH2O con presión cricoidea) sopesando los riesgos/beneficios potenciales individualizados132,159,223,266,268,318,323,324. Esta práctica excluyendo a pacientes de alto riesgo de aspiración se asoció a una prevalencia significativamente menor de desaturación sin afectar negativamente a las tasas de aspiración325,326.
Para la IT se recomienda utilizar el laringoscopio y la pala con más probabilidades de éxito al primer intento. No hay evidencia que respalde un dispositivo específico. La elección dependerá de la situación clínica y la preferencia del operador266. La VL con estilete podría ser la mejor opción211,327–330.
RecomendaciónSe recomienda el bloqueo neuromuscular para mejorar las condiciones de IT y reducir la incidencia de eventos adversos relacionados con la VA en la población general.
Recomendación fuerte; nivel de evidencia moderada (⊕⊕⊕⊝)
El binomio rocuronio+sugammadex no es inferior a la succinilcolina para la ISR
Recomendación fuerte; nivel de evidencia moderada (⊕⊕⊕⊝)
Las estrategias de búsqueda y las tablas GRADE se muestran en material suplementario.
FB: fibrobroncoscopia; HFNO: oxigenoterapia nasal de alto flujo; ISR: Inducción de secuencia rápida; IT: intubación traqueal; LD: laringoscopia directa; NO DESAT: oxigenoterapia nasal durante los esfuerzos para asegurar un TET; SAHS: Síndrome de apneas-hipopneas del sueño; TET: tubo endotraqueal; VA: vía aérea; VL: videolaringoscopia; VNI: ventilación no invasiva.
| N.° | Recomendación | Nivel de evidencia | Grado derecomendación |
|---|---|---|---|
| Evaluación y planificación preprocedimiento | |||
| 1. | El diagnóstico de SAHS es un predictor de VMF difícil | Baja | Fuerte |
| 2. | El diagnóstico de SAHS es predictor de IT difícil | Moderada | Fuerte |
| 3. | Se recomienda la exploración ecográfica gástrica para evaluar el riesgo de aspiración en situaciones de riesgo | Baja | Fuerte |
| Preparación | |||
| 4. | Se recomienda la forma de onda de capnografía como patrón oro para confirmar la ventilación alveolar | Moderada | Fuerte |
| 5. | Se recomienda el uso de posición en rampa o cabecera elevada 30° en la población obesa para mejorar las condiciones de IT | Baja | Fuerte |
| 6. | La posición en rampa prolonga el tiempo de apnea segura en población obesa | Moderada | Fuerte |
| Oxigenación periprocedimiento | |||
| 7. | Se recomienda el HFNO como técnica de preoxigenación de primera línea para pacientes con hipoxemia leve | Baja | Fuerte |
| 8. | Se recomienda la VNI comparado con oxigenoterapia convencional para la inducción anestésica del paciente obeso | Moderada | Fuerte |
| 9. | Se recomienda la oxigenación durante la apnea con gafas nasales de alto flujo (NO DESAT/HFNO) | Baja | Fuerte |
| Inducción de secuencia rápida | |||
| 10. | Se recomienda el bloqueo neuromuscular para mejorar las condiciones de IT y la incidencia de eventos adversos relacionados con la VA en la población general | Moderada | Fuerte |
| 11. | El binomio rocuronio+sugammadex no es inferior a la succinilcolina para la ISR | Moderada | Fuerte |
| Vía aérea difícil no prevista | |||
| Intubación traqueal | |||
| 12. | Se recomienda el uso rutinario de la VL frente a la LD como dispositivo primario para la IT | Moderada | Fuerte |
| 13. | Se recomienda el uso de un introductor dinámico o articulado (tipo flex-tip o FB) frente a un estilete convencional para la IT en pacientes con VAD | Baja | Fuerte |
| 14. | Se recomienda el uso de TET Parker Flex comparado con TET convencional para la IT con FB en población general | Moderada | Fuerte |
| 15. | Se sugiere el uso de TET Parker Flex comparado con TET convencional para la IT con FB y laringoscopia en población general para reducir complicaciones | Baja | Fuerte |
| Ventilación con mascarilla facial | |||
| 16. | Se recomienda la VMF con triple maniobra modificada frente a la técnica CE para la población general | Baja | Fuerte |
| Acceso infraglótico invasivo | |||
| 17. | Se recomienda el uso de ultrasonografía sobre la palpación para identificar la membrana cricotiroidea | Baja | Fuerte |
| Monitorización del neumotaponamiento | |||
| 18. | Se sugiere la monitorización continua con manometría de la presión del neumotaponamiento | Baja | Fuerte |
| Extubación | |||
| 19. | Se recomienda la administración profiláctica de corticoides antes de la extubación en pacientes con alto riesgo de obstrucción de la VA | Moderada | Fuerte |
AII: acceso infraglótico invasivo; BNM: bloqueo neuromuscular; CI: consentimiento informado; DEG: dispositivo extraglótico; DEG2G: dispositivo extraglótico de segunda generación; ECMO: oxigenación por membrana extracorpórea; EtCO2: concentración de dióxido de carbono al final de la espiración; EtO2: concentración de oxígeno al final de la espiración; FB: fibrobroncoscopia; FiO2: fracción inspiratoria de oxígeno; HFNO: oxigenoterapia nasal de alto flujo; ISR: inducción de secuencia rápida; IT: intubación traqueal; LD: laringoscopia directa; PaO2: presión parcial arterial de oxígeno; SpO2: saturación periférica de oxígeno; TET: tubo endotraqueal; TVAPD: tratamiento de la VA con paciente despierto; VA: vía aérea; VAD: vía aérea difícil; VDEG: ventilación con dispositivo extraglótico; VL: videolaringoscopia; VMF: ventilación con mascarilla facial; VNI: ventilación no invasiva.
| N.° | Cuestión | Porcentaje a favor [A favor; neutral; en contra] |
|---|---|---|
| Factores humanos | ||
| 1. | El número de intentos de cada plan de tratamiento no invasivo debe limitarse a 3 | 88,6 [31; 2; 2] |
| 2. | El primer intento debe efectuarse en las condiciones a priori óptimas | 100 [35; 0; 0] |
| 3. | La técnica primaria más apropiada debe ser la que ofrece mayor garantía para alcanzar el éxito al primer intento | 94,3 [33; 1; 1] |
| 4. | Se recomienda disponer de ayudas cognitivas visuales para el manejo de las crisis emergentes | 97,1 [34; 1; 0] |
| 5. | Se recomienda disponer de un carro de VAD estandarizado en las áreas donde se trata la VA | 100 [35; 0; 0] |
| 6. | Se recomienda usar listados de verificación (checklist) para reducir la incidencia del error humano, mejorar el tiempo de ejecución de tarea y reforzar la cultura de seguridad en el manejo de la VA | 100 [35; 0; 0] |
| 7. | Se recomienda el uso de modelos ergonómicos y de comunicación | 91,4 [32; 3; 0] |
| Evaluación y planificación preprocedimiento | ||
| 8. | Se recomienda la evaluación preprocedimiento en todo paciente que requiere un tratamiento de la VA | 100 [35; 0; 0] |
| 9. | La evaluación preprocedimiento de la VA debe ser multifactorial, estructurada y orientada a la detección de una VAD anatómica, fisiológica y contextual | 97,1 [34; 1; 0] |
| 10. | La exploración de la VA puede comenzar por la detección de predictores de dificultad o fallo para el plan primario y posteriormente para los 3 planes alternativos | 97,1 [34; 1; 0] |
| 11. | Los modelos multivariantes podrían tener una mayor capacidad de predicción | 97,1 [34; 1; 0] |
| 12. | La toma de decisiones debe ser individualizada según paciente, operador, contexto y tiempo | 97,1 [34; 1; 0] |
| 13. | Es necesaria la restricción de la ingesta de alimentos y líquidos siguiendo las pautas de ayuno preoperatorio | 97,1 [34; 1; 0] |
| 14. | La presencia de estómago lleno indica que la VA debe protegerse con una IT | 88,6 [31; 2; 2] |
| Preparación | ||
| 15. | La forma de onda de capnografía debe estar disponible en todas las localizaciones donde se trata la VA para testar el éxito de cualquiera de los 4 planes empleados | 97,1 [34; 1; 0] |
| Opciones básicas para el manejo de la vía aérea difícil | ||
| 16. | Antes de cada procedimiento debe evaluarse la pertinencia del tratamiento y realizar un análisis riesgo beneficio | 97,1 [34; 1; 0] |
| 17. | Se recomienda un tratamiento con paciente despierto cuando existe un grado alto de dificultad o imposibilidad de IT, predictores de dificultad combinados o alteraciones fisiológicas y condiciones contextuales negativas | 82,9 [29; 5; 1] |
| 18. | Se sugiere la inducción de anestesia general con preservación de la ventilación espontánea en aquellas situaciones que hacen recomendable un tratamiento con paciente despierto, pero la anestesia general es inevitable por falta de cooperación o urgencia y no presenta predictores fisiológicos ni contextuales de dificultad ni enfermedad obstructiva | 91,4 [32; 2; 1] |
| 19. | Cuando existan predictores de dificultad de VA fisiológicos o contextuales se podrá valorar el beneficio del aplazamiento si supera el riesgo de proceder al tratamiento, o valorar la posibilidad de establecer estrategias anestésicas alternativas | 85,7 [30; 5; 0] |
| Vía aérea difícil conocida o prevista | ||
| 20. | El tratamiento con el paciente despierto es la opción de elección para asegurar una VAD conocida o prevista | 85,7 [30; 4; 1] |
| 21. | Se recomienda la oxigenoterapia nasal de alto flujo frente a las cánulas convencionales de bajo flujo | 91,4 [32; 3; 0] |
| 22. | La VNI con mascarilla endoscópica podría tener un papel en la IT del paciente crítico con hipoxemia | 82,9 [29; 6; 0] |
| 23. | Se recomienda la premedicación con un antisialogogo para optimizar la eficacia del anestésico local y el campo de visión siendo el glicopirrolato de elección | 80 [28; 5; 2] |
| 24. | La sedación es un elemento opcional complementario a una adecuada anestesia tópica en el TVAPD | 88,6 [31; 2; 2] |
| 25. | Los objetivos de la sedación consciente para el tratamiento de la VA con paciente despierto son amnesia efectiva, satisfacción del paciente y analgesia para reducir reflejos tusígenos, nauseoso y hemodinámicos, preservando la permeabilidad de la VA, la ventilación espontánea y los reflejos laríngeos protectores | 94,3 [33; 2; 0] |
| 26. | Si la técnica primaria seleccionada (FB o VL) fracasa debe emplearse la técnica alternativa | 80 [28; 6; 1] |
| 27. | Un tercer intento puede beneficiarse de un abordaje multimodal (VL + CI: consentimiento informado; FB) | 100 [35; 0; 0] |
| 28. | La combinación de un DEG de IT y FB puede ser útil como técnica de rescate para mantener la oxigenación, la permeabilidad de la VA y realizar una IT a su través | 100 [35; 0; 0] |
| 29. | Se recomienda un TET de menor calibre al habitual con la VL y FB | 85,7 [30; 4; 1] |
| 30. | Se recomienda disminuir la diferencia entre el diámetro externo del FB y el diámetro interno del TET para facilitar la IT con FB | 85,7 [30; 3; 2] |
| 31. | No se recomiendan los TET de PVC estándar en la IT con FB por tener más probabilidad de impactar en las estructuras glóticas | 71,9 [23; 4; 5] |
| 32. | Tras la confirmación visual de la IT se recomienda inducir la anestesia general tras el establecimiento del neumotaponamiento y la confirmación capnográfica de la IT | 94,3 [33; 2; 0] |
| 33. | Las técnicas y abordajes alternativos deben ser planificados con anticipación y aplicarse sin demora tras el fallo de los primarios | 100 [35; 0; 0] |
| 34. | Ante una alta probabilidad de fracaso de IT con paciente despierto, se recomienda preparar en paralelo al plan de tratamiento invasivo para realizar un AII en caso de obstrucción total de la VA | 88,6 [31; 4; 0] |
| 35. | Se recomienda la traqueotomía con paciente despierto bajo anestesia local en presencia de compromiso crítico preexistente de la VA | 82,9 [29; 6; 0] |
| 36. | La cricotirotomía con paciente despierto sería la técnica más indicada ante un compromiso crítico emergente | 91,4 [32; 3; 0] |
| 37. | La ECMO bajo anestesia local en el paciente despierto puede ser la opción más segura cuando se prevé la imposibilidad de ejecución, el fracaso o la ineficacia de los 4 planes convencionales con riesgo de obstrucción completa de la VA | 90,6 [29; 1; 2] |
| Vía aérea difícil no prevista | ||
| Oxigenación periprocedimiento | ||
| 38. | El HFNO debe considerarse como técnica de preoxigenación de primera línea para pacientes con hipoxemia leve (PaO2/FiO2>200mmHg), mientras que la VNI es la técnica de elección en aquellos con hipoxemia severa (PaO2/FiO2≤200mmHg) | 87,5 [28; 3; 1] |
| 39. | La preoxigenación con VNI+HFNO y la oxigenación apneica con HFNO debe ser una opción prioritaria para los pacientes críticamente enfermos durante la IT | 85,7 [30; 4; 1] |
| Inducción de secuencia rápida | ||
| 40. | La ISR es la técnica recomendada cuando existe un riesgo considerable de aspiración en una VA sin predictores de dificultad | 97,1 [34; 1; 0] |
| 41. | Se recomienda usar ISR con o sin maniobra de Sellick en todas las IT de urgencia | 84,4 [27; 1; 4] |
| 42. | Para la preparación segura de la ISR se sugiere el uso de checklist | 97,1 [34; 1; 0] |
| 43. | Se sugiere la premedicación con antiácido no particulado inmediatamente antes de la inducción y un antagonista del receptor H2 40-60min antes o un inhibidor de la bomba de protones para aumentar el pH y reducir el volumen del contenido gástrico en pacientes con alto riesgo de aspiración | 82,9 [29; 5; 1] |
| 44. | El tratamiento con sonda nasogástrica debe ser individualizado | 88,6 [31; 4; 0] |
| 45. | Ante una posible regurgitación debe garantizarse la disponibilidad de dispositivos de succión de alta eficiencia con sondas de gran calibre multiorificio | 100 [35; 0; 0] |
| 46. | Se recomienda una posición con cabeza elevada 20-30° para prevenir la regurgitación pasiva y, en caso de producirse, la posición de Trendelenburg, girar la cabeza hacia un lado y aspirar la orofaringe y la tráquea antes de iniciar la ventilación con presión positiva | 94,3 [33; 2; 0] |
| 47. | La elección del hipnótico, así como la dosis y la velocidad de administración debe ser individualizada | 91,4 [32; 3; 0] |
| 48. | Se sugiere la realización de una inducción de secuencia retardada en enfermos agitados y no colaboradores para realizar una preoxigenación adecuada | 71,9 [23; 3; 6] |
| 49. | No se puede recomendar el uso rutinario de la presión cricotiroidea | 81,3 [26; 2; 4] |
| 50. | Se puede aplicar una «ISR modificada» en pacientes con alto riesgo de hipoxia no candidatos a un TVAPD | 85,7 [30; 5; 0] |
| Intubación traqueal | ||
| 51. | Los dispositivos con pala estándar tipo Macintosh (permite laringoscopia directa e indirecta) son los apropiados para el tratamiento de la VA sin predictores de dificultad, mientras que aquellos con pala hiperangulada (sin o con canal guía) son los indicados para la VAD conocida o prevista | 94,3 [33; 1; 1] |
| 52. | Se recomienda la disponibilidad de un introductor en toda localización donde se trata la VA | 97,1 [34; 1; 0] |
| 53. | La ausencia de registro capnográfico (grado 3 de ventilación) indica una IT fallida hasta que se demuestre lo contrario | 80 [28; 6; 1] |
| 54. | La monitorización de la onda de capnografía durante el mantenimiento de la ventilación mecánica es altamente recomendable en todas las ubicaciones | 100 [35; 0; 0] |
| Ventilación con dispositivo extraglótico | ||
| 55. | Debe procederse sin demora a la inserción de un DEG para preservar la oxigenación alveolar ante una IT difícil o fallida | 85,7 [30; 3; 2] |
| 56. | Se recomienda la disponibilidad inmediata de un DEG2G, así como poseer la competencia necesaria para su uso en todas las localizaciones donde se trata la VA | 100 [35; 0; 0] |
| 57. | Durante la inserción de un DEG debe liberarse la presión cricoidea en caso de estar siendo utilizada | 80 [28; 5; 2] |
| 58. | La rotación de 90°, la tracción mandibular y el uso de LD o VL (de elección) con la técnica «insertar/detectar/corregir sobre la marcha» aumentan la eficacia y seguridad del DEG al facilitar la inserción, incrementan la tasa de éxitos al primer intento reduciendo los traumatismos a nivel faríngeo | 82,9 [29; 4; 2] |
| 59. | Puede optarse por la IT guiada por FB a través del DEG si la situación es estable, bajo un BNM adecuado y si el operador tiene la competencia necesaria para la técnica | 97,1 [34; 1; 0] |
| Ventilación con mascarilla facial | ||
| 60. | Para la VMF se recomienda utilizar de inicio la técnica óptima (triple maniobra de hiperextensión cervical, desplazamiento mandibular anterior y apertura bucal, colocación de cánula oro o nasofaríngea y técnica VE a 2 manos, en un paciente con posicionamiento óptimo y BNM intenso) | 80 [28; 3; 4] |
| 61. | La declaración de VMF fallida implica la transición inmediata a VDEG | 85,7 [30; 2; 3] |
| Acceso infraglótico invasivo | ||
| 62. | El fracaso de los 3 planes no invasivos (primario y de rescate), independientemente del valor de SpO2, exige la verbalización de la necesidad y posterior realización de un AII | 90,6 [29; 0; 3] |
| 63. | La cricotirotomía es la técnica de elección en una situación NINO | 91,4 [32; 2; 1] |
| 64. | Para la cricotirotomía se recomienda la técnica quirúrgica de bisturí/introductor/tubo | 91,4 [32; 2; 1] |
| 65. | La realización de un AII debe ser factible en cualquier lugar donde se trata la VA | 100 [35; 0; 0] |
| 66. | La cricotirotomía de urgencia debe convertirse a un TET o una traqueotomía ya que no hay evidencia suficiente como tratamiento a largo plazo | 85,7 [30; 3; 2] |
| 67. | El fallo de una cricotirotomía para asegurar la VA hace recomendable la realización de una traqueotomía por un operador experto | 94,3 [33; 1; 1] |
| 68. | Todo profesional que trata la VA debe adquirir y mantener la competencia necesaria para realizar una cricotirotomía quirúrgica o percutánea con técnica de Seldinger | 100 [35; 0; 0] |
| Monitorización del neumotaponamiento | ||
| 69. | El neumotaponamiento debe establecerse con la mínima presión necesaria para garantizar un sellado efectivo y seguro. La presión debe permanecer entre 20-30cmH2O en el caso de TET y cánulas de traqueotomía y cricotirotomía, y <60 cmH2O para los DEG | 94,3 [33; 1; 1] |
| Extubación | ||
| 70. | Toda reintubación puede considerarse potencialmente difícil ya que su manejo implica una complejidad adicional | 97,1 [34; 1; 0] |
| 71. | El test de fugas, preferentemente la evaluación cuantitativa, la evaluación ecográfica y la visualización laríngea con VL o FB pueden facilitar la toma de decisiones | 97,1 [34; 1; 0] |
| 72. | La extubación con paciente despierto y uso de técnicas avanzadas es el método más adecuado para la VAD | 94,3 [33; 2; 0] |
| 73. | La capnografía debe estar disponible en las unidades de recuperación y usarse en casos de alto riesgo | 97,1 [34; 1; 0] |
| Documentación | ||
| 74. | La historia de fracaso en procedimientos previos es el predictor más preciso de fallo en posteriores tratamientos | 97,1 [34; 1; 0] |
| Gestión en el ámbito de la vía aérea | ||
| 75. | Se recomienda la asignación de un líder en VA en cada institución | 100 [35; 0; 0] |
| Docencia y entrenamiento | ||
| 76. | La adquisición de competencias debe ser gradual, mediante una fase cognitiva, simulación y capacitación clínica con resolución de problemas hasta completar la curva de aprendizaje, con evaluación y feedback del instructor en cada fase | 100 [35; 0; 0] |
| 77. | Se requieren una formación continua y un entrenamiento regular para el desarrollo de nuevas habilidades o técnicas y el mantenimiento de competencias, preferentemente con una periodicidad anual | 97,1 [34; 1; 0] |
- •
Manuel Á. Gómez-Ríos: redacción del manuscrito, elaboración de todas las ayudas cognitivas y material gráfico, tablas y anexos, revisión bibliográfica, lectura crítica, niveles de evidencia y revisión final del documento.
- •
José Alfonso Sastre: borrador secciones ISR, DEG y checklist, tablas de factores de riesgo, modelos de documentos de información, revisión bibliográfica, lectura crítica, niveles de evidencia y revisión final del documento.
- •
Xavier Onrubia-Fuertes: contribución AII, algoritmo de intubación traqueal difícil no prevista, revisión bibliográfica y revisión final del documento.
- •
Teresa López: borrador secciones DEG y ECMO, revisión bibliográfica, lectura crítica, niveles de evidencia y revisión final del documento.
- •
Alfredo Abad-Gurumeta: revisión bibliográfica, lectura crítica, niveles de evidencia y revisión final del documento.
- •
Rubén Casans-Francés: revisión bibliográfica, lectura crítica y revisión final del documento.
- •
David Gómez-Ríos: revisión bibliográfica, lectura crítica y revisión final del documento.
- •
José Carlos Garzón: revisión bibliográfica, lectura crítica y revisión final del documento.
- •
Vicente Martínez-Pons: algoritmo de intubación traqueal difícil no prevista, revisión bibliográfica y revisión final del documento.
- •
Marta Casalderrey-Rivas: revisión bibliográfica, lectura crítica y revisión final del documento.
- •
Miguel Ángel Fernández-Vaquero: algoritmo de intubación traqueal difícil no prevista, revisión bibliográfica y lectura crítica dirigida a predictores y evaluación de la VA y revisión final del documento.
- •
Eugenio Martínez-Hurtado: algoritmo de intubación traqueal difícil no prevista y revisión final del documento.
- •
Ricardo Martín-Larrauri: algoritmo de intubación traqueal difícil no prevista y revisión final del documento.
- •
Laura Reviriego-Agudo: algoritmo de intubación traqueal difícil no prevista, revisión bibliográfica y revisión final del documento.
- •
Uxía Gutierrez-Couto: estrategias de búsqueda bibliográfica.
- •
Javier García-Fernández: lectura crítica y revisión final del documento.
- •
Alfredo Serrano Moraza: sección medio prehospitalario, revisión bibliográfica, lectura crítica y revisión final del documento.
- •
Luis Jesús Rodríguez Martín: sección medio prehospitalario y revisión final del documento.
- •
Carmen Camacho Leis: sección medio prehospitalario y revisión final del documento.
- •
Salvador Espinosa Ramírez: sección medio prehospitalario y revisión final del documento.
- •
José Manuel Fandiño Orgeira: lectura crítica y revisión final del documento.
- •
Manuel José Vázquez Lima: lectura crítica y revisión final del documento.
- •
Miguel Mayo-Yáñez: contribución AII y revisión final del documento.
- •
Pablo Parente-Arias: contribución AII y revisión final del documento.
- •
Jon Alexander Sistiaga-Suárez: lectura crítica y revisión final del documento.
- •
Manuel Bernal-Sprekelsen: lectura crítica y revisión final del documento.
- •
Pedro Charco-Mora: coordinación, algoritmo de intubación traqueal difícil no prevista, borrador de opciones ergonómicas, borrador docencia y entrenamiento, revisión bibliográfica, lectura crítica y revisión final del documento
MAGR recibió honorarios por conferencias de Medtronic. XOF recibió honorarios por conferencia y taller práctico de bloqueo neuromuscular de Merck Sharp & Dohme. RCF recibió honorarios por conferencias de FreseniusKabi. AAG recibió honorarios por conferencias de Merck Sharp& Dohme y 3M Edwards.
Panel de expertos DelphiManuel Á. Gómez-Ríos, José Alfonso Sastre, Xavier Onrubia-Fuertes, Teresa López, Alfredo Abad-Gurumeta, José Carlos Garzón, Vicente Martínez-Pons, Marta Casalderrey-Rivas, Miguel Ángel Fernández-Vaquero, Eugenio Martínez-Hurtado, Ricardo Martín-Larrauri, Laura Reviriego-Agudo, Javier García-Fernández, Pedro Charco-Mora, Raquel García Álvarez, Alfredo Panadero Sánchez, Alejandra Prieto Gundín, María Luisa Santos Marqués, David Domínguez García, Irma María Barrio, Uxío García-Aldao, Aixa Espinosa, Carmen M. Holgado Pascual, Jesús Carazo Cordobés, Cristobal Añez Simón, Natividad Quesada Gimeno, Marina Gómez-Morán Quintana, Silvia Bermejo, Pilar Cabrerizo Torrente, Francisca Llobell, Roque J. Company Teuler, Teresa del Castillo Fernández de Betoño, Carlos González Perrino y Paola Hurtado.
Revisores externosJaideep Pandit, Luis Gaitini, Tomasz Gaszyński y Pavel Michalek.
ColaboradoresSe puede consultar el listado de colaboradores en material suplementario.