La osteotomía periacetabular (OPA) es una técnica utilizada para el tratamiento de la displasia residual, incluso en caderas inestables con cobertura acetabular limitada. El objetivo de este estudio es analizar los resultados funcionales, radiológicos y las complicaciones en pacientes tratados mediante OPA mini-invasiva.
Materiales y métodosEstudio retrospectivo que analiza 131 casos intervenidos con OPA en nuestro centro. Se determinó de forma prequirúrgica y al final del seguimiento el grado de degeneración articular con la escala de Tönnis, el ángulo de Wiberg, el índice acetabular, el ángulo de cobertura anterior, el espacio articular, las posibles complicaciones y el resultado funcional mediante la escala Non-Arthritic Hip Score.
ResultadosLa edad media de 32,3±9,5 (DE) años, 102 (77,9%) fueron mujeres y 29 (22,1%) fueron hombres. El seguimiento fue de 7,7±2,8 (DE) años. Se obtuvo una mejora en los parámetros radiológicos entre el momento prequirúrgico y al final del seguimiento, ángulo de Wiberg de+18,5° (18,3° versus 36,8°, IC 95%: 17,3 a 19,7), ángulo de cobertura anterior de+13,5° (26,2° versus 39,7°, IC 95%: 11,6 a 15,4) y el índice acetabular de –11,1° (19,5° versus 8,4°; IC 95%: –12,1 a –10,1). Además, los resultados funcionales con la escala Non-Arthritic Hip Score mejoraron en+31,3 puntos (60,7 prequirúrgico versus 92 último seguimiento posquirúrgico; IC 95%: 28,7 a 33,8). La complicación más frecuente fue la disestesia transitoria del nervio fémoro-cutáneo lateral en 10 casos (7%).
ConclusiónLa osteotomía periacetabular mediante el abordaje mini-invasivo es una técnica reproducible, permite restaurar la cobertura acetabular y proporciona una mejora en las escalas funcionales según confirma nuestra serie.
Periacetabular osteotomy (PAO) is an accepted and worldwide technique recognized for residual dysplasia treatment and even in unstable hips with limited acetabular coverage. The aim of this study is to analyse the functional, radiological and complication results in patients treated with mini-invasive PAO.
Material and methodsWe performed a retrospective study in which we analysed 131 cases undergoing mini-invasive PAO at our centre. The degree of joint degeneration was evaluated with Tönnis scale, Wiberg angle, acetabular index (AI), anterior coverage angle (AC), joint space, complications and functional outcome with the Non-Arthritic Hip Score (NAHS) were analysed preoperatively and at the end of follow-up.
ResultsThe average age was 32.3±9.5 (SD) years, 102 (77.9%) were female and 29 (22.1%) were male. 7.7±2.8 (SD) years follow up. The radiological parameters improved between the pre-surgical phase and the end of follow-up, Wiberg angle+18.5° (18.3° versus 36.8°, 95% CI 17.3 to 19.7), AC angle+13.5° (26.2° versus 39.7°, 95%CI 11.6 to 15.4) and the AI -11.1° (19.5° versus 8.4°; 95%CI -12.1 to -10,1). In addition, the functional results, with the NAHS scale, improved+31.3 points (60.7 pre-surgical versus 92 at the end of follow-up, 95% CI 28.7 to 33.8). The most common complication was transient lateral femoral cutaneous nerve hypoaesthesia in 10 cases (7%).
ConclusionThe mini-invasive PAO approach is a reproducible technique, it allows restoration of acetabular coverage and provides an improvement in functional scales as confirmed by our series.
La displasia residual y del desarrollo de la cadera, conocida en la literatura anglosajona como developmental dysplasia of the hip (DDH), consiste en una serie de anormalidades anatómicas, de las que resulta, como la más destacable, una cobertura acetabular insuficiente, condicionando una distribución anómala de las cargas. En consecuencia, se produce un aumento de presión de contacto al nivel del cartílago articular e inestabilidad articular, predisponiendo al daño del complejo condrolabral, estructuras periarticulares y a una eventual coxartrosis1–3.
El objetivo de la cirugía de preservación de cadera consiste en corregir fundamentalmente las anormalidades anatómicas y los daños condrolabrales que llevan a la degeneración articular temprana, con la intención de prevenir o retrasar la aparición de una artrosis secundaria4. Por tanto, en ausencia de degeneración del cartílago articular, los pacientes jóvenes (15-40 años), activos y con estos cambios anatómicos sintomáticos son candidatos al tratamiento quirúrgico5.
La osteotomía periacetabular (OPA), osteotomía de Ganz o también conocida como osteotomía Bernesa, ha ganado en las últimas décadas una progresiva aceptación, convirtiéndose actualmente en el gold-standard en pacientes esqueléticamente maduros4,6,7.
La OPA consiste en una osteotomía alrededor del acetábulo, de corte poligonal, que permite su reorientación, pudiéndose de esta manera obtener:
- -
Distribución equilibrada de las cargas sobre la cabeza femoral.
- -
Mejor cobertura acetabular en todos los planos.
- -
Mantenimiento del contacto del cartílago hialino acetabular con el femoral.
Ganz et al.6 describieron esta técnica en 1988 a través de un abordaje de Smith-Petersen modificado con desinserción/reinserción de los músculos de la espina ilíaca anterosuperior y el recto anterior, proporcionando así una correcta exposición del acetábulo.
En 2008 la escuela de Aarhus (Prof. Søballe; Troelsen et al.7) describió una modificación mini-invasiva de la técnica clásica de OPA, basada principalmente en un cambio del abordaje quirúrgico. Este abordaje consiste en un abordaje inguinal trans-sartorial, y presenta varios beneficios respecto a la técnica clásica6, entre los cuales destaca una manifiesta disminución del tiempo quirúrgico, directamente en relación con la curva de aprendizaje, pero con menor pérdida sanguínea y con disminución de los requerimientos transfusionales, menor dolor postoperatorio, rápida recuperación funcional y beneficios estéticos, debido a que la incisión se realiza en la misma dirección que las líneas de Langer.
Además de los beneficios inherentes a los distintos tipos de abordaje8,9, resalta la relevancia de los resultados clínico-funcionales de estos pacientes. El seguimiento clínico a corto-medio plazo muestra un alivio sintomático y una mejoría funcional en un 40-97% de los pacientes10,11. Además, se ha descrito hasta un 71% de reincorporación a actividades deportivas, similar o incluso de mayor intensidad después de la OPA12–14. En este grupo de pacientes cabe destacar una mejoría clínica en relación con el dolor y sin comprometer el reinicio de actividades deportivas a niveles previos preoperatorios12.
Los objetivos del estudio son:
- 1.
Descripción de nuestra serie inicial de pacientes tratados de DDH mediante OPA mini-invasiva.
- 2.
Descripción de los resultados funcionales de nuestros pacientes.
- 3.
Enumerar los consejos técnicos del procedimiento, basándonos en nuestra experiencia.
- 4.
Descripción de las complicaciones, con la curva de aprendizaje realizada, relacionadas con este procedimiento.
Realizamos un estudio retrospectivo de los pacientes intervenidos en nuestro centro mediante OPA con abordaje mini-invasivo, descrito por Troelsen et al.7, en un periodo de 9 años que va desde 2007 hasta diciembre de 2016.
Se incluyeron en el estudio aquellos pacientes que tuvieran dolor de características mecánicas de cadera persistente, displasia de cadera, interlínea articular congruente, espacio articular mayor de 3mm, flexión de cadera mayor de 110° y rotación interna de la cadera menor de 15°.
De un total de 145 OPA con abordaje mini-invasivo realizadas en el periodo señalado, 3 fueron excluidas por no estar los parámetros radiológicos integrados en nuestro sistema radiológico digital, 4 por faltar tanto parámetros radiológicos digitales como funcionales y 7 por no disponer de su completo seguimiento. En consecuencia, se incluyeron 131 casos realizados en 118 pacientes (13 bilateral).
Se determinaron como variables los parámetros demográficos (edad, sexo), lado de la intervención, los parámetros radiológicos (ángulo de Wiberg o ángulo borde-centro-lateral15, ángulo de cobertura lateral16, índice acetabular o ángulo de Tönnis17 e interlínea articular de la articulación coxa-femoral) en el momento prequirúrgico y al final del seguimiento. Además, se midieron las complicaciones (disestesias transitorias del nervio fémoro-cutáneo lateral, paresia del nervio ciático, conversión a prótesis total de cadera, choque femoroacetabular) durante el seguimiento y los resultados funcionales mediante la escala Non Arthritic Hip Score (NAHS)18 en el momento prequirúrgico y al final del seguimiento.
Técnica quirúrgicaEl paciente es colocado en decúbito supino sobre una mesa radiotransparente. Se administra la profilaxis antibiótica (cefazolina 2g) y ácido tranexámico (1g) antes de la intervención. La anestesia, general, debe hacerse con bajas dosis de relajante muscular (tabla 1).
Consejos y trucos para la realización de la osteotomía periacetabular mini-invasiva
| Pre-operatorio |
| Planificación pre-operatoria de los cortes periacetabulares y de la orientación acetabular esperada. |
| Radiológicos |
| El equipo de rayos X debe poder movilizarse de una proyección AP a un falso perfil de Lequesne. De lo contrario, no seremos precisos en la realización de cada uno de los cortes que componen la OPA |
| El falso perfil de Lequesne requiere una inclinación de 30° a 40°, permitiendo una mejor exposición de la columna posterior |
| La modificación de la altura de la mesa quirúrgica permite aumentar la visión frontal con el equipo de rayos X, para permitir el centrado de la sínfisis púbica, intentando que sea lo más parecida a la radiografía de la pelvis ortoestática |
| Neurológicos |
| Colaboración de un neurofisiólogo para monitorizar las respuestas motoras y sensitivas del nervio femoral, ciático y obturador |
| Vasculares |
| Colaboración de un cirujano vascular por riesgo de lesión de la corona mortis que suele estar localizada a 1cm medial del corte del pubis |
| Utilizar un sistema de autotransfusión continua para minimizar la pérdida de sangre durante el procedimiento |
| Quirúrgicos |
| Posicionar al paciente en decúbito supino en mesa radiotransparente |
| Anestesia general con baja dosis de relajante muscular para no interferir en las mediciones neurofisiológicas. No se recomienda anestesia epidural, ya que podría enmascarar una complicación vascular y neurológica |
| Los osteotomos deben estar siempre lo suficientemente afilados |
| Seguir el orden estricto de las osteotomías |
| No traccionar demasiado el músculo iliopsoas, ya que puede dañar el nervio femorocutáneo lateral y el nervio femoral |
| Durante el 2.°, 3.er y 5.° corte la cadera debe descansar con una ligera rotación externa de 20.° a 30.° y 90.° de flexión de rodilla para desplazar lateralmente y mantener el nervio ciático y las arterias glúteas relajadas |
| En el 4.° corte puede ser útil delimitar la osteotomía introduciendo una aguja de Kirschner al lado de la corteza del ilion lateral, y utilizar un retractor romo retrovertido radiolúcido para proteger los vasos glúteos superiores |
| No coloque el retractor romo retrovertido demasiado alto para no dañar el plexo lumbar |
| La reorientación acetabular se debe realizar con la cadera en flexión. Si se realiza en extensión la cápsula y los ligamentos iliofemorales se tensan y pueden llevar a la retroversión del fragmento |
| Para la reorientación acetabular la pinza de Hernández-Ros o un tornillo de Schanz bicortical roscado de 8mm, utilizado en forma de joystick, puede servir de ayuda. Se debe colocar en la parte más superomedial del fragmento para no forzarlo; de lo contrario, tiene riesgo de una rotura inesperada |
| Dolor postoperatorio |
| Utilizar un catéter local intralesional durante las primeras 24-48horas para infiltrar cada 8horas un bolo de 20cc que contiene 10cc de ropivacaina al 0,7%, 9cc de suero fisiológico y 1cc de ketorolaco (30mg) |
En nuestro centro esta intervención se realiza siempre con un equipo de rayos X (OEC Fluorostar 7900 series, GE OEC Medical Systems Inc, Wendelstein, Alemania), monitorización neurofisiológica intraoperatoria, un cirujano vascular y un sistema de autotransfusión continua (Continuous AutoTransfusion System C.A.T.S® plus, Fresenius Kabi AG, Bad Homburg, Alemania) (tabla 1). El equipo de rayos X se coloca por debajo de la mesa quirúrgica, y antes de finalizar la colocación del paciente debemos de asegurarnos de que se pueden realizar las proyecciones anteroposterior (AP) y falso perfil de Lequesne (tabla 1). La monitorización neurofisiológica intraoperatoria se realiza por un neurofisiólogo que recoge la actividad motora y sensitiva de los grupos musculares abductores, recto anterior, vasto medial, isquiotibiales, gastrocnemio, peroneo largo, tibial posterior y aductor del primer dedo del pie. Esto nos permite monitorizar las señales motoras y sensitivas del nervio femoral, ciático y obturador, mientras se realizan las osteotomías (tabla 1). La presencia de un cirujano vascular es debido a que existe un riesgo de lesión de la corona mortis que se trata de una anastomosis retropúbica entre la arteria ilíaca externa (o vasos epigástrico profundos) y la arteria obturatriz. Esta arteria suele estar localizada 1cm medial del corte del pubis (tabla 1).
A continuación, se colocan los campos quirúrgicos, se realiza el abordaje inguinal trans-sartorial descrito por Söballe (Troelsen et al.7), con especial hincapié en la identificación y liberación subfascial del nervio femorocutáneo lateral, con la finalidad de proporcionarle la máxima capacidad de desplazamiento, y se realizan las osteotomías en el siguiente orden:
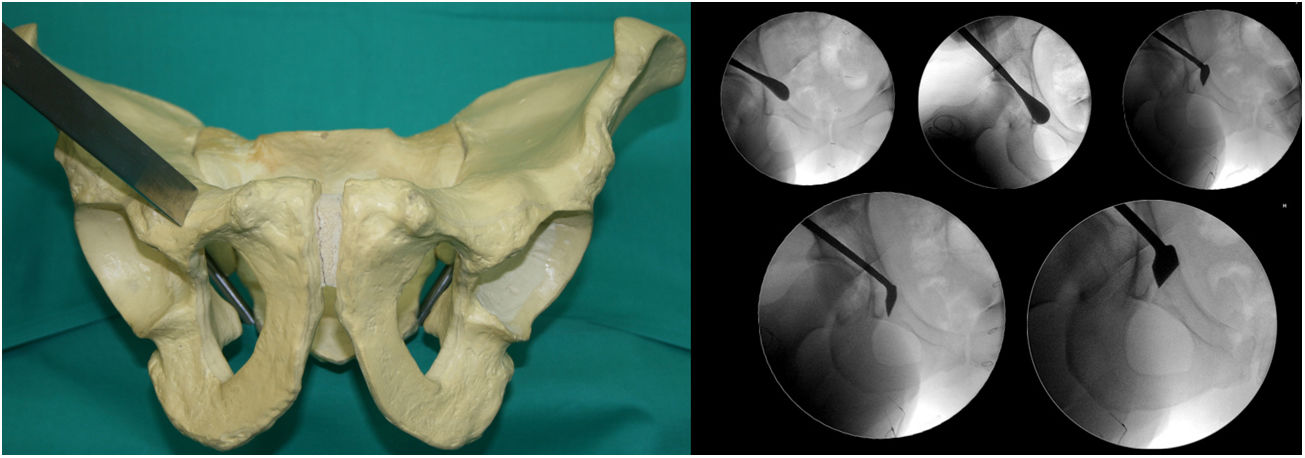
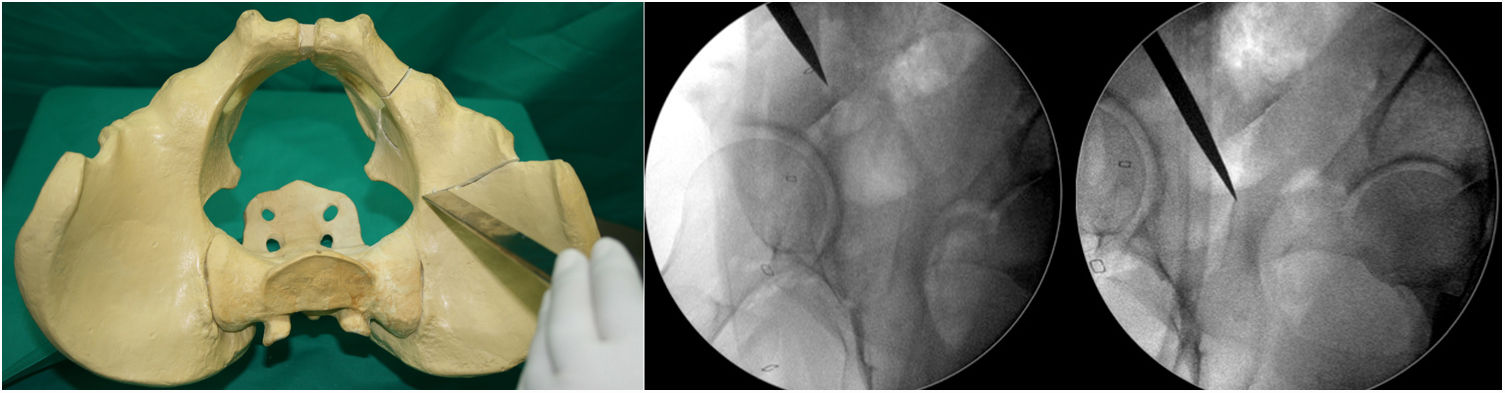
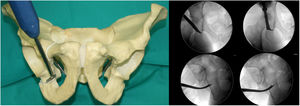
- 1.
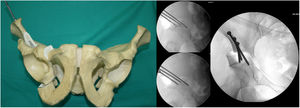
Primera osteotomía (fig. 1). Osteotomía, con escoplo, de la rama iliopubiana a 1cm medial al acetábulo. Se realiza flexionando la cadera de 80° a 90° y una ligera rotación interna para relajar el psoas ilíaco y el nervio femoral. La osteotomía debe ser precisa, a no más de 1cm del ángulo superolateral del foramen obturador, y es controlada con rayos X mediante las proyecciones AP y neutra y oblicuas inlet y outlet.
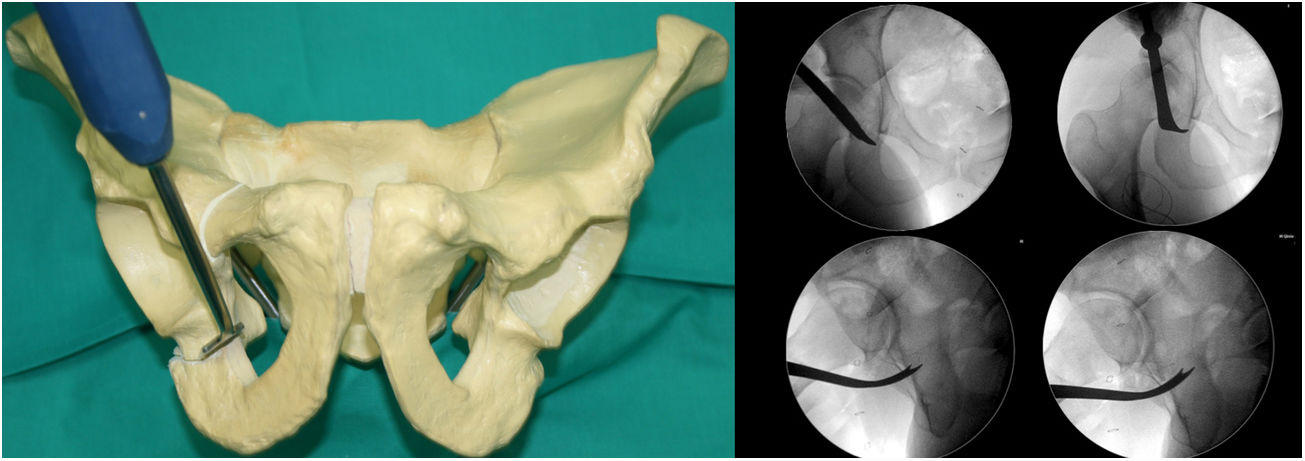
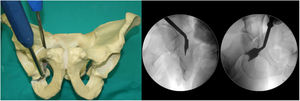
- 2.
Segunda osteotomía (fig. 2). Osteotomía, con escoplo, de la fosa infra-acetabular bajo control fluoroscópico con las proyecciones AP y Lequesne. En primer lugar se realiza disección roma con tijeras largas de Metzenbaum para crear un orificio por donde se pueda introducir sobre el borde exterior del agujero obturatriz el osteotomo de Ganz o Matta. La osteotomía no debe sobrepasar la cortical posterior del isquion. Importante mantenerse aproximadamente 1cm antes de la cortical posterior del isquion para no crear una discontinuidad pélvica.
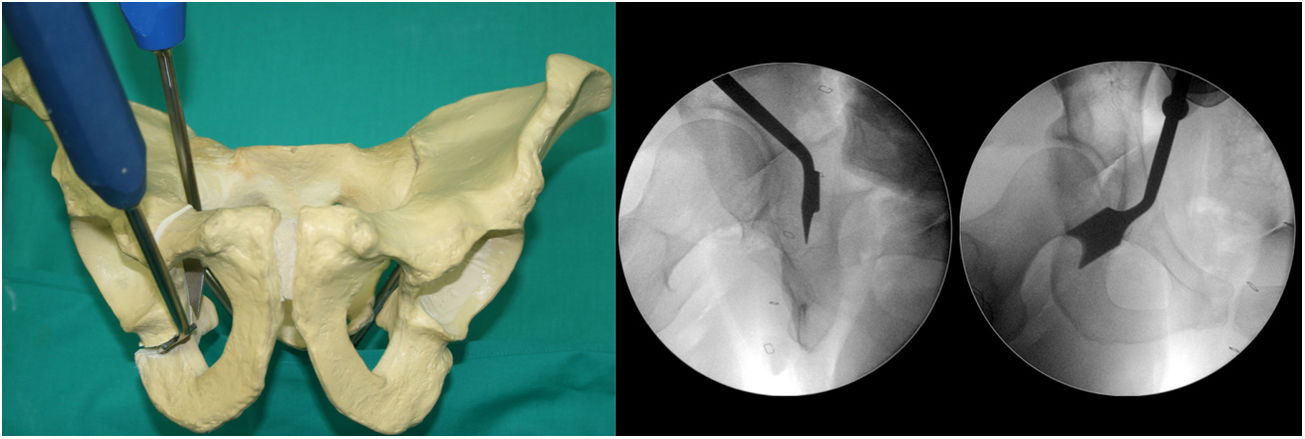
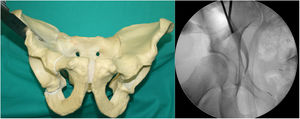
- 3.
Tercera osteotomía (fig. 3). Con el escoplo angulado de Ganz de doble punta y 2,5cm de ancho se realiza un corte que conecta un punto situado a media distancia entre la línea articular acetabular y la espina ciática. Este corte se realiza en proyección alar de Lequesne (nos dará la longitud) y anteroposterior (nos dará la anchura) y con la cadera en flexión de 80-90° con discreta rotación externa para relajar el nervio ciático, debido a su cercanía.
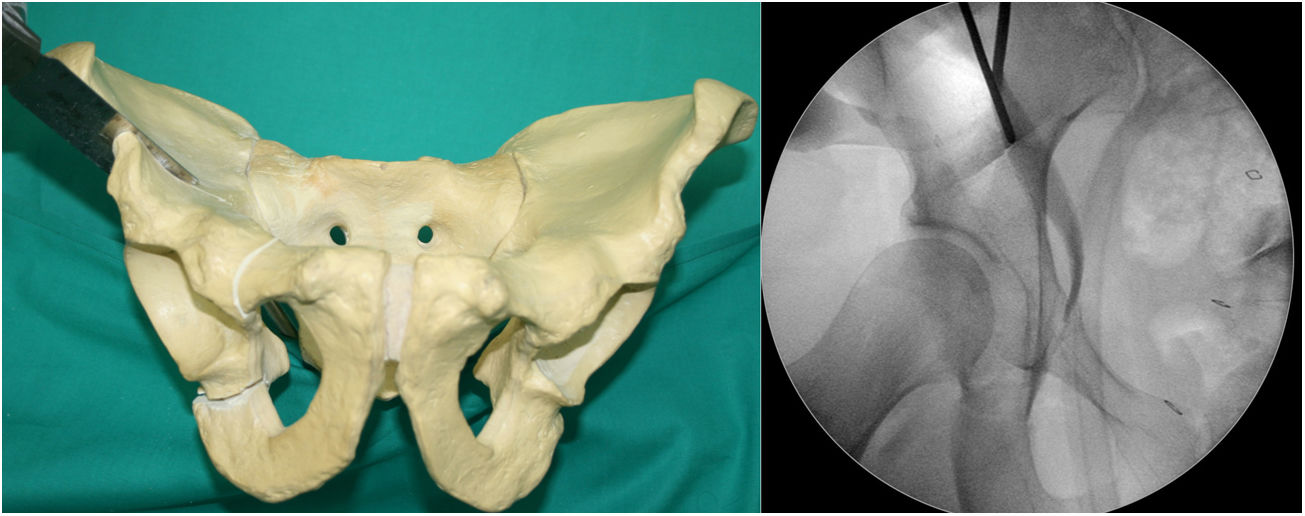
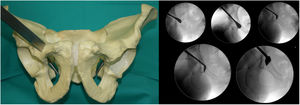
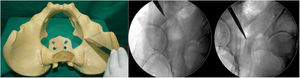
- 4.
Cuarta osteotomía (fig. 4). Único corte que se realiza con sierra oscilante y visualización directa. La osteotomía discurre desde el ala ilíaca, debajo de la espina ilíaca anterosuperior (3,5cm supracetabular), hasta 1cm del borde pélvico (tabla 1). Se controla con fluoroscopia en proyección de pelvis AP.
- 5.
Quinta osteotomía (fig. 5). Llamada «osteotomía de unión». Va desde 1cm del ala pélvica a unirse con la parte más alta de la tercera osteotomía. Esta osteotomía, a diferencia de todos los autores, la realizamos con 2 osteotomos de Lambotte, y bajo control fluoroscópico con proyección de Lequesne y AP. En este momento el acetábulo se separa del resto de la pelvis.
- 6.
Reorientación del acetábulo. Este es el paso de mayor complejidad (tabla 1). A veces, el anestesista debe inducir relajación muscular adicional (especialmente en pacientes muy musculados) para poder reorientar el acetábulo. El objetivo es obtener una ligera medialización del fragmento acetabular y una cubierta lateral y anteversión fisiológica según lo planificado. Para ello:
- -
El centro de la cabeza femoral debe estar localizado a 4 o 5mm del borde posterior acetabular.
- -
El borde anterior acetabular no debe cruzar el borde posterior y debe ser proyectado aproximadamente a 1/3 de la pared posterior.
- -
La espina ciática no debería ser visible en la proyección AP estricta (lo que significaría retroversión) y la segunda osteotomía (infra-acetabular-isquion) debe haber experimentado una angulación que se corresponde con la obtenida en la cobertura de la cabeza femoral.
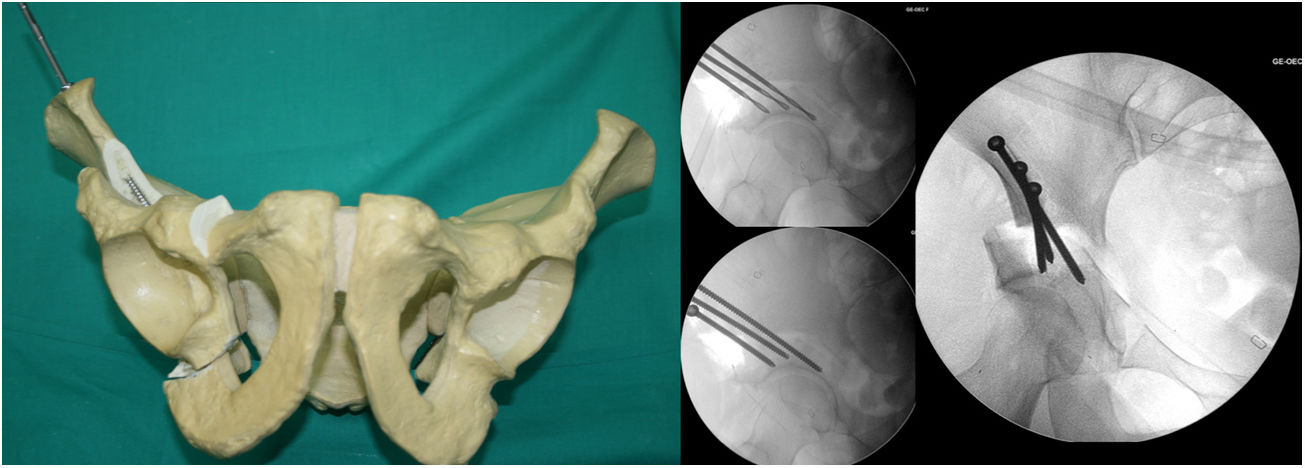
- 7.
Fijación del acetábulo (fig. 6). Utilizamos 2 o 3 tornillos bicorticales de 4,5mm (Matta Pelvic System, Stryker Trauma AG, Selzach, Suiza) con una longitud que varía de 60 a 140mm, comenzando desde lateral a medial en V invertida. Durante la fijación realizamos proyecciones AP y Lequesne para garantizar que no invadimos la articulación coxa-femoral.
El cierre se realiza por planos (con atención de no atrapar al nervio femorocutáneo lateral), no usamos drenaje, y para la piel utilizamos sutura continua absorbible intradérmica.
Seguimiento postoperatorio y protocolo de rehabilitaciónPara el dolor postoperatorio utilizamos un catéter local intralesional durante las primeras 24-48horas para infiltrar cada 8horas un bolo de 20cc que contiene 10cc de Ropivacaina al 0,7%, 9cc de suero fisiológico y 1cc de ketorolaco (30mg) (tabla 1). Se puede usar rescate analgésico adicional, si se requiere, o incluso se puede aplicar un sistema de bomba de analgesia controlada por el paciente.
La duración de la estancia hospitalaria es, por lo general, de 6 a 8 días. Con el paciente hemodinámicamente estable (no se espera una pérdida de hemoglobina por debajo de 3g/l) por lo general se inicia la rehabilitación en el primer día posquirúrgico. En las primeras 6 semanas se realizan movimientos pendulares pasivos y cinesiterapia suave gradual sin sobrepasar los 90° flexión, 40° abducción, 60° rotación externa, 20° aducción y 20° rotación interna (un exceso de rotación interna forzaría sobremanera la fijación acetabular). Además, se realizan ejercicios isométricos cuadricipitales, glúteo mayor y glúteo medio. La deambulación es con carga parcial a partir de las 48horas con ayuda de 2 bastones ingleses. Según la evolución radiológica, en la séptima semana se retira el apoyo externo del lado de la intervención y en la novena semana comienza la deambulación sin apoyo externo y potenciación de la musculatura pelvitrocantérica. A partir de la undécima semana se realizan los ejercicios de propicepción.
Las revisiones se realizan a las 3, 6 y 12 semanas posquirúrgicas, donde se realiza una exploración física y control radiológico mediante las proyecciones anteroposterior y falso perfil de Lequesne.
Análisis estadísticoEl análisis estadístico se realizó con la versión 12.0 de Stata para Macintosh (Data Analysis and Statistical Software, Texas, EE. UU.). Se realizó un estudio descriptivo de las variables, expresándolas en media y desviación estándar (DE). Además, se utilizó la prueba de Shapiro-Wilk para confirmar la distribución normal de las variables. Cuando no se pudo confirmar la distribución normal o no se cumplieron los requisitos para realizar la prueba de la «t» de Student para datos emparejados, se utilizó una prueba no paramétrica, la prueba de Wilcoxon. Se aceptó como criterio de significación estadística un nivel de probabilidad de 0,05 para todas las pruebas estadísticas y los intervalos de confianza se calcularon, cuando fue posible, con un nivel de confianza del 95%.
ResultadosLa edad media de los pacientes fue de 32,3±9,5 (DE) años, 102 (77,9%) fueron mujeres y 29 (22,1%) fueron hombres. El 53,4% (70) de las OPA se realizaron en el lado derecho y el 46,5% (61) en el lado izquierdo. La media de seguimiento fue de 7,7±2,8 (DE) años de seguimiento.
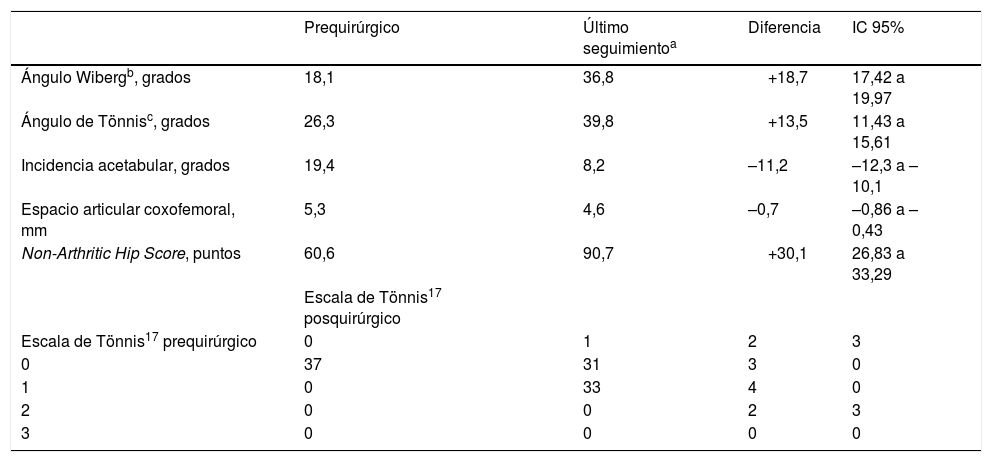
En cuanto a los resultados radiológicos (tabla 2) el ángulo de Wiberg pasó de 18,3°±7,6 (DE) a 36,8°±7,83 (DE). El cambio fue estadísticamente significativo con una ganancia de cobertura de+18,5° (IC 95%: 17,26 a 19,74; «t» de Student para muestras emparejadas, p=0,000). El ángulo de cobertura anterior incrementó de 26,2°±9,71 (DE) a 39,7°±9 (DE) al final del seguimiento. Por tanto, se obtuvo una ganancia de+13,5° (IC 95%: 11,6 a 15,42; «t» Student para muestras emparejadas, p=0,000). El índice acetabular mejoró, pasando de 19,5°±6,4 (DE) a 8,4°±3,6 (DE) al final del seguimiento. Esta reducción también fue estadísticamente significativa (–11,1°; IC 95%: –12,13 a –10,12; «t» de Student para muestras emparejadas, p=0,000).
Resultados radiológicos
| Prequirúrgico | Último seguimientoa | Diferencia | IC 95% | |
|---|---|---|---|---|
| Ángulo Wibergb, grados | 18,1 | 36,8 | +18,7 | 17,42 a 19,97 |
| Ángulo de Tönnisc, grados | 26,3 | 39,8 | +13,5 | 11,43 a 15,61 |
| Incidencia acetabular, grados | 19,4 | 8,2 | –11,2 | –12,3 a –10,1 |
| Espacio articular coxofemoral, mm | 5,3 | 4,6 | –0,7 | –0,86 a –0,43 |
| Non-Arthritic Hip Score, puntos | 60,6 | 90,7 | +30,1 | 26,83 a 33,29 |
| Escala de Tönnis17 posquirúrgico | ||||
| Escala de Tönnis17 prequirúrgico | 0 | 1 | 2 | 3 |
| 0 | 37 | 31 | 3 | 0 |
| 1 | 0 | 33 | 4 | 0 |
| 2 | 0 | 0 | 2 | 3 |
| 3 | 0 | 0 | 0 | 0 |
IC: intervalo de confianza.
En cuanto a los resultados funcionales el NAHS experimentó una mejoría de 60,7±10,42 (DE) puntos a 92±11,3 (DE), siendo el incremento de+31,3 puntos (IC 95%: 28,7 a 33,8, p=0,000). En la tabla 2 se recoge el ángulo cérvico-diafisario femoral, el espacio articular y el grado de degeneración articular según la escala de Tönnis17.
Tuvimos complicaciones en 20 casos (15,26%) de los 131 incluidos en el estudio, que diferenciamos en menores (que no requirieron segunda cirugía) y mayores (requirieron segunda cirugía). Complicaciones menores (12,21%): la complicación más frecuente fue la disestesia transitoria del nervio femorocutáneo lateral (FCL), que ocurrió en 10 casos (58% global de todas las complicaciones). Además, tuvimos un caso con algodistrofia simpaticorrefleja, un caso de coxa saltans, un caso de seudoartrosis asintomática de la rama iliopúbica, un caso de infección cutánea superficial que se resolvió con antibioticoterapia, un caso de paresia transitoria de la rama externa del nervio ciático que se resolvió con tratamiento médico y rehabilitador en menos de un año, un caso de retraso de consolidación de la columna posterior y un caso de tendinitis del glúteo medio. Complicaciones mayores (2,29%): ninguna de ellas neurovascular. En un caso se tuvo que recurrir a la conversión en artroplastia total de cadera a vástago corto con par cerámica/cerámica, y en 2 casos con ángulo alfa femoral de más de 55° a la osteoplastia fémoro-acetabular mini open. Estas últimas complicaciones hoy día las evitamos directamente combinando la OPA con la osteoplastia femoral artroscópica.
En cuanto al grado de progresión según la escala de Tönnis observamos que un 37,6% de los pacientes con Tönnis 0 pasó a Tönnis 1, y que el 9,8% de los pacientes con Tönnis 1 pasó a Tönnis 2 (tabla 2).
DiscusiónEste estudio retrospectivo evalúa los resultados funcionales y la capacidad de orientación acetabular mediante la OPA mini-invasiva, obteniendo que los pacientes tratados con esta técnica consiguen una correcta cobertura acetabular con escasas complicaciones y con una mejora importante en los resultados funcionales.
En el ámbito nacional existen pocos estudios que valoren los resultados tras una OPA19,20, y de estos solo el estudio de Díaz et al.19 realiza la OPA según la técnica descrita por Ganz et al.6, utilizando el abordaje Smith-Petersen modificado y no el abordaje mini-invasivo descrito por Troelsen et al.7. Nuestra experiencia se remonta a 2002, cuando comenzamos (al igual que Díaz et al.19) a realizar la OPA mediante abordaje Smith-Petersen. En 2007 aprendimos con el profesor Søballe el abordaje mini-invasivo7, y debido a sus ventajas (misma capacidad de orientación acetabular, disminución del tiempo quirúrgico, pérdida sanguínea muy moderada [en nuestro caso no más de 500cc que se retransfunde una vez filtrada]), menor dolor postoperatorio, menor manipulación de partes blandas y menor proporción de complicaciones) realizamos desde entonces este tipo de abordaje.
Nuestros resultados, con el abordaje mini-invasivo, son similares y comparables con los reportados en la literatura7,21,22, y con aquellos que con una curva de experiencia establecida utilizan el abordaje Smith-Petersen modificado4,7,10,22,23. Obtuvimos, al final del seguimiento, un ángulo de Wiberg de 36,8° y un índice acetabular de 8,4° (tabla 2). Troelsen et al.23 realizaron un estudio que analizó 263 OPA (165 mediante el abordaje mini-invasivo y 98 mediante el abordaje ilioinguinal) y observaron una corrección similar con ambos abordajes, pero que con el abordaje mini-invasivo se obtenían más ventajas que con el abordaje ilioinguinal24. No podemos comparar nuestros resultados con los resultados de OPA mediante el abordaje ilioinguinal4,11,19, porque no es el mismo abordaje, y además utilizan escalas funcionales diferentes a la que nosotros hemos empleado.
A pesar de ello, considerando que nuestro trabajo no es comparativo, basándonos en la literatura podríamos valorar las ventajas del abordaje mini-invasivo en relación con otros abordajes, las cuales consisten, según Troelsen et al.7, en un menor daño a nivel muscular con una afectación selectiva del sartorio, menor tiempo quirúrgico debido a menor tiempo de abordaje y cierre. Al realizar el abordaje mini-invasivo trans-sartorial los músculos sartorio e iliopsoas protegen los vasos y nervios femorales de lesiones indirectas, motivo por el que la prevalencia reportada de lesiones neurovasculares moderadas y severas es nula (0%), en comparación con el abordaje iliofemoral, donde la prevalencia de lesiones neurovasculares moderadas y severas es de un 2-3%7. En relación con la pérdida sanguínea se reporta en la literatura con el abordaje ilioinguinal una pérdida aproximada de 0,7-2l6,23, utilizando el abordaje de Smith-Petersen modificado, según los resultados reportados por Trousdale y Cabanela25, la pérdida media fue de 350ml, y utilizando el abordaje mini-invasivo trans-sartorial la pérdida media fue de 250ml aproximadamente23. En cuanto al requerimiento transfusional Troelsen et al.7, utilizando el abordaje mini-invasivo, describen que fue necesario aproximadamente en un 3% de los procedimientos, mientras que Bryan et al.26, utilizando el abordaje Smith-Petersen modificado, describen un porcentaje de transfusiones de aproximadamente el 21%.
Sin embargo, observamos que, independientemente del abordaje utilizado, la OPA mejora el estado funcional del paciente. Alcobía Díaz et al.19 obtuvieron en la escala Merle-D’Aubigne-Postel 14,3 puntos sobre los 18 posibles, correspondiendo a un buen resultado. Steppacher et al.4 observaron que tras 20 años de seguimiento los pacientes tenían una puntuación de 15,8±2,1 puntos sobre los 18 posibles en la escala Merle-D’Aubigne-Postel. Peters et al.27 obtuvieron con la escala Harris Hip Score una mejora de 54 (rango, 20-81) puntos preoperatorio a 87 (rango, 49-100) puntos al final del seguimiento. Nosotros, con la escala NAHS, obtuvimos un aumento en la puntuación al pasar de 60,7 puntos preoperatorio a 92 puntos al final del seguimiento (tabla 2).
La progresión de la coxartrosis puede ocurrir entre el 5% al 33%5,28. En nuestros resultados observamos que un 37,6% de los pacientes con Tönnis 0 pasó a Tönnis 1 y que un 9,8% de los pacientes con Tönnis 1 pasó a Tönnis 2 (tabla 2). Alcobía Díaz et al.19 observaron que el aumento de al menos un grado en la escala Tönnis ocurre en un 20% de los pacientes a los 5 años de seguimiento, y del 54% a los 10 años. Matta et al.29 demostraron una progresión de la coxartrosis en un 21% en los pacientes con Tönnis 1, en un 35% con Tönnis 2 y en un 83% para Tönnis 3.
La aparición de complicaciones está relacionada con la curva de aprendizaje del cirujano ortopédico30. En general la OPA es una intervención que tiene alto riesgo de desarrollar algún tipo de complicación. La tasa de complicaciones y su severidad, tales como lesiones neurológicas o vasculares, suceden a unas tasas muy bajas en manos de cirujanos expertos según Zaltz et al. y el grupo ANCHOR30; existe un 5,9% de que surjan complicaciones que impliquen nueva intervención quirúrgica30.
El grupo ANCHOR clasifica las complicaciones en 5 grados: grado i aquellas que no requieren tratamiento y no altera el curso postoperatorio, grado ii son aquellas que alteran el curso postoperatorio normal, requiriendo tratamiento farmacológico o controles más frecuentes, grado iii aquellas que requieren intervención quirúrgica y reingreso no planificado, grado iv son aquellas que amenazan la vida si no son tratadas o con potencial para una discapacidad permanente y grado v aquellas que ocasionan la muerte30.
Wells et al.31 realizó un estudio que incluía a 154 OPA con el método descrito por Ganz6 con un seguimiento mínimo de 4 años. Observó que en 66 de las 154 OPA (42,8%) desarrollaron alguna complicación, siendo la más frecuente aquellas que no requirieron tratamiento postoperatorio (48,31%), como pueden ser la presencia de una osificación heterotópica asintomática, no-unión asintomática o disestesia del nervio FCL. Troelsen et al.23, al comparar el abordaje mini-invasivo con el abordaje ilioinguinal observaron que en el grupo ilioinguinal hubo 3/98 casos de trombosis arterial, mientras que en el grupo mini-invasivo no hubo complicaciones neurovasculares o complicaciones moderadas/graves derivadas de la técnica.
Nosotros tuvimos complicaciones en 20/131 casos (15%). La complicación más frecuente (7,63%) fue la disestesia temporal del nervio FCL, complicación de grado i según ANCHOR30, que en todos los pacientes se resolvió satisfactoriamente durante el seguimiento.
El 5% de las complicaciones fueron de grado ii. Un caso con algodistrofia simpaticorrefleja, un caso de coxa saltans, un caso de seudoartrosis de la rama púbica asintomático, un caso de infección cutánea superficial, un caso de paresia transitoria del nervio ciático, un caso de retraso de consolidación y un caso de tendinitis de glúteo medio.
Solamente 3/131 casos (2,29%) tuvieron complicaciones de grado iii según los criterios ANCHOR, que requirió tratamiento quirúrgico postoperatorio (una conversión a prótesis total de cadera y 2 osteoplastias por choque femoroacetabular por técnica mini-invasiva). Como tratamiento coadyuvante, cuando se presenta un conflicto femoroacetabular tras una OPA, el tratamiento quirúrgico ofrece resultados satisfactorios32–34. No tuvimos complicaciones que pudiesen ser clasificados como grado iv y v.
La supervivencia en cohortes a largo plazo ha sido reportada. Steppacher et al. describen una supervivencia del 60% en su serie a 20 años de seguimiento4. De igual manera, según reportaron Ziran et al.35 el 60% de los pacientes intervenidos con OPA mantienen su cadera nativa tras 20 años de seguimiento. Aunque la conversión de una OPA a una artroplastia total de cadera (ATC) puede considerarse como un fracaso terapéutico, no debe verse así, sino como un complemento a la ATC. Baqué et al.36 concluyeron que la OPA previa a una ATC optimiza la recuperación del paciente y aporta una mayor estabilidad a la cadera.
Reconocemos ciertas limitaciones de nuestro estudio. Primero, se trata de un estudio retrospectivo, por lo que presenta condicionantes inherentes a este tipo de estudios. Segundo, no se realizó un estudio comparativo con otras técnicas de OPA, enfocándonos únicamente en la técnica utilizada en nuestro centro. Tercero, no analizamos si la edad ha influido en la evolución de los cambios degenerativos según la escala Tönnis17.
En resumen, de acuerdo con nuestros resultados, hemos llevado a cabo la descripción de nuestra serie de pacientes tratados de DDH mediante OPA mini-invasiva, sus resultados funcionales, la descripción de los pasos técnicos del procedimiento basándonos en nuestra experiencia y la descripción de las complicaciones relacionadas con dicho procedimiento.
ConclusiónLa osteotomía periacetabular mediante el abordaje mini-invasivo es una técnica reproducible, permite restaurar la cobertura acetabular y proporciona una mejora en las escalas funcionales, según confirma nuestra serie.
Es un procedimiento seguro con baja tasa de complicaciones que entendemos, y así también lo refleja la literatura, en manos de cirujanos expertos. Nuestros datos sugieren que la mayoría de estas complicaciones no se asocian a la necesidad de nuevos procedimientos quirúrgicos.
Creemos firmemente en la necesidad de expandir nuestros conocimientos técnicos a un mayor número de cirujanos de cadera interesados en el tratamiento mini-invasivo de la displasia residual juvenil y del adulto joven.
Nivel de evidenciaNivel de evidencia iii.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.