Información de la revista
Vol. 18. Núm. 3.
Páginas 190-196 (mayo 1999)
Vol. 18. Núm. 3.
Páginas 190-196 (mayo 1999)
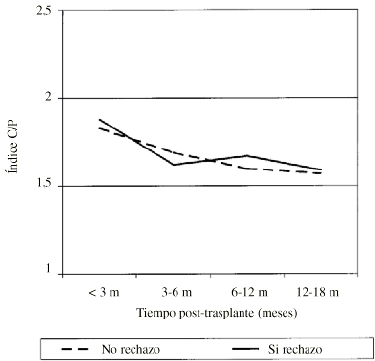
Valoración de la utilidad del índice de captación de anticuerpos monoclonales antimiosina (AMA) en el diagnóstico de rechazo en el trasplante cardíaco (TC).
EVALUATION OF THE USEFULNESS OF THE ANTIMYOSIN MONOCLONAL ANTIBODY (AMA) UPTAKE IN THE DIAGNOSIS OF HEART TRANSPLANT (HT) REJECTION
Visitas
1698
P. Bello Arqués, L. Almenar Bonet, J F. Martí Vidal, R. Pérez Velasco, D. López Aznar, A. Mateo Navarro, M. Palencia Pérez
Este artículo ha recibido
Información del artículo
Opciones para acceder a los textos completos de la publicación Revista Española de Medicina Nuclear e Imagen Molecular
Socio
Si es usted socio de la Sociedad Española de Medicina Nuclear e Imagen Molecular (SEMNIM) puede acceder al texto completo de los contenidos de la Revista Española de Medicina Nuclear e Imagen Molecular desde los enlaces a la revista publicados en la web de la SEMNIN (enlace a https://semnim.es/iniciar-sesion/), previo inicio de sesión como socio. Si tiene problemas de acceso puede contactar con la Secretaría Técnica de la SEMNIM en el correo electrónico secretaria.tecnica@semnim.es o en el teléfono: + 34 619 594 780
Suscriptor
Suscribirse
Contactar
Teléfono para suscripciones e incidencias
De lunes a viernes de 9h a 18h (GMT+1) excepto los meses de julio y agosto que será de 9 a 15h
Llamadas desde España
932 415 960
Llamadas desde fuera de España
+34 932 415 960
E-mail