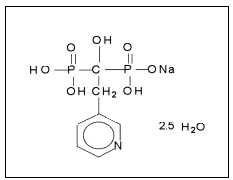
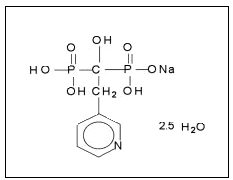
El risedronato sódico es un difosfonato aminado comercializado recientemente en España para el tratamiento de la osteoporosis y de la enfermedad ósea de Paget. Su estructura química se representa en la figura 1 y se caracteriza por la presencia de un átomo de nitrógeno en el anillo cíclico, lo que le convierte en uno de los difosfonatos más potentes.
Figura 1. Estructura química del risedronato.
El risedronato, como otros difosfonatos, es un inhibidor de la resorción ósea mediada por los osteoclastos. Los difosfonatos reducen la actividad osteoclástica al disminuir la formación y el reclutamiento de nuevos osteoclastos, favorecer su apoptosis y modificar la estructura y funcionamiento de los osteoclastos activos1. En la actualidad, no conocemos totalmente los mecanismos bioquímicos por los que los difosfonatos inhiben a los osteoclastos, pero estudios recientes sugieren que los difosfonatos que contienen nitrógeno, como el risedronato, impiden la prenilación de las proteínas recién sintetizadas2. La prenilación es esencial para que la proteína alcance la membrana celular y actúe en los procesos de transducción de la señal que controlan el transporte en la membrana y las diferentes funciones celulares. El osteoclasto sufriría diferentes alteraciones celulares que originarían la alteración del citosqueleto, la pérdida del borde ondulado, la alteración de los mecanismos del proceso de acidificación en el borde en cepillo y la apoptosis3. Otras células que intervienen en la resorción ósea, diferentes a los osteoclastos, también se afectan, en especial los precursores hematopoyéticos de los osteoclastos, que ven frenada su diferenciación, y los osteoblastos, que incrementan la liberación de factores inhibidores de la resorción4.
El perfil farmacocinético del risedronato se conoce en su totalidad. Como todos los difosfonatos, cuando se administra por vía oral, se absorbe intestinalmente en una cantidad muy escasa, inferior al 1% y su biodisponibilidad disminuye si existen alimentos en el estómago. La absorción intestinal del risedronato es similar cuando se administra 30 min antes del desayuno o 2 h después de la comida, lo que permite una gran flexibilidad para elegir el momento de su administración5. El tiempo medio de tránsito esofágico de los comprimidos de risedronato es de 3,3 s, lo que minimiza el contacto con la mucosa esofágica y disminuye el potencial riesgo de su irritación6. El ácido risedrónico no se metaboliza y se excreta a través del riñón. Su vida plasmática es corta porque la mayoría del medicamento se fija de forma rápida al hueso, en especial en las zonas en remodelado, donde permanece durante años. Los estudios de histomorfometría realizados en diferentes pacientes ponen de manifiesto una reducción de los parámetros del remodelado óseo del 50%, sin que se observen alteraciones en la mineralización, ni en la estructura lamelar del hueso en formación.
Su perfil de seguridad, dado que el fármaco lleva poco tiempo comercializado, se ha valorado en estudios preclínicos y clínicos, que incluyen múltiples ensayos clínicos controlados con más de 30.000 pacientes tratados. En general, la mayoría de los efectos adversos son leves o moderados, tienen escasa trascendencia y rara vez obligan a la suspensión de la medicación. Los efectos secundarios del tracto gastrointestinal alto son los más frecuentes y en los ensayos clínicos realizados están presentes en el 20-25% de los pacientes en tratamiento con risedronato, sin que las diferencias respecto a los pacientes que toman placebo alcancen la significación estadística. Hay que tener en cuenta que en estos ensayos se han incluido también pacientes con enfermedades gastrointestinales previas y en tratamiento con antiinflamatorios no esteroides. Dada su reciente comercialización, aún no disponemos de datos de farmacovigilancia a largo plazo pero parece que el perfil de seguridad digestiva del risedronato es más favorable que el del alendronato. Otros efectos adversos observados son disminuciones leves, transitorias y asintomáticas de los valores séricos de calcio y fosfato al iniciar el tratamiento. También se ha comunicado algún caso de elevación de las enzimas hepáticas.
El risedronato está comercializado en España para el tratamiento de la enfermedad ósea de Paget, a dosis de 30 mg diarios, y de la osteoporosis, a dosis de 5 mg diarios. El objetivo de nuestra publicación es analizar las bases científicas en que se basa la eficacia de risedronato en el tratamiento de la osteoporosis y que ha permitido su autorización para las siguientes indicaciones terapéuticas:
Tratamiento de la osteoporosis posmenopáusica establecida.
Prevención de la osteoporosis posmenopáusica.
Prevención y tratamiento de la osteoporosis inducida por glucocorticoides.
Eficacia en el tratamiento de la osteoporosis posmenopáusica establecida
El risedronato ha demostrado en tres ensayos clínicos aleatorizados, de 3 años de duración, que incluyen a más de 15.000 mujeres posmenopáusicas que es eficaz para reducir el riesgo de fracturas vertebrales y periféricas, incluidas las de cadera7-9.
La eficacia del risedronato en disminuir las fracturas vertebrales se confirmó en dos ensayos clínicos denominados Vertebral Efficacy with Risedronate Therapy (VERT). El primero de los estudios publicados se realizó en Norteamérica e incluyó a 2.458 mujeres con una edad media de 69 ± 7 años7. El segundo ensayo es el VERT internacional que se realizó en centros de Europa y Australia e incluyó a 1.226 enfermas con una edad media de 71 ± 7 años8. Para ser incluidas en los ensayos VERT se requería que las mujeres estuvieran en la época de la menopausia desde, al menos, 5 años antes y que tuvieran menos de 85 años de edad en el momento de iniciar el tratamiento. También era necesario que presentasen una osteoporosis establecida definida por la presencia de dos o más fracturas vertebrales; aunque en el estudio norteamericano también se incluyeron mujeres con una fractura vertebral siempre que la densitometría de columna lumbar presentara un T-score ¾ 2. Las pacientes de ambos estudios recibieron de forma aleatoria placebo o risedronato a dosis de 2,5 o de 5 mg/día. Todas las enfermas recibieron suplementos de calcio de 1.000 mg/día y además a las pacientes con niveles basales bajos de vitamina D (< 40 nmol/l) se les administraron 500 U/día de vitamina D.
Los resultados de ambos estudios se representan en la tabla 1, y en ellos destaca que 5 mg diarios de risedronato reducen el riesgo de fractura vertebral a los 3 años en un 41% en el estudio VERT norteamericano y en un 49% en el estudio multinacional. En ambos ensayos se observó que al año de tratamiento el risedronato redujo el riesgo de fracturas vertebrales en las mujeres con osteoporosis establecida en más del 60% respecto al grupo control. También es llamativo el escaso número de enfermas con alto riesgo de sufrir una fractura vertebral, como son las incluidas en estos estudios, que tenemos que tratar para prevenir que una paciente sufra una nueva fractura vertebral.
Aunque los estudios VERT se diseñaron específicamente para valorar la eficacia en la reducción de fracturas vertebrales, en el estudio VERT norteamericano se observó una reducción significativa en el riesgo de fracturas no vertebrales del 39%.
Otros de los objetivos secundarios de los estudios VERT fueron la evolución de la densidad mineral ósea (DMO) y de los marcadores del remodelado. En ambos estudios se observó que los enfermos tratados con 5 mg diarios de risedronato durante 3 años incrementaron de forma significativa la DMO en más del 5% en columna lumbar y del 1,5% en cuello femoral. Asimismo, se objetivó una reducción significativa temprana de los valores séricos de la isoenzima ósea de la fosfatasa alcalina y de los valores urinarios de deoxipiridinolina superiores al 30%.
Recientemente se han publicado los resultados de un ensayo clínico, de 3 años de duración, diseñado para comprobar la eficacia del risedronato en la prevención de la fractura de cadera. Este estudio es el Hip Intervention Program Study Group (HIP) que incluyó a 9.331 mujeres con una edad media de 78 ± 3 años9. Todas las mujeres tenían más de 70 años y severa osteoporosis densitométrica en cuello femoral o más de 80 años con uno o varios factores de riesgo de fractura de cadera. Las pacientes fueron aleatorizadas para recibir placebo o 2,5 o 5 mg/día de risedronato. Todas las enfermas recibieron suplementos de 1.000 mg/día de calcio y el 22% precisó 500 U diarias de vitamina D al tener basalmente valores séricos de vitamina D inferiores a 16 ng/ml.
En la tabla 1 se recogen los resultados de este trabajo en los que se observa una reducción del riesgo de fractura de cadera del 30%. El gran tamaño de la muestra permite a los autores analizar los beneficios del risedronato en los diferentes subgrupos incluidos. En el subgrupo de mujeres con osteoporosis densitométrica se observó una mayor eficacia del risedronato en la reducción de la incidencia de fracturas de cadera que descendió del 3,2% en el grupo placebo al 1,9% en las mujeres tratadas con el fármaco (riesgo relativo [RR] = 0,6; intervalo de confianza [IC] del 95%: 0,4-0,9). La mayor eficacia del medicamento se objetivó en el subgrupo de mujeres con fracturas vertebrales previas donde el risedronato reduce el riesgo de fractura de cadera en un 60% (RR = 0,4; IC del 95%: 0,2-0,8). Por el contrario, en el subgrupo de población seleccionado basándose en edad superior a 80 años y factores de riesgo de fractura de cadera no se objetivaron diferencias significativas. Los resultados del estudio HIP muestran que el risedronato es eficaz en la reducción del riesgo de fractura de cadera en las mujeres ancianas con osteoporosis severa densitométrica y reafirma la conveniencia de realizar estudios de densitometría en las personas de edad avanzada y en el gran riesgo de fractura de cadera que representa la marcada disminución de la masa ósea.
Prevención de la osteoporosis posmenopáusica
Durante los primeros años de la menopausia se produce una pérdida de masa ósea anual del 1-3%, que en mujeres con bajo pico de masa ósea y/o con pérdidas más acusadas ocasiona un incremento de la fragilidad ósea y del riesgo de fracturas. En estas pacientes la terapia hormonal sustitutiva (THS) es el tratamiento de primera elección. En ocasiones, los estrógenos están contraindicados o las mujeres se niegan a tomarlos y debemos utilizar en su lugar otros antirresortivos que también han demostrado su eficacia, como raloxifeno, calcitonina o diferentes difosfonatos.
El risedronato ha demostrado que no solamente frena la pérdida de masa ósea que ocurre tras la menopausia, sino que incluso la incrementa levemente durante los primeros años de tratamiento10,11. Este efecto beneficioso se produce tanto en el período inmediato a la menopausia como en las mujeres sin función ovárica prolongada11, y beneficia tanto a las mujeres con masa ósea normal10 como a aquellas que tienen una DMO disminuida11.
En un ensayo aleatorizado doble ciego, Mortensen et al10 demostraron que, en los primeros años de la menopausia, a las mujeres con masa ósea normal, 5 mg diarios de risedronato durante 2 años incrementaban la DMO en un 1,4% en columna lumbar frente a una pérdida del 4,3% que sufrían las mujeres con placebo. En otro estudio realizado por Fogelman et al11 se demostró que las mujeres menopáusicas con baja masa ósea (T-score < 2 en columna lumbar) tratadas con 5 mg/día de risedronato, durante 2 años, incrementan un 4,1% la DMO en columna lumbar y 1,3% en cuello femoral, frente a las tratadas con suplementos de 1.000 mg de calcio diario que presentaron una disminución del 1% en cuello femoral permaneciendo estable la masa ósea en columna. En este ensayo el efecto beneficioso del risedronato es similar tanto en las mujeres que llevan menos de 5 años de menopausia como en las que tienen más de 5 años desde la supresión de la función ovárica11.
Aunque el risedronato ha demostrado su eficacia en la prevención de la osteoporosis posmenopáusica, en la actualidad carecemos de estudios comparativos de risedronato frente a otros antirresortivos y de estudios de coste-efectividad a largo plazo en la prevención de la osteoporosis posmenopáusica. Por estos motivos, parece razonable utilizar el risedronato para la prevención de la osteoporosis posmenopáusica solamente para las mujeres con baja masa ósea y con contraindicación de la THS o que se niegan a tomar estrógenos.
Prevención y tratamiento de la osteoporosis inducida por glucocorticoides
La administración prolongada de glucocorticoides a dosis superiores a 7,5 mg de prednisona diarias se asocia con el desarrollo de osteoporosis y con la consiguiente aparición de fracturas osteoporóticas, especialmente en la columna vertebral12. Este tipo de osteoporosis ocurre tanto en varones como en mujeres de todas las edades, pero es más acusado en las mujeres posmenopáusicas y/o en los enfermos con procesos, en sí, osteopenizantes como la artritis reumatoide13. La pérdida de masa ósea producida por los glucocorticoides es más acusada en las zonas de hueso trabecular y más acentuada durante los primeros meses del tratamiento corticoide, con una disminución posterior más lenta pero progresiva en tanto se mantenga el tratamiento con glucocorticoides12.
La osteoporosis inducida por glucocorticoides es uno de los problemas clínicos más habituales que nos encontramos en nuestras consultas de reumatología y para su prevención y tratamiento se utilizan medidas generales, suplementos de calcio y/o vitamina D, tiazidas y diferentes antirresortivos14,15. Durante la fase de investigación del risedronato se han realizado dos estudios controlados frente a placebo, de un año de duración, que demuestran la eficacia del risedronato tanto en la prevención como en el tratamiento de la osteoporosis inducida por glucocorticoides16,17.
El estudio de prevención realizado por Cohen et al16 incluyó a 224 pacientes con una edad media de 59 ± 14 años, que habían iniciado el tratamiento con glucocorticoides en los últimos 3 meses. El 95% de los enfermos precisaban los glucocorticoides por procesos reumatológicos. La dosis media de prednisona recibida durante el año del estudio fue de 11 ± 1 mg/día. Los pacientes recibieron de forma aleatoria placebo, o risedronato 2,5 mg/día o 5 mg/día. Todos los enfermos recibieron además suplementos de 500 mg de calcio diarios y los que tenían valores séricos de vitamina D bajos recibieron también 500 U/día de vitamina D. Al año de evolución se observó que los enfermos tratados con 5 mg de risedronato habían incrementado levemente su DMO, pero de forma significativa respecto al grupo placebo que sufrió una disminución del 2,8% en columna lumbar y del 3,1% en cuello femoral. El efecto beneficioso sobre la masa ósea se observó tanto en los varones como en las mujeres pre y posmenopáusicas.
En el ensayo de tratamiento realizado por Reid et al17 se incluyeron 290 enfermos con una edad media de 59 ± 12 años que recibían dosis diarias de prednisona superiores a 7,5 mg desde hacía más de 6 meses. La dosis media de prednisona que recibieron durante el año de seguimiento fue de 14 ± 14 mg/día y el tiempo medio de duración del tratamiento glucocorticoide era superior a 5 años en el momento de iniciar el estudio. En este estudio los pacientes también fueron aleatorizados para recibir placebo, o risedronato 2,5 mg/día o 5 mg/día, pero además todos los enfermos recibieron suplementos de 1.000 mg de calcio y 400 U de vitamina D diarios. En los pacientes tratados con 5 mg diarios de risedronato se observó un incremento significativo de la DMO del 2,9% en columna lumbar y del 1,8% en cuello femoral.
Recientemente Wallace et al18 han realizado un metaanálisis que incluye los dos ensayos de prevención y tratamiento de la osteoporosis inducida por glucocorticoides cuyos resultados se muestran en la tabla 2. En este estudio se demuestra que el risedronato a dosis de 5 mg diarios no sólo incrementa la DMO sino que reduce en un 70% la aparición de fracturas vertebrales y solamente con tratar a 9 pacientes durante un año evitamos que un enfermo presente nuevas fracturas vertebrales.
En conclusión, el risedronato es un fármaco seguro, bien tolerado, que ha demostrado en diferentes ensayos clínicos que es eficaz en la prevención y tratamiento tanto de la osteoporosis posmenopáusica como de la osteoporosis inducida por glucocorticoides.
Fe de errores
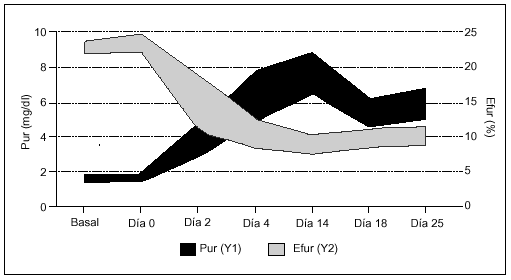
En el artículo de Pérez Ruiz F et al «Utilidad de muestras de orina espontánea para el control del tratamiento con uricosúricos» (Rev Esp Reumatol 2001; 28: 57-61) se produjo un error por la inversión de las tramas de colores. El color negro corresponde al Pur y el color gris al Efur. Se reproduce a continuación la figura correcta.
Figura 1. Efecto de la benziodarona sobre el ácido úrico en plasma (Pur) y la excreción fraccionada (Efur). Las áreas expresan la media con los intervalos de confianza del 95%.