La candidiasis invasora es una micosis que presenta una mortalidad alta (alrededor del 40%), especialmente en pacientes inmunodeficientes20. Su diagnóstico es difícil, porque no hay signos ni síntomas específicos de la infección, y es difícil diferenciar la infección de la colonización por Candida. El diagnóstico convencional de la candidiasis invasora, que incluye la demostración de la invasión tisular por el hongo y su cultivo en localizaciones corporales habitualmente estériles, generalmente presenta una sensibilidad y especificidad bajas, y a menudo requiere procedimientos invasores que no pueden realizarse en muchos de los pacientes con sospecha de candidiasis invasora. Como consecuencia de estos problemas, el tratamiento antifúngico suele iniciarse con retraso, lo que influye de forma determinante en la mortalidad.
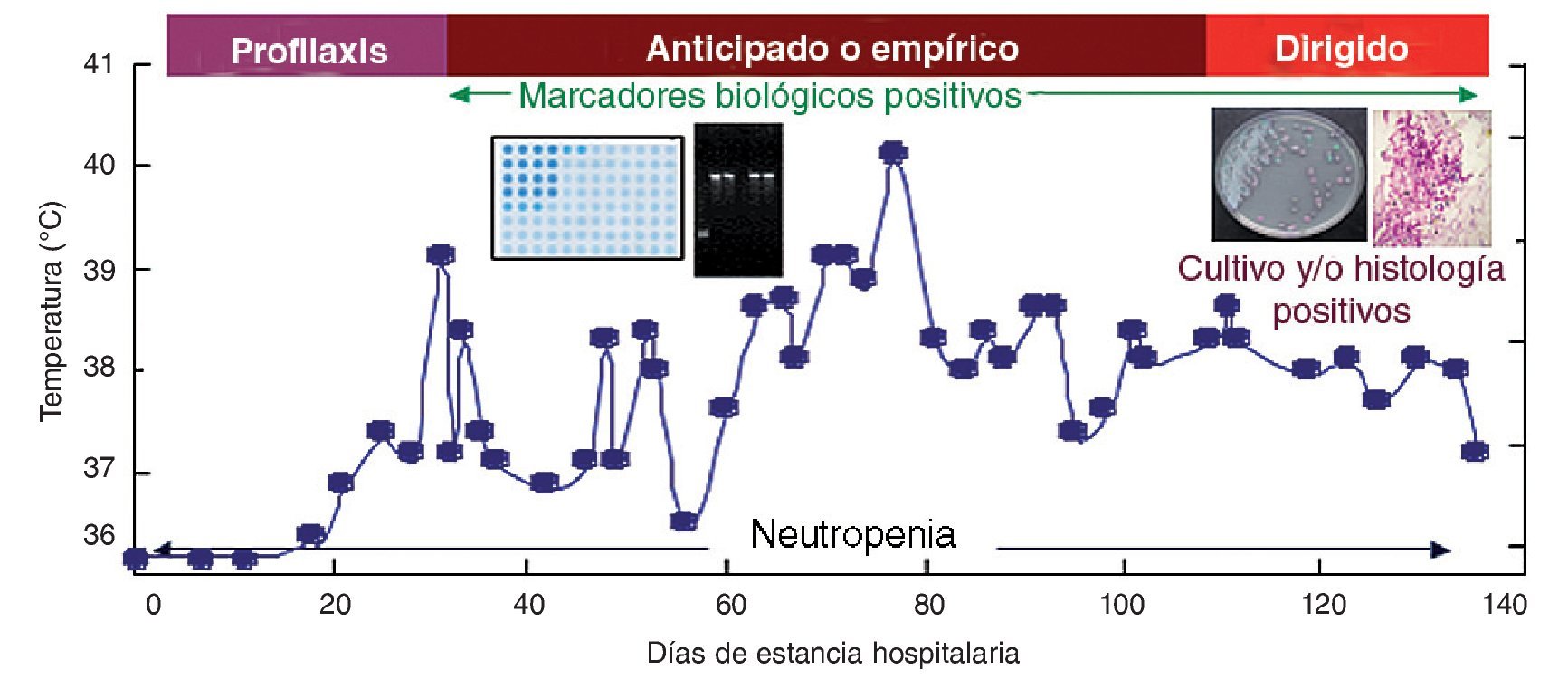
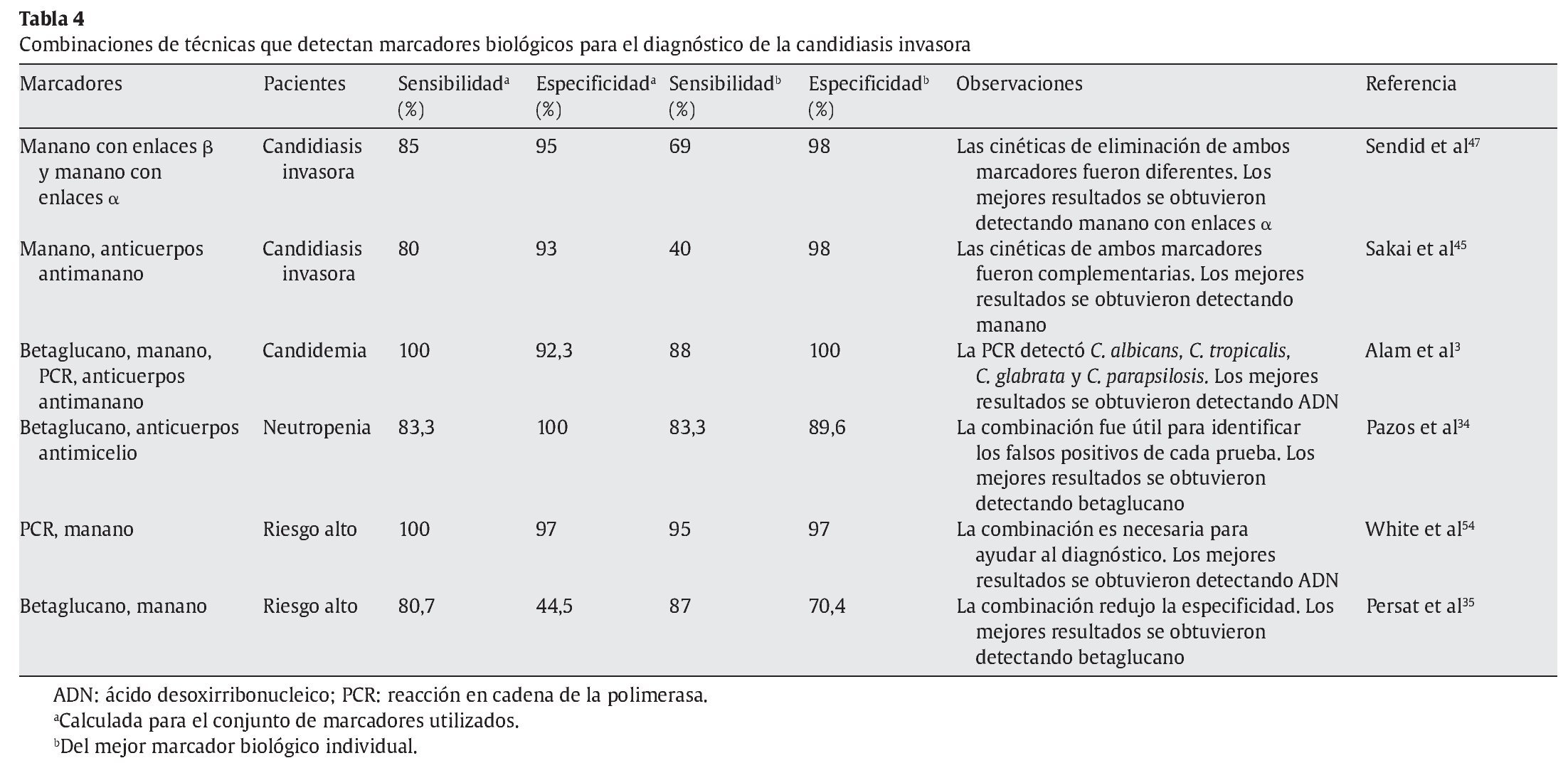
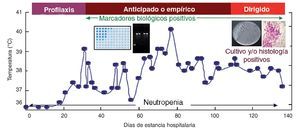
Con el fin de instaurar de forma temprana el tratamiento antifúngico para reducir la alta mortalidad de la candidiasis invasora, se han diseñado diversas estrategias terapéuticas que incluyen la profilaxis, el tratamiento anticipado, el tratamiento empírico y el tratamiento dirigido (fig. 1). El tratamiento anticipado se basa en la administración de antifúngicos después de detectar una serie de marcadores biológicos y de imagen que anteceden a la aparición de los síntomas inespecíficos de la infección fúngica invasora y al diagnóstico definitivo. Una vez iniciado el tratamiento antifúngico, los marcadores biológicos pueden ser de utilidad en el seguimiento de la eficacia terapéutica. En este artículo se revisan los avances que se han obtenido en la detección de marcadores biológicos de utilidad en el diagnóstico y el seguimiento de la eficacia del tratamiento antifúngico en pacientes con candidiasis invasora.
Figura 1. Estrategias terapéuticas utilizadas en el tratamiento de la candidiasis invasora en un paciente con neutropenia grave prolongada que presenta períodos febriles. El tratamiento anticipado se basa en la administración de antifúngicos después de la detección de una serie de marcadores biológicos y de imagen que anteceden a la aparición de los síntomas inespecíficos de la infección fúngica invasora y al diagnóstico definitivo.
Los marcadores biológicos en el diagnóstico de laboratorio de la candidiasis invasora
El diagnóstico de laboratorio de la candidiasis invasora se basa en 3 estrategias complementarias: la observación del hongo en la muestra clínica, el cultivo y la detección de marcadores biológicos, componentes que circulan por el torrente sanguíneo de los pacientes con candidiasis invasora23,40. Actualmente, los marcadores biológicos de interés diagnóstico son el manano, el β-1,3-D-glucano, el ácido desoxirribonucleico (ADN) de Candida y algunos anticuerpos que se producen contra antígenos de la pared celular de Candida.
Manano
Los escasos estudios que se realizan en la actualidad sobre la detección de manano en pacientes con candidiasis invasora se han realizado con la prueba Platelia Candida Ag. La prueba es un ELISA (del inglés enzyme linked immuno sorbent assay) que detecta residuos de manosa unidos por enlaces α del manano, el antígeno mayoritario e inmunodominante de la pared celular de Candida. Su capacidad para inducir anticuerpos es tan grande que los anticuerpos antimanano están presentes en prácticamente todas las personas y forman complejos con el manano cuando pasa a la sangre. La liberación del manano de los inmunocomplejos que forma con los anticuerpos es probablemente el paso más crítico de la prueba de detección y, junto con la transitoriedad de la mananemia, son la causa de la sensibilidad baja de la prueba, que suele estar entre el 40 y el 70%3,23,39,46,48. La prueba se realiza normalmente en suero, pero se han comunicado buenos resultados en líquido cefalorraquídeo de pacientes con meningitis por Candida demostrada por cultivo53.
Un aumento de la sensibilidad diagnóstica de la detección de manano con la prueba Platelia Candida Ag puede obtenerse al complementarla con la detección de residuos de manosa unidos por enlaces β, ya que ambos antígenos tienen cinéticas de aclaramiento diferentes. La detección combinada de ambos antígenos alcanzó una sensibilidad diagnóstica del 90%, una especificidad del 95%, un valor predictivo positivo del 79% y un valor predictivo negativo del 97%, precediendo la detección de manano al cultivo una media de 4,7 días en el 55% de los pacientes47. Una segunda posibilidad puede ser el inmunoanálisis Unimedi Candida monotest (Unitica Ltd. [Japón]), una prueba comercializada recientemente que en un trabajo se ha mostrado más sensible que el Platelia Candida Ag (el 82 frente al 53%), sobre todo para el diagnóstico de las infecciones por Candida parapsilosis17.
β-1,3-D-glucano
El glucano es un componente de la pared celular fúngica formado por monómeros de glucosa unidos con enlaces β-1,3 y β-1,6. El β-1,3-D-glucano se libera durante la infección y puede detectarse en los líquidos biológicos (principalmente suero) de pacientes con distintos tipos de micosis invasoras. El β-1,3-D-glucano se detecta en pacientes con candidiasis, aspergilosis, neumocistosis y algunos con criptococosis, pero no en las zigomicosis. Por tanto, una prueba positiva puede utilizarse como marcador de infección fúngica, pero no permite identificar la especie41.
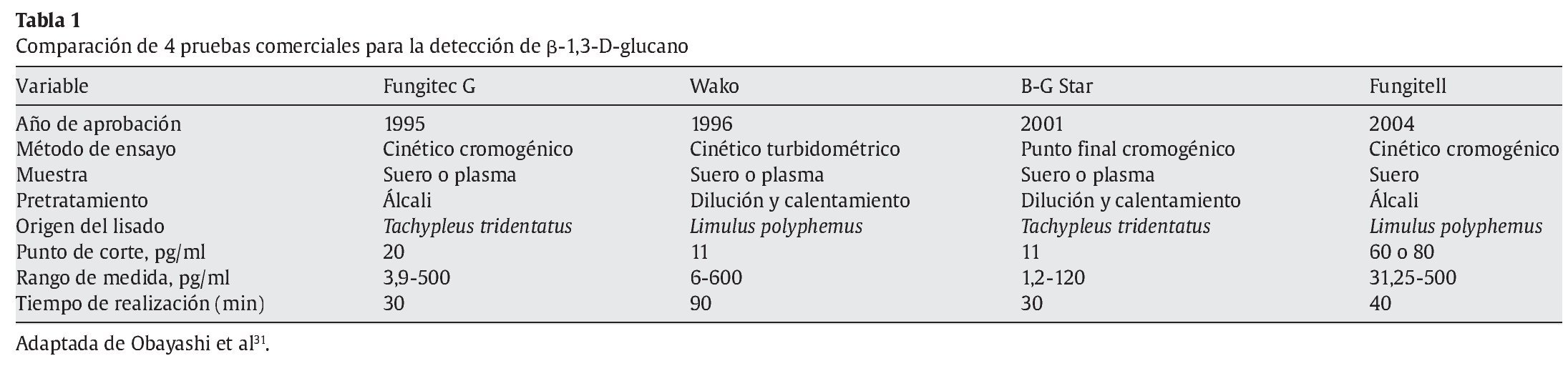
Actualmente hay varias pruebas comercializadas para detectar β-1,3-D-glucano: Fungitec G (Seikagaku Kogyo Corporation [Japón]), Wako (Wako Pure Chemical Industries [Japón]) y B-G Star (Maruha Corporation [Japón]) que se utilizan en Japón, y Fungitell (Associates of Cape Cod Inc. [Estados Unidos]), que se está utilizando en Estados Unidos y Europa. Aunque las 4 pruebas detectan β-1,3-D-glucano, cada una presenta diferencias en su reactividad con el polisacárido y, por tanto, son necesarios puntos de corte diferentes para cada prueba. Las diferencias en reactividad con el β-1,3-D-glucano presentadas por cada prueba pueden reflejarse en la sensibilidad final de la prueba. Así, se ha comunicado que Fungitec G es más sensible que Wako31. En la tabla 1 se muestra un resumen de las características de estas pruebas.
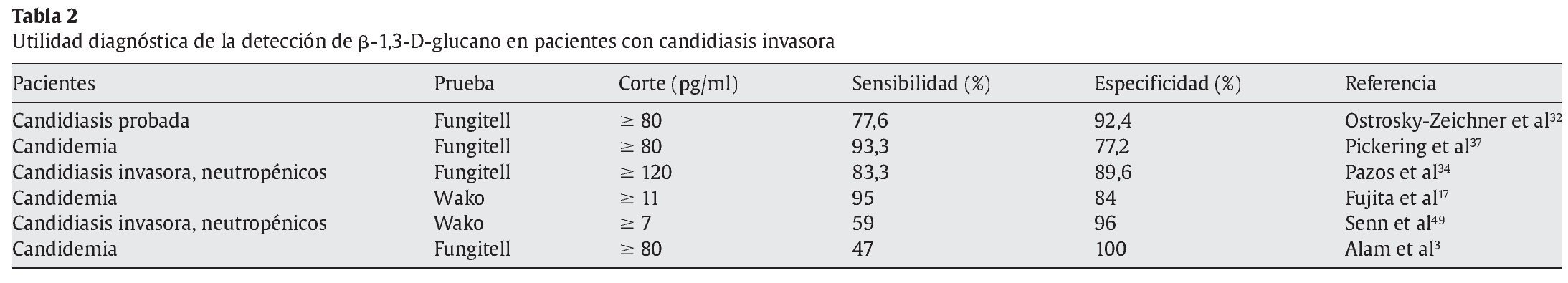
Los resultados publicados recientemente indican que la detección de β-1,3-D-glucano es un buen marcador de enfermedad fúngica invasora y la prueba es positiva en un gran número de pacientes con candidiasis invasora (tabla 2).
Fungitell presenta una sensibilidad del 64,4%, una especificidad del 92,4%, un valor predictivo positivo del 89% y un valor predictivo negativo del 73% en el diagnóstico de la infección fúngica invasora, utilizando un punto de corte de 80 pg/ml32. En este estudio, de los 107 pacientes con candidiasis invasora, el 77,6% fueron positivos utilizando un punto de corte de 80 pg/ml. También con Fungitell, pero con un punto de corte ≥ 120 pg/ml, Pazos et al34 obtuvieron una sensibilidad del 83,3%, una especificidad del 89,6%, un valor predictivo positivo del 62,5% y un valor predictivo negativo del 96,3% en el diagnóstico de la candidiasis invasora en 35 pacientes que presentaban un riesgo alto de tener una infección fúngica invasora y en los que se diagnosticaron 3 candidiasis probadas y 3 candidiasis posibles13. La detección de β-1,3-D-glucano fue positiva en el 100% de las candidiasis probadas y en el 66% de las candidiasis probables. Se observaron un 10,3% de falsos positivos, y uno de los 3 casos probablemente estaba relacionado con una bacteriemia por Escherichia coli. En estos casos, el análisis de la cinética de los valores de β-1,3-D-glucano en cada paciente fue de utilidad para detectar los falsos positivos, ya que se produjeron ascensos y descensos abruptos, una observación que también se ha realizado en pacientes con aspergilosis invasora33. La detección de β-1,3-D-glucano fue un marcador temprano que precedió a la fiebre, al diagnóstico clínico y radiológico, y al tratamiento antifúngico, en la mayoría de los pacientes.
En algunos estudios, la especificidad del Fungitell ha sido baja, debido a la detección de β-1,3-D-glucano en pacientes con bacteriemia. Pickering et al37 estudiaron la utilidad de la prueba en varios grupos de pacientes y observaron que 13 de 15 pacientes (87%) con candidemia fueron positivos. Sin embargo, también lo fueron 14 de 25 pacientes (56%) con bacteriemia. Estos autores obtuvieron una sensibilidad del 93,3%, una especificidad del 77,2%, un valor predictivo positivo del 51,9% y un valor predictivo negativo del 97,8% en el diagnóstico de la candidiasis invasora, y sugieren que el Fungitell puede ser más útil para excluir la existencia de una infección fúngica invasora. Digby et al14 también han observado valores elevados de β-1,3-D-glucano en 46 pacientes críticos, pero estos valores no eran diferentes de los encontrados en pacientes con bacteriemia. Los autores concluyeron que la prueba podría ser útil para excluir la existencia de una infección.
Estudios realizados en modelos experimentales han puesto de manifiesto que la detección de β-1,3-D-glucano con la prueba Fungitell puede ser de utilidad en el diagnóstico de las candidemias asociadas a catéteres y en la meningoencefalitis candidiásica. Utilizando un modelo experimental de candidiasis asociada a biopelículas en catéter venoso central, Nett et al30 observaron que los valores de β-1,3-D-glucano en los animales con candidiasis asociada a catéter eran 10 veces mayores que los observados en animales infectados por vía intravenosa con la misma cepa de C. albicans, a pesar de que la extensión de la infección en el riñón era menor. Petraitiene et al36 detectaron β-1,3-D-glucano en el líquido cefalorraquídeo (LCR) de conejos neutropénicos con meningoencefalitis candidiásica y observaron que la prueba era muy sensible (100%) en contraste con el cultivo (8,1%). La negativización de C. albicans en los hemocultivos no predijo la erradicación del hongo en el LCR. Sin embargo, los valores de β-1,3-D-glucano en el LCR predijeron la respuesta terapéutica a la micafungina y se correlacionaron con la extensión de la infección en el tejido cerebral.
Fungitec G presenta una sensibilidad del 85,4%, una especificidad del 95,2%, un valor predictivo positivo del 70,4% y un valor predictivo negativo del 98% en el diagnóstico de la infección fúngica invasora utilizando un punto de corte de 60 pg/ml31. Diecisiete de los 21 pacientes con hemocultivos positivos (11 casos por Candida) presentaron valores de β-1,3-D-glucano por encima del corte.
La utilidad diagnóstica de la prueba Wako se ha estudiado en varios trabajos. Fujita et al17 estudiaron los valores de β-1,3-D-glucano en 76 pacientes con candidemia y obtuvieron una sensibilidad y una especificidad diagnóstica del 95 y el 84%, respectivamente. En el 85% de los pacientes positivos para β-1,3-D-glucano, la prueba se anticipó al hemocultivo. Senn et al49 estudiaron a 95 pacientes con neutropenia en los que se diagnosticaron 30 infecciones fúngicas invasoras probadas o probables (17 candidiasis, 13 aspergilosis y 2 mixtas), y se obtuvo una sensibilidad del 63%, una especificidad del 96%, un valor predictivo positivo del 79% y un valor predictivo negativo del 91% en el diagnóstico de la infección fúngica invasora utilizando como criterio de positividad 2 valores consecutivos de β-1,3-D-glucano ≥ 7 pg/ ml. La detección de β-1,3-D-glucano se positivizó antes de que se obtuviesen evidencias clínicas, microbiológicas, radiológicas y/o histopatológicas de las infecciones fúngicas invasoras. En el subgrupo de pacientes con candidiasis invasora, la prueba presentó una sensibilidad del 59%, una especificidad del 96%, un valor predictivo positivo del 67% y un valor predictivo negativo del 94%. Se obtuvieron resultados negativos en la detección de β-1,3-D-glucano en 2 candidiasis invasoras probadas (una candidiasis diseminada por Candida humicola y una candidemia por Candida norvegensis) y en 5 candidiasis invasoras probables con lesiones hepatoesplénicas.
La detección de β-1,3-D-glucano presenta resultados falsos positivos y negativos que deben tenerse en cuenta para obtener el máximo rendimiento de la prueba. Dado que el β-1,3-D-glucano se encuentra ampliamente distribuido en un gran número de materiales, una de las causas de falsa positividad es la contaminación de los materiales de laboratorio con β-1,3-D-glucano. Además, se han descrito resultados falsos positivos en pacientes en hemodiálisis con membranas de acetato de celulosa, en contacto con gasas y esponjas quirúrgicas o en tratamientos con inmunoglobulinas humanas intravenosas, polisacáridos antitumorales (lentinano y polisacárido K), albúmina, factores de coagulación, proteínas plasmáticas, quimioterapia antitumoral, amoxicilina-ácido clavulánico y piperacilina-tazobactam. Los sueros hemolizados y algunas bacteriemias por grampositivos (Streptococcus) y gramnegativos (Alcaligenes, Pseudomonas aeruginosa) son otras causas conocidas de resultados falsos positivos. Los falsos negativos se asocian con la existencia de sueros hiperpigmentados (bilirrubina y triglicéridos elevados), el tratamiento empírico o profilaxis antifúngica y con la especie infectante, ya que no todas liberan la misma cantidad de β-1,3-D-glucano durante la infección.
La detección del β-1,3-D-glucano se está consolidando en el diagnóstico de las infecciones fúngicas invasoras y una prueba positiva se considera un criterio microbiológico de enfermedad invasora probable en los criterios conjuntos de la European Organization for Research and Treatment of Cancer (EORTC) y el Mycoses Study Group del NIAID (National Institute of Allergy and Infectious Diseases) de Estados Unidos13. Sin embargo, ya que el β-1,3-D-glucano es un marcador panfúngico, la prueba debe complementarse con otras que permitan la identificación del género o especie fúngica infectante.
La detección del β-1,3-D-glucano puede ser de ayuda en el establecimiento del tratamiento antifúngico anticipado. Akamatsu et al2 determinaron los valores de β-1,3-D-glucano en el plasma de 180 trasplantados de hígado durante el año posterior al trasplante. El tratamiento anticipado comenzó si los valores de β-1,3-D-glucano eran ≥ 40 pg/ml en 2 muestras consecutivas y continuó hasta que los valores de β-1,3-D-glucano eran ≤ 20 pg/ml. En 14 de 40 pacientes en los que se estableció un tratamiento anticipado se pudo demostrar una infección fúngica invasora (7 candidiasis), siendo la mortalidad debida a la infección fúngica del 0,6%.
ADN
La detección de ADN microbiano utilizando la tecnología de la reacción en cadena de la polimerasa (PCR) en tiempo real ha supuesto un gran avance en el campo del diagnóstico de algunas enfermedades infecciosas causadas por bacterias y virus. Sin embargo, en el diagnóstico de la candidiasis invasora, los avances son muy modestos, ya que la mayoría de las publicaciones utilizan técnicas desarrolladas en cada laboratorio y no hay pruebas comercializadas, por lo que no hay una prueba estandarizada que pueda utilizarse de forma universal. Como consecuencia de este hecho, la detección de ADN fúngico no se ha incluido entre los criterios microbiológicos de enfermedad invasora fúngica probable establecidos por la EORTC/MSG de Estados Unidos13. El desarrollo de pruebas comercializadas en el futuro es fundamental para la realización de estudios en los que se pueda evaluar, por diferentes grupos de trabajo, la utilidad de la detección de ADN de Candida como marcador biológico de la candidiasis invasora. Una revisión reciente de la utilidad de la detección de ADN de Candida en el diagnóstico de la candidiasis invasora puede encontrarse en los trabajos de Laín et al23, Arancia et al4, Colom et al12, Ellepola y Morrison16 y Bretagne y Costa10.
Actualmente hay una serie de problemas que deben resolverse en la detección de ADN para el diagnóstico de la candidiasis invasora, incluidos la elección de la muestra óptima (suero o sangre completa; ambas muestras pueden ser complementarias ya que el origen del ADN puede ser diferente: libre en el suero y procedente de células inviables e intracelular en la sangre completa, procedente de células viables9), el método de extracción del ADN, la especificidad de los cebadores, el formato de la PCR, la detección y la identificación de varias especies del género Candida simultáneamente (ya que no todas las especies de Candida tienen la misma sensibilidad a los antifúngicos), el coste y, sobre todo, la interpretación de un resultado positivo para poder diferenciar una infección de una colonización, especialmente en pacientes con colonización alta por Candida. La introducción de la PCR en tiempo real y los métodos automáticos de extracción han solucionado algunos de los problemas asociados con la contaminación de la muestra y con el tiempo de realización de la prueba.
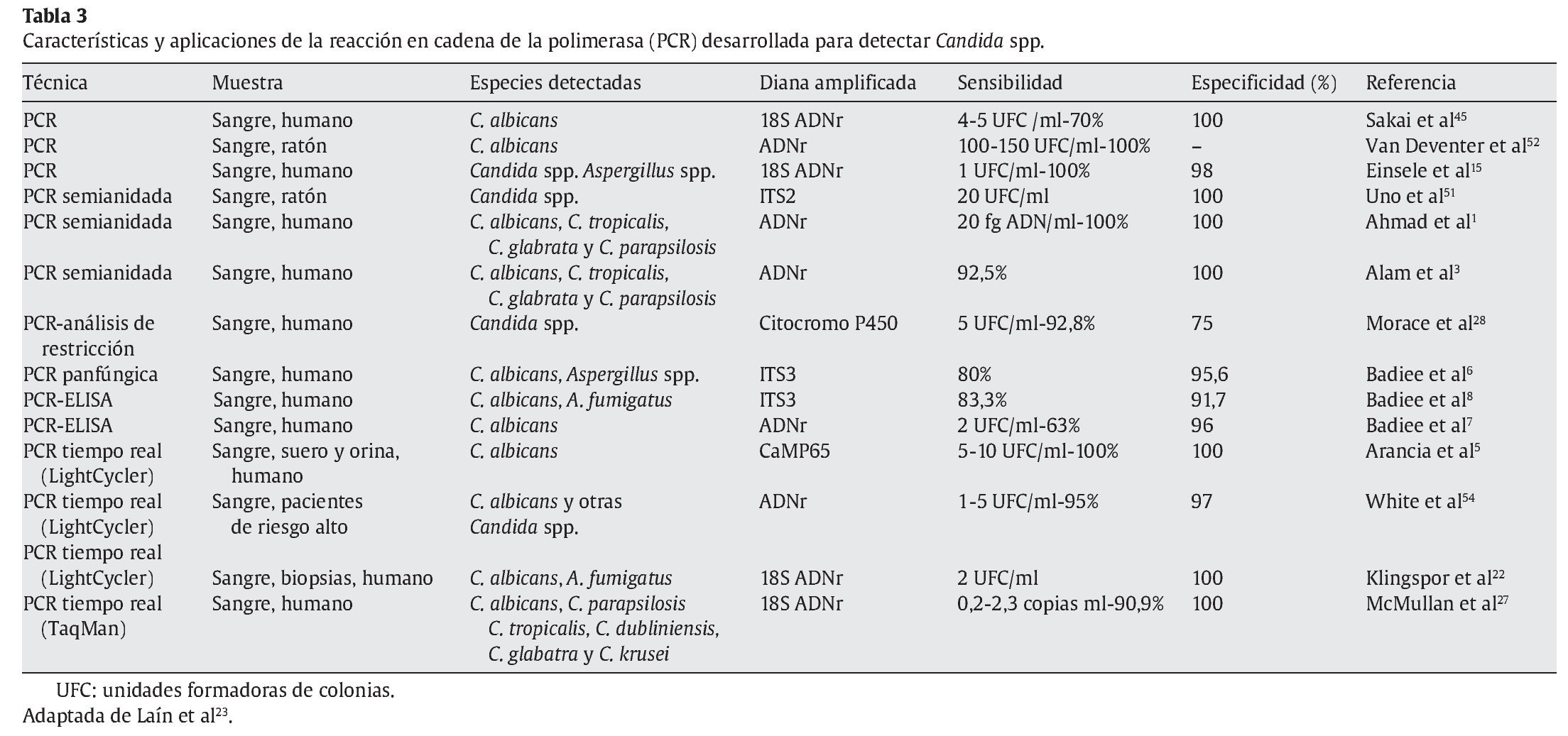
Los estudios realizados hasta el momento indican que la detección de ADN de Candida para el diagnóstico de la candidiasis invasora es sensible y específica (tabla 3) y en algunos casos se ha utilizado para establecer el comienzo del tratamiento antifúngico y el seguimiento de su eficacia19,26. La sensibilidad de la técnica es muy necesaria, ya que en las fases iniciales de la infección el número de unidades formadoras de colonias en los tejidos puede ser muy bajo. Sin embargo, como se ha comentado anteriormente, el principal problema en la actualidad es la reproducibilidad entre laboratorios que impide obtener resultados ampliamente validados.
Anticuerpos
Los avances en el campo de la detección de anticuerpos en el diagnóstico de la candidiasis invasora se han producido en la detección de anticuerpos antimicelio y frente a una serie de antígenos recombinantes de C. albicans. La comercialización de la prueba Candida albicans IFA IgG, para la detección de anticuerpos antimicelio, ha conseguido la estandarización de la técnica y permite el diagnóstico de la candidiasis invasora con una sensibilidad del 84,4% y una especificidad del 94,7%29, resultados similares a los obtenidos con la prueba no comercializada original18,21,42-44.
Los anticuerpos antimicelio van dirigidos frente a antígenos de C. albicans que se expresan mayoritariamente en la superficie de la pared celular de la fase micelial del hongo y que se asocia con la invasión tisular. Dado que algunos de estos antígenos pueden obtenerse en el laboratorio como proteínas recombinantes, Laín et al24 desarrollaron un ELISA para detectar anticuerpos contra el fragmento aminoterminal de la Hwp1, una proteína específica de la fase micelial de C. albicans50. Con esta prueba se consiguió una sensibilidad del 88,9%, una especificidad del 82,6%, un valor predictivo positivo del 80% y un valor predictivo negativo del 90,2%. Estos valores fueron muy similares a los obtenidos al detectar anticuerpos antimicelio (el 80,6, el 91,1, el 87,9 y el 85,4%, respectivamente). La cinética de ambos anticuerpos fue similar, a pesar de que los pacientes con infección por especies diferentes de C. albicans suelen tener títulos más bajos de anticuerpos anti-Hwp1 que los infectados por C. albicans.
Clancy et al11 utilizaron un ELISA para evaluar la respuesta de anticuerpos séricos frente a 15 antígenos recombinantes de C. albicansen 60 pacientes con candidiasis invasora debida a diferentes Candida spp. y en 24 controles sin infección. Los antígenos utilizados comprendían proteínas de la pared celular (Bgl2p, Muc1p-1 y Muc1p-2), enzimas glicolíticas localizadas en la pared celular (Eno1p, Fba1p, Gap1p, Pgk1p-1 y Pgk1p-2), proteínas intracelulares localizadas en la pared celular (Not5p, Met6p-1 y Met6p-2) y proteínas intracelulares probablemente no localizadas en la pared celular (Car1p, Rbt4p, Set1p e IPF9162). La media de la respuesta inmunoglobulina (Ig) G frente a los 15 antígenos fue significativamente más alta en los pacientes con candidiasis invasora que en los controles. Al utilizar un análisis diferenciador, que incluía la respuesta IgG frente a los 15 antígenos, se obtuvo un modelo de predicción matemática que identificó a los pacientes con candidiasis invasora con una sensibilidad del 96,6% y una especificidad del 95,6%. Con un modelo de predicción más refinado que comprendía la respuesta IgG frente a 4 antígenos (Set1p, Eno1p, Pgk1p-2 y Muc1p-2), se obtuvieron resultados idénticos a los obtenidos con todos los antígenos. Estos resultados confirman los obtenidos por Laín et al25, los cuales detectaron anticuerpos frente a una enolasa recombinante de C. albicans con el Candida enolasa ELISA IgG kit (Laboratorios Vircell, Granada [España]) y se obtuvo una sensibilidad del 81%, una especificidad del 83,9%, un valor predictivo positivo del 79,1% y un valor predictivo negativo del 85,5% en el diagnóstico de la candidiasis invasora. Los anticuerpos contra la enolasa de C. albicans asociada a la pared celular podrían tener valor pronóstico, ya que Pitarch et al38 han observado que los pacientes con candidiasis invasora que presentaban estos anticuerpos tenían un riesgo reducido de mortalidad a los 2 meses. Estos autores también han observado que los anticuerpos frente a la 1,3-β-glucosidasa del glucano y a la fosfoglicerato cinasa de la pared celular de C. albicanspredecían la candidiasis invasora en los pacientes estudiados.
Utilizando un corte > 10 AU/ml, la detección de anticuerpos anti-manano presenta una sensibilidad baja (47%), pero una especificidad alta (100%)3. Sin embargo, en combinación con otros marcadores biológicos, la sensibilidad puede aumentar al 100%. Sendid et al48 han combinado la detección de anticuerpos antimanano con la detección de manano de C. albicans, anticuerpos contra el manano de Saccharomyces cerevisiae (ASCA) y anticuerpos contra fragmentos del glucano (ALCA) y quitina (ACCA) en el diagnóstico de la candidemia, obteniendo un 100% de sensibilidad diagnóstica. Los valores de ACCA, ASCA y ALCA se encontraban elevados en los pacientes con candide-mia, aunque los valores de ASCA y ALCA no fueron diferentes de los encontrados en pacientes con enfermedad de Crohn.
Combinaciones de marcadores biológicos
Dado que todas las técnicas utilizadas en el diagnóstico de laboratorio de la candidiasis invasora tienen limitaciones, la combinación de técnicas diagnósticas es una posibilidad que se recomienda en muchos trabajos, porque los resultados obtenidos con una técnica pueden suplir las deficiencias de las otras40. La realización de varias pruebas diagnósticas presenta el inconveniente de la complejidad de realización y de su elevado coste, pero puede ser necesaria para obtener resultados óptimos. Sin embargo, en algunos estudios, la combinación no ha dado resultados satisfactorios. Prácticamente, se han estudiado todas las combinaciones posibles en el diagnóstico de la candidiasis invasora, incluidos antígenos y anticuerpos, antígenos y ADN, y antígenos, metabolitos y ADN. En la tabla 4 se muestra un resumen de estas combinaciones.
Conclusiones
La detección combinada de algunos marcadores biológicos de la candidiasis invasora como el manano, el β-1,3-D-glucano, la detección de anticuerpos antimicelio y frente a algunos antígenos recombinantes, así como la detección de ADN de Candida, puede ser de importancia no sólo en el diagnóstico de la candidiasis invasora, sino también en la evolución de las estrategias terapéuticas, y en particular en el establecimiento de un tratamiento antifúngico anticipado. Este tratamiento podría reemplazar al tratamiento empírico, una vez que se consolide el uso de estos marcadores20.
Ya que el diagnóstico de la candidiasis invasora, basado en la detección de un marcador biológico en una única muestra, carece de sensibilidad, es necesario estudiar muestras seriadas, tomadas teniendo en cuenta la cinética de cada marcador, mientras el paciente presenta un riesgo alto de tener la micosis.
Agradecimiento
La investigación del autor se ha financiado con los proyectos PI070376 del Fondo de Investigación Sanitaria, IT-264-07 del Departamento de Educación, Universidades e Investigación del Gobierno Vasco y Saiotek del Departamento de Industria, Comercio y Turismo del Gobierno Vasco.
Declaración del autor
El autor no tiene nada que declarar.
Historia del artículo:Recibido el 2 de febrero de 2009 Aceptado el 9 de febrero de 2009
Correo electrónico: jose.ponton@ehu.es