INTRODUCCIÓN
La prostatitis afecta del 2 al 10% de la población mundial. De acuerdo con la clasificación de consenso de Estados Unidos del Instituto Nacional de Salud, hay 4 categorías de prostatitis1:
- Categoría I: prostatitis bacteriana aguda.
- Categoría II: prostatitis bacteriana crónica.
- Categoría III: prostatitis crónica/síndrome doloroso pélvico crónico (PC/SDPC), subclasificada en: A, con evidencia objetiva de inflamación en secreciones prostáticas (en orina por masaje prostático o semen), y B, sin evidencia de inflamación en secreciones prostáticas.
- Categoría IV: prostatitis inflamatoria asintomática.
La prostatitis crónica/síndrome doloroso pélvico crónico es un problema de salud pública, pues provoca deterioro de la calidad de vida de quienes la presentan, causando 2 millones de visitas medicas al año en Estados Unidos2.
La inervación del piso pélvico no está bien comprendida. Recientemente se descubrió el nervio del músculo elevador del ano que procede de los segmentos S3 a S5 e inerva el tercio superior del piso pélvico3. Las fibras nerviosas son mixtas, con fibras aferentes y eferentes, somáticas y autónomas. Las fibras nerviosas aferentes, desde la uretra viajan a la medula espinal a través de los nervios pudendo, pélvico e hipogástrico. El nervio pudendo transmite la sensación de la mucosa uretral, piel del área genital y canal anal, y transmite los impulsos propioceptivos del piso pélvico, así como impulsos eferentes somáticos desde S2 a S4, en compañía de los nervios pélvicos4.
El piso pélvico es el soporte de las vísceras abdominales y pélvicas, y permanece tónicamente contraído en las posiciones de sentado y de pie. Además de contribuir a la continencia urinaria y fecal, el piso pélvico se ha involucrado en funciones posturales y respiratorias al modificar la presión intraabdominal, junto con los músculos de la pared abdominal5.
Hay estudios que sugieren que los pacientes con PC/SDPC tienen alteraciones en las vías aferentes y eferentes del sistema nervioso autónomo2. Yilmaz et al6 demostraron cambios en la respuesta autónoma cardíaca de pacientes con SDPC comparado con voluntarios sanos. Esos cambios se atribuyen a sensibilización central con hiperexcitabilidad de las neuronas del asta posterior de la médula sacra, especialmente a estímulos nociceptivos de calor y dolor2; por ello, los pacientes presentan dolor real, no porque esté en su mente, sino porque esos nervios tienen el umbral al dolor muy disminuido, especialmente los nervios perineales. Lo anterior explica la dificultad para controlar el cuadro doloroso de los tratamientos convencionales en el SDPC, que básicamente se han enfocado en el manejo antibiótico y antiinflamatorio.
Las fibras musculares pueden volverse hiperexcitables, iniciando contracciones espontáneamente, esto da lugar a potenciales de fibrilación que pueden aparecer en varias semanas7 y en el caso de los músculos del piso pélvico, provocando inestabilidad2 y disfunción.
El SDPC en varones se ha relacionado con prostatitis, y alteraciones vesicales y del piso pélvico2,8 . Esta incapacitante y debilitante patología se ha vuelto refractaria al tratamiento estándar con antibióticos y antiinflamatorios, por ello, para su tratamiento, se han usado terapias de rehabilitación física como la biorretroalimentación9. La electromiografía (EMG) de la musculatura del piso pélvico (MPP) mediante aguja o con electrodo rectal se ha usado para evaluar varones con SDPC, sin embargo no hay reportes usando EMG con electrodos de superficie cutáneos10 (EMS) comparando voluntarios sanos con varones con SDPC, que provean información diagnóstica para una mejor selección terapéutica.
Objetivo
Comparar la EMS en varones con SDPC y voluntarios sanos, para obtener un parámetro diagnóstico usando este sencillo recurso diagnóstico y terapéutico.
PACIENTES Y MÉTODO
Se incluyeron 11 voluntarios sanos (grupo control [GC]) y 12 varones con SDPC (grupo problema [GP]). Todos firmaron consentimiento informado11, no pagaron por el estudio y, a cambio, se les dio la consulta gratuita y/o se les donaron servicios médicos no relacionados con la patología en estudio.
El criterio de inclusión en el GP fue dolor pélvico crónico con un mínimo de 3 meses de evolución, sin causa patológica específica que explicara el cuadro clínico. Se excluyeron los pacientes con cultivo de orina y/o semen positivos, con historia de litiasis, tuberculosis genitourinaria, biopsia y/o cirugía prostática o vesical, cáncer vesical o prostático y radiación. Se reportaron edad, promedio de microvoltios (µV) de la EMS en reposo (PAVRG), mínimo del trazo, máximo del trazo y amplitud del trazo electromiográfico, evolución en meses, usando una base de datos comercial Excel y se analizó con el software estadístico comercial SPSS10.0, se usó análisis multivariado con intervalo de confianza del 95%.
Se usó el equipo de EMG Verimed®, con electrodos cutáneos para EKG marca 3M, aplicados a 3 cm del esfínter anal en los radios de 2 y 10 h después de practicar tricotomía y preparación de la superficie cutánea con alcohol metílico de uso médico.
El estudio se realizó por la misma enfermera-técnica especializada en terapia de biorretroalimentación, sin conocer los datos de los sujetos. Se usó la sala de Urodinamia y Uroneurología del Centro de Urología Avanzada. Siempre se evitó que los sujetos observaran el monitor de EMG.
Casos y controles fueron sometidos a un protocolo modificado de EMS diseñado por Glazer. El protocolo de Glazer se define por una secuencia de contracciones voluntarias de los músculos del piso pélvico y mediciones estadísticamente definidas por EMS durante esas contracciones10. El protocolo se realizó como sigue: con el paciente con la vejiga previamente vacía; en posición sentado, semirreclinado y con las piernas ligeramente semiflexionadas por almohadas en la parte posterior12, para evitar respuesta postural del piso pélvico5, asegurando la ausencia del deseo de orinar:
- Fase 1: trazo en reposo basal (60 s).
- Fase 2: contraer repetidamente el periné y relajar.
- Fase 3: contraer sostenidamente durante 10 s.
- Fase 4: durante 60 s contraer intensa y sostenidamente.
- Fase 5: trazo en reposo posbasal (60 s).
RESULTADOS
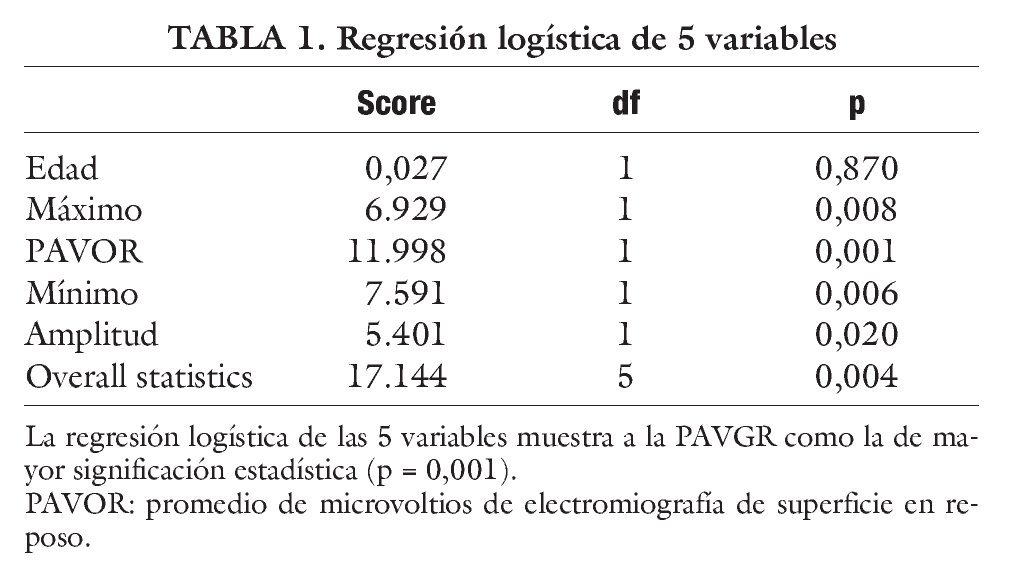
La media de la edad fue de 46,36 años (± 10,63 años) en el GC y de 45,58 años (± 12,96 años) en el GP. La regresión logística demostró que la variable mas importante es PAVGR (Wald = 5,4; p = 0,019) como se muestra en la tabla 1.
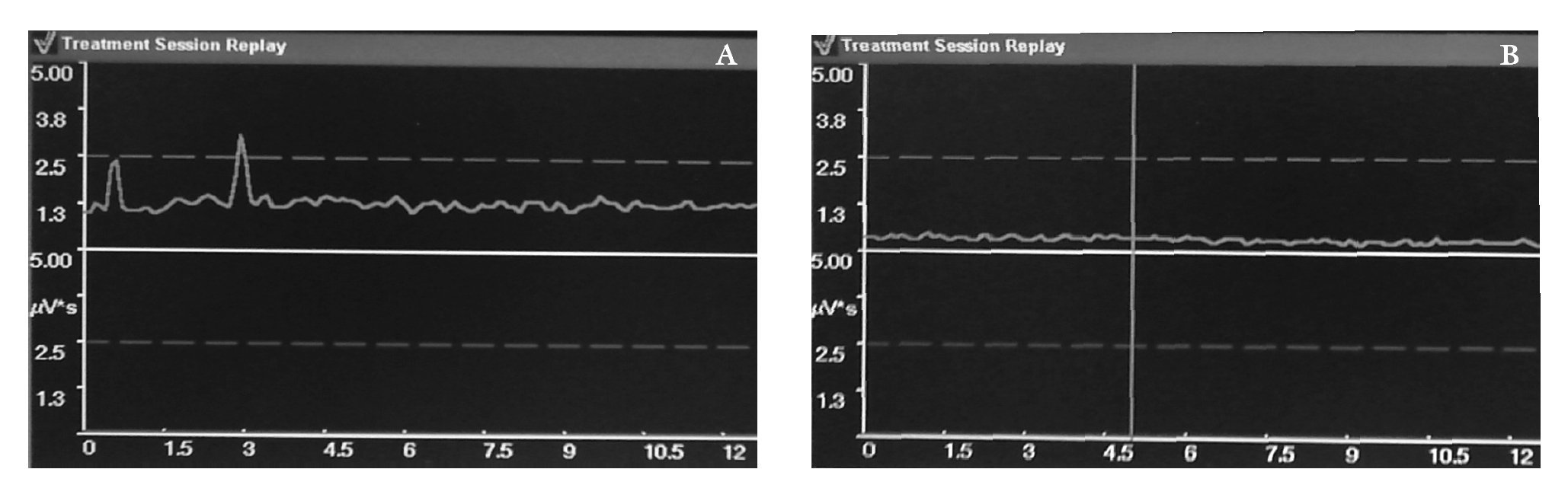
El PAVRG representa el tono muscular en reposo y fue de 0,079 µV (± 0,084 µV) en el GC y de 0,49 µV (± 0,27 µV) en el GP, siendo 0,41 µV mayor en el GP (p = 0,000). En la figura 1 se muestra el trazo de EMS de un paciente con SDPC comparado con un control. La media de la amplitud del trazo de EMS representa la actividad eléctrica del músculo en reposo, y fue de 0,044 µV (± 0,026 µV) en el GC y de 0,65 µV (± 0,79 µV) en el GP, siendo 0,60 µV mayor en el GP (p = 0,019). La media del tiempo de evolución del GP fue de 25,5 meses (± 20,3 meses).
DISCUSIÓN Y CONCLUSIONES
La EMS con parches cutáneos es suficientemente fina para registrar la actividad eléctrica muscular en el piso pélvico, proporcionando medidas estadísticamente útiles para diferenciar los casos de los controles.
La variable más importante en la EMS es la media del PAVRG, que representa el tono muscular del piso pélvico en reposo. La diferencia significativa de la media del PAVRG demuestra un elevado tono muscular en varones con SDPC comparado con los voluntarios sanos. Además, los pacientes con SDPC tienen un piso pélvico inestable, demostrado por la mayor amplitud del trazo del EMS (p = 0,019).
En la figura 1 se muestra el trazo de electromiografía de un paciente con SDPC, el cual tiene una curva con mayor amplitud que se interpreta como inestabilidad de la MPP comparado con un voluntario sano, también se muestra la hipertonía muscular que se caracteriza por mayor microvoltaje en los casos que en los controles, con una diferencia estadísticamente significativa entre ambos grupos.
Figura 1. Electromiografía de superficie. (A) Trazo de electromiografía de un paciente con síndrome doloroso pélvico crónico, el cual tiene una curva con mayor amplitud (inestabilidad muscular) y de mayor microvoltaje (hipertonía muscular) comparado con un voluntario sano (B).
Estos datos sugieren que la EMS puede ser de gran utilidad diagnóstica en pacientes con SDPC, y abre la posibilidad de diferenciar los pacientes que van a tener una buena respuesta al tratamiento "convencional" de los que tendrán mayor dificultad para el control del cuadro doloroso.
La sugerencia de usar alternativas terapéuticas enfocadas a la inestabilidad e hipertonía del piso pélvico es clara2,6, como la biorretroalimentación, la neuromodulación9 y el uso del botox13, en virtud del componente neurológico del SDPC demostrado previamente2,6 y confirmado por el presente estudio realizado en varones latinos.
Correspondencia:
Dr. C. Pérez-Martínez.
Centro de Urología Avanzada.
Avda. Agricultura Pte. 514, Col. Centro. Cd. Delicias 33000, Chih., México.
Correo electrónico: carlosperezm@prodigy.net.mx