El virus del papiloma humano (HPV por sus siglas en inglés) es una de las infecciones de transmisión sexual más frecuentes en el mundo y es descrito como el principal agente causal del cáncer cervicouterino (99,7%). En mujeres existe abundante información sobre esta infección, mientras que sus características en población masculina son poco conocidas.
Material y métodoSe realizó una búsqueda de bibliografía actualizada de la infección por HPV en hombres y su relación con distintos tipos de cáncer.
ResultadosLa infección por HPV en hombres podría estar asociada a tumores de piel, región perianal, amígdala, orofaringe, laringe, esófago, próstata y uretra. La infección por HPV generalmente es silente, por lo cual no produce síntomas o signos clínicos evidentes, provocando que un gran número de personas estén infectadas sin saberlo, lo cual constituye un problema tanto para el hombre como para su pareja sexual. Los estudios de prevalencia muestran que las zonas de mayor presencia del virus son en poblaciones jóvenes de África y América Latina, donde los programas de vacunación contra este virus tardarán en concretarse.
DiscusiónEs importante incorporar métodos diagnósticos para HPV en la población masculina e incrementar la vacunación de esta. Asimismo, el control periódico de la población de hombres infectados por la asociación entre HPV y cáncer es crucial, especialmente en las áreas anatómicas asociadas a las enfermedades de transmisión sexual.
Human papillomavirus (HPV) is one of most frequent sexually transmitted infections worldwide. It has been described as the principal agent for cervical uterine carcinoma (99.7%). There is abundant information on this infection in women, however, its characteristics in the male population still remains unclear.
Materials and methodsA search of updated bibliography on HPV infection in males and its relationship with several forms of cancer was conducted.
ResultsHPV infection in men could be associated to skin, perianal, tonsils, oropharynx, pharynx, esophagus, prostate and urethra carcinoma. HPV infection is usually silent, so that there are no clear symptoms or clinical signs. Therefore, there are many infected people who are unaware that they have HPV infection. This is a problem for men as well as their sexual partner. Prevalence studies show that the areas having the greatest presence of the HPV virus are in the young populations of Africa and Latin America. This is where the vaccine programs against this virus are slow in materializing.
DiscussionIt is important to incorporate diagnosis methods in male population and to increase HPV vaccine in men. Furthermore, periodic control of the HPV-infected male population is crucial, especially in the anatomical areas associated to sexual transmission diseases.
El virus del papiloma humano (HPV por sus siglas en inglés) corresponde al microorganismo más frecuentemente aislado en infecciones de transmisión sexual (ITS) en el mundo, infectando a hombres y mujeres por igual1. Se estima que la tasa de infección en la población varía entre el 2 y el 44%, dependiendo de la región geográfica, pero las tasas más altas se han reportado en el África subsahariana y en Sudamérica2.
El HPV es un virus pequeño, sin envoltura, perteneciente a la familia de los Papillomaviridae3. Su cápside icosaédrica está compuesta por 72 capsómeras (60 hexámeros y 12 pentámeros), con un diámetro aproximado de 55nm. El contenido genético consiste en un ADN circular de doble hebra con aproximadamente 7.900 pares de bases. Su material genético se divide en 3regiones: una región de control LCR (long control region), una región temprana E (early) y una región tardía L (late)4.
Existen más de 200 tipos virales, de los cuales aproximadamente 40presentan tropismo por el área anogenital y mucosas. Estos genotipos pueden ser agrupados en HPV de alto riesgo y bajo riesgo oncogénico1. Los HPV de bajo riesgo oncogénico incluyen los tipos 6, 11, 40, 42, 43, 44, 54, 61, 70, 72 y 81, y los de alto riesgo oncogénico, los tipos 16, 18, 31, 33, 34, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68, 70, 73 y 825. A nivel mundial los genotipos virales más frecuentes en el cáncer cervicouterino son HPV16 y HPV186,7.
El HPV es estable extracelularmente, ya que es resistente al calor y la desecación y puede ser transmitido directamente a otros individuos o a través de fómites8. Alternativamente las células infectadas permanecen en el ambiente antes de que el virus sea transmitido a una nueva superficie epitelial, como ocurre en virus que infectan superficies cutáneas8-10.
Virus del papiloma humano en hombresLa infección por HPV en el hombre fue considerada como un problema menor y de escasa relevancia. En general, se ha catalogado al hombre como vector silencioso de este microorganismo, ya que a pesar de jugar un papel importante en la transmisión del virus, solo el 1% de ellos presentan algún signo o síntoma clínico11. Sin embargo, la frecuencia de infección en la población masculina en general es elevada, con porcentajes que varían desde el 1,3 al 84%, dependiendo de la región geográfica y del rango etario estudiado. En Chile, un estudio realizado a estudiantes universitarios reveló que el 84% de los casos estudiados eran positivos para HPV12, porcentaje mayor a lo reportado en estudios similares realizados en Estados Unidos (62%)13 y Corea del Sur (8,7%)14. La frecuencia de HPV en hombres de la Universidad de Washington (EE.UU.), en diferentes tipos de muestras (cuerpo del pene, prepucio, glande, escroto y orina), demostró porcentajes variables (6 al 28%), siendo el prepucio el área con mayor porcentaje de positividad para HPV15. En México, un estudio en jóvenes asintomáticos de 20 a 29 años reveló un 50% de casos positivos para HPV16. Estudios realizados en jóvenes militares revelaron porcentajes variables dependiendo del país en estudio. En México, el 48% de los soldados estudiados fueron positivos para HPV17, mientras que en Finlandia solo lo fueron el 9,1%18 y en Suecia el 12%19. Esta tendencia a un incremento de la infección en América ha sido confirmada con un estudio de Giuliano et al. (2008)20 que encontró un mayor porcentaje de positividad de HPV en hombres en Brasil (72,3%), seguido de México (61,9%) y de Estados Unidos (61,3%). El grupo etario con mayor frecuencia de infección fue entre 30 y 34 años, y el de menor frecuencia en hombres, entre 18 y 19 años. Otro estudio realizado en pacientes con uretritis indicó un porcentaje muy bajo de pacientes con HPV, alcanzando solo el 1,3% en Japón21. En el análisis de 12estudios realizados entre 1991 y 2005 se describe una frecuencia de infección por HPV en hombres heterosexuales de entre el 3,5 y el 45%, con predominio de HPV16 en todos los casos13.
Entre los estudios estadísticos se pueden observar variaciones en los porcentajes de frecuencia de HPV, lo cual puede ser debido a las diferentes poblaciones evaluadas, a la diferente sensibilidad de los métodos usados y a la forma de toma de muestra, debido a que la carga viral de cada zona del tracto genital masculino es diferente15.
El estudio de la infección por HPV en hombres se ha incentivado desde mediados de los años ochenta, debido a la asociación entre HPV y otros cánceres distintos al de cuello uterino y, además, a la asociación de una mayor frecuencia de cáncer en pacientes portadores del virus de la inmunodeficiencia humana (VIH)22. Por ello es de gran relevancia la actualización de la bibliografía en cuanto a la relación de la infección por HPV en hombres y el desarrollo de cáncer en los mismos infectados o en sus parejas sexuales.
Materiales y métodosSe realizó una revisión bibliográfica del estado del arte de la infección por HPV en hombres y su relación con el desarrollo de diversos tipos de cáncer. Para ello se realizó una búsqueda en el servidor <www.pubmed.com> en relación con palabras claves tales como «HPV infection», «HPV in male», «HPV and cancer», etc., el mes de mayo de 2012. Los criterios de inclusión en la revisión fueron la atingencia de los artículos, la relevancia y su nivel de actualidad. En esta revisión se incluyeron 57artículos relacionados con la epidemiología y las características generales del HPV, las diferencias en el estudio del HPV en mujeres y en hombres, la infección por HPV en hombres y su relación con el cáncer.
ResultadosVirus del papiloma humano y cáncer en hombresEn mujeres, como consecuencia de la infección por HPV, se desarrollan displasias en las células cervicales, lo que se manifiesta por alteraciones en la forma, el tamaño y la organización del epitelio. Cuando estas lesiones traspasan la lámina basal hacia el estroma del tejido se denomina carcinoma invasor del cuello uterino (CCU)1. En hombres, la infección por HPV se ha asociado principalmente a condilomas genitales y cáncer de pene, que es poco frecuente en esta población23. Recientes estudios han demostrado la asociación entre la infección por HPV en el hombre y el cáncer perianal, oral, de piel, de próstata, de tonsila palatina, pulmonar, orofaríngeo, laríngeo, de esófago y de uretra20,24.
En países desarrollados la frecuencia de HPV en cáncer de pene, oral y anal son similares a lo descrito en CCU en la mujer20. Su incidencia se ha mantenido constante (cáncer de pene y oral), pero el cáncer anal ha incrementado su incidencia en la población general tanto en hombres como en mujeres, encontrándose presencia de HPV16 en al menos el 70% de los casos. Este cáncer está siendo más frecuente en la mujer que en el hombre, con una incidencia anual de un caso por cada 100.000 mujeres, especialmente asociado a una mayor positividad de HPV a nivel anal que cervical, cuya frecuencia se incrementa notablemente en mujeres VIH positivas25. Por otro lado, el cáncer anal en hombres que tienen sexo con hombres presenta elevadas tasas de incidencia, con valores de 37 casos por cada 100.000 hombres25. Estos datos muestran la real necesidad de desarrollar nuevos métodos diagnósticos eficaces y de bajo coste para que los hombres que portan HPV no infecten a sus parejas hetero u homosexuales y a su vez inicien controles médicos con el fin de detectar precozmente lesiones neoplásicas o preneoplásicas del ano.
En zonas no genitales la frecuencia de cáncer con presencia de HPV ha aumentado. Se ha estimado que el 58% de los tumores a nivel orofaríngeo están relacionados con la presencia del virus26. Existe similitud entre lesiones genitales inducidas por HPV (condilomas) y tumores de células escamosas (papilomas y carcinomas) de la mucosa esofágica, esto apoyado por la demostración de proteínas estructurales de HPV en esas lesiones mediante inmunohistoquímica27-29 y la asociación genética de HPV con lesiones esofágicas benignas y malignas, lo que ha originado un amplio espectro de antecedentes publicados en diferentes regiones geográficas30. La infección por HPV en la mucosa esofágica ha recibido un creciente interés científico como posible factor de riesgo para carcinoma epidermoide esofágico (CEE). La presencia de HPV en mucosa esofágica normal y en lesiones precursoras de cáncer sugiere una participación temprana del HPV en la clásica secuencia displasia-carcinoma31. El porcentaje de pesquisa de ADN de HPV ha mostrado diferencias entre diferentes áreas geográficas, y el aporte de HPV oncogénico al riesgo de CEE es mayor en áreas de mayor frecuencia de este30. En zonas de alto riesgo de CEE se encontró aproximadamente el 60% de positividad para HPV en muestras de tumor32.
La patogenicidad del virus ha orientado la búsqueda de su participación en otros tipos de cáncer, como por ejemplo el pulmonar, donde presenta una incidencia promedio del 24,5%, considerando entre el 15 y el 17% la frecuencia en Europa y Estados Unidos, y del 35,7% en población asiática33,34.
Otro de los cánceres asociados a HPV es el cáncer de próstata, cuya asociación se realizó por primera vez en 1990 por McNicol y Dodd35. Desde entonces se han realizado varios estudios, con la detección de HPV entre el 4,2 y el 53% de las muestras36.
Un hecho importante a considerar es la co-infección de HPV con VIH. Al poco tiempo del descubrimiento del VIH, durante la década de 1980, se comenzó a asociar la infección por VIH con una mayor prevalencia de HPV, debido a que existía una alta tasa de cánceres producidos por HPV en pacientes inmunodeprimidos, principalmente en hombres que tienen sexo con hombres que presentaban una alta incidencia de cáncer anal37. En general, los países con una alta frecuencia de VIH también poseen las más altas incidencias de cánceres producidos por HPV, debido a que ambos son transmitidos por vía sexual y se asocian a promiscuidad38. La circuncisión masculina es una de las medidas preventivas que se han tomado en África para disminuir la incidencia tanto de infección por VIH como por HPV en hombres. Además, la circuncisión masculina es capaz de disminuir la transmisión de HPV a la pareja, aunque el varón se encuentre infectado con este virus, pero no tiene efecto en la trasmisión de VIH.
Comportamiento del virus del papiloma humano en el aparato reproductor masculinoMuy pocos estudios hacen mención al comportamiento del HPV en el tracto reproductor masculino39. La localización más frecuente hasta ahora descrita es el prepucio del pene, aunque la relación entre la pareja sexual y el tipo viral en el hombre todavía no está dilucidada39.
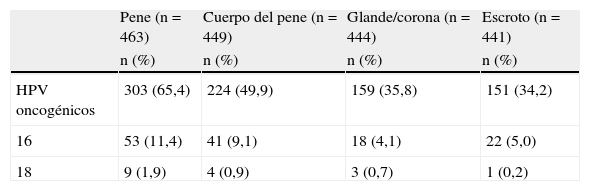
El tipo de reservorio del virus en áreas anogenitales del hombre usando la técnica reverse line blot (RLB) demostró que el HPV se encuentra con más frecuencia en el cuerpo (49,9%) y en el glande o corona del pene (35,8%)40. El porcentaje de semen infectado con HPV es relativamente bajo (5,3%); sin embargo, es importante su estudio, debido a que este fluido es el que entrara en contacto y permanecerá mayor tiempo en el tracto genital femenino (tabla 1).
Prevalencia de infección por HPV en varios tipos de muestras del aparato reproductor masculino
| Pene (n=463) | Cuerpo del pene (n=449) | Glande/corona (n=444) | Escroto (n=441) | |
| n (%) | n (%) | n (%) | n (%) | |
| HPV oncogénicos | 303 (65,4) | 224 (49,9) | 159 (35,8) | 151 (34,2) |
| 16 | 53 (11,4) | 41 (9,1) | 18 (4,1) | 22 (5,0) |
| 18 | 9 (1,9) | 4 (0,9) | 3 (0,7) | 1 (0,2) |
| Área perianal (n=436) | Canal anal (n=436) | Uretra (n=278) | Semen (n=337) | |
| n (%) | n (%) | n (%) | n (%) | |
| HPV oncogénicos | 87 (20,0) | 68 (17,6) | 28 (10,1) | 18 (5,3) |
| 16 | 8 (1,8) | 6 (1,5) | 3 (1,1) | 5 (1,5) |
Adaptado de Nielson et al., 200740.
El virus HPV se une a los espermatozoides, pero hay escasa información de las bases moleculares de esta interacción. La presencia del virus está asociado a diferentes zonas del espermatozoide, principalmente en el cuello y en la cola (16% de muestras positivas para HPV6, 16, 18 y 31)41. Esta ubicación varía según el genotipo viral y es probablemente dependiente de las proteínas localizadas en el sector42. Existe una posible asociación de proteínas de membrana, de la familia de proteoglicanos de heparán sulfato (HSPG), y proteínas de la cápside viral, como L1. Más específicamente, el HPV podría interactuar con el complejo Syndecan-1, el cual es un proteoglicano ampliamente expresado en la membrana de las células epiteliales, cuya función es prácticamente desconocida en espermatozoides43. Asimismo, espermatozoides transfectados con los genes tempranos E6 y E7 son capaces de penetrar y expresar estos genes en ovocitos de hámster (HEPT test)43.
La persistencia del virus en la membrana de los espermatozoides tras procesos de selección espermática y lavados realizados previamente a procedimientos de reproducción asistida42 genera la necesidad de estudiar compuestos para separar el virus antes de desarrollar estos procedimientos, pues el espermatozoide podría actuar como vector del virus, siendo un riesgo de potencial de infección a la pareja sexual del donante44. El método experimental más utilizado para separar el HPV de los espermatozoides ha sido la incubación con heparinasa-iii, aunque no todos los genotipos de HPV tienen el mismo comportamiento. Para el HPV16, la heparinasa inhibe la unión del virus a la membrana del espermatozoide por su capacidad de hidrolizar los HSPG de las membranas plasmáticas donde este se uniría45,46. A pesar de los prometedores resultados obtenidos con HPV16 (el HPV más frecuente a nivel mundial)47 y la heparinasa-iii, se ha reportado una disminución de la motilidad de los espermatozoides expuestos a este compuesto, así como un posible aumento de la fragmentación del ADN espermático, entre otras alteraciones que no han sido totalmente caracterizadas ni medidas, lo cual hace necesario más estudios sobre el tema, y también testear otros compuestos de menor valor comercial e inocuos43,44,46.
DiscusiónLa alta frecuencia de HPV en el hombre, y su asociación con CCU y con otros cánceres, sugiere prevenir esta infección primero en hombres que en mujeres. Esto permitiría disminuir la tasa de mortalidad por CCU, que es la segunda neoplasia más prevalente en mujeres a nivel mundial y la quinta causa de muerte por cáncer en esta población47-51.
Entre los métodos de prevención se encuentran mantener una sola pareja sexual, la circuncisión, el uso de condón y la vacunación, debido a que existe una fuerte asociación entre el número de parejas sexuales que han tenido tanto la mujer como su compañero a lo largo de su vida y la adquisición de HPV16. Otra posible acción de prevención es la circuncisión del hombre, que ha sido uno de los procedimientos que ha promovido la disminución en la frecuencia de infección por el virus52,53 con una menor probabilidad de infección prevalente por HPV en el área genital de hombres circuncidados comparados con aquellos que no lo están (OR: 0,57). El efecto de la circuncisión fue más notorio al disminuir la infección en el glande, en la corona del pene y en la uretra, comparado con otras zonas distales hacia el prepucio.
El uso del condón también ha sido materia de estudio, aunque los reportes no llegan a un consenso. Se ha señalado al condón como un protector de la infección por HPV, pues se observa una disminución en la incidencia de patologías cervicales54. No obstante, la prevalencia de HPV no presenta una disminución tan significativa, pues existe un 65,9 vs 71,9% entre la población que usa condón y la que no lo usa55.
Un tema que genera controversia es la posibilidad de vacunar contra el HPV a los hombres en vez de las mujeres. Actualmente se encuentran disponibles en el mercado 2vacunas contra el HPV: Gardasil™, una vacuna que cubre los genotipos virales 6, 11, 16 y 18, producida por Merck & Co., Inc., y Cervarix™, vacuna bivalente que abarca a HPV16 y 18, producida por Glaxo-Smith Kline. La FDA aprobó el uso de las vacunas tanto en hombres como en mujeres, informando que en las mujeres prevendría el desarrollo del cáncer cervical y en hombres la aparición de verrugas genitales causadas por los HPV6 y 11 y el cáncer anal56; sin embargo, no mencionan la posible asociación de HPV y otros cánceres en el hombre, ni tampoco que el hombre es el vector silencioso del CCU, por lo que su vacunación podría disminuir radicalmente la incidencia del cáncer cervical uterino, como también el cáncer anal en hombres que tienen sexo con hombres57. Actualmente en Estados Unidos y en Australia se ha optado por la vacunación de hombres, lo cual ha permitido disminuir la incidencia del CCU, como consecuencia de la disminución de los tipos virales HPV16 y 1849.
En forma conjunta a la vacunación, se debería avanzar hacia el diagnóstico precoz de esta enfermedad —ya que, a diferencia del sida, no existen programas para detectar este virus oncológico en el hombre—, y ver si estos pacientes deberían asumir su futura paternidad de forma similar a los pacientes portadores de virus inmunosupresores, en los que se recomienda técnicas de medicina reproductiva, y en caso del HPV, una mayor dedicación a obtener medios que logren desprenderlo de la membrana espermática y evitar la transmisión de proteína viral al embrión, del cual desconocemos su efecto o la asociación con aborto precoz. Asimismo, evitar el alto coste que implican la terapia contra el CCU en la mujer y en el propio hombre.
Responsabilidades éticasDerecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Protección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
FinanciaciónEste trabajo fue financiado en parte por Proyecto FONDECYT postdoctorado 3120141, Proyecto FONDECYT postdoctorado 3130630, Proyecto Creación del centro de excelencia en estudios genéticos e inmunológicos (CEGIN) 09CN14-5960 y Núcleo de Desarrollo Científico Tecnológico en Biorecursos (BIOREN).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.