La biopsia es una etapa importante en el diagnóstico de los tumores óseos y de partes blandas. No es un procedimiento sencillo. El objetivo de este artículo es ofrecer algunas sugerencias a los médicos que se encargan del cuidado de estos pacientes y evitar los riesgos inherentes de la biopsia. Las decisiones relacionadas con la indicación de una biopsia y la zona exacta que debe ser biopsiada puede ser la diferencia entre una biopsia eficaz y un desastre. Se debe planificar el proceso de la biopsia, tan cuidadosamente como la cirugía definitiva. Si el cirujano ortopédico o la institución no están convenientemente preparados para realizar los estudios diagnósticos correctos, la cirugía definitiva, ni los tratamientos adyuvantes, el paciente debería ser canalizado a un centro con experiencia en esta dolencia y con un equipo multidisciplinario antes de la realización de la biopsia.
Biopsy is a significant step in the diagnosis of a bone or soft tissue tumor. It is not a simple procedure. The purpose of this article is to offer some suggestions to physicians who care for such patients, to assistance them in avoiding the hazards inherent in the biopsy procedure. Decisions concerning the indication for biopsy, the exact region of the lesion that has to have a biopsy and the anatomic approach and biopsy procedure can make the difference between an efficacious biopsy and a disaster. Plan the biopsy procedure as carefully as the definitive surgery. If the orthopaedic surgeon or the institution is not equipped to accomplish accurate diagnostic studies or definitive surgery and/or adjunctive treatment, the patient should be referred to center, which has experience of these types of neoplasms and equipped with multidisciplinary team prior to performance the biopsy.
La biopsia se define como el procedimiento diagnóstico que extrae una muestra de tejido, mediante métodos cruentos, para ser analizada, al microscopio, con fines diagnósticos. La biopsia no es un evento inofensivo y puede influir en la clasificación y estadificación del tumor, en el tratamiento y tiene un valor pronóstico sobre la morbilidad del paciente. Sin una planificación y ejecución adecuadas, la biopsia puede determinar un curso inadecuado del tratamiento e incluso el pronóstico del paciente.
Antes de hacer una biopsia debemos preguntarnos, en primer lugar, si la lesión debe ser biopsiada y qué parte de la lesión debe ser tomada. También hay que definir la vía anatómica más segura para llegar al objetivo y saber si el equipo está capacitado para realizar el tratamiento completo del paciente y si el centro es experto en el tratamiento de tumores óseos y partes blandas ya que los tumores primarios del sistema músculo-esquelético son raros, siendo difícil adquirir la experiencia necesaria para su tratamiento si no se trabaja en centros con equipos multidisciplinarios expertos en esta enfermedad. Además, la biopsia debe ser efectuada por el mismo equipo multidisciplinario (radiólogo o cirujano) que realizará la cirugía definitiva, y en el caso de que el paciente vaya a ser canalizado a un centro de referencia, no se debería realizar la biopsia.
A pesar de la rareza de estos tumores, el cirujano ortopédico general debe tener un conocimiento amplio de estas lesiones y la forma de efectuar el diagnóstico, además de conocer los diferentes tipos de lesiones y cuándo deben ser derivadas a un centro de referencia para el tratamiento de esta dolencia. El manejo clínico, que incluye pruebas diagnósticas, terapias coadyuvantes, tratamiento quirúrgico y análisis de los especímenes resecados, debe ser llevado a cabo por un grupo de especialistas con formación específica en este tipo de lesiones; no concibiéndose otra estrategia terapéutica1. Todo ello es debido a la complejidad de la interpretación de las imágenes radiológicas y de la morfología histopatológica, en adición a los serios problemas y consecuencias que se originan de biopsias y tratamientos inadecuados para el paciente.
Es fundamental la comunicación entre el cirujano ortopédico oncológico, el radiólogo y el patólogo para evitar errores diagnósticos y el consecuente tratamiento inadecuado de la lesión. Este tipo de enfermos exige que la comunicación entre los diferentes especialistas sea constante, tanto en encuentros informales, como en las reuniones formales de los comités multidisciplinarios periódicos, para una toma de decisiones consensuadas que siempre debe quedar reflejada en la historia clínica.
En comparación con todos los cánceres, el porcentaje de tumores de partes blandas representa el 0,7% del total y el porcentaje de tumores óseos el 0,2%2. Como extrapolación, se puede estimar que la incidencia de sarcomas óseos es de 1/100.000 habitantes al año, es decir, 10 casos por cada millón de habitantes y la incidencia de sarcomas de partes blandas de las extremidades es, aproximadamente, 3 veces superior a la de los tumores óseos, con una incidencia de 35 casos por millón de habitantes. Aunque la probabilidad de tener un tumor de este tipo es remota, cuando un individuo resulta afectado las estadísticas dejan de tener sentido para él, y solo espera poder ser diagnosticado y tratado con los mejores recursos humanos y técnicos que podamos ofrecerle.
Los errores en el manejo de los pacientes con tumores óseos y sarcomas de partes blandas se producen en uno de cada 10 pacientes, afectando su pronóstico por retraso en el diagnóstico, por una biopsia inadecuadamente planificada, por errores en el diagnóstico o por un tratamiento incorrecto. Y ocurre de 3 a 5 veces más frecuentemente cuando la biopsia se realiza en centros de no referencia1,3.
Mankin et al. con miembros de la sociedad americana de tumores músculo-esqueléticos (Musculoskeletal Tumor Society)3 analizaron las biopsias realizadas en 329 pacientes con tumores malignos del aparato locomotor y observaron que en el 8,2% hubo errores importantes en el diagnóstico, en el 10,3% las biopsias fueron no representativas, en el 17,3% tuvieron problemas con la herida quirúrgica de la biopsia, en el 18,2% el plan óptimo de tratamiento tuvo que ser modificado por problemas relacionados con la biopsia, en el 4,5% se realizó una amputación innecesaria, y lo más importante, en el 8,5% el pronóstico quedó adversamente alterado. Esta situación, lejos de mejorar como habría sido de esperar, permanecía prácticamente inalterada 14 años después, cuando el mismo grupo4,5 realizó una nueva revisión, indicando una escasa mejoría sobre los potenciales perjuicios que para el paciente puede acarrear un manejo inadecuado de la biopsia. Sin embargo, el Grupo de Sarcoma Escandinavo1 presentó unos datos más tranquilizadores, su información ha trascendido mejor hacia la comunidad médica y sus recomendaciones de referir todos los pacientes previos a la biopsia han sido más exitosas.
En el manejo de los tumores músculo-esqueléticos existen 2 fases, la etapa diagnóstica, que incluye la fase prebiopsia y la biopsia, y la etapa terapéutica6–12.
En la fase diagnóstica, la biopsia es la etapa final y se realiza después de haber hecho todas las pruebas de imagen y de laboratorios pertinentes. Al valorar la extensión del tumor, mediante las pruebas de imagen y conocer el diagnóstico histopatológico, se procede a la fase de estadificación y de tratamiento. La estadificación se realiza siguiendo los conceptos establecidos por Enneking, reconocidos por la sociedad americana de tumores musculo-esqueléticos (Musculoskeletal Tumor Society), que permiten realizar una evaluación pronóstica y terapéutica de la lesión13.
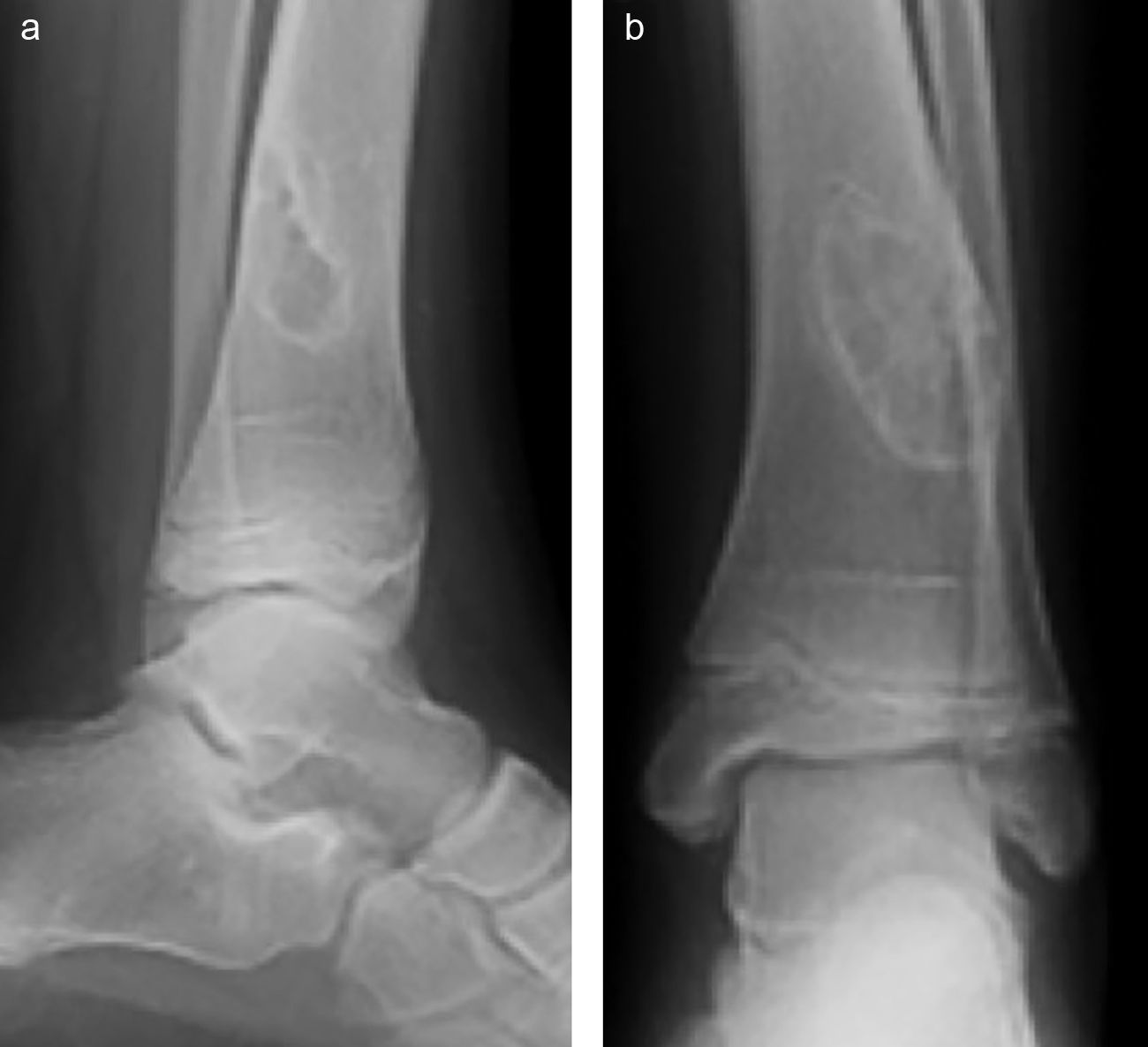
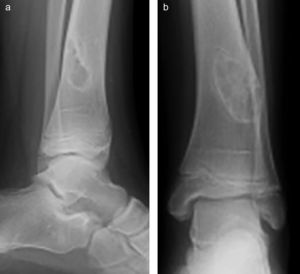
Es preciso destacar que no todos los tumores requieren la realización de una biopsia. En los tumores benignos inactivos, en los que el diagnóstico clínico-radiológico resulta evidente, no es necesario. Sirvan como ejemplo el fibroma no osificante/defecto fibroso cortical (fig. 1), el quiste óseo simple, la displasia fibrosa, el hemangioma vertebral, el osteocondroma y los encondromas en falanges.
a) y b). Lesión osteolítica de tipo geográfico, metafiso-diafisaria distal de la tibia en una paciente de 10 años. Asintomática y hallazgo casual. El diagnóstico radiológico es compatible con fibroma no osificante. No se realizó biopsia y el tratamiento fue seguimiento clínico-radiológico.
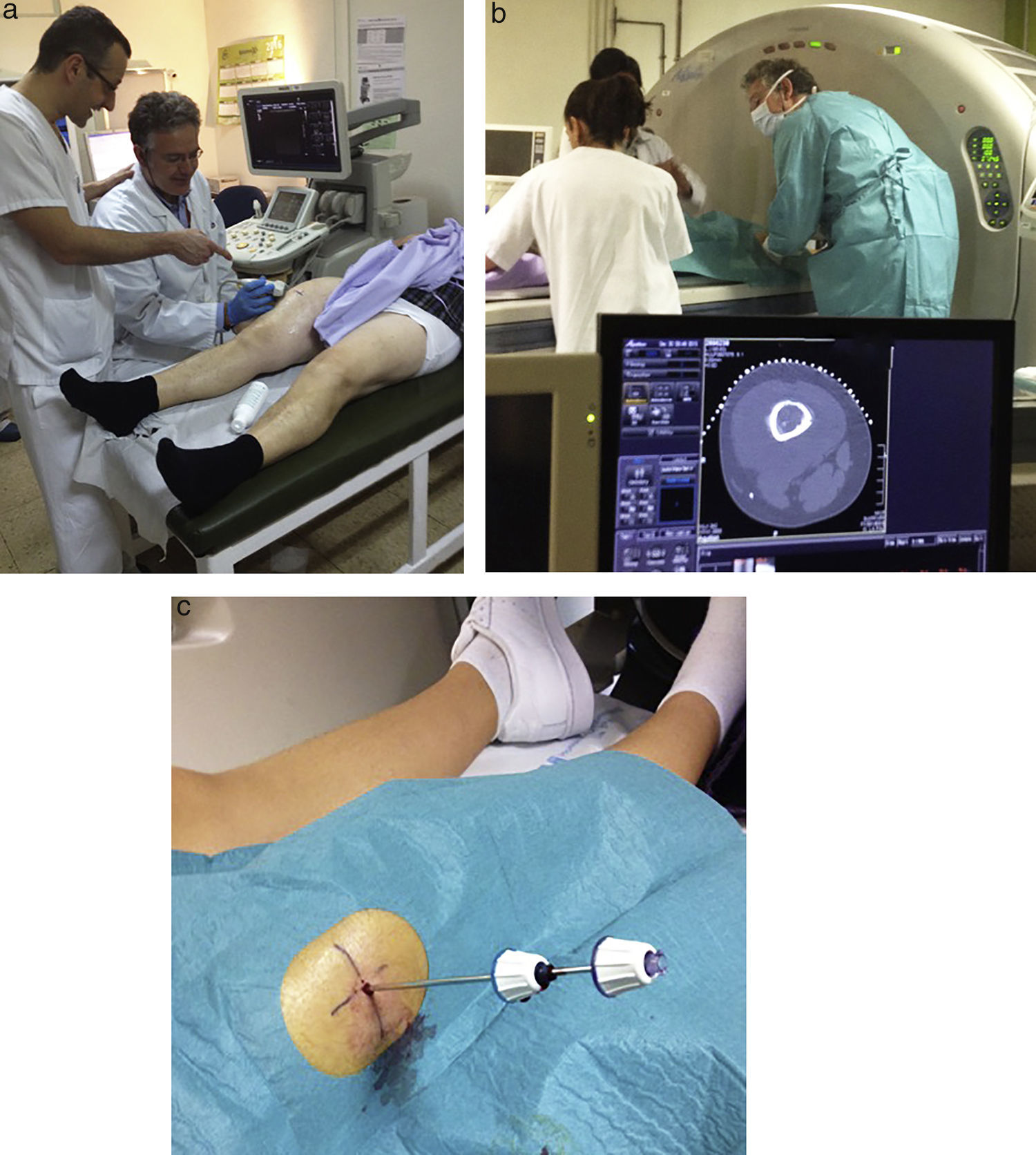
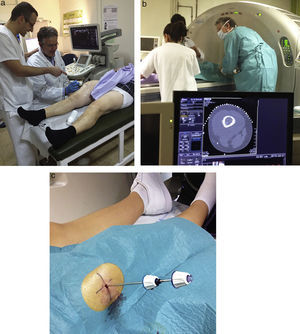
La radiología y el diagnóstico por la imagen son de gran ayuda en la localización de áreas viables del tumor, evitando la toma de biopsias de zonas no representativas que pueden confundir en el diagnóstico histopatológico; por ello, en la mayoría de los casos, los radiólogos deberían realizar las biopsias percutáneas, guiadas mediante TC en caso de tumor óseo o por la ecografía cuando la biopsia es de partes blandas y accesible14. El radiólogo debe estar en comunicación con el cirujano para conocer su vía de abordaje, y tener experiencia en la realización y requisitos de esta técnica percutánea15–18 (fig. 2).
El patólogo músculo-esquelético debe conocer los diagnósticos diferenciales previos a la recepción del tejido en el laboratorio. Un patólogo que se aventure a realizar un diagnóstico sin el conocimiento clínico y radiológico del caso puede cometer errores en el diagnóstico. El patólogo no debería ofrecer un diagnóstico sin conocer el caso, y menos si no ha evaluado en conjunto con el radiólogo y el cirujano ortopédico oncológico las pruebas de imagen19.
Tipos de biopsiaLas biopsias pueden ser abiertas o cerradas. Las técnicas abiertas se llevan a cabo mediante incisiones quirúrgicas, mientras que las cerradas, también llamadas percutáneas, son realizadas mediante agujas finas y gruesas.
Biopsias percutáneasPunción aspiración con aguja finaEs la toma de una muestra mediante la punción del tejido a analizar con una aguja de escaso calibre (23 o 25G) conectada a una jeringa para efectuar una aspiración20,21. Se obtienen células que se extienden en una laminilla; es lo que se denomina citología o extendido citológico. Cuando se estima que es suficiente con obtener una muestra citológica, la punción se realiza con agujas finas (calibre igual o inferior a 18G, ideal 23G) tipo vacu-cut.
Entre sus inconvenientes, resulta imprescindible disponer de un patólogo experto en citología, se pueden tener errores en la toma de la muestra o contar con material insuficiente para el diagnóstico. Además, no se observa la arquitectura del tejido por lo que es difícil que determine el tipo de tumor, aunque sí puede aportar su benignidad o malignidad o de escasa agresividad. Una citología resulta muy difícil en lesiones óseas si la cortical ósea esta íntegra.
Pero entre sus ventajas está que no requiere la resección del trayecto de la biopsia y sirve para el estudio de recurrencias locales y diseminación linfática, así como en tumores con un tipo celular homogéneo, tales como el mieloma, las metástasis y el sarcoma de Ewing. Es un procedimiento ambulatorio que se puede hacer en la propia consulta, con menor coste21 y mayor rapidez en el procesado de la muestra y obtención del resultado.
Biopsia por punción con aguja gruesaTambién se le denomina «core biopsia» o «tru-cut». El tejido de la biopsia se toma mediante pistolas automáticas o semiautomáticas, que reducen la molestia para el paciente. Una vez se coloca la aguja en posición de predisparo, guiada mediante palpación o por técnicas de imagen, como sería la ecografía (fig. 2) o la TC, se presiona el disparador y la parte inferior de la aguja, que es la que succiona el tejido, se proyecta atravesando la lesión y saliendo de ella con la muestra rápidamente. Con esta técnica se toman muestras con mayor cantidad de tejido y no solo extendidos citológicos como sucede en la punción aspiración con aguja fina.
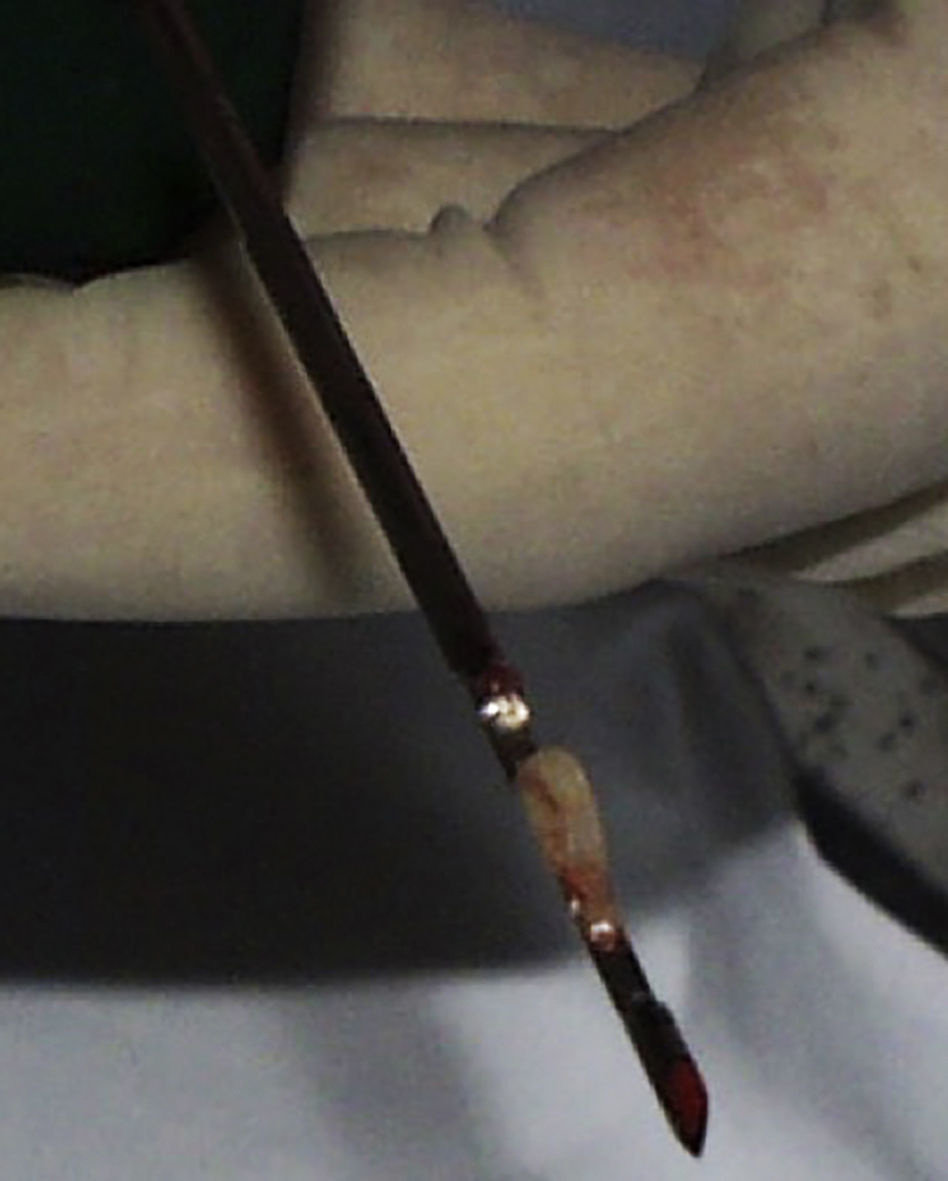
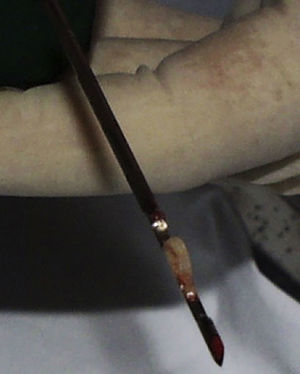
Para obtener material para estudio histológico usaremos agujas tipo tru-cut o core-biopsia, que tienen un calibre entre 18 y 14G. Se indica cuando una lesión ósea tiene componente de partes blandas o es una masa de partes blandas, ya que se obtiene un fragmento de tejido suficiente, de hasta un máximo de 2cm de longitud (fig. 3). En caso de que la lesión ósea no tenga masa de partes blandas, se utilizan las agujas de corte, tipo Ostycut®, Bonopty® o Jamshidi®, que penetran en el hueso. Se ha demostrado que en más del 90% de los casos permiten diferenciar el diagnóstico de benignidad o malignidad20–22. Entre los inconvenientes de la técnica están que resulta imprescindible disponer de un patólogo experto, que hay errores en la toma de la muestra, por disponer de material insuficiente, aunque menor que con la punción aspiración con aguja fina, que su trayecto debe ser resecado en la cirugía definitiva, a diferencia de la punción aspiración con aguja fina, y tiene un mayor potencial de producir un hematoma.
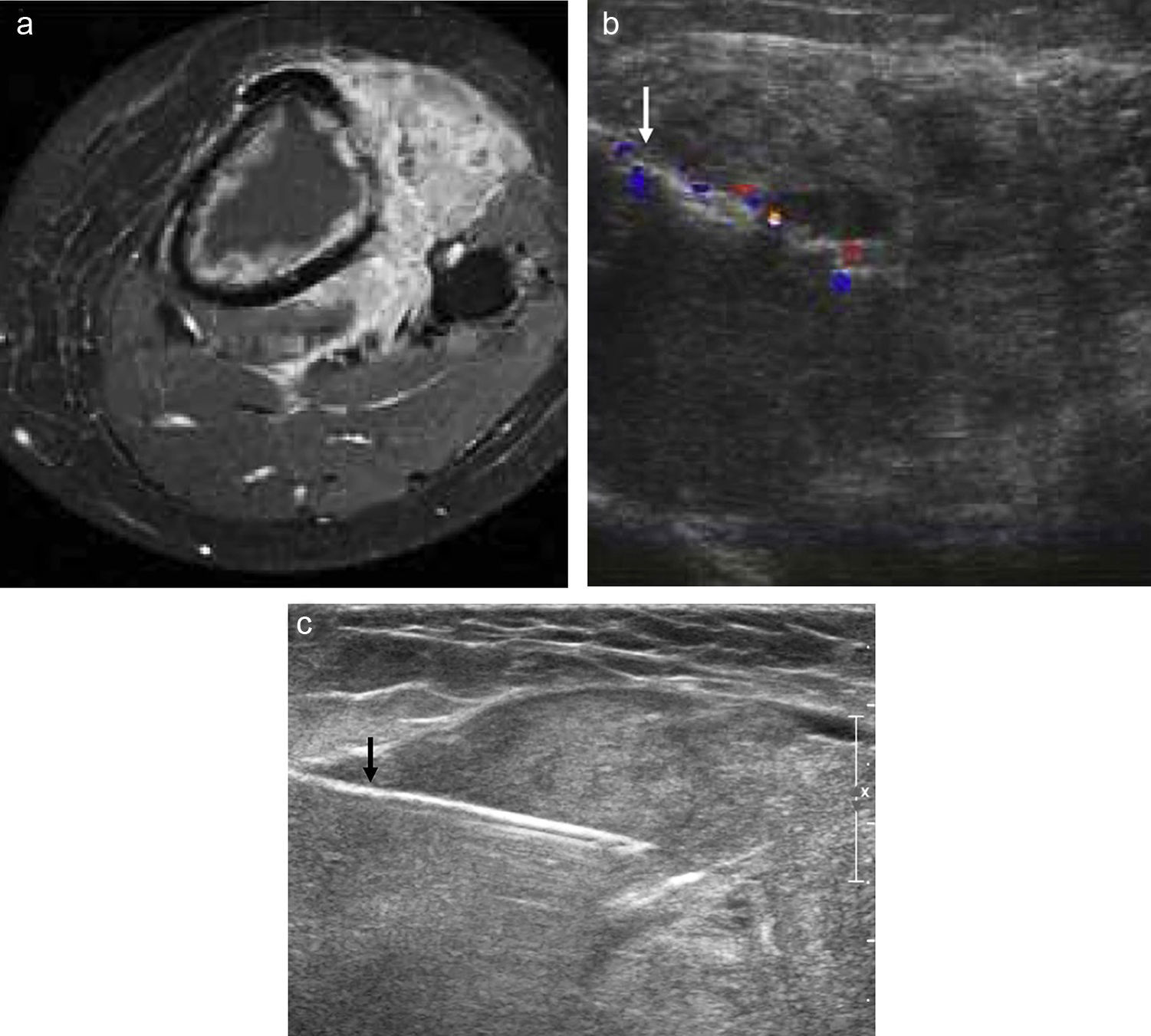
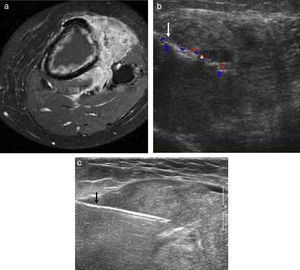
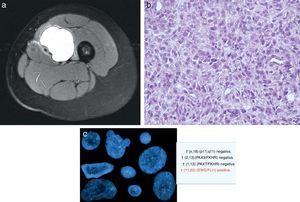
a) RM de un paciente de 48 años con lesión osteolítica en la tibia proximal. b) Se realiza biopsia percutánea guiada con ecografía (flecha). El diagnóstico histopatológico fue linfoma no Hodgkin. c) Mujer de 32 años con tumoración de partes blandas en el codo. Biopsia percutánea con aguja tru-cut 16G y control mediante ecografía, de un sarcoma sinovial.
Pero también es un procedimiento ambulatorio que consigue mayor cantidad de tejido (fig. 4) con menor probabilidad de obtener muestras insuficientes y con mejor acceso a las áreas de difícil abordaje quirúrgico, como es la columna o la pelvis23 (fig. 5).
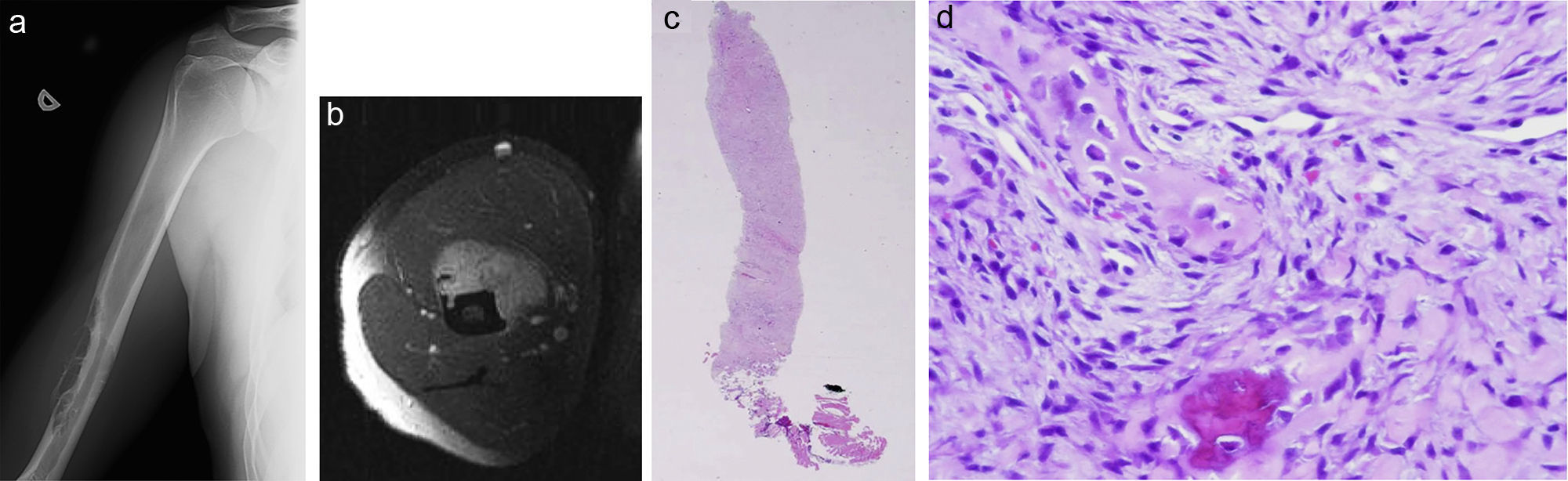
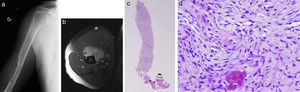
Paciente de 43 años, con un dolor en el brazo derecho. a) radiografía de lesión osteolítica. b) La RM confirma la lesión y las partes blandas adyacentes. c) Se realizó una biopsia con tru-cut. Correlacionando las imágenes con la anatomía patológica, el diagnóstico fue osteosarcoma yuxtacortical humeral. d) El estudio histopatológico de la pieza tras la resección del tumor confirmó el hallazgo de la biopsia con tru-cut.
Las biopsias abiertas, como su nombre indica, están tomadas mediante incisiones quirúrgicas y se realizan en quirófano, con las técnicas asépticas de una cirugía convencional24.
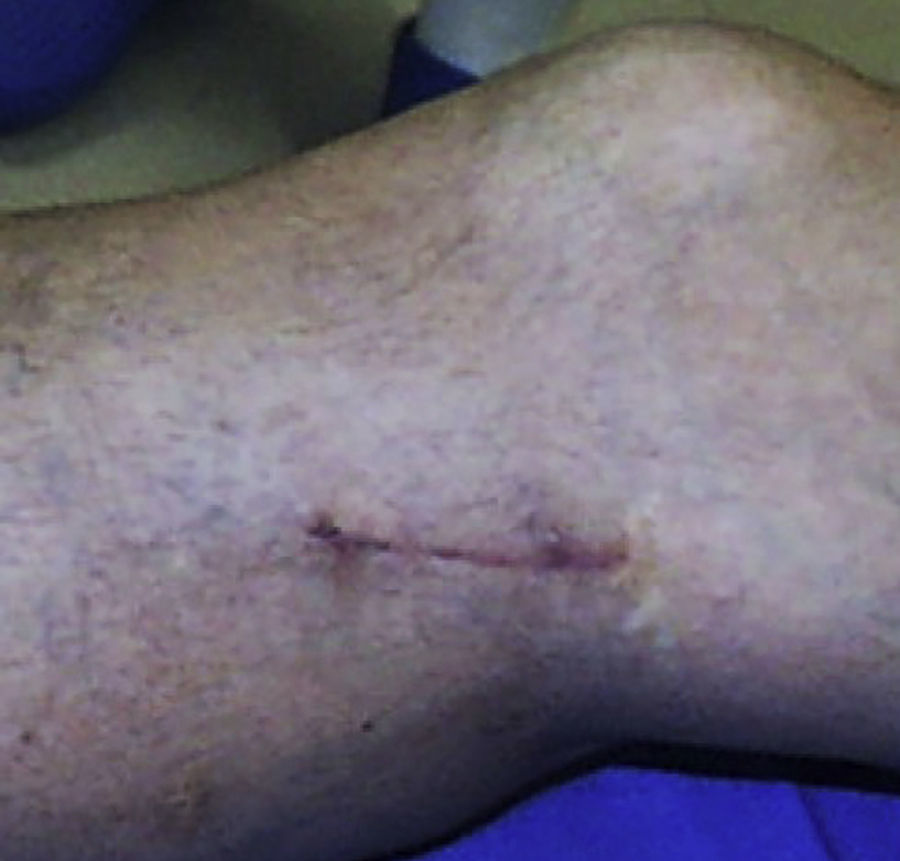
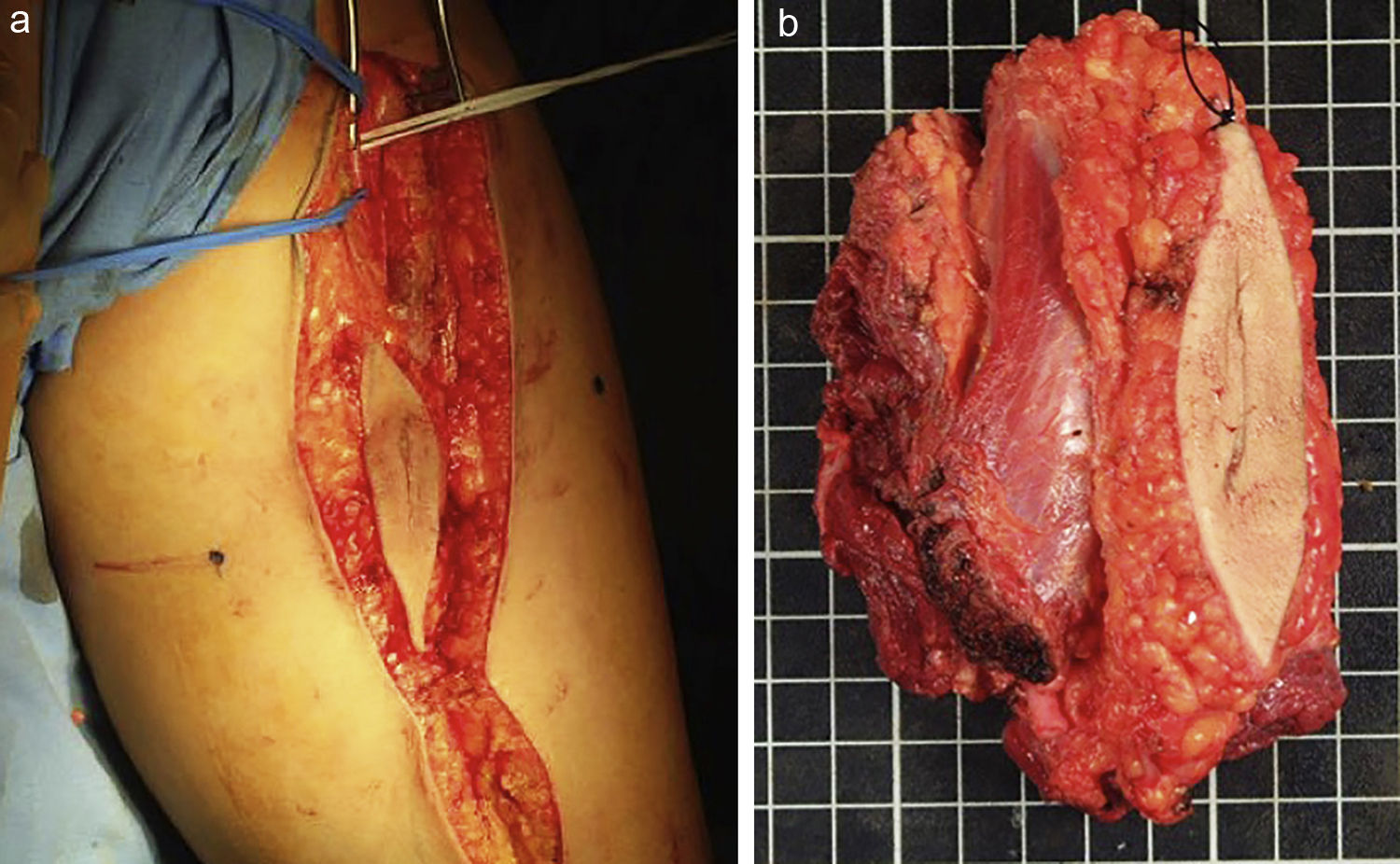
IncisionalEs la biopsia en la que se extrae solo un fragmento del tumor. Se realiza mediante una mínima incisión (fig. 6). Se obtiene mayor cantidad de tejido para el diagnóstico y para pruebas complementarias como son la inmunohistoquímica, citogenética, genética molécula, citometría de flujo y microscopia electrónica, que ayudan a clasificar mejor el tumor22 (fig. 7).
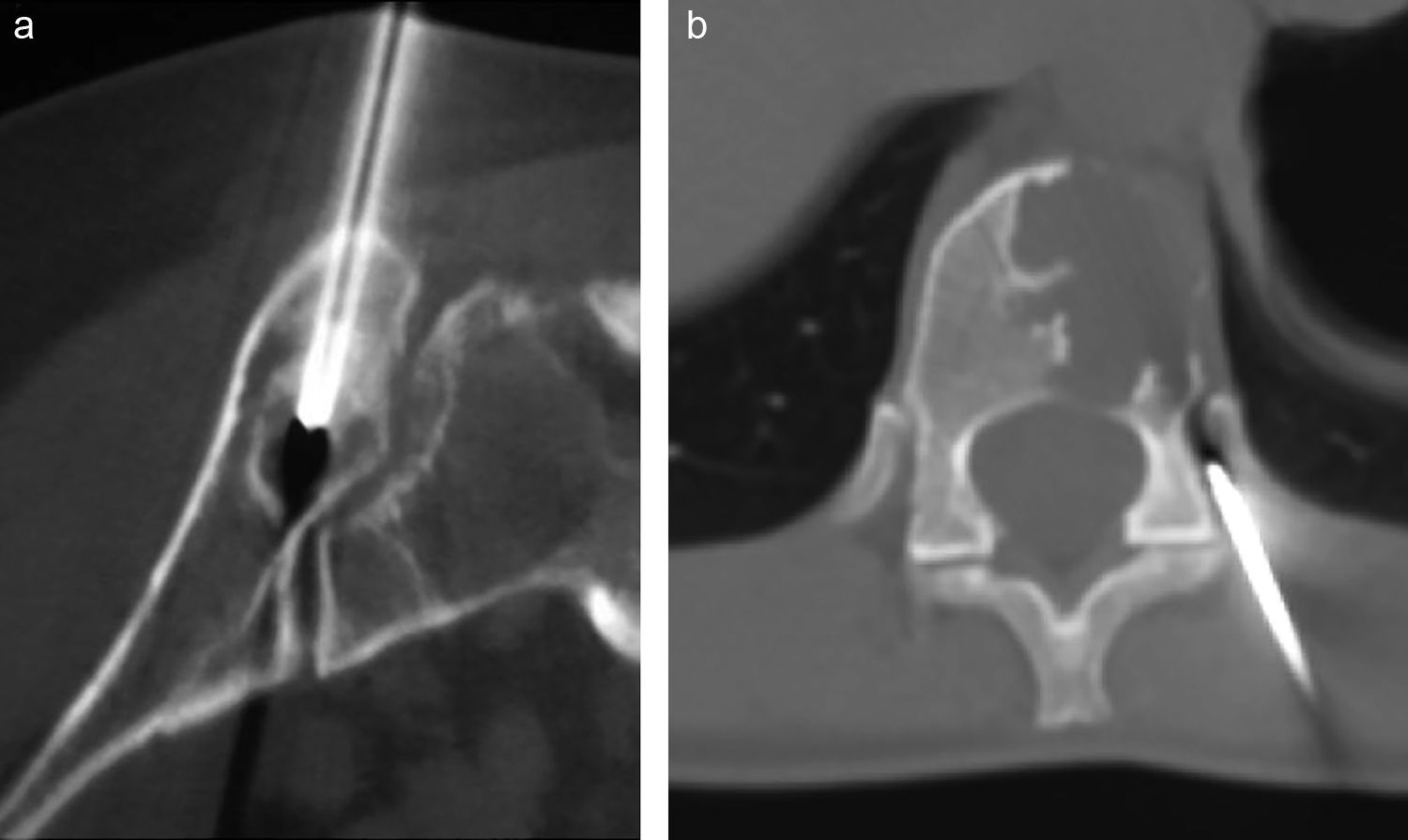
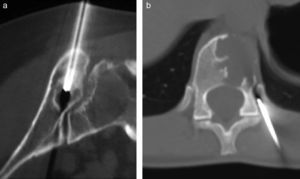
Lesiones óseas localizadas en columna y pelvis. La biopsia percutánea es el método de elección en estas localizaciones. La biopsia en estas localizaciones se realiza guiada con TC. a) Lesión osteolítica en el ilíaco cercana a la articulación sacro-iliaca. Biopsia percutánea con diagnóstico de osteoblastoma. b) Lesión osteolítica en el cuerpo vertebral de T11. Biopsia percutánea que confirma un diagnóstico de tumor de células gigantes.
Pero presenta mayor potencialidad de siembra tumoral en el trayecto de la biopsia y el trayecto debe ser resecado en la incisión de la cirugía definitiva (fig. 8). Es más laboriosa la resección del trayecto de una incisión que el trayecto de un tru-cut y también de mayor costo.
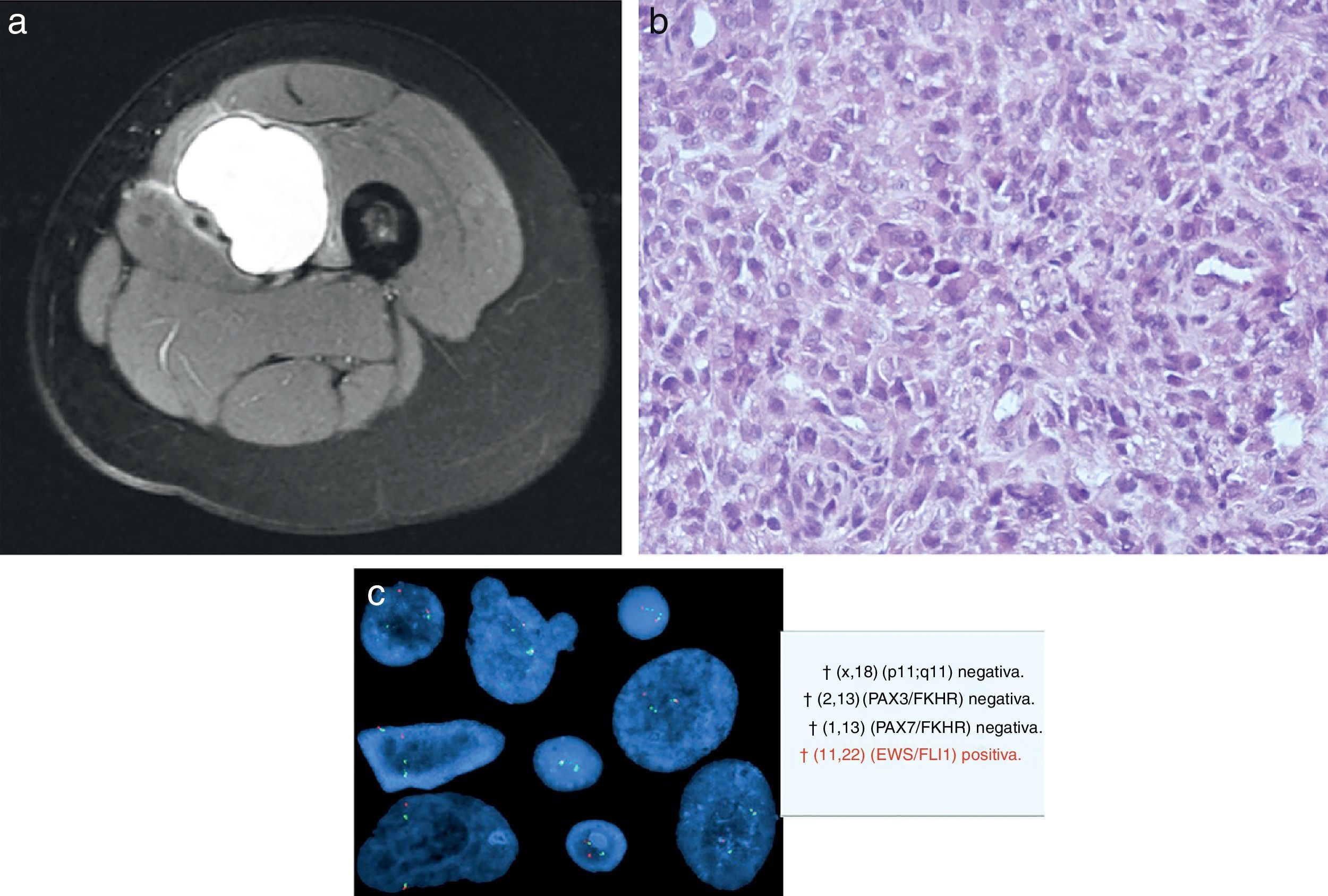
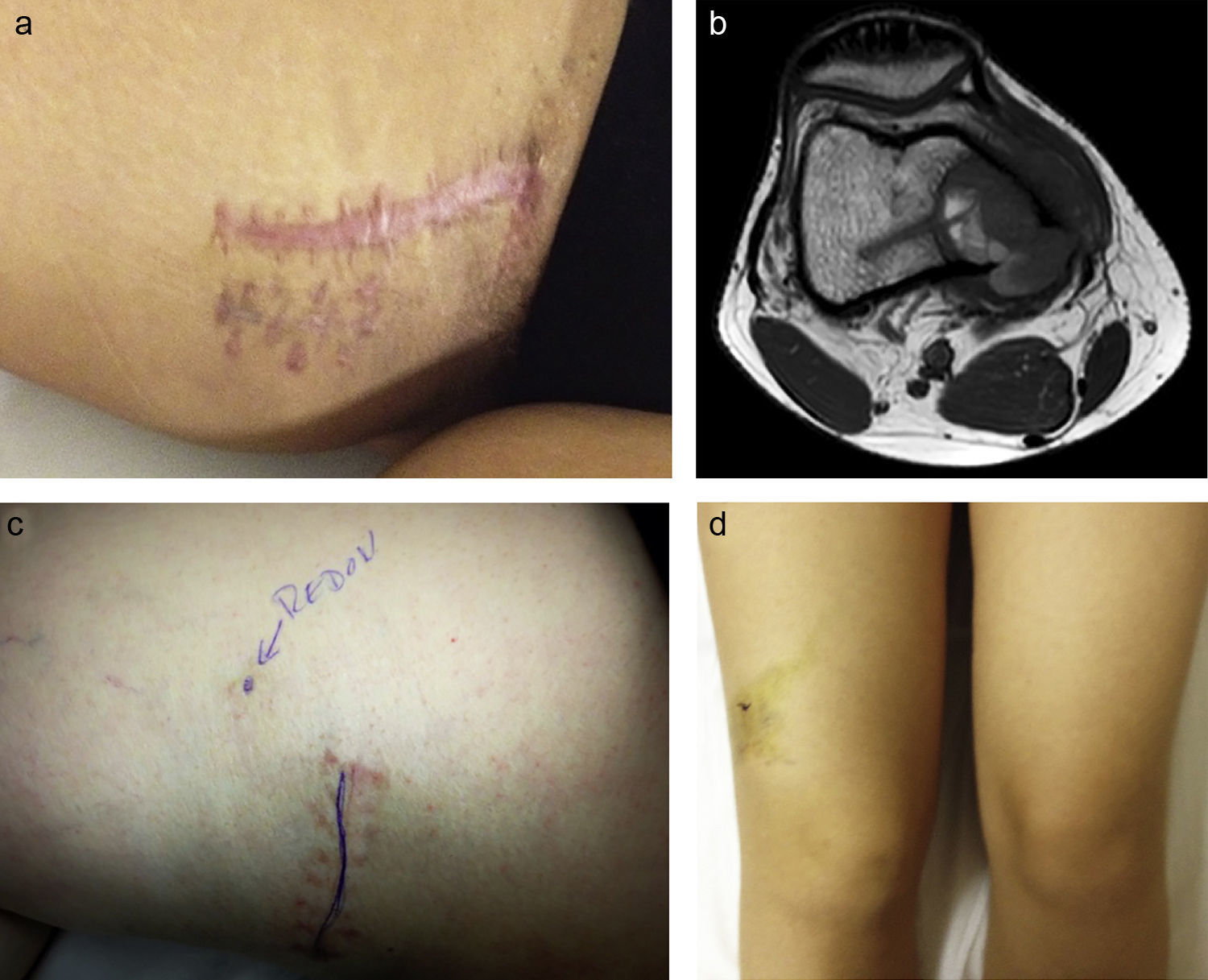
a) Mujer de 22 años, con dolor en cara interna de muslo y con cojera. Se aprecia un bulto. La RM demuestra masa de partes blandas en la cara anteroexterna del muslo. Se realizó biopsia percutánea con material insuficiente, por lo que fue necesaria una biopsia incisional. b) Biopsia compatible con sarcoma de Ewing, aunque fue necesario la realización de estudio de translocación mediante FISH. c) FISH del material extraído en la biopsia incisional que confirma el diagnóstico de sarcoma de Ewing, mediante la confirmación de la translocación t11,22 (EWS/FLI1).
Es la toma de tejido de toda la lesión tumoral, lo que conlleva la extracción de todo el tumor y no se debe realizar a menos que la impresión diagnóstica sea claramente la de un tumor benigno, como un osteocondroma, o un lipoma (fig. 9). A la mínima duda durante el procedimiento de una biopsia excisional o extirpación de una masa, en lugar de resecar la masa, se debe realizar una biopsia incisional y no seguir adelante con el procedimiento.
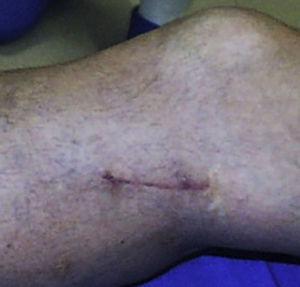
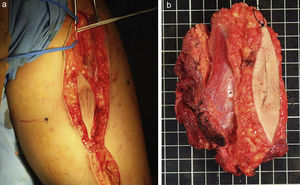
a) Resección del trayecto de la biopsia incisional de la paciente de la figura 8. b) Resección con márgenes amplios del tumor y con el trayecto de la biopsia incluido en la misma.
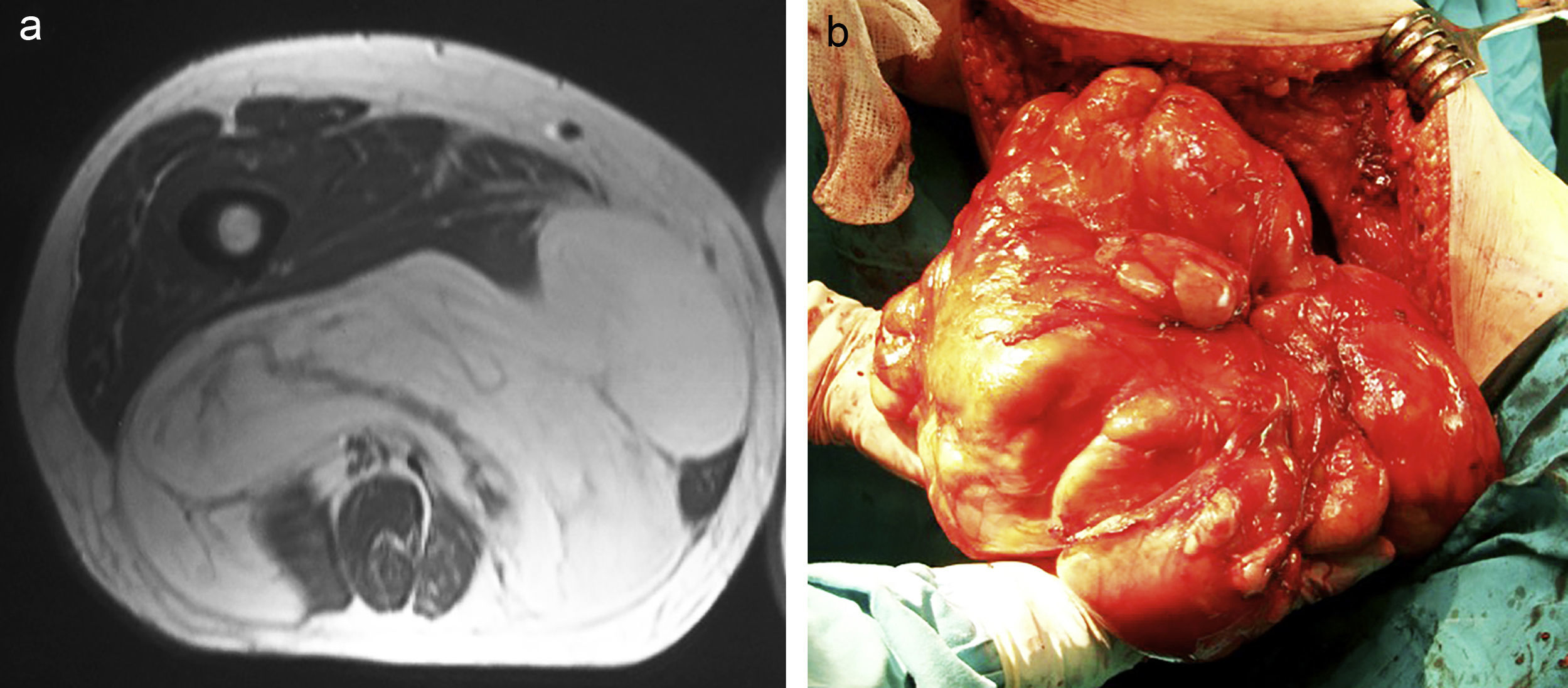
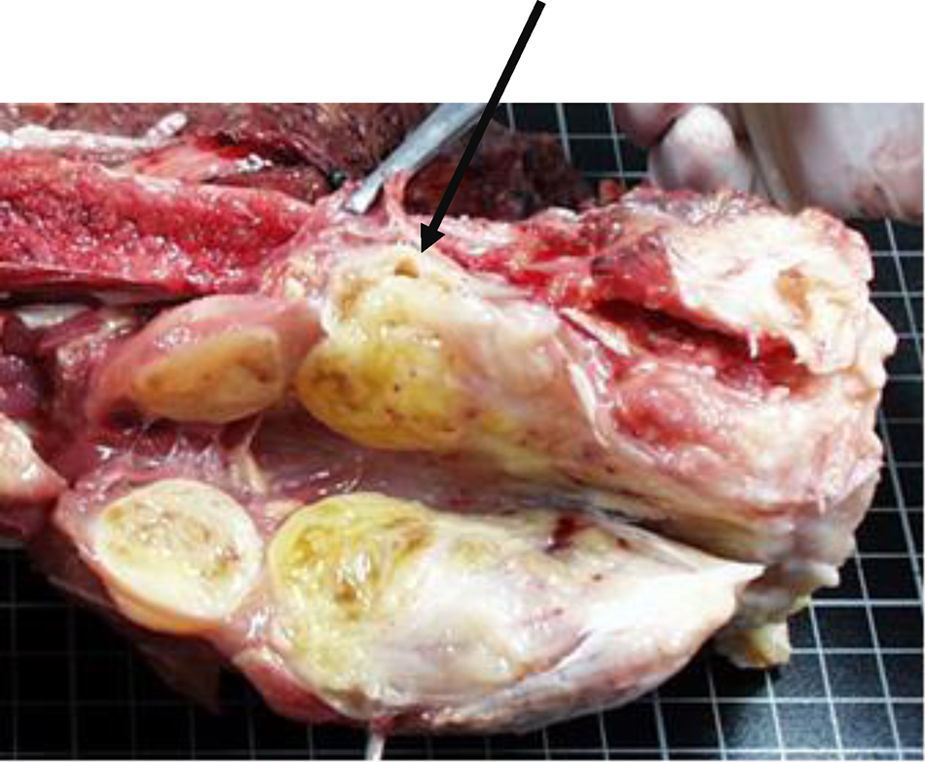
Una biopsia excisional en un tumor maligno crea graves problemas. Los sarcomas de partes blandas pueden poseer una seudocápsula que da una falsa sensación de seguridad al cirujano para la resección (fig. 10). El margen quirúrgico es inadecuado ya que, por lo general, este margen será intralesional o marginal y se contaminan de células tumorales los tejidos vecinos, pudiéndose dar el caso que la cirugía conservadora fuese imposible y se deba efectuar una amputación, que no estuviese indicada previa a la biopsia excisional. En otras ocasiones será imposible conseguir un margen amplio y realizar una cirugía conservadora, siendo necesaria una amputación innecesaria inicialmente3.
Requisitos para realizar una biopsiaLa biopsia siempre se debe efectuar después de evaluar las pruebas de imagen pues, si se realiza antes, los cambios secundarios a la biopsia pueden alterar la apariencia de la lesión y el hematoma puede llevar a confusión acerca de la localización o extensión (fig. 11). Se debe realizar en el trayecto que seguirá la cirugía definitiva, tanto si es una herida abierta o si es la punción del tru-cut. La periferia del tumor es el lugar donde existen más células viables, mientras la región central es comúnmente donde encontramos mayor necrosis tumoral; por lo tanto, la primera es la ideal para la toma del tejido a analizar.
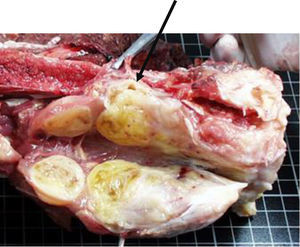
Sarcoma de partes blandas en el que fue necesaria la amputación por la imposibilidad de conseguir un margen amplio. En la foto se aprecia la seudocápsula del tumor, y donde se muestra la facilidad con la que se puede separar del tumor (flecha), por lo que en caso de una cirugía con biopsia excisional de esta pieza la disección es fácil, pero siempre quedarán restos tumorales en el paciente.
Si la biopsia es abierta no se debe realizar la exanguinación del miembro con venda de Smarch. Se debe dejar el miembro en elevación durante 10min y posteriormente inflar el manguito de isquemia.
Además, la incisión debe ser siempre longitudinal al eje del miembro y se debe tener conocimiento de todas las vías de abordaje de la cirugía oncológica, tanto de la cirugía conservadora, como de las amputaciones, pues la herida quirúrgica no debe estar localizada en un lugar diferente de las mismas.
El cirujano debe tener un plan de tratamiento quirúrgico previo a la realización de la biopsia, y debe conocer las diferentes opciones que realizará, ya sea cirugía conservadora o amputación. Se puede decir que la biopsia debe confirmar el juicio clínico que emite el equipo multidisciplinario que trata al paciente.
El abordaje quirúrgico no debe atravesar más de un compartimento y no se debe realizar una disección intermuscular para llegar a la lesión, pues la contaminación sería sustancial y se produciría mayor hematoma posquirúrgico y gran riesgo de contaminación tumoral iatrogénica, creada por el cirujano.
Cuando sea necesario realizar una ventana en el hueso, una apertura de la cortical, se debe sellar con cemento óseo, para evitar la salida de material neoplásico tras la biopsia. La ventana ósea debe ser realizada de forma oval y no cuadrada o rectangular y lo más pequeña posible, debido al riesgo de que se produzca una fractura patológica.
Cuando se va a tomar la muestra, se debe realizar con el bisturí o con un cucharilla, teniendo cuidado de no dañar la arquitectura de la tumoración, ni aplastar el tejido, y se debe manejar con mucho cuidado la muestra que se toma.
Posterior a la toma de la biopsia, se debe cambiar todo el instrumental quirúrgico y los guantes de los cirujanos y del instrumentista antes de proceder al cierre por planos.
Se debe realizar una hemostasia cuidadosa, y si se ha colocado un manguito de isquemia, se debe soltar y realizar la hemostasia ya que el hematoma de una biopsia se considera parte de la lesión, por lo que se debe evitar. Los grandes hematomas pueden disecar los tejidos blandos y el tejido celular subcutáneo y contaminar toda la extremidad, haciendo imposible la cirugía conservadora. Si se coloca un drenaje, debe estar adyacente y en la línea de la incisión definitiva, con el objeto de que pueda ser resecado posteriormente.
No se debe exponer el paquete neurovascular pues cuando se expone durante la biopsia ello será parte del problema.
Se debe tomar una biopsia intraoperatoria, para confirmar que con el tejido extraído se puede efectuar un diagnóstico18 y no olvidarse de tomar cultivos cuando entre los diagnósticos diferenciales se incluye la infección.
Errores que se deben evitar en una biopsiaEntre los errores más frecuentes está la realización de la biopsia antes que los estudios de imagen complementarios. Se debe evitar la presión de realizar el diagnóstico lo antes posible y saber que es más perjudicial para el paciente la realización de una biopsia sin los estudios de imagen previos que la espera de la realización de estos estudios.
Realizar la biopsia en un centro que no tiene la infraestructura para el tratamiento definitivo. Es por ello que cuando la presunción diagnóstica incluye un tumor maligno, no se debe realizar la biopsia y se debe consultar o remitir al paciente a un centro de referencia que ofrezca un tratamiento multidisciplinario, y en el caso que un cirujano ortopédico se encuentre en una cirugía «no tumoral» con un probable tumor, se debe evitar la tentación de continuar la cirugía realizando una resección intralesional inadecuada («debulking»).
Además la biopsia intraoperatoria, más que para el diagnóstico inmediato, sirve para que el patólogo confirme la adecuada toma de la muestra y si hay material suficiente para realizar un diagnóstico certero22,25,26.
Reevaluar las pruebas de imagen en el quirófano, y ante la menor duda, lo mejor es finalizar el procedimiento, realizando una hemostasia cuidadosa, evitando la contaminación de más planos. En este caso, se deben tomar todas las precauciones de la biopsia abierta mencionadas previamente.
Insistimos en la necesidad de conocer las incisiones estándares más utilizadas para la cirugía conservadora o para realizar los colgajos de las amputaciones. Evitar exanguinar el miembro con una venda de Smarch y no «soltar» el torniquete y no hacer hemostasia.
No se deben realizar incisiones transversales en las extremidades (fig. 12) y hay que evitar la disección de los compartimentos, para llegar a la zona tumoral. Tampoco se debería realizar el abordaje a través de los tendones o exponiendo el paquete vásculo-nervioso.
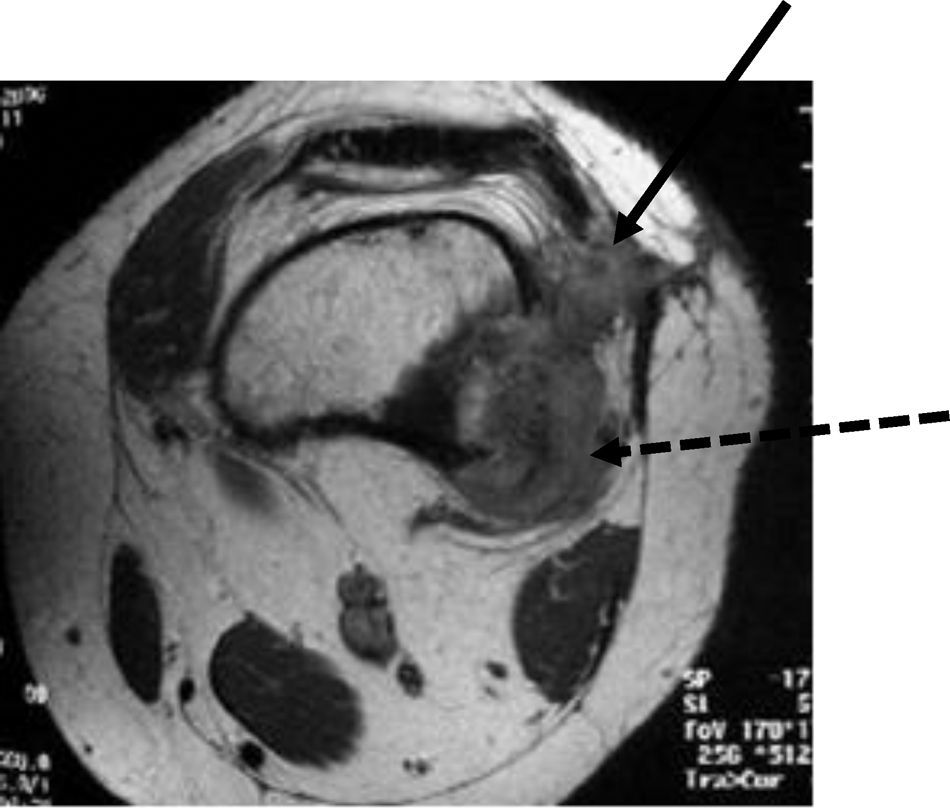
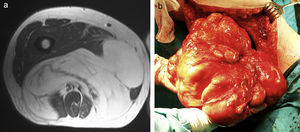
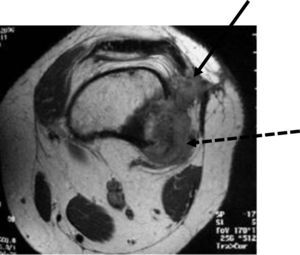
Lesión osteolítica de márgenes permeativos, con rotura de la cortical y matriz intratumoral, compatible con osteoide en la radiología simple y con una impresión diagnóstica de osteosarcoma. Se realizó una biopsia incisional previa a las pruebas complementarias de extensión. RM en T1, obtenida tras la biopsia incisional, en la que se aprecia la masa de partes blandas propia del tumor (flecha discontinua) y la del trayecto de la biopsia incisional (flecha continua) con hematoma y probable contaminación.
Nunca se debe ubicar la salida del drenaje en un sitio diferente de la incisión. En el caso que la biopsia percutánea sea realizada por el radiólogo, guiada por TC o ecografía, el principal error es no evaluar la localización de tru-cut, pues como se ha comentado debe corresponder con la incisión definitiva. En este punto se insiste en la comunicación con el radiólogo14 (fig. 13).
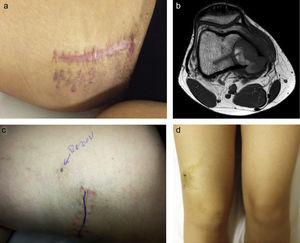
a) Dos incisiones transversas para realizar una biopsia excisional en un paciente que presentaba una masa de partes blanda en la cara medial y proximal del muslo. b) Paciente que tras biopsia percutánea requirió nueva RM, para una nueva revaloración del tumor y sorprendentemente se aprecia que la punción traspasa la zona del tumor, aumentando la contaminación. c) Lugar inadecuado de salida del drenaje en herida quirúrgica transversa (2 errores en el mismo caso). d) Hematoma tras biopsia percutánea, que puede aumentar la contaminación del tumor.
El diagnóstico y tratamiento correcto de los tumores del sistema músculo-esquelético se deben basar en la evaluación cuidadosa de la historia clínica, la exploración física, los estudios por imagen y el diagnóstico anatomo-patológico22,26. La importancia de un abordaje cuidadoso, y de la planificación y realización de la biopsia, no puede ser minimizada, pues un error en esta fase puede tener un efecto negativo en la supervivencia, en el pronóstico, y comprometer la realización de una cirugía conservadora del miembro. Recomendamos las biopsias cerradas (percutáneas) mediante tru-cut guiadas con ecografía o TC. No se concibe el manejo de estos tumores en centros sin experiencia en esta dolencia.
La biopsia es una de las claves del manejo de los tumores músculo-esqueléticos, si se realiza adecuadamente guiará de forma satisfactoria el tratamiento del paciente, pero si no es así, la biopsia puede ser el origen de complicaciones serias, errores diagnósticos y tratamientos inadecuados, llevando al paciente a una morbilidad significativa que podría haber sido evitada. También, en ocasiones, el material insuficiente tras la toma de una biopsia percutánea, en un centro con experiencia, puede llegar a ser útil, pero debe ser valorado en conjunto en un comité de sarcomas27
Debe existir una consulta previa con el radiólogo óseo y con el patólogo, para determinar el método de imagen (radioscopia, ecografía o TC) más apropiado para guiar la biopsia, para elegir el tipo de aguja y determinar en qué zona de la lesión se obtiene el material más adecuado y significativo. Si los diagnósticos diferenciales son conocidos, probablemente con una pequeña cantidad de tejido sea posible conseguir el diagnóstico.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.