Se trata de una paciente de 58 años, sexo femenino, que se presenta con hematuria, proteinuria severa y función renal normal. Pocas semanas después, ella desarrolla una trombosis de vena renal, embolia pulmonar secundaria y un episodio de insuficiencia renal aguda. Este caso clínico ilustra las distintas presentaciones clínicas de una nefropatía por IgA grave, incluyendo hematuria, síndrome nefrótico y trombosis de vena renal. Además muestra otras complicaciones serias, como embolia pulmonar y falla renal aguda. La paciente fue sometida a 2 biopsias renales, que permitieron una correlación adecuada entre las manifestaciones clínicas y la patología renal.
This is a female, 58 years old patient, who presented with hematuria, heavy proteinuria and normal kidney function. Few weeks later she developed a renal venous thrombosis, pulmonary embolism and acute kidney injury. This clinical case illustrates the variable presenting features of a severe IgA nephropathy including hematuria, nephrotic syndrome and renal venous thrombosis. Further it shows its possible severe complications such as lung embolism and acute renal failure. The patient was kidney biopsied in two opportunities, which allows assessing the correlation between the variable clinical characteristics and the renal pathology.
Paciente de 58 años, sexo femenino, con antecedentes de migraña de tipo vascular, rinitis alérgica y terapia de sustitución hormonal post-menopáusica. Los fármacos de uso habitual eran tibolona, calcio más vitamina D y desloratadina. Consulta en el servicio de urgencia de esta clínica el 01/12/2009 por un cuadro de edema de extremidades inferiores de 48 horas de evolución. Al examen físico de ingreso presentaba signos vitales normales y al examen segmentario edema moderado de ambas piernas, sin signos de trombosis venosa profunda. En el laboratorio de ingreso se constata un dímero-D elevado en 3.75ug/ml (normal < 0.5ug/ml), por lo que se realiza un eco-doppler venoso de extremidades inferiores que resulta normal. Además se pesquisa hipoalbuminemia (2.5gr/dl) e hipercolesterolemia (colesterol total 271mg/dl), no presentes en exámenes de 3 meses atrás (septiembre 2009). La creatinina plasmática era de 1.0mg/dl (velocidad de filtración glomerular estimada en 60ml/min). En forma dirigida la paciente refiere orinas espumosas desde hace varios días. La orina completa mostraba hematuria (70–80 glóbulos rojos/campo), proteinuria (500mg/dl), cilindros hialinos y granulosos y gotas de grasa. La relación albumina/creatinina en orina de muestra aislada fue de 12468 (normal < 30). La radiografía de tórax y la ecografía renal son normales. El estudio inmunológico mostró anticuerpos antinucleares 1/40, pero anti-DNA negativos, anti ENA negativos, factor reumatoideo (−), C3–C4 y CH50 normales, ANCA (−), crioglobulinas (−), anticardiolipinas (−), anticoagulante lúpico (−) y serología viral negativa (AgS.VHB, VHC e HIV). Además se realizó una inmunofijación en sangre y orina de 24 horas, que fueron normales.
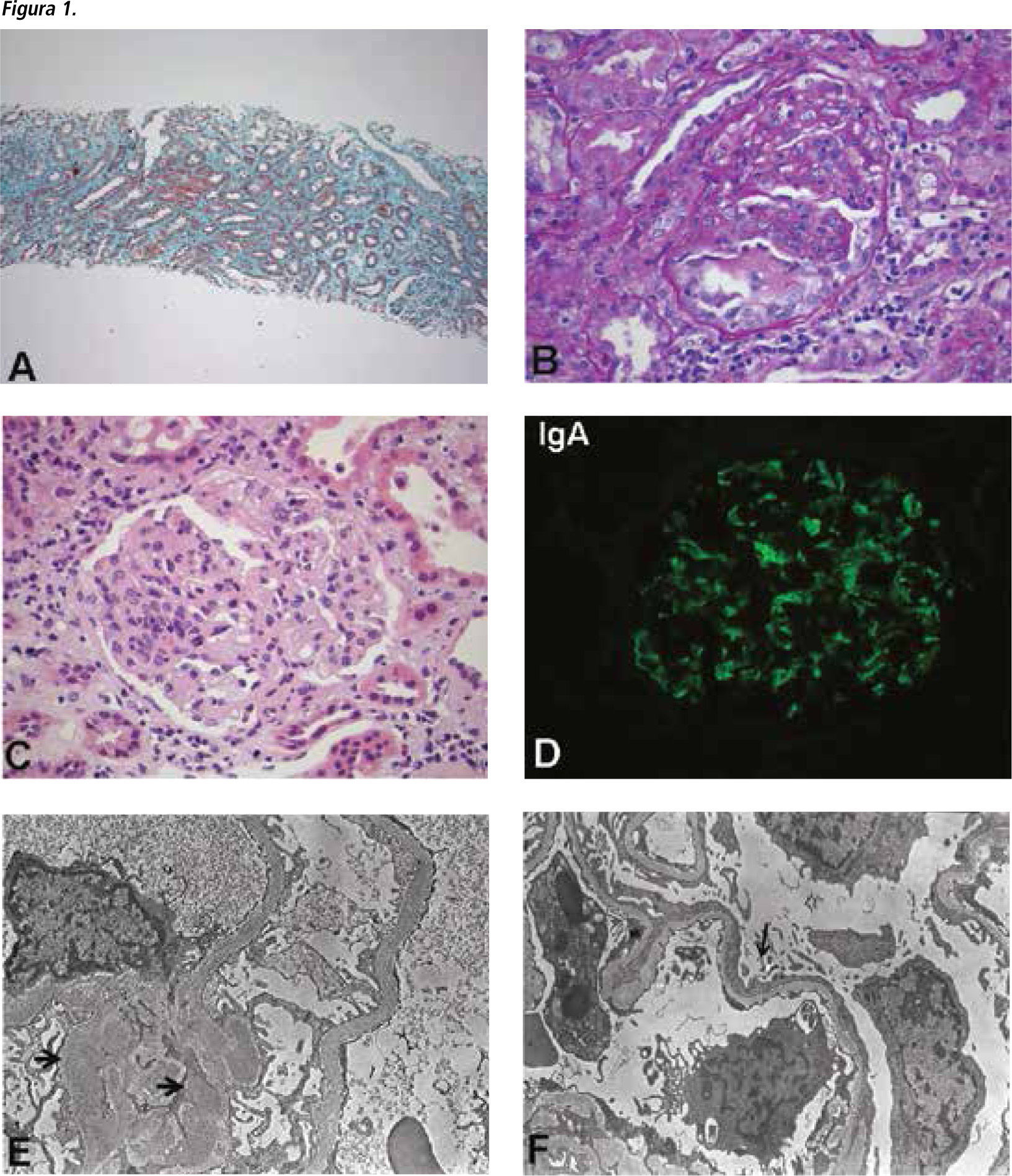
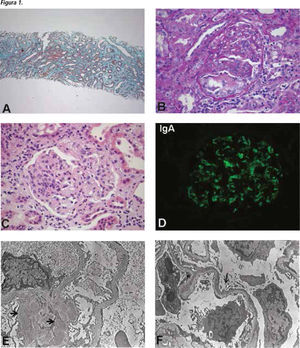
Se realiza la primera biopsia renal el 16/12/2009, con el diagnóstico clínico de síndrome nefrótico y posible glomerulopatía membranosa. Se había iniciado terapia con lisinopril 10mg, hidroclorotiazida 25mg y atorvastatina 20mg. La biopsia demostró a la microscopia óptica, la presencia de hipercelularidad glomerular moderada tanto mesangial como endocapilar, presencia de crecientes celulares en 2 de 12 glomérulos, con fibrosis intersticial de aproximadamente un 20% y presencia de cilindros hemáticos aislados. La inmunofluorescencia fue positiva con patrón mesangial +++/+++ para IgA, cadenas livianas kappa, lambda y C3c. La microscopĺa electrónica demostró membranas basales de espesor normal y abundantes depósitos paramesangiales amorfos de material electrón denso, además de fusión pedicelar extensa. Se diagnosticó como una glomerulonefritis por IgA sub-clase IV de Hass, con daño podocitario difuso (Figura 1).
A: Tejido renal con fibrosis intersticial leve (Masson 100x); B y C: Glomérulos con marcada hipercelularidad y creciente celular en C (PAS y HE 400x); D: Tinción con IgA positiva mesangial (FITC 400x). E: Depósitos paramesangiales de material electrón denso (flechas); F: Fusión pedicelar extensa con degeneración microvellosa.
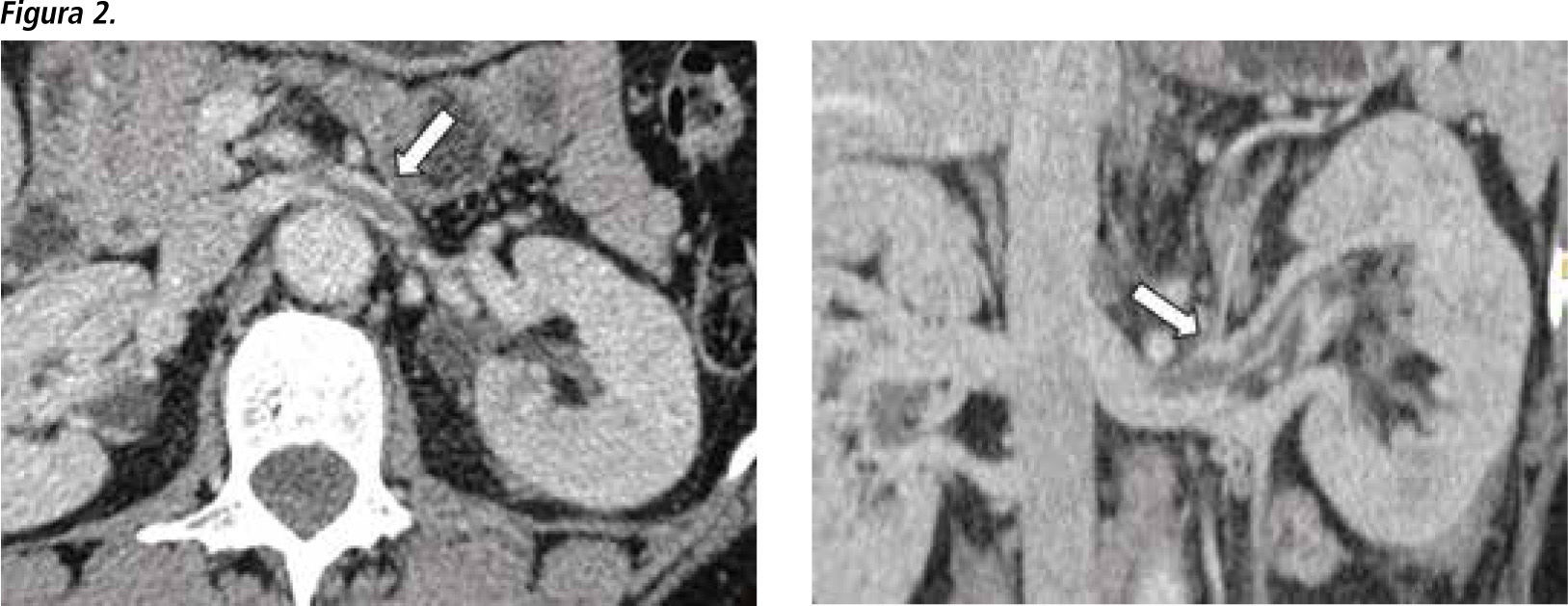
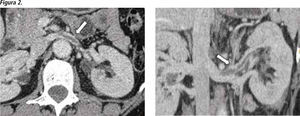
Se hospitaliza nuevamente el 19/12/2009 por un cuadro de vómitos alimentarios, sin diarrea, compromiso del estado general, cefalea holocranea y postración. Se realiza estudio neurológico con TAC y RNM de cerebro que resultan normales. La cefalea cede, pero se adiciona dolor abdominal inespecífico por lo que se realiza angio-TAC de abdomen que muestra una trombosis de vena renal izquierda (Figura 2) y tromboembolismo pulmonar sub-segmentario en lóbulo inferior derecho. Se inicia anticoagulación con heparina de bajo peso molecular y luego traslape a warfarina al alta.
En control ambulatorio el 05/01/2010 se decide iniciar terapia esteroidal con Prednisona 60mg/día. Su creatinina plasmática es de 1.2mg/dl, con proteinuria severa (índice proteinuria/creatininuria de 13), hipoalbuminemia de 2.5gr/dl e INR terapéutico.
En control ambulatorio del 19/01/10 la paciente refiere gran compromiso del estado general, temblor, mialgias, dolor lumbar bilateral inespecífico, menor volumen urinario y hematuria macroscópica constante. El laboratorio muestra una creatinina plasmática de 4.5mg/dl (velocidad de filtración glomerular de 7ml/min), BUN de 70mg/dl y kalemia de 5.8mEq/L. Se hospitaliza de urgencia con el diagnóstico de insuficiencia renal aguda.
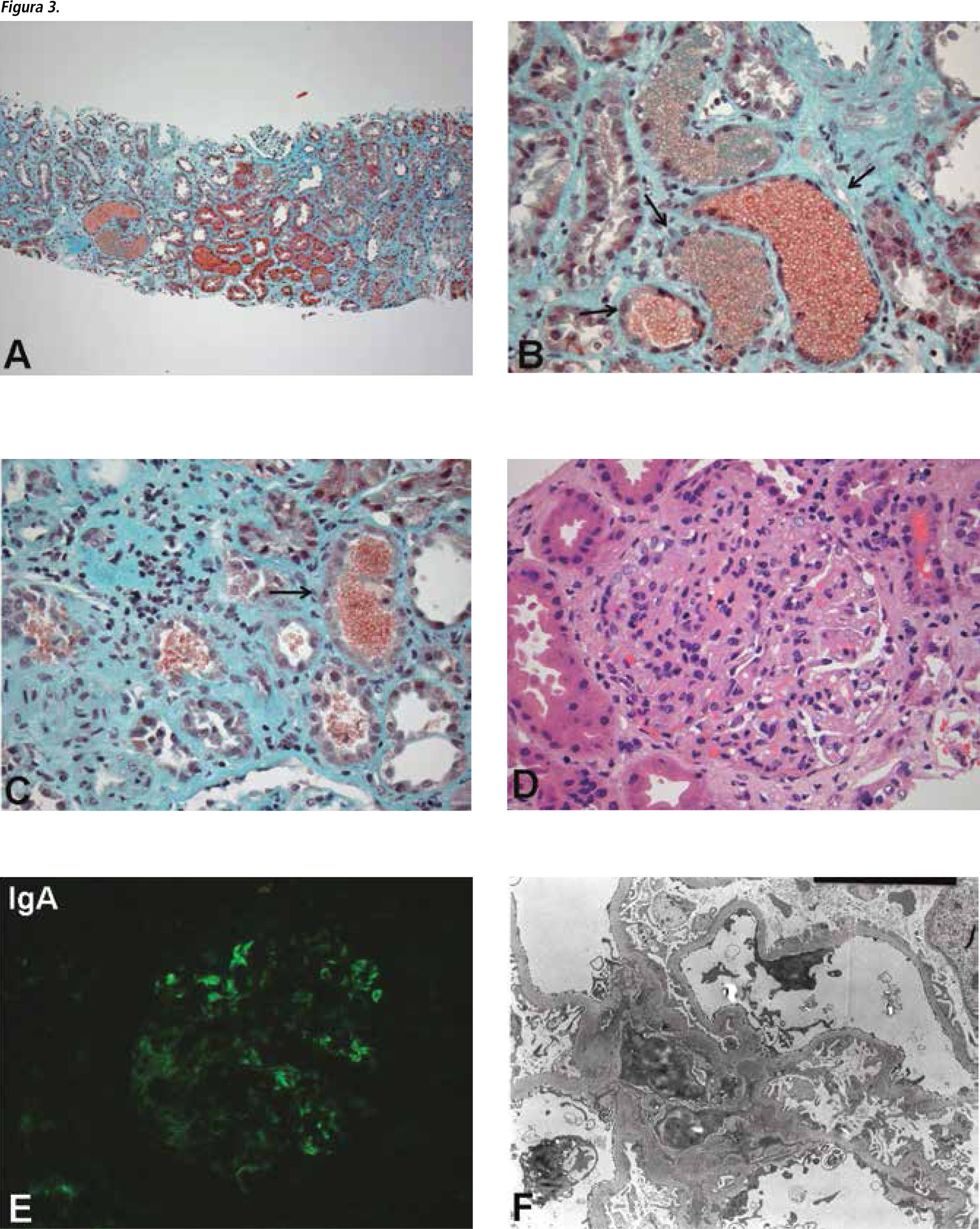
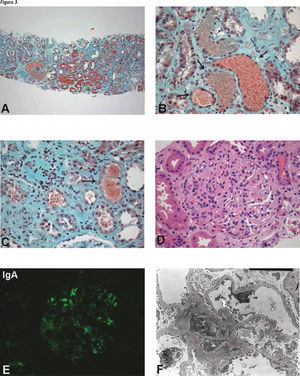
Se descartan las causas habituales de falla renal aguda y ante la sospecha de una forma crecentica de su enfermedad de Berger, se administran 3 bolos de metilprednisolona de 500mg y se repite una segunda biopsia renal el 25/01/10. La biopsia se complica de un hematoma perirrenal derecho, a pesar de haberse suspendido la anticoagulación previamente, requiriendo de hemoderivados. Posteriormente presenta una sepsis de probable foco digestivo por Alcaligenes faecalis. Se trata con Imipenem y luego Ciprofloxacino por 3 semanas. A pesar de todas estas complicaciones, su falla renal aguda permanece no oligúrica y no requiere soporte con diálisis. La biopsia renal es también informada como una glomerulonefritis por IgA subclase IV de Hass. Pero en esta segunda biopsia destaca la presencia de abundantes cilindros hemáticos con obstrucción tubular por estos cilindros y elementos de necrosis tubular aguda. No se observaba mayor cantidad de crecientes (2/13), respecto de la primera biopsia (Figura 3). La prednisona se había reducido a 40mg al día y ante el resultado de la biopsia se difiere otra terapia inmunosupresora. Se suspende toda anticoagulación, pero en la evolución posterior presenta una trombosis venosa profunda distal, por lo que se decide reiniciar. Su función renal mejora paulatinamente con los día, pero se estabiliza en alrededor de una creatinina plasmática en 2.0mg/dl. Siempre mantiene un síndrome nefrótico con un sedimento de orina muy activo y proteinuria mayor de 3gr/día. Se da de alta a fines de febrero, luego de un mes de hospitalización.
A: Tejido renal con fibrosis intersticial leve (Masson 100x); B y C: cilindros hemáticos abundantes con focos de necrosis tubular aguda, flechas (Masson 200x) D: Glomérulo con marcada hipercelularidad (HE 400x); E: Tinción con IgA positiva mesangial (FITC 400x); F: E: Depósitos paramesangiales de material electrón denso (flechas) y fusión pedicelar de menor cuantía que biopsia anterior.
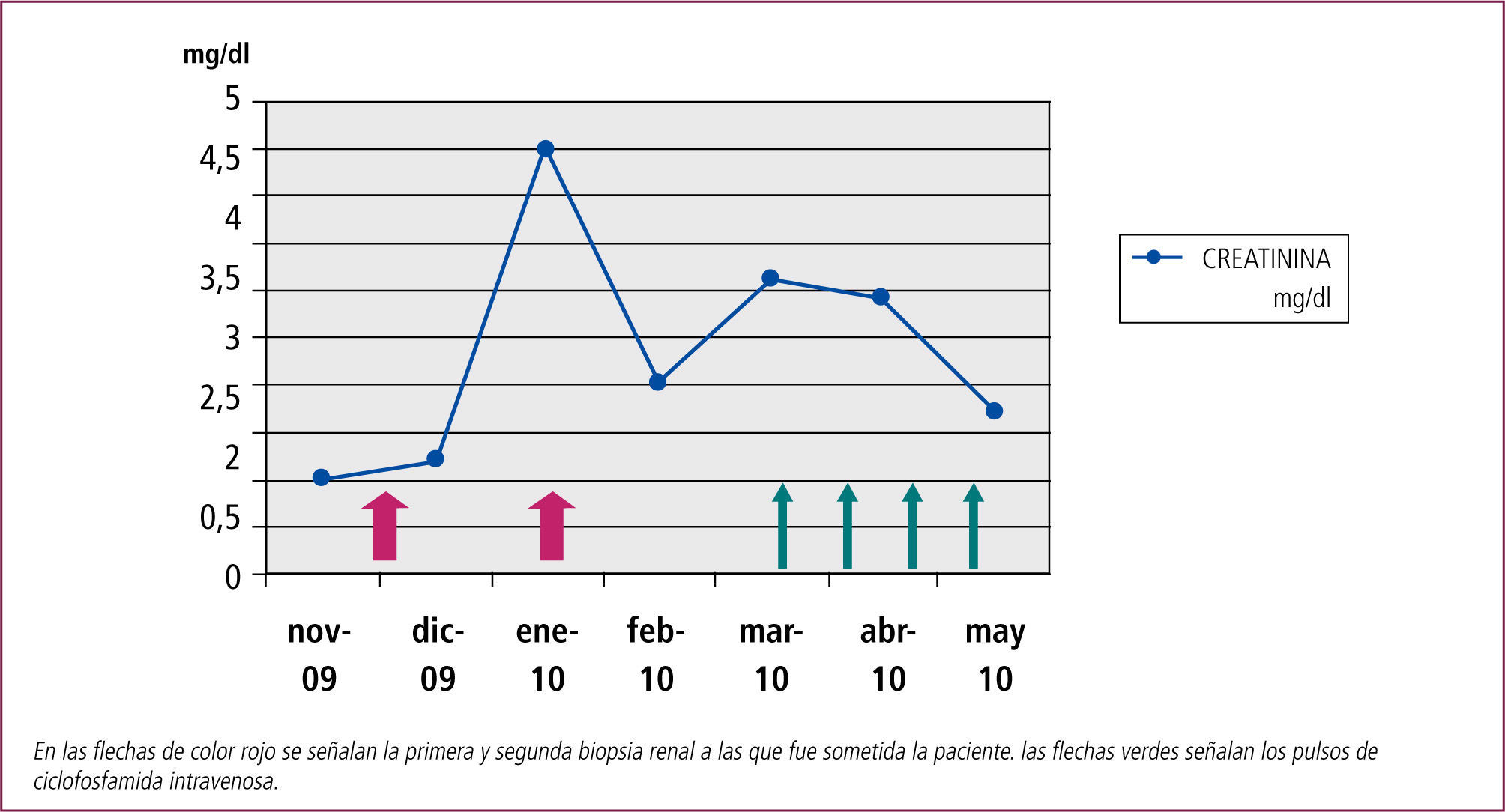
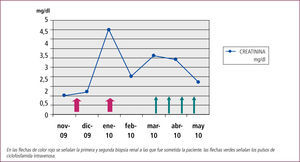
En control ambulatorio su función renal sigue deteriorándose, sin causa aparente, hasta llegar a una creatinina plasmática de 3.0mg/dl, y persiste nefrótica. En reunión clínica se decide tratar con ciclofosfamida por vía intravenosa, por 3–6 pulsos y luego micofenolato mofetil. Recibe el primer pulso de ciclofosfamida 500mg el 10/03/2010, y luego se continúa con 750mg cada 3 semanas. Luego de 4 pulsos, bien tolerados, su creatinina plasmática ha descendido a 1.6mg/dl (velocidad de filtración glomerular estimada en 35ml/min) y la proteinuria a 2.5gr/día (Figura 4). La cistatina C es de 1.48mg/L (rango normal: 0.47–1.09mg/L), lo que permite calcular una tasa de filtración glomerular de 55ml/min.
DiscusiónLa nefropatía por IgA se caracteriza por el deposito mesangial difuso de IgA en los glomérulos. Es la enfermedad glomerular más frecuente en los países occidentales y en Chile (1). La nefropatía por IgA puede ocurrir en el contexto de una enfermedad glomerular primaria, cuando es así se conoce también con el nombre de enfermedad de Berger, o en forma sistémica como el Púrpura de Henoch-Schönlein. Existen otras formas secundarias de depósito de IgA como el lupus o el daño hepático crónico. La nefropatía por IgA primaria (o enfermedad de Berger) se caracteriza por hematuria macroscópica recurrente en relación a infecciones respiratorias o de otras mucosas, hematuria microscópica persistente, proteinuria y evolución hacia la insuficiencia renal crónica en un porcentaje de casos. La presentación clínica como síndrome nefrótico es infrecuente (3 a 7% de los casos). En general el síndrome nefrótico aparece en estadios avanzados de la enfermedad, observándose grados importantes de obsolescencia glomerular en la biopsia renal. Cuando el síndrome nefrótico ocurre al inicio de la enfermedad, éste se asocia en la biopsia a lesiones glomerulares del tipo cambios mínimos o a proliferación mesangial activa. Estas dos últimas condiciones estaban presentes en la primera biopsia de nuestra paciente. Cuando predomina la fusión pedicelar sobre la proliferación mesangial, el comportamiento clínico simula una enfermedad por cambios mínimos. En este tipo de pacientes, en general niños o jóvenes, se observa una buena respuesta del síndrome nefrótico a los corticoides. Los mecanismos de esta asociación son desconocidos, planteándose una relación por azar (2 y 3). Si bien en el caso de nuestra paciente existía en la primera biopsia desaparición pedicelar extensa, también se describía intensa proliferación mesangial difusa, además de proliferación extracapilar con 2 crecientes celulares. Es probable que por esta razón, en este caso, no se observara ninguna respuesta inicial con el uso de corticoides.
El fenómeno tromboembólico que ella presentó, podría haberse sospechado por el dímero D elevado al inicio del cuadro clínico. Como sucede con frecuencia en el síndrome nefrótico, el origen de la embolia pulmonar era la trombosis de la vena renal (izquierda en este caso). Es por esto que el eco-doppler venoso de extremidades inferiores puede ser insuficiente para descartar complicaciones tromboembólicas en estos pacientes. La trombosis de venas renales se describe como hecho clínico en un 8% de los pacientes con síndrome nefrótico (4). En estudios donde se ha buscado la trombosis en forma dirigida, mediante ecografía o scanner, se reportan frecuencias de 10 a 50%. La trombosis de venas renales ocurre en forma preponderante en pacientes con glomerulopatía membranosa, especialmente si la proteinuria es mayor a 10 gramos/día (5). Este evento trombótico en una paciente con una enfermedad de Berger es un suceso muy infrecuente.
La presentación clínica del Berger como una insuficiencia renal aguda es rara, en general inferior al 5% de los casos. Aunque puede ser más frecuente en algunos grupos como los pacientes mayores de 65 años (6). Su patogenia puede ser originada por 2 causas principales. La primera es una injuria inmunológica grave, con una glomerulonefritis crecentica en la biopsia. Algunos de estos pacientes tienen ANCA positivos de tipo IgA; este subgrupo de pacientes con esta forma de glomerulonefritis IgA crecéntica asociada a títulos elevados de anticuerpos anti-mieloperoxidasa (MPO), constituiría una sobreposición entre una enfermedad de Berger y una vasculitis de tipo poliangeitis microscópica (7). La segunda opción es el desarrollo de una falla renal aguda provocada por hematuria severa, con oclusión de los túbulos renales y daño tubular agudo asociado. Este fenómeno se asocia a episodios de hematuria macroscópica. La insuficiencia renal aguda es en general reversible, aunque se reportan casos con una recuperación incompleta de la función renal (8). En este trabajo un 25% de los pacientes no recuperaba la función renal basal luego del cese de la hematuria macroscópica. En el caso de esta paciente, los factores asociados a una recuperación incompleta incluyeron: edad mayor de 50 años, duración de la falla renal mayor a 10 días, velocidad de filtración glomerular reducida de base y el grado de daño tubular agudo. El diagnóstico diferencial entre estas 2 causas, de distinto tratamiento y pronóstico, requiere de una biopsia renal. Es por esto que nuestra paciente fue sometida, en nuestra opinión, en forma acertada a una segunda biopsia renal, que descartó la evolución a una forma crecéntica como causa de su insuficiencia renal aguda. La paciente en cuestión reunía varios de los factores descritos para una recuperación incompleta de la función renal. Aparte del daño renal inicial se suman el episodio de hipovolemia por hemorragia retroperitoneal y la sepsis a enterobacteria.
El tratamiento inmunosupresor en la nefropatía por IgA depende de la forma clínica a la cual nos enfrentamos y el pronóstico renal esperado. Los factores de mal pronóstico clínico son la creatinina plasmática elevada, siendo muy frecuente la progresión cuando es > 2.5mg/dl, la proteinuria > 500–1000mg/día y la hipertensión arterial (9). En pacientes que desarrollan proteinuria o elevación de creatinina plasmática se reportan tasas de progresión a la falla renal terminal del 15–25% a 10 años y del 20–30% a 20 años (10). La velocidad de progresión es aún más rápida si la función renal se deteriora, en un estudio japonés se observó que si la creatinina sérica es > 1.7mg/dl, la tasa de insuficiencia renal crónica terminal es > del 70% a los 7 años (11). Además existen factores de mal pronóstico de tipo histológicos, como la esclerosis glomerular, fibrosis intersticial, formación de crecientes y daño vascular (12). En esta paciente teníamos como factores de mal pronóstico: creatinina en constante elevación, proteinuria severa y en la biopsia proliferación difusa severa, con crecientes aisladas (sin llegar a ser una forma crecéntica) y fibrosis túbulointersticial. En pacientes como ésta, con una nefropatía por IgA severa, activa y progresiva, se recomienda el uso de terapia inmunosupresora, especialmente en pacientes con lesiones predominantemente agudas y escasa cronicidad en la biopsia. Este factor influyó en la elección de agregar ciclofosfamida a los corticoides, tal como se ha descrito en un estudio prospectivo y randomizado (13). En este estudio se utilizó ciclofosfamida oral (1.5mg/kg/día) por 3 meses y luego traslape a azatioprina por un mínimo de 2 años. Este trabajo incluyó pacientes con creatinina elevada, entre 1.5 -2.8mg/dl, con proteinuria entre 4-5 gramos al día, condiciones semejante a la de nuestra paciente. Este trabajo aunque pequeño, tuvo resultados alentadores, con una sobrevida renal a los 5 años de 72 vs. 6% en el grupo placebo (terapia de soporte). Es importante señalar que la terapia no debe retardarse, pues el pronóstico renal es desfavorable cuando la creatinina plasmática supera los 3mg/dl, en ausencia de una forma crecéntica (14). Por otra parte la inmunosupresión no está indicada en casos de insuficiencia renal aguda asociadas a hematuria macroscópica. En el caso de nuestra paciente luego del episodio de falla renal aguda, se observó un deterioro progresivo y rápido de su función renal a pesar de los esteroides. Se decidió utilizar ciclofosfamida en pulsos intravenosos, porque nos permitía realizar una protección vesical óptima. En esta enferma, la toxicidad vesical de la ciclofosfamida oral podía pasar desapercibida porque mantenía una hematuria macroscópica ocasional, pero frecuente.
Este caso clínico pone en evidencia las distintas presentaciones clínicas que puede tener la nefropatía por IgA. Nuestra paciente debutó con un síndrome nefrótico y luego se complicó de una falla renal aguda y siguió con una forma de rápida progresión. Estas presentaciones clínicas, si bien son poco frecuentes, si no se diagnostican y manejan adecuadamente pueden ser causa de morbilidad y riesgo de daño renal crónico. En la nefropatía por IgA, la biopsia renal tiene un rol demostrado en el diagnóstico inicial y diferencial y en determinar pronóstico. El tratamiento inmunosupresor se reserva para los casos de nefropatía por IgA de mal pronóstico, porque son estos los que progresan a una enfermedad renal crónica avanzada (etapa 5). No debe olvidarse la terapia general de las glomerulopatías cónicas, eficaz en retardar la progresión de esta enfermedad, como son el uso de inhibidores de la enzima de conversión y/o antagonistas del receptor de angiotensina II y las estatinas (15).
Los autores declaran no tener conflictos de interés, en relación a este artículo.