La hipersomnia idiopática (HI) es una patología frecuentemente crónica, incapacitante, polimórfica, de etiología y prevalencia desconocida. No existen marcadores biológicos ni test diagnósticos específicos, alcanzando el diagnóstico definitivo por exclusión de otras enfermedades.
Clínicamente el cuadro se caracteriza por somnolencia diurna excesiva, despertar emborrachado, performance reducido con problemas de atención y memoria asociados a manifestaciones autonómicas. La terapia continúa siendo sintomática, utilizando fármacos que han resultado efectivos en narcolepsia.
En este artículo revisaremos algunos puntos claves en relación a la prevalencia, etiología, criterios diagnósticos y manejo de la HI.
Idiopathic hypersomnia (HI) is a chronic polymorphic disorder that frequently reduces the quality of life, with unknown prevalence and etiology. There are neither biomarkers nor specific diagnostic tests and the definitive diagnosis is only achieved by exclusion of other causes.
Clinically this disorder is characterized by excessive daytime sleepiness, sleep drunkenness, suboptimal performance, impairment of attention and memory, and some autonomic manifestations. Until now the treatment has been directed to symptomatic management, with medication frequently used in narcolepsy.
This article reviews some keys points in relation to the prevalence, etiology, diagnostic criteria and treatment of HI.
El término somnolencia diurna excesiva (ESD) está definido como una incapacidad de mantener la vigilia y la alerta en el periodo de mayor vigilia durante el día. La palabra hipersomnolencia corresponde a una tendencia anormal a entrar en sueño, mientras hipersomnia se refiere a una cantidad elevada de sueño en un periodo de 24 horas. Lamentablemente, estas distinciones no siempre son específicas ni se utilizan adecuadamente en todos los trabajos científicos; en esta revisión usaremos como está definida la palabra hipersomnolencia indiferentemente de ESD.
Por otro lado, debe diferenciarse la ESD de la fatiga (dificultad en iniciar y mantener en forma voluntaria las actividades) y de la apatía (reducción de la voluntad o del ánimo), lo que en la práctica no es fácil para el paciente ni para el clínico.
Las causas de somnolencia diurna excesiva (Tabla 1), son múltiples, pudiendo ser primarias o secundarias, estas últimas las más frecuentes, por ejemplo: la privación crónica de sueño, somnolencia diurna asociada a fármacos, el síndrome apnea obstructiva del sueño y el síndrome fase retrasada de sueño (SFRS) entre otras.
Causas de excesiva somnolencia diurna
| - Narcolepsia tipo 1 |
| - Narcolepsia tipo 2 |
| - Hipersomnia idiopática |
| - Síndrome de Kleine-Levin |
| - Hipersomnia asociada a enfermedad médica |
| - Hipersomnia asociada a medicación o sustancias |
| - Hipersomnia asociada a enfermedad siquiátrica |
| - Síndrome de sueño insuficiente |
Las hipersomnias de origen central son la narcolepsia con cataplexia (NT1), narcolepsia sin cataplexia (NT2), la hipersomnia idiopática (HI) y mucho menos frecuente la hipersomnia recurrente o Síndrome Kleine Levin (Tabla 2).
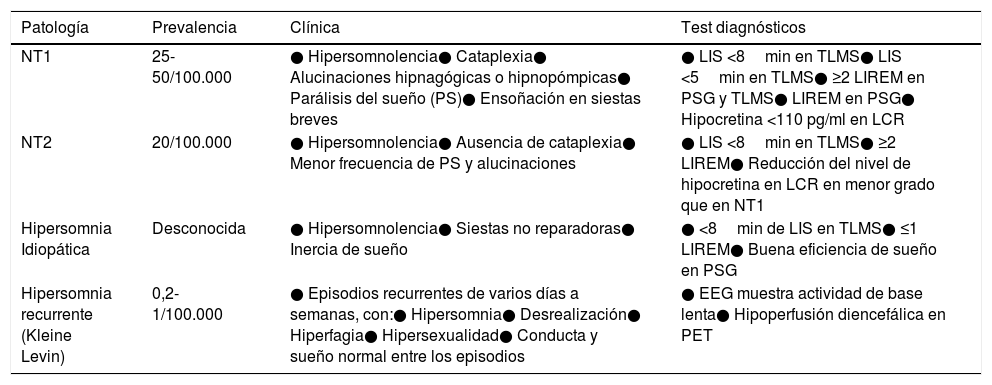
Características clínicas de las hipersomnias primarias
| Patología | Prevalencia | Clínica | Test diagnósticos |
|---|---|---|---|
| NT1 | 25-50/100.000 | ● Hipersomnolencia● Cataplexia● Alucinaciones hipnagógicas o hipnopómpicas● Parálisis del sueño (PS)● Ensoñación en siestas breves | ● LIS <8min en TLMS● LIS <5min en TLMS● ≥2 LIREM en PSG y TLMS● LIREM en PSG● Hipocretina <110 pg/ml en LCR |
| NT2 | 20/100.000 | ● Hipersomnolencia● Ausencia de cataplexia● Menor frecuencia de PS y alucinaciones | ● LIS <8min en TLMS● ≥2 LIREM● Reducción del nivel de hipocretina en LCR en menor grado que en NT1 |
| Hipersomnia Idiopática | Desconocida | ● Hipersomnolencia● Siestas no reparadoras● Inercia de sueño | ● <8min de LIS en TLMS● ≤1 LIREM● Buena eficiencia de sueño en PSG |
| Hipersomnia recurrente (Kleine Levin) | 0,2-1/100.000 | ● Episodios recurrentes de varios días a semanas, con:● Hipersomnia● Desrealización● Hiperfagia● Hipersexualidad● Conducta y sueño normal entre los episodios | ● EEG muestra actividad de base lenta● Hipoperfusión diencefálica en PET |
LIS: latencia inicio de sueño; TLMS: test latencia múltiple de sueño; PSG: polisomnograma; LIREM: latencia inicio sueño REM; PET: Tomografía por emisión de positrones; LCR: Líquido céfalo-raquídeo; EEG: Electroencefalograma.
Las primeras descripciones de la hipersomnolencia se inician en 1956, cuando Roth se refiere al término “sleep drunkenness” o “sleep inertia” para describir principalmente una dificultad y/o lentitud para adquirir una adecuada vigilia; 20 años más tarde, el mismo Bedrich Roth1 acuña el término “hipersomnia idiopática” (HI). Desde esa fecha la HI ha estado presente en las International Classification of Sleep Disorders (ICSD) 1, 2 y 3, con múltiples cambios en sus definiciones. Sin embargo, el principal desafío de la definición de la HI es la falta de elementos clínicos patognomónicos que la puedan diferenciar completamente de las otras hipersomnias de origen central, que sí tienen características definidas como la narcolepsia con cataplexia (N1) o la hipersomnia episódica recurrente (sd. Kleine Levin). El diagnóstico de la HI se basa principalmente en la exclusión de la cataplexia, ausencia del déficit de hipocretina y ausencia de dos o más LIREMs (latencia de inicio de sueño REM) en el TLMS (test de latencia múltiple de sueño) y de otras condiciones que puedan explicar mejor los síntomas.
EpidemiologíaLas dificultades diagnósticas en cuanto a los criterios y la falta de estudios epidemiológicos adecuados no permiten conocer la exacta prevalencia de la HI. En centros de sueño, su prevalencia es menos frecuente que la narcolepsia, con una amplia variabilidad entre 5-47% del total de los diagnósticos de narcolepsia, otros sugieren prevalencias entre 1-2/10.000.
Cabe destacar que en un estudio de población general el 1,6% de los adultos reporta dormir más de 9 horas/24 horas, acompañado de efectos diurnos2. La prevalencia de desorden de hipersomnia según los criterios del DSM-IV R fue 0,5% (Diagnostic and Statistical Manual of Mental Disorders), sugiriendo un sub-diagnóstico. Sin embargo, la muestra poblacional presenta un alto porcentaje de mujeres jóvenes, desempleados, retirados, con enfermedades del sistema nervioso central (trastornos del ánimo, accidentes cerebrovasculares), enfermedades musculo-esqueléticas y cardíacas, lo que posiblemente no es representativo.
EtiologíaLa etiología de la HI sigue siendo desconocida; sin embargo, se han descrito algunos factores gatillantes como infecciones virales y traumatismos encefalocraneanos.
Los estudios han encontrado posibles mecanismos involucrados:
- •
Genéticos, hay antecedentes familiares en una importante proporción de casos, entre 26-37%3,4. Estudios japoneses en pacientes diagnosticados como hipersomnia esencial han mostrado mayor susceptibilidad con los alelos del HLA: DRB1*1501 y DQB1*06025.
- •
Base neuroquímica: inicialmente se describió hipersomnia en modelos animales, al producir una noxa en porción rostral del Locus Coeruleus, esta gatillaría una reducción de norepinefrina en el LCR y un aumento del sueño REM y NREM. Estudios posteriores no han logrado demostrar el déficit de norepinefrina en LCR de pacientes con HI. La histamina y sus metabolitos se encuentran reducidos en el LCR de NT1 y NT2, sin embargo, no se ha pesquisado diferencias específicas entre controles y pacientes con hipersomnia de origen central.
- •
Autoinmunidad e inflamación: Tanaka y Honda5 evaluaron el perfil de inmunoglobulina G (IgG) en pacientes con NT1 (positivos para alelo HLA-DQB1*0602), HI y controles. Encontraron un patrón específico en HI diferente al de NT1, sugiriendo una diferencia inmunológica entre estas condiciones.
- •
Diferencias homeostáticas. Pese a que muchos pacientes refieren que su sueño no es normal, la arquitectura de sueño en HI es normal o “súper normal” con eficiencia sobre 90% y escaso fraccionamiento. Algunos estudios han demostrado un menor nivel de actividad de ondas lentas en la primera parte del sueño y otros, una mayor densidad de husos de sueño y N3 al final de la noche, lo que podría explicar el despertar emborrachado.
- •
Por otro lado, se describe un cronotipo vespertino, así como retraso en la secreción de melatonina6 y periodos circadianos más prolongados7, que podrían contribuir a un patrón genético en HI, elementos que no han sido confirmados.
- •
Factores hipnóticos endógenos: como la inapropiada liberación de sustancias endógenas hipnóticas que activan los receptores GABAA. Esta ha sido demostrada en algunos grupos de pacientes con hipersomnolencia: HI, NT2, largos dormidores y pacientes con hipersomnia subjetiva8.
La hipersomnnolencia es el elemento clave de la HI, se inicia en la adolescencia, afectando tres veces más a mujeres que hombres, así como a descendientes con origen europeo y es considerada menos intensa que en la NT1, con escasos ataques de sueño. Roth en su descripción de 1976 y hasta la ICSD-2 describió dos formas de HI, una forma mono sintomática con excesiva somnolencia diurna y sueño nocturno de duración normal (6-10 horas) y una segunda forma polisintomática, con excesiva somnolencia diurna, aunque sin ataques de sueño pero con sueño nocturno prolongado (más de 10 horas, en 1/3 de los casos de HI) con gran dificultad para despertar llamado “sleep drunkenness” que podría ser traducido como despertar emborrachado y se refiere la dificultad para adquirir una adecuada vigilia, acompañada de confusión, desorientación, mala coordinación motora y episodios en que el sujeto frecuentemente se vuelve a dormir salvo que sea fuertemente estimulado. Esta mayor “inercia de sueño” ocurre principalmente y en forma más intensa al despertar en la mañana que de las siestas.
Los pacientes con HI reportan hipersomnolencia que los mantiene con la sensación de nunca estar completamente vigiles, sienten la “mente nublada”, con alerta y atención inadecuadas. Requieren múltiples alarmas para despertar y levantarse y necesitan de ayuda de familiares para sacudirlos y mantenerlos despiertos.
Se reportan manifestaciones autonómicas asociadas como: la hipotensión ortostática, fatiga, cefalea, extremidades frías, palpitaciones y alteraciones gastrointestinales. Dificultad en mantenerse enfocado, déficit de memoria, problemas de atención e hiperactividad como una forma de mantener la vigilia9.
Así, el fenotipo de la HI no es unitario, reflotando la posibilidad de dividir el cuadro en dos o tres diferentes condiciones. A ello se suma las similitudes entre la NT2 y la HI con longitud de sueño normal, ambas sin fisiopatología ni biomarcadores identificados, lo que ha llevado a proponer que estas dos entidades puedan ser consideradas una sola patología en la próxima clasificación, dejando a la HI con sueño prolongado aparte10.
Evaluación clínicaLos criterios diagnósticos actuales para la HI de la International Classification of Sleep Disorders, ICSD-3, (Tabla 3) requieren una combinación de elementos clínicos basados en la hipersomnolencia de al menos 3 meses de duración, que no pueda ser explicada por otra patología o por el uso de sustancias y que cumplan los criterios polisomnográficos o actigráficos.
- -
Sueño de larga duración*, aunque actualmente no se diferencia entre dormidores largos o cortos, la presencia de largos periodos, más de 11 horas/24 horas, apoya el diagnóstico.
- -
Siestas prolongadas y no reparadoras a diferencia de los que ocurre en NT1.
- -
Marcada y larga dificultad para despertar, principalmente en la mañana y en menor grado desde las siestas, que se presenta en casi el 50% de los pacientes con HI.
- -
Disfunción cognitiva o “mente nublada”, con reportes de problemas de memoria en 79%, atención 55%, errores frecuentes en hasta 61%9.
Criterios diagnósticos de HI de la ICSD-3 2014*
| Deben cumplirse todos: |
| 1. Somnolencia diurna excesiva, definida como “necesidad incontrolable de dormir o somnolencia diurna” >3 meses. |
| 2. Ausencia de Cataplexia |
| 3. TLMS sin evidencia de NT2 (<2 LIREM entre polisomnograma nocturno y TLMS) |
| 4. Evidencia electrofisiológica de hipersomnolencia, definida por uno o ambos: |
| - Promedio de latencia de sueño en el TLMS de <8 minutos |
| - ≥11 horas de sueño por cada 24 horas (evaluado por polisomnograma de 24 horas o promediado por actigrafía de 7 días, ad libitum). |
| 5. Excluido el insuficiente sueño (incluidas las 24 horas previas al PSG) |
| 6. Ninguna otra causa que pueda explicar mejor el cuadro clínico y si la existe, ésta debe haber sido adecuadamente tratada. |
*American Academy of Sleep Medicine. International Classification of Sleep Disorders. 3rd ed. Darien, IL: American Academy of Sleep Medicine; 2014.
HI: hipersomnia idiopática; ICSD: international clasification sleep disorders; TLMS: test latencia múltiple de sueño; NT2: Narcolepsia tipo 2; LIREM: latencia inicio de sueño REM; PSG: Polisomnograma.
*Mención especial requiere la duración de sueño en la HI. La cantidad de horas de sueño en pacientes con HI va desde normal (7-8 horas) a extensiones increíbles (10-15 horas), con alta eficiencia. Hasta la ICSD-2, se separa la HI con largos periodos de sueño y la sin prolongado sueño, en la siguiente clasificación se descarta esta división. Sonka et al. en el 201511, realizan un estudio de pacientes con hipersomnolencia y en base al cuadro clínico propone separarlos en tres grandes grupos de Hipersomnia Central: NT1 (narcolepsia con cataplexia), HI con largo periodo de sueño (polisomnomática con un principal periodo de sueño de más de 10 horas) y en un tercer tipo que agrupa la NT2 y la HI sin periodo de sueño prolongado, las que comparte características clínicas.
Una vez establecido el diagnóstico de HI su curso es en general continuo, si bien puede presentar fluctuaciones e incluso se reportan remisiones hasta en 33% de los casos12.
Diagnósticos diferencialesLo primero es asegurarse de que efectivamente estamos hablando de hipersomnolencia diurnas y no de fatiga ni apatía.
Las causas secundarias de somnolencia diurna excesiva (Tabla 4), como: la privación crónica de sueño, somnolencia diurna asociada a fármacos, el sd. apnea obstructiva del sueño y el sd. fase retrasada de sueño (SFRS) son mucho más frecuentes que las causas de hipersomnia de origen central.
Causas secundarias de hipersomnolencia
| Farmacológicas | Uso de drogas inductoras de sueñoSuspensión de psicoestimulantes |
|---|---|
| Trastornos respiratorios del sueño | ● Sd. Apnea obstructiva del sueño● Sd. hipoventilación obesidad● Sd. Resistencia vía aérea superior● Sd. Apnea Central |
| Sueño insuficiente | ● Insomnio● Sd. privación de sueño |
| Desórdenes del ciclo circadiano | ● Sd. fase retrasada● Jet lag● Trabajo en turnos● Esquemas irregulares |
| Trastornos psiquiátricos | ● Enfermedad bipolar tipo 1 y 2● Depresión mayor● Depresión atípica● Desorden disfórico premenstrual● Desorden somatomorfo |
| Otras causas médicas | ● Sd. fatiga crónica● Hipersomnia post viral● Hipotiroidismo● Accidente cerebrovascular● Encefalopatía hepática● Anemia● Post traumatismo encéfalo-craneano● Enfermedad de Parkinson● Distrofia miotónica |
Una historia clínica detallada es clave para excluir causas secundarias de hipersomnolencia, ya que no existe un biomarcador válido de HI. Debe haber especial preocupación a las patologías asociadas y al uso de fármacos (Tabla 5) así como la suspensión de estimulantes (café, mate, bebidas energizantes, anorexígenos, etc). El examen físico completo nos permite plantear diagnósticos diferenciales de la somnolencia: sd. apnea del sueño, hipotiroidismo, hipoventilación-obesidad.
Fármacos que podrían inducir hipersomnia
| Clase de droga | Droga |
|---|---|
| Hipnóticos | ● Triazolam● Zolpidem● Eszopiclona● Zopiclona● Suvorexant |
| Sedantes | ● Antihistamínicos● Anticolinérgicos● Agonistas GABA● Opiáceos |
| Drogas de abuso | ● Alcohol● Cannabis● Opiáceos |
| Anti-hipertensivos | ● Bloq. α 1 Adrenérgico● Agonista α 2 adrenérgico● Bloq. β adrenérgico |
| Anti-epilépticos | ● Carbamacepina● Fenobarbital● Ácido Valproico |
| Anti-parkinsonianos | ● Agonistas dopa● Levodopa |
| Relajantes musculares | ● Baclofeno● Ciclobenzaprina● Clormezanona |
| Antipsicóticos | ● Quetiapina● Olanzapina● Haloperidol, etc. |
| Antidepresivos | ● Antidepresivos tricíclicos sedantes● Antidepresivos sedantes atípicos |
Enfermedad bipolar, sd. depresivo mayor, sd. depresivo persistente, sd. disfórico premenstrual y sd. depresivo con elementos atípicos entre otros.
Los dormidores largos, son aquellos sujetos que duermen más que el promedio de su edad, en adultos se considera 10 o más horas, otros estudios usan el límite en 8-10 horas. A los dormidores largos a diferencia de los pacientes con HI, una vez que se les permite dormir “ad libitum”, no presentan queja de somnolencia diurna excesiva ni sueño emborrachado.
La NT1, presenta como elementos clásicos la tétrada de hipersomnolencia con ataques de sueño, cataplexia, parálisis de sueño y alucinaciones hipnagógicas e hipnopómpicas. Característicamente el sueño nocturno es fraccionado, con baja eficiencia, pero las siestas son muy reparadoras. El diagnóstico diferencial con NT2, es más complejo, ya que tienen más cosas en común que diferencias (Tabla 6).
Características clínicas diferenciales entre NT2 e HI
| NT2 | HI |
|---|---|
| ● Hipersomolencia● Ausencia de cataplexia● Sueño total normal● Puede presentar parálisis de sueño, alucinaciones hipnagógicas.● Siestas en general reparadoras. | ● Hipersomnolencia● Ausencia de cataplexia● Podría tener sueño prolongado o normal● Parálisis de sueño (24%), alucinaciones hipnagógicas (26%)● Despertar “emborrachado”● Siestas no reparadoras |
Traducido de Berkowski et al., 2016 (Ref. 13).
NT2 Narcolepsia tipo 2, HI Hipersomnia idiopática.
El uso de diarios de sueño ayuda a diferenciar por ejemplo sd. privación crónica de sueño y sd. fase retrasada (SFRS), así como esquemas irregulares. Los pacientes con SFRS comparten algunos elementos con HI; en la primera la privación crónica de sueño y el desajuste del ciclo circadiano en el SFRS pueden gatillar elementos clásicos de la HI como en despertar emborrachado. Por otro lado, los pacientes con HI presentan una tendencia a fase retrasada. Una forma de diferenciar esto es el uso de diarios de sueño, la actigrafía y permitir un sueño ad libitum, lo que en SFRS mejora la somnolencia diurna y el despertar.
TratamientoActualmente no existe un tratamiento específico para la HI y las terapias utilizadas están basadas los tratamientos de la NT1 y NT2, así como en consensos de expertos14.
Algunas estrategias no farmacológicas utilizadas son:
- -
Esquemas de sueño regulares. Pueden ayudar a establecer ciclos circadianos y evitar tendencia al retraso de fase.
- -
Siestas preventivas. Son útiles en no más del 50% de los pacientes con HI, ya que frecuentemente despiertan embotados, sin obtener beneficios de siestas breves ni prolongadas.
- -
Mejorar los horarios de trabajo. Adaptar éstos a una fase retrasada de sueño, reducir los tiempos de transporte: vivir cerca del lugar de trabajo/estudio, trabajo semi-presencial.
- -
Apoyo de familiares. La seria dificultad para despertar en la mañana puede requerir múltiples alarmas, luz brillante, música, ayuda de familiares e incluso de mascotas.
El manejo de la hipersomnolencia es en espejo al de la narcolepsia: estimulantes y promotores de la vigilia.
- -
En 1988 el primer estudio en 15 pacientes con HI se utilizó 200 a 500mg de modafinilo, dividido en dos dosis y logró reducir significativamente la somnolencia y el número de episodios de sueño en 15/18 sujetos. Estudios randomizados, controlados y doble ciego, con bajo número de pacientes y nivel de evidencia Ib15 han demostrado mejoría en escala Epworth, test de conducción e impresión clínica global (CGI), sin embargo, no mejora significativamente la latencia múltiple de sueño en el test de mantención de la vigilia.
- -
El armodafinilo es un enantiómero-R del modafinilo, con una vida media de 15 horas es usado en dosis única entre 150-250mg en la mañana.
- -
Metilfenidato, es considerado terapia de segunda línea en HI desde la aparición del modafinilo. Habitualmente se utiliza en formulación de liberación lenta asociado a liberación inmediata, con tasas de respuesta de 95% versus 88% a modafinilo16.
- -
Dextroanfetamina, metanfetamina y anfetamina, solas o en combinaciones entre ellas o con modafinilo, han demostrado utilidad en rangos de 25-50%.
- -
Mazindol, discontinuado desde 2016, estimulante tricíclico no anfetamínico, en pacientes con HI resistentes a terapia, en dosis de 3,6mg/d, demostraron buena respuesta.
- -
Antidepresivos como el bupropión, reboetina y protriptilina, que tienen como efecto adverso el insomnio y fármacos usados en Sd. de déficit atencional como la atomoxetina, podrían tener algún efecto en la hipersomnolencia.
- -
se ha descrito la utilidad de la melatonina de liberación lenta, al acostarse, con efectos beneficiosos en el despertar emborrachado, lo mismo que la aplicación de parches de nicotina 20 minutos antes de levantarse.
- -
Pitolisant agonista anti-H3, bloquea la recaptura presináptica de histamina, ha demostrado utilidad en un tercio de pacientes con HI resistentes a otras terapias.
- -
Flumazenil antídoto a la acción sedante de las benzodiacepinas, antagonista de sitio de unión de BZP en el receptor GABAA. Ha demostrado utilidad en uso continuo subcutáneo en un paciente con HI, pero sus potenciales efectos adversos y mala biodisponibilidad limitan su uso.
- -
Claritromicina modulador alostérico de receptor GABAA. Se han encontrado resultados promisorios con tasa de retención sobre el 50% en dosis de 500mg/d17.
- -
Levotiroxina en dosis de 25μg/d, en estudio muy pequeños de 9 pacientes con HI, demuestra reducir el número de horas de sueño y la escala de somnolencia de Epworth (ESS) entre 7-8 puntos.
- -
Oxibato de sodio, aprobado en NT1, estimula los receptores GABAA y mejora la cataplexia y disomnia. Un estudio observacional en 46 pacientes con HI en una dosis al ir a acostarse, demostró reducción de ESS y mejoría del despertar emborrachado en 70% de los casos18.
- -
Una nueva droga denominada solriamfetol, promotor de la vigilia vía noradrenalina y dopamina, muestra eficacia en prolongar el tiempo de mantención de la vigilia en pacientes con NT1, NT2 y en somnolencia residual en Sd. apnea obstructiva del sueño.
La ausencia de criterios diagnósticos, polisomnográficos y marcadores biológicos específicos, asociado a una baja prevalencia, hacen de la HI un desafío tanto en el diagnóstico como en su tratamiento. La HI causa somnolencia diurna grave y afecta significativamente la calidad de vida, pese a lo cual ha recibido poca atención, con escasos avances en su fisiopatología y terapéutica específica. Recientemente algunos estudios neuroquímicos y genómicos prometen entregarnos mayores conocimientos. Por otro lado, el manejo farmacológico, actualmente similar a la narcolepsia, deja un porcentaje significativo de pacientes sin beneficios, los que podrían potencialmente mejorar con nuevos fármacos como los agonistas inversos H3 (pitolisant) y moduladores de GABAA (claritromicina).
Las similitudes fenotípicas entre la NT2 y la HI sin sueño prolongado, hacen plantear la posibilidad de que ellas se unan en la siguiente clasificación ya que con las herramientas diagnósticas actuales no es posible una separación convincente.
Declaración de conflicto de interésLa autora no tiene conflictos de intereses.