La implementación de un laboratorio clínico moderno es una necesidad actual debido a una creciente solicitud de exámenes, la necesidad de nuevas prestaciones, mayores exigencias en términos de la calidad y un mayor cuidado del medioambiente. Para lograr esta implementación es necesaria la planificación del espacio físico y de la infraestructura, que incluye revisión de la normativa actual y de guías nacionales e internacionales para garantizar un uso adecuado del espacio acorde con el equipamiento. Además, requiere la incorporación de sistemas preanalíticos y equipo automatizado e integrado con el sistema informático que permita el procesamiento de un número importante de muestras, y su trazabilidad. Una vez montados los equipos es necesario asegurar un correcto flujo de trabajo y de muestras que optimice el tiempo de procesamiento y la fluidez del sistema. En relación al cuidado medio ambiental, debe haber un adecuado manejo de los deshechos y un uso racional del papel. Todos estos elementos deben enmarcarse en un Sistema de Gestión de la Calidad para asegurar una mejor calidad de atención, resultados confiables y oportunos, facilidad de acceso a la información, estandarización de los procesos, sistemas de alerta y trabajo en un ambiente bioseguro.
The implementation of a modern Clinical Laboratory is an actual necessity due an increasing test requirement, new tests needed, greater requirements in terms of quality and a better care of the environment. For the implementation is necessary a correct planning of physical spaces and architecture, that includes the review of local and international guidelines to warranty an optimal use of the spaces according the equipment. It is also required the incorporation of pre-analytical systems, automated equipment and their integration to the laboratory Informatics System (LIS) equipment that allows the processing and tracking of an important number of samples. Once the equipment is installed a correct workflow and samples flow with optimal time around times (TAT) and fluency of the system is necessary. For an environmental care, a good management of waste and a rationale use of paper are needed. All these elements must be inserted in the framework of a Quality Assurance System for a better quality service, reliable results, easy data access, process standardization alert systems and a biosafe work.
En la actualidad, la implementación de un laboratorio moderno resulta menos complicado que años atrás, debido al enorme abanico de equipos y técnicas disponibles en el mercado para diagnóstico de uso in vitro y a la incorporación en los laboratorios clínicos a sistemas de gestión de calidad, facilitando la entrega de resultados confiables y en un tiempo adecuado1.
Un aspecto importante a considerar en la implementación de en un laboratorio moderno es la infraestructura. En Chile existe una guía de planificación y diseño de laboratorios clínicos que se refiere al tamaño requerido para implementar un laboratorio de acuerdo a su complejidad y por secciones (MINSAL 1998). Esta normativa es muy importante de considerar, pues el tamaño de un laboratorio depende de su complejidad y del número de muestras a analizar y es útil para gestionar el aumento de espacio en las instituciones de salud2.
Debe considerarse además la implementación de una Unidad de Toma de Muestras completamente equipada, que cuente entre otras cosas con sistema de código de barras, conectada a un sistema informático y funcional y con flujos optimizados de pacientes y muestras.
Un laboratorio moderno debe tener más capacidad de procesamiento de exámenes y una mayor diversidad de exámenes, lo cual además de permitir la reducción de los costos por determinación, permite optimizar la organización de los laboratorios mejorando los tiempos de respuesta1.
Actualmente los laboratorios clínicos que originalmente se encontraban en áreas poco adecuadas y con secciones separadas, se están implementando en áreas centrales para mejorar el flujo de trabajo. Además se encuentran disponibles sistemas como las balas de transporte a distancia que permiten el envío de muestras desde servicios distantes1.
Los laboratorios clínicos pueden ser de dos tipos, estructuralmente hablando:
- a)
Laboratorio modular, que se caracteriza por tener áreas o secciones separadas.
- b)
Laboratorio abierto, que consiste en muchos laboratorios unidos sin muros de separación.
El primero es el más frecuentemente observado en muchas de nuestras instituciones, mientras que el segundo modelo es el más recomendable para un laboratorio moderno. En el laboratorio abierto, pueden realizarse muchas determinaciones diferentes con técnicas distintas acopladas en un mismo sistema, que puede estar comunicado además con un sistema preanalítico que transporta las muestras hacia los equipos que realizarán las determinaciones, siendo el funcionamiento del laboratorio continuo (Figura 1A y 1B)1.
En este último modelo, además se establece un área central o “core” que integra las secciones con mayor carga (bioquímica, hematología) que se encuentran completamente automatizadas y conectadas a un sistema preanalítico y al sistema informático de laboratorio. En el área central se encuentra la recepción de muestras, lo que optimiza el tiempo de procesamiento. El resto de las secciones del laboratorio, las más especializadas y/o de poco flujo se encuentran situadas alrededor del “core”1. Cabe señalar que en el último tiempo algunos exámenes especializados como los de biología molecular han ido incorporándose a la rutina por su mayor sensibilidad y especificidad, por una mayor demanda y porque actualmente existen equipos completamente automatizados, incluso equipos que entregan resultados dentro de una hora de procesamiento considerados “point of care testing” (POCT).
Cuando se desea incorporar la robótica a la fase preanalítica, se debe analizar cómo es el flujo de las muestras y su origen (ambulatorias, de hospitalizados y/o servicio de urgencias). Este análisis permite optimizar el sistema para que su incorporación no afecte los tiempos de respuesta de los exámenes tanto de pacientes hospitalizados como del servicio de urgencias. A modo de ejemplo, en el sistema preanalítico EnGenTM (Johnson y Johnson, Chile), instalado en el laboratorio de Clínica Dávila, las muestras de hospitalizado y ambulatorio ingresan por la cadena transportadora a los equipos, mientras que las muestras de los servicios de urgencias (adultos, pediátrico y maternidad), son ingresadas por delante directamente por el operador para darles prioridad (Figura 2). Además este sistema ha permitido una disminución del error preanalítico y la estandarización de algunos procesos como la preparación y gestión de serotecas y la optimización del recurso humano3.
CUMPLIMIENTO DE LOS REQUISITOS ESTÁNDARCuando se planifica la construcción de un laboratorio y se decide modernizar lo que ya existe se debe cumplir con determinados estándares de laboratorio (Ej. Norma ISO 15189)4.
Dentro de los requisitos estándar que un laboratorio moderno debe cumplir se encuentran los siguientes:
- a)
Debe poseer flujos de trabajos adecuados y libres de deshechos.
- b)
El funcionamiento debe estandarizarse a través de un mapa de procesos que sea conocido por todo el personal y que además se actualice cada vez que se produzca un cambio en el sistema.
- c)
Las funciones del personal deben estar por escrito en un sistema documental, que abarque todos los procesos
- d)
Se deben monitorizar las etapas de pre-analíticas, analíticas y post-analíticas, a través de indicadores.
- e)
Se debe contar con un sistema de comunicación interno y externo expedito y adecuado.
- f)
Se debe colaborar con el cuidado del medio ambiente4.
- g)
A continuación se desarrolla cada uno de estos puntos, que son fundamentales al momento de implementar un laboratorio moderno.
- a)
Flujos de trabajo adecuados y libres de desechos
Se deben analizar los flujos de trabajo de cada una de las áreas de operación para evitar las ineficiencias en el sistema de rutina. Un buen ejemplo de esto es el ordenamiento del acceso a los módulos de toma de muestra, para permitir que el ingreso de los pacientes sea en forma ordenada y que no se produzcan aglomeraciones que generen demoras en la atención. Por ejemplo, uno de los exámenes que entorpece el flujo en la toma de muestra es el examen de orina, ya que el paciente debe ingresar al baño a tomarse el examen. En este caso el flujo de trabajo debe ser diferenciado optimizando el uso de los módulos de atención y evitando la confluencia de pacientes producto de la entrada y salida del baño y el retorno al módulo de atención (Figura 3).
El análisis de flujo, debe ser realizado antes de diseñar el plano de un laboratorio. Debe contener una revisión de los flujos de los pasillos de circulación, la mueblería, la disposición de los mesones, las vías de acceso, las vías de emergencia y el requerimiento más básico, como lo es la definición de área limpia y área sucia.
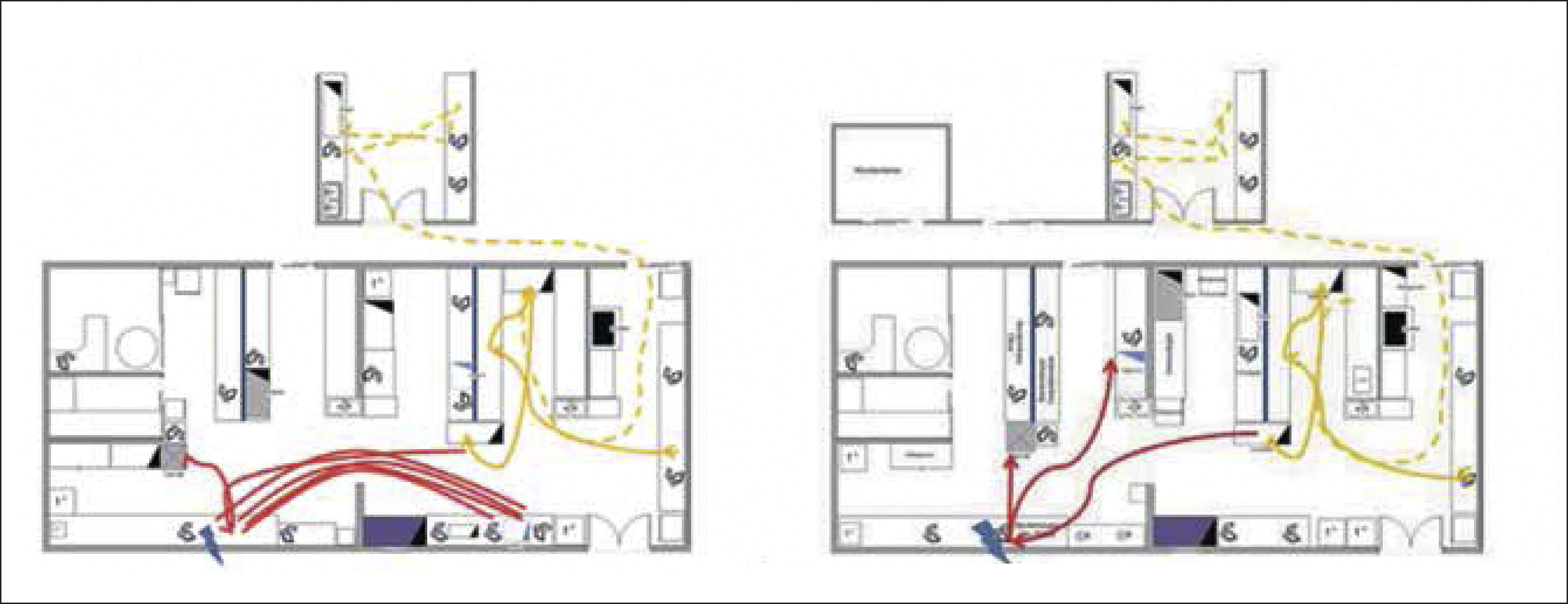
La gestión de flujo es aplicable a todas las áreas de laboratorio y de esta manera el movimiento del personal de laboratorio se concentra las distintas zonas de manera secuencial optimizando el tiempo de trabajo. Para ello se utilizan los “diagramas de spaguetti” que permiten analizar la ubicación de los puestos y el flujo del trabajo (Figura 4).
Figura 4.Adecuación de los flujos en un laboratorio (Diagrama de “espagueti”).Observar líneas rojas A) Previo a la intervención para optimizar los flujos. B) Después de la intervención para optimizar los flujos. Se observa un flujo optimizado después de la intervención. Gentileza de bioMérieux, Chile.
(0.34MB). - b)
Funcionamiento estandarizado a través de un mapa de procesos conocido por todo el personal y actualizado
La gestión de procesos, entrega herramientas claves para que el personal asimile lo importante que es su rol dentro del sistema y el aporte a la satisfacción del paciente. Esta herramienta debe ser canalizada a través de un “mapa de procesos” que representa en forma gráfica el funcionamiento del sistema y permite entender la importancia de todos los estamentos involucrados.
La primera etapa para entender la Gestión de Procesos, es conocer todos los flujos que se pueden dar dentro del laboratorio y después construir cada proceso. Considerando a los propietarios, las entradas, salidas, variables de control y actividades que se desarrollan en cada proceso4.
- c)
Las funciones del personal deben estar por escrito en un sistema documental, que abarque todos los procesos
Esta actividad permite lograr que el personal realice las acciones de una forma estandarizada y realizar las mejoras de manera objetiva mediante intervenciones que depuren el sistema4.
Un buen sistema documental, es aquel que de forma simple, permite el cumplimento de alguna normativa (nacional o internacional) proporcionando trazabilidad de todos los procesos. Se debe evitar tener un sistema hipertrofiado, con gran cantidad de documentos inútiles que entorpecen el funcionamiento de las áreas.
- d)
Monitorización de las etapas de preanalíticas, analíticas y posanalíticas, a través de indicadores
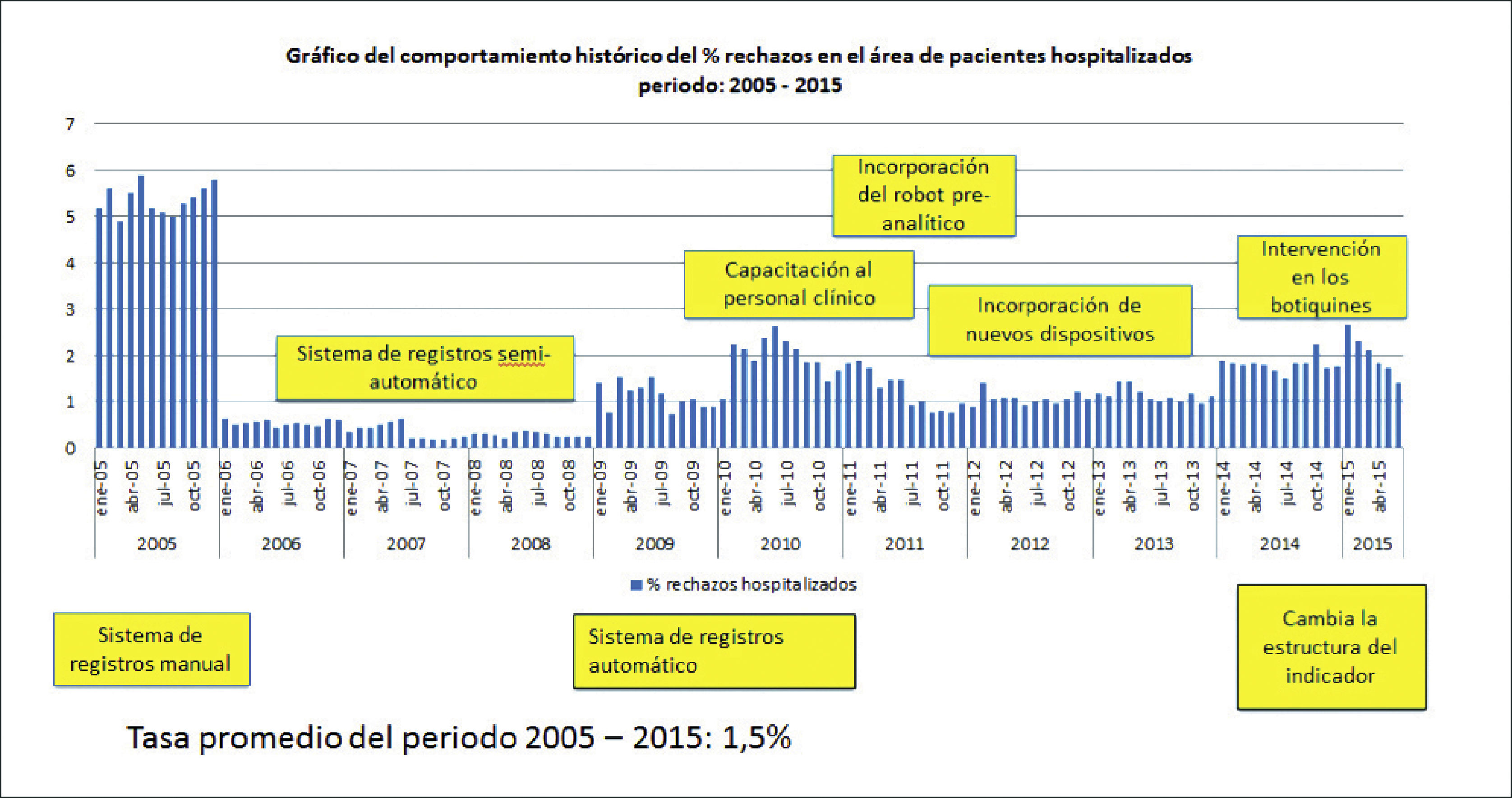
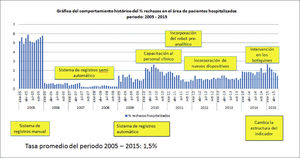
El laboratorio debe establecer indicadores de la calidad para hacer seguimiento y evaluar el desempeño en todos los aspectos críticos de los procesos preanalíticos, analíticos y postanalíticos y realizar intervenciones enmarcadas en la denominada “mejora continua”4. Los indicadores se deben revisar periódicamente, para asegurar su continua adecuación. Un laboratorio actualizado debe difundir estos indicadores en tiempo real y realizar un análisis de éstos. Un indicador muy utilizado es el de “rechazos de muestras” permitió en nuestra institución, obtener la información real e intervenir en las áreas clínicas para disminuir estos eventos. La Figura 5 muestra el comportamiento del indicador de rechazos de muestras a través de los años y sus respectivas intervenciones.
Figura 5.Comportamiento del indicador de rechazos de muestras a través de los años e intervenciones realizadas
Se observan aumentos y disminuciones del indicador en relación al sistema de registro (manual o automatizado), capacitaciones del personal, incorporación de sistema preanalítico, de nuevos dispositivos, intervención en botiquines y cambio en la estructura del indicador. Datos del Laboratorio Clínica Dávila.
(0.68MB). - e)
Poseer un sistema de comunicación interno y externo expedito y adecuado
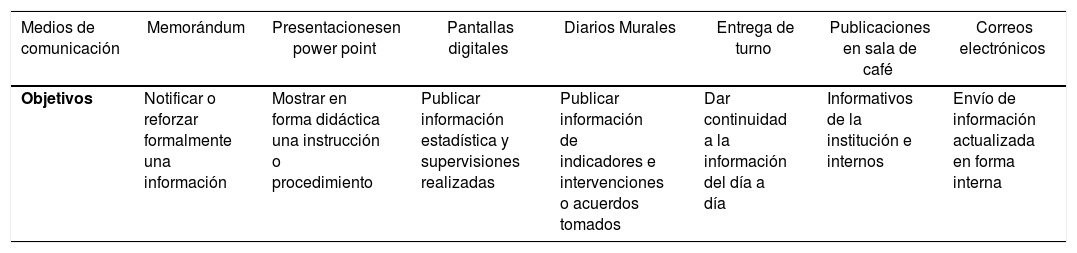
La finalidad de este sistema es entregar la información necesaria para el correcto desempeño del personal, la comunicación con el personal clínico y cumplir con la entrega de información al paciente. Incluye el envío de memorandos, presentaciones en power point, pantallas digitales, diarios murales, entregas de turno, publicaciones en sala de café y correos electrónicos (Tabla 1).
Tabla 1.Sistema de comunicación interno y externo de laboratorio
Medios de comunicación Memorándum Presentacionesen power point Pantallas digitales Diarios Murales Entrega de turno Publicaciones en sala de café Correos electrónicos Objetivos Notificar o reforzar formalmente una información Mostrar en forma didáctica una instrucción o procedimiento Publicar información estadística y supervisiones realizadas Publicar información de indicadores e intervenciones o acuerdos tomados Dar continuidad a la información del día a día Informativos de la institución e internos Envío de información actualizada en forma interna Medios de comunicación TGR* – Consulta de exámenes Correos electrónicos Llamadas telefónicas Página Web Portal de los médicos RCE** Objetivos Entregar información de los requisitos de las muestras Información a los proveedores internos y externos Responder dudas sobre algún examen o método utilizado Entregar información sobre los resultados y requisitos de los exámenes Información sobre nuevos métodos implementados Información sobre nuevos métodos implementados - f)
Colaborar con el cuidado del medio ambiente
Una de las principales preocupaciones de la dirección del laboratorio es la eliminación de los residuos generados y la eliminación del papel en todas las áreas de trabajo (Figura 6).
MODERNIZACÓN DE LABORATORIOS ESPECÍFICOSComo ejemplos se analizará la modernización del laboratorio de microbiología y de biología molecular.
1. Laboratorio de microbiología: automatización e integraciónLa automatización en microbiología es un fenómeno que desde la década de los ochenta ha crecido en forma exponencial, principalmente debido a los avances tecnológicos, que involucran además sistemas informáticos. Esto ha permitido, no sólo estandarizar los procesos, sino mejorar la oportunidad en la información, la productividad del laboratorio, la calidad de los resultados y muchas veces reducir costos5.
Actualmente la automatización en microbiología ha alcanzado un gran desarrollo y procesos anteriormente manuales, como la lectura de hemocultivos, el antibiograma y la siembra de placas, entre otros, se han automatizado, lo que ha liberado horas de personal para ser dedicado a otras actividades, principalmente de gestión y control y ha mejorado la reproducibilidad inter e intralaboratorio.
Existen muchos ejemplos donde la automatización ha permitido en gran medida absorber la demanda, cada vez mayor, del análisis microbiológico de muestras clínicas asociadas con una mayor exigencia en cuanto a calidad y a tiempos de respuesta. La integración de los sistemas automatizados con el LIS (Laboratory Information Systems) y el HIS (Hospital Information System) ha permitido el intercambio bidireccional de información, que puede ser transmitida desde los equipos al laboratorio, al equipo médico e incluso al propio paciente, además de permitir el trabajo en línea del tecnólogo médico5.
Esto último se ha traducido en una desaparición de las transcripciones manuales de información, que junto con disminuir las posibilidades de errores operacionales, producen una reducción del papel en el laboratorio, traduciéndose en beneficios también ecológicos, lo cual ya fue discutido previamente. De esta manera, y ajustándose a normas internacionales como la norma ISO 15489, la desaparición del papel ofrece una mejor gestión de los documentos, que pueden ser archivados en formato digital, facilitando el acceso y uso de la información4.
En relación a la identificación de especies microbianas, la tecnología MALDI-TOF MS (matrix-assisted laser desorption/ionization time-of-flight mass spectrometer), ha revolucionado la microbiología, permitiendo en pocos minutos obtener la identificación con un alto porcentaje de certeza. Su implementación requiere un estudio de costo y proyección en el tiempo, pues la inversión en el equipamiento se recupera en un plazo relativamente bajo dado que el costo de la determinación es bajísima comparada con las metodologías convencionales6.
Además ha habido importantes cambios en los procesos que pueden ser automatizados de un laboratorio tradicionalmente considerado manual. Por ejemplo en la actualidad se cuenta con sembradores automáticos integrados en la rutina (Figura 7) e incluso incubadores automáticos que permiten analizar las colonias microbianas con un perfil de alta resolución, en pantallas táctiles, ampliar imágenes y analizarlas en un ambiente bioseguro7,8.
Para gestionar la implementación de un laboratorio de microbiología automatizado e integrado, la principal justificación la constituye la reducción de los tiempos de respuesta de los cultivos que impactan en la morbimortalidad del paciente hospitalizado y en los costos institucionales por infecciones asociadas a la atención en salud.
2. Laboratorio de Biología MolecularLa biología molecular ha mejorado el conocimiento de la patogenia de las enfermedades a nivel genético lo que se traduce en un diagnóstico más certero, lo cual puede mejorar pronóstico y brindar un tratamiento oportuno.
La técnica de reacción de la polimerasa en cadena (PCR) se ha convertido en una herramienta esencial en el laboratorio clínico para el diagnóstico de enfermedades infecciosas, oncológicas, endocrinas y otras.
Dentro del diseño de un laboratorio de biología molecular hay que considerar las instalaciones, el equipamiento y el personal. En relación a las instalaciones es fundamental contar con el espacio físico adecuado, que idealmente debe planificarse con antelación2. Cuando no existe el espacio ideal, se debe adaptar el laboratorio, separando las áreas como para evitar contaminación con amplicones (Figura 8). En relación al equipamiento y reactivo deben elegirse aquellos aprobados para uso en diagnóstico in vitro (IVD), ya sea por la FDA (Food and Drug Administration) o por la CE (autorización europea). En relación al personal para trabajar en un laboratorio de biología molecular debemos seleccionarlo de acuerdo a sus cualidades profesionales (competencias en el área y en gestión de calidad) y personales (capacidad de concentración y de trabajo en equipo). Este último punto es extremadamente importante para evitar contaminación con productos de PCR, que es el principal problema de este tipo de laboratorio.
Para argumentar la necesidad de implementar un laboratorio de biología molecular hay que tomar en cuenta la complejidad del centro clínico, necesidad de los médicos, sensibilidad de las técnicas, costo beneficio y contingencia. En relación a esto último, en nuestra experiencia, el brote de Influenza H1N1 de 2009, nos permitió implementar la Reacción de Polimerasa en Cadena (PCR) en tiempo real.
Los elementos clave de un laboratorio de biología molecular es la separación de las áreas y un flujo de trabajo unidireccional (Figura 8).
Finalmente, el laboratorio de biología molecular debe ser incorporado al sistema de gestión de calidad al igual que otras áreas de laboratorio, lo cual incluye manejo de la documentación, realización de control de calidad, hacer la verificación o validación de método molecular, auditorías, manejo de no conformidades y otras9.
CONCLUSIONESLa implementación de un laboratorio moderno implica varios requisitos que incluyen una planificación adecuada del espacio físico e infraesctructura o una adecuación del flujo de trabajo cuando esto no es posible, incorporación de equipamiento automatizado e integrado con el sistema informático, el adecuado manejo de los desechos y la incorporación del laboratorio a un sistema de gestión de calidad, entre otros. Cuando existe planificación se obtienen resultados óptimos. Una vez implementado, el sistema debe permitir trazabilidad de los resultados, facilidad de acceso a la información, sistemas de alerta, trabajo en un ambiente bioseguro y principalmente la entrega de resultados fiables y oportunos al usuario.
Los autores declaran no tener conflictos de interés, en relación a este artículo.