La tecnología aplicada al manejo de la diabetes ha experimentado notables avances dentro de la última década. Hoy contamos con dispositivos de infusión de insulina subcutánea continua o bombas de insulina, que intentan imitar la secreción fisiológica del páncreas, y con el monitoreo continuo de glucosa que entrega información de la glicemia intersticial durante las 24 horas del día. Los modelos más modernos incorporan ambas tecnologías en un mismo dispositivo, teniendo incluso la capacidad de detener la infusión de insulina frente a una hipoglicemia. En esta revisión se abordará el funcionamiento de la bomba de insulina y monitor continuo de glucosa, así como las indicaciones de su uso, selección de pacientes, ventajas y desventajas de ambas tecnologías.
During the last decade remarkable development has occurred in the field of new technologies for diabetes care. Continuous subcutaneous insulin infusion (⿿insulin pumps⿿) with new functions and integration with glucose sensors have been developed. Continuous glucose monitoring system which reports interstitial glucose levels in real time during 24hours are commercially available. This article reviews the indications, clinical care and benefits of using technologies in diabetes, with a special focus in type 1 diabetes.
En la última década han existido importantes avances en el desarrollo y uso de nuevas tecnologías para la administración de insulina, destacando las bombas de infusión continua al subcutáneo y el páncreas artificial, este último aún en fase de investigación. Por otra parte para el ajuste de la terapia se cuenta actualmente con monitores continuos de glucosa. El uso de la tecnología se ha popularizado principalmente para diabetes mellitus tipo 1 (DM1) y en países como Estados Unidos, en promedio el 60% de los pacientes con este tipo de diabetes usan bomba de insulina y el 11% usa monitor continuo de glucosa1. En el caso de diabetes mellitus tipo 2 (DM2), el uso de este tipo de tecnología es más infrecuente.
En este artículo se revisará el estado actual del uso del infusor continuo de insulina, que en inglés se conoce como Continuous Subcutaneous Insulin Infusion (CSII), y el monitoreo continuo de glucosa (CGM).
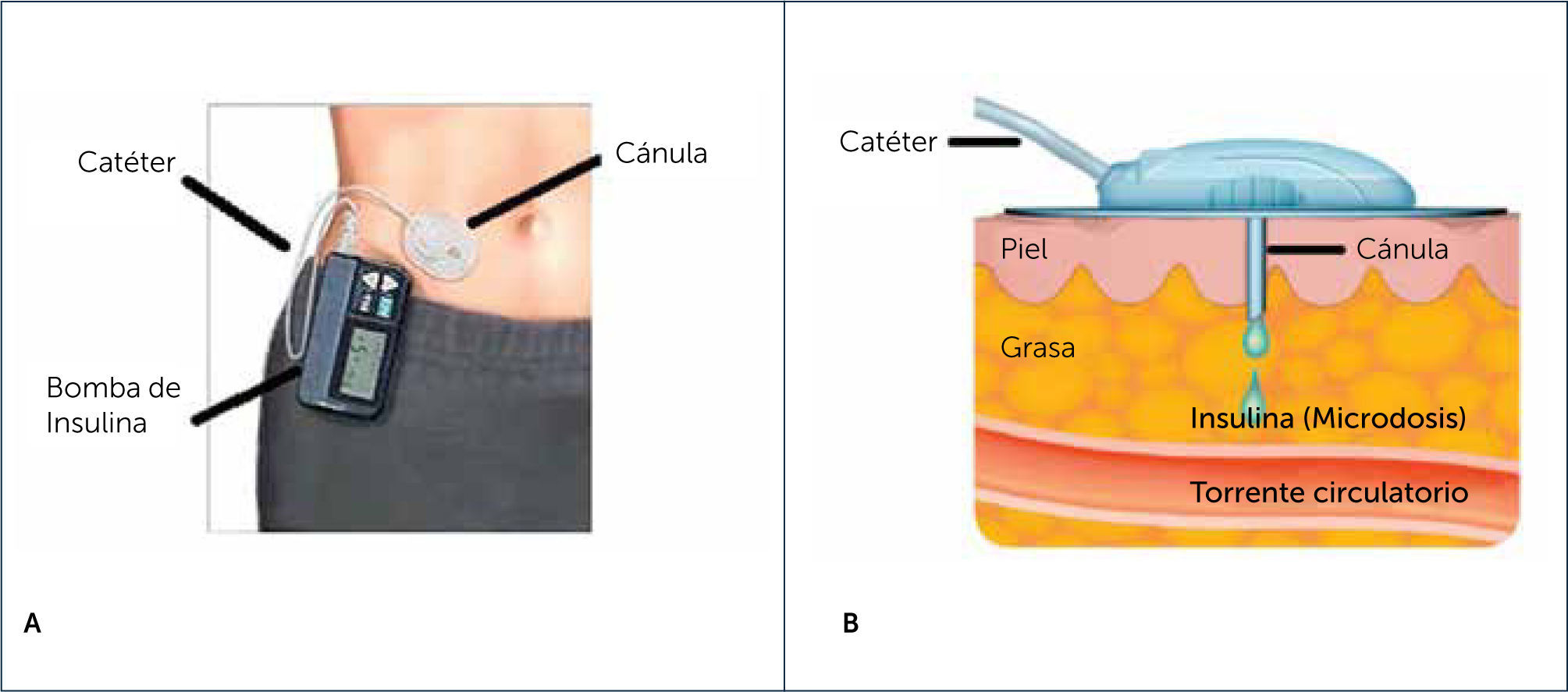
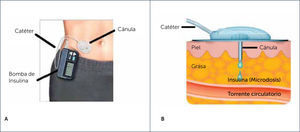
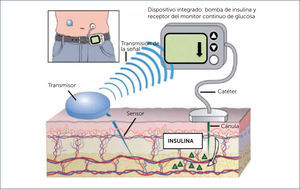
INFUSOR CONTINUO SUBCUTÿNEO DE INSULINA (CSII) O BOMBA DE INSULINA CONCEPTOS GENERALESUna bomba de insulina es un dispositivo electrónico diseñado para administrar insulina de forma continua. Dentro de la bomba se coloca un reservorio con análogo de insulina rápida (insulina ultrarrápida), que está conectado a un catéter que la transfiere al tejido subcutáneo a través de una cánula (Figura 1A).
BOMBA DE INSULINA Y SET DE INFUSIÿN (A), POSICIÿN DE LA CÿNULA EN EL TEJIDO SUBCUTÿNEO (B)
2A) Modificado de https://www.nlm.nih.gov/medlineplus/spanish/ency/esp_imagepages/18028.htm
2B) Modificado de Guía Información básica sobre el tratamiento con bomba de insulina. Medtronic.
CSII entrega la insulina al subcutáneo en dos patrones principales: como infusión basal y como bolos de insulina. El aporte basal es continuo y en poca cantidad. Al tratarse de volúmenes pequeños, su absorción es muy rápida desde el subcutáneo a la circulación sistémica (Figura 1B). Este tipo de infusión imita la secreción endógena continua de insulina desde el páncreas, que ocurre en los períodos de ayuno. En el caso de pacientes que previamente usaban terapia con múltiples dosis de insulina (MDI) reemplaza la insulina de acción prolongada, como glargina, determir o degludec.
El aporte de insulina basal es configurado por el médico, quién determina horarios y dosis durante las 24 horas, los que pueden ser diferentes en distintos segmentos del día, según los requerimientos individualizados del paciente. Por ejemplo, si uno quisiera aportar 24 unidades de insulina basal al día, una alternativa sería entregar 1UI/hora, pero por lo general se programa una mayor entrega en las horas que el individuo tenga mayor insulinoresistencia y menor cantidad en las horas en que existe más sensibilidad a esta hormona. En este mismo caso, por ejemplo, podrían existir períodos en que se entregue 0,7UI/hora, otros en que se aporte 1UI/hora y finalmente algunas horas en que se entregue 1,3UI/hr. Los rangos de incremento o disminución de la dosis administrada por hora son mucho más pequeños de lo que permiten los lapiceros de insulina usados en terapia MDI. Esto es de vital importancia en lactantes y preescolares que usan dosis mucho más pequeñas que los adultos.
Por otra parte, la infusión de los bolos corresponde a aportes agudos de insulina que son indicados por el usuario antes de cada comida y también en caso de requerirse corrección de glicemias. De esta manera la insulina es entregada al subcutáneo en forma rápida, y en mayor dosis que el aporte basal continuo. El objetivo de los bolos es lograr una insulinemia alta que se asemeje a las concentraciones sanguíneas más elevadas que se producen fisiológicamente en el período prandial. En el caso de pacientes previamente en terapia MDI reemplaza las inyecciones de insulina prandial antes de cada comida.
La mayoría de las bombas contiene un programa (⿿bolus wizard⿿ o ⿿asistente para el bolo⿿) que ayuda al paciente a calcular la dosis adecuada del bolo. El raciocinio para el asistente de bolos, es el mismo que se utiliza para calcular la dosis de insulina prandial en terapia MDI. Cada paciente posee un factor de sensibilidad o de corrección, que teóricamente corresponde a cuántos mg/dl de glicemia baja una unidad de insulina administrada. Por otra parte posee una ratio o relación insulina: hidratos de carbono, que corresponde a la cantidad en gramos de hidratos de carbono que metaboliza una unidad de insulina. Ambos factores son variables de sujeto a sujeto y también dentro de cada persona van cambiando en el tiempo. En el caso de la bomba de insulina, esta información debe ser ingresada en la configuración del dispositivo y debe ser prescrita por el médico. La forma de calcular estos factores se detalla en la Tabla 1A.
CÿLCULO DE LA DOSIS TOTAL DE INSULINA, DOSIS DE INSULINA BASAL, RATIO INSULINA: HIDRATOS DE CARBONO Y FACTOR DE SENSIBILIDAD
| ⿿ Dosis Total de Insulina para iniciar bomba (DTI) = 80% de la dosis total diaria previamente usada con inyecciones |
| ⿿ Dosis Inicial de Insulina Basal = 40 a 50% de la dosis total diaria (dependiendo del control metabólico del paciente al momento de iniciar la terapia) |
| ⿿ Ratio insulina: hidratos de carbono = 450/DTI |
| ⿿ Factor de Sensibilidad o Factor de Corrección = 1.700/DTI |
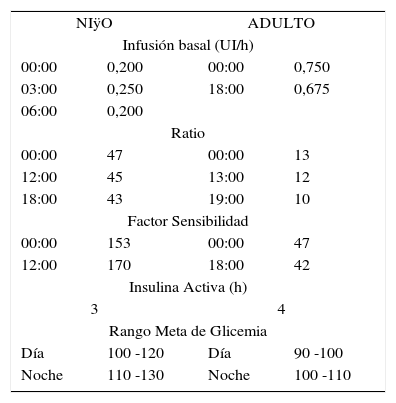
Un ejemplo de la programación de la bomba de un niño pre escolar de 5 años y un adulto se detalla en la Tabla 1B. En ella se puede apreciar que la infusión basal, ratio de insulina: hidratos de carbono y factor de sensibilidad son configurados en diferentes horarios del día. Los segmentos horarios y dosis son modificables en el tiempo pudiendo añadirse nuevos bloques y cambiar dosis según sea necesario de acuerdo a los requerimientos del paciente.
EJEMPLO DE PROGRAMACIÿN DE LA BOMBA DE INSULINA EN UN NIÿO PRE ESCOLAR Y UN ADULTO
| NIÿO | ADULTO | ||
| Infusión basal (UI/h) | |||
| 00:00 | 0,200 | 00:00 | 0,750 |
| 03:00 | 0,250 | 18:00 | 0,675 |
| 06:00 | 0,200 | ||
| Ratio | |||
| 00:00 | 47 | 00:00 | 13 |
| 12:00 | 45 | 13:00 | 12 |
| 18:00 | 43 | 19:00 | 10 |
| Factor Sensibilidad | |||
| 00:00 | 153 | 00:00 | 47 |
| 12:00 | 170 | 18:00 | 42 |
| Insulina Activa (h) | |||
| 3 | 4 | ||
| Rango Meta de Glicemia | |||
| Día | 100 -120 | Día | 90 -100 |
| Noche | 110 -130 | Noche | 100 -110 |
El tratamiento con CSII logra eliminar las inyecciones frecuentes, pero requiere que el paciente de forma activa indique a la bomba realizar el aporte de bolos antes de cada comida y/o corrección de glicemia. Para ello es necesario que ingrese al dispositivo la glicemia del momento y la cantidad de hidratos de carbono que va a ingerir. Por otra parte, se debe realizar continuamente evaluación del tratamiento buscando patrones glicémicos que permitan ajustar la tasa de infusión basal, metas glicémicas y factores involucrados en la configuración del calculador de bolos.
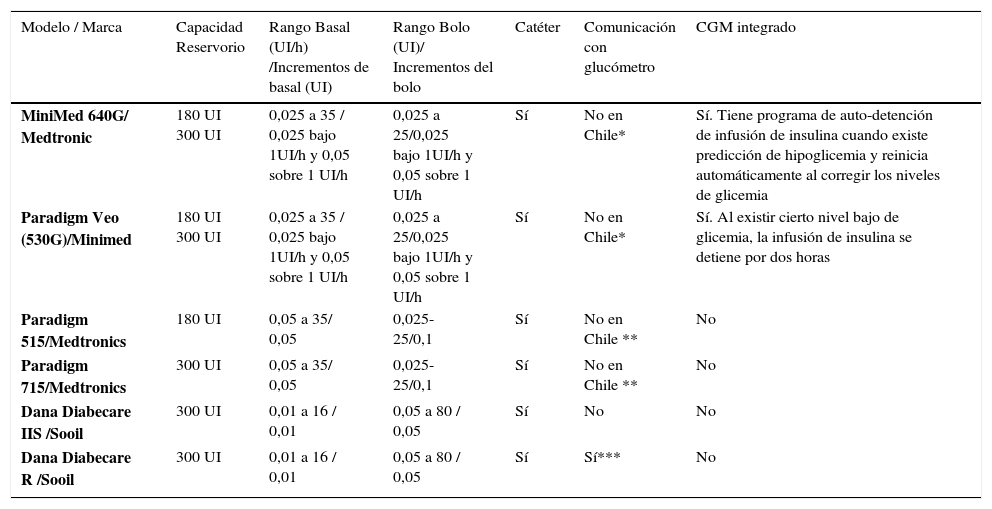
Los diferentes tipos de bombas de insulina que se encuentran disponibles en Chile se detallan en Tabla 2. Dependiendo del tipo de bomba existen diferentes set de infusión, los que incluyen cánula, reservorio y catéter, y deben ser reemplazados cada 3 días (Tabla 3). La cánula puede ser de teflón, metal, silicona o poliuretano, y se inserta bajo la piel con un insertor especialmente diseñado para ello. Además se dispone de reservorios de insulina con distinta capacidad de almacenamiento, adecuada a la dosis total de insulina que usa el paciente.
BOMBAS DE INFUSIÿN CONTINUA SUBCUTÿNEA DE INSULINA DISPONIBLES EN CHILE1
| Modelo / Marca | Capacidad Reservorio | Rango Basal (UI/h) /Incrementos de basal (UI) | Rango Bolo (UI)/ Incrementos del bolo | Catéter | Comunicación con glucómetro | CGM integrado |
|---|---|---|---|---|---|---|
| MiniMed 640G/ Medtronic | 180 UI 300 UI | 0,025 a 35 / 0,025 bajo 1UI/h y 0,05 sobre 1 UI/h | 0,025 a 25/0,025 bajo 1UI/h y 0,05 sobre 1 UI/h | Sí | No en Chile* | Sí. Tiene programa de auto-detención de infusión de insulina cuando existe predicción de hipoglicemia y reinicia automáticamente al corregir los niveles de glicemia |
| Paradigm Veo (530G)/Minimed | 180 UI 300 UI | 0,025 a 35 / 0,025 bajo 1UI/h y 0,05 sobre 1 UI/h | 0,025 a 25/0,025 bajo 1UI/h y 0,05 sobre 1 UI/h | Sí | No en Chile* | Sí. Al existir cierto nivel bajo de glicemia, la infusión de insulina se detiene por dos horas |
| Paradigm 515/Medtronics | 180 UI | 0,05 a 35/ 0,05 | 0,025-25/0,1 | Sí | No en Chile ** | No |
| Paradigm 715/Medtronics | 300 UI | 0,05 a 35/ 0,05 | 0,025-25/0,1 | Sí | No en Chile ** | No |
| Dana Diabecare IIS /Sooil | 300 UI | 0,01 a 16 / 0,01 | 0,05 a 80 / 0,05 | Sí | No | No |
| Dana Diabecare R /Sooil | 300 UI | 0,01 a 16 / 0,01 | 0,05 a 80 / 0,05 | Sí | Sí*** | No |
1. Modificado de Diabetes Forecast 2015, marzo-abril (http://www.diabetesforecast.org/2015/mar-apr/consumer-guide-2015.html)
* Requiere tiras reactivas de glicemia capilar Contour Next/Plus Link 2.4 de Bayer que no están disponibles en Chile. ** Requiere tiras reactivas de glicemia capilar ⿿One touch ultra⿿ incluidas en canasta GES de varias ISAPRES de Chile ⿿ Ese modelo de glucómetro no está a la venta en Chile pero se puede conseguir por internet *** Requiere tiras reactivas de glicemia capilar en venta en Chile en distribuidor Dana pero no están incluidas en canasta GES Diabetes tipo 1.
SET DE INFUSIÿN DISPONIBLES EN CHILE1
| Marca | Set de Infusión | ÿngulo inserción /longitud de la cánula | Material cánula | Longitud catéter (cm) |
|---|---|---|---|---|
| Medtronic Diabetes | Quick-set | 90° / 6 a 9 mm | Teflón | 60 y 110 |
| Sooil (Dana Diabecare) | Easy Release I y II | 90° / 7 a 9 mm | Acero | 71 y 110 |
| Soft Release-O | 90° / 6 a 9 mm | Teflón | 30,60 |
1 Modificado de Diabetes Forecast 2015, marzo-abril (http://www.diabetesforecast.org/2015/mar-apr/consumer-guide-2015.html)
* Medtronic trae a Chile otros tipos de set de infusión de distintas dimensiones a petición del usuario: Silhouette con ángulo variable de inserción para personas muy delgadas y Sure-T con cánula metálica y doble sistema de adhesivo para mayor seguridad, además permite desconexión a distancia del sitio de inserción, especialmente útil en lactantes delgados que requieren usar la cánula en la zona del pañal.
El tratamiento con bomba de insulina se puede iniciar a cualquier edad2. El momento para el cambio desde terapia MDI a CSII depende fundamentalmente de la motivación y compromiso con el tratamiento por parte del paciente y/o familia, junto con su nivel de conocimiento y entrenamiento en diabetes. Es por ello que los pacientes candidatos a este tipo de tratamiento deben cumplir con algunos requisitos mínimos para así poder lograr el beneficio que esta terapia ofrece (Tabla 4).
REQUISITOS PARA QUE UN PACIENTE SEA UN BUEN CANDIDATO A USO DE BOMBA DE INSULINA
| Uso previo de terapia con insulina basal-bolo a través de múltiples dosis ( 4 inyecciones al día) |
| Control frecuente de glicemias capilares ( 4 veces al día) |
| Motivación para alcanzar un buen control metabólico |
| Entender conceptos de insulinoterapia basal y prandial |
| Instrucción en conteo de hidratos de carbono |
| Utilizar y aplicar ratio o relación hidratos de carbono/insulina y factor de sensibilidad |
| Capacidad de ajustar dosis de insulina basal y ratio o relación de hidratos de carbono/insulina |
| Compromiso y disposición a seguir una terapia, que es más demandante y compleja que la terapia MDI |
| Contacto frecuente y expedito con el equipo de salud a cargo, compuesto por profesionales expertos de centros especializados en esta terapia |
| Ausencia de patología psiquiátrica en el paciente y/o familiar a cargo de la terapia |
| Expectativas realistas de la terapia con bomba de insulina |
Modificado del consenso para el manejo con bomba de insulina. Asociación Americana de Endocrinólogos Clínicos (AACE) y Colegio Americano de Endocrinología (ACE) 20143.
En algunos centros de excelencia, que cuentan con equipo multidisciplinario experto en este tipo de tratamiento, los lactantes y preescolares inician la terapia con CSII al momento del debut de la diabetes sin pasar por un periodo de transición con terapia MDI. Asimismo, en pacientes seleccionadas, como por ejemplo debut de DM1 durante un embarazo en curso, también podría ser una excepción y se puede considerar comenzar el tratamiento con CSII.
Entrenamiento en manejo intensificado de la diabetes1. Dominio de aspectos básicos del tratamiento con insulina. Los pacientes deben previamente tener claridad en aspectos básicos de la terapia con insulina basal - bolo, conocer los objetivos del tratamiento y saber cómo manejar complicaciones agudas como hipoglicemia y cetosis. El hecho de tener claro los conceptos y objetivos de la insulina basal y prandial, permitirá entrenarse más fácilmente en cómo funciona la bomba. Al contrario, en el caso de una persona que realiza insulinoterapia fija sin múltiples dosis, y que no esté dispuesta a avanzar a una insulinoterapia moderna no debería usar bomba de insulina. También es importante que el paciente conozca cuáles son las metas glicémicas deseadas y sepa cómo realizar ajustes de dosis de insulina y correcciones de glicemia.
2. Conocimiento en el conteo de hidratos de carbono, relación insulina: hidratos de carbono y factores de sensibilidad o corrección. Previo al uso de bomba de insulina los pacientes deben estar entrenados en el conteo de hidratos de carbono. En base a ello y a los niveles de glicemia que tengan antes de una comida, deben saber calcular la dosis de insulina prandial que deben administrase.
3. Dedicación al cuidado de la diabetes y autocontrol de glicemia capilar. El control frecuente de glicemia capilar, al menos 4 o 5 veces diarias, es clave para un resultado exitoso con la bomba.
4. Motivación y adherencia al tratamiento. Tanto el paciente como su familia, en el caso de los niños, deben estar motivados a tener un tratamiento demandante que exige dedicación permanente. En aquellos pacientes en que la motivación es disminuir el número de inyecciones, deben estar conscientes que tendrán nuevas tareas que realizar y que la bomba, al igual que la terapia MDI, exige dedicación y autocuidado. Es fundamental que se cumpla con la administración de los bolos pre-prandiales y los cambios del set y sitios de infusión en los tiempos debidos. Si no existen estos hábitos, la hemoglobina glicosilada (HbA1c) podría incluso empeorar con el uso de la bomba.
5. Buena comunicación con el equipo de salud. Las primeras semanas se requiere un estrecho contacto con el equipo de salud para ajustar la configuración inicial de la bomba de insulina.
6. Cobertura de salud del equipo e insumos. Al decidir el inicio de bomba de insulina, debe existir seguridad de que el paciente dispondrá de medios para contar con los insumos necesarios en forma constante e ininterrumpida.
7. Nivel de educación. El nivel de educación no es una limitante, sin embargo, el paciente y/o familiar debe tener un nivel cognitivo adecuado para entender el manejo integral de la diabetes y la bomba de insulina.
VENTAJAS DEL USO DE BOMBA DE INSULINA1. Mejoría en el control glicémico. La mejoría en el control metabólico con el uso de bomba de insulina es variable en diferentes individuos. La evidencia publicada a lo largo de los años muestra resultados heterogéneos en cuanto al impacto del uso de esta tecnología sobre la HbA1c, pero en general existe una disminución en el promedio de HbA1c entre -0,3% y -0,5%4⿿7. Por otra parte, en estos mismos análisis, cuando se hizo la evaluación de bombas más modernas, con monitoreo continuo de glucosa integrado (SAPT; del inglés Sensor Augmented Pump Therapy) y se le comparó con terapia MDI, se encontró un mayor beneficio, con una reducción promedio de HbA1c de -0,68%; CI95%; (p<0,001)4⿿6.
En la práctica clínica, el beneficio metabólico de la terapia con bomba de insulina es dependiente del uso que le da el paciente, así como la dedicación y perseverancia que invierta en ello. Por lo anterior y como ya se mencionó, es fundamental un buena selección del paciente y su adecuado entrenamiento en la terapia.
2. Disminución de las hipoglicemias severas. El tratamiento con CSII permite un tratamiento más fácil de la hipoglicemia debido a que la suspensión de la infusión detiene rápidamente el aporte de insulina al subcutáneo, a diferencia de las inyecciones en que la dosis ya está administrada y su efecto puede durar muchas horas. La reducción de la tasa de hipoglicemia severa ha sido demostrada recientemente con el uso de SAPT con incorporación de la suspensión de la infusión de insulina en hipoglicemia8,9. Por otra parte, el número de episodios totales (incluyendo tasa de hipoglicemia leve) puede ser menor debido a la mayor flexibilidad en la programación y administración de dosis que es característica del tratamiento con CSII4⿿6,8y 9. En pacientes de corta edad, la factibilidad de entregar dosis ínfimas de insulina más acordes a sus requerimientos, hace que este riesgo disminuya en forma importante, lo que es una gran ventaja.
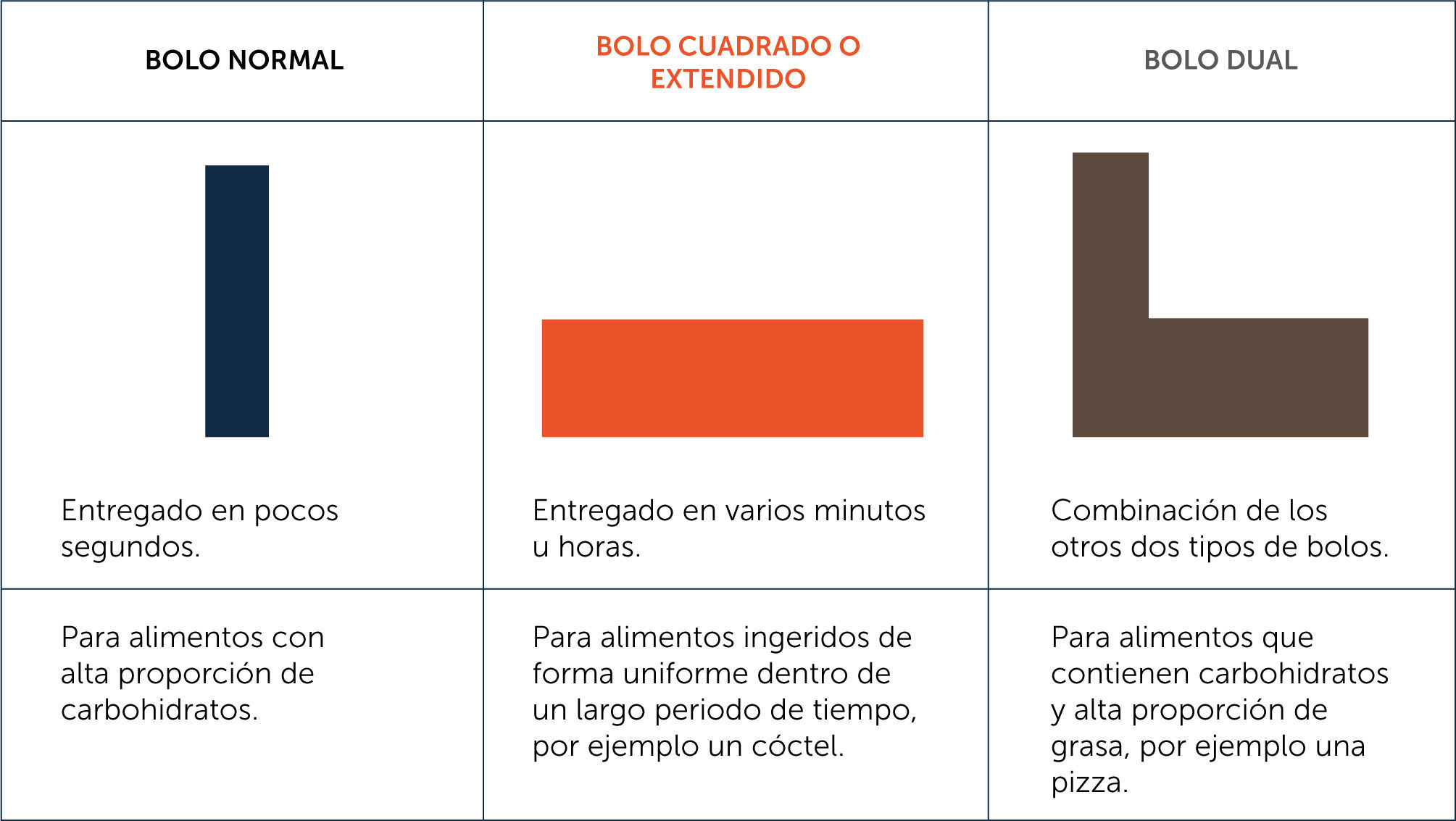
3. Aumento del número de bolos diarios y uso de diferentes tipos de bolo. La posibilidad que la insulina prandial se administre con el dispositivo, sin la necesidad de inyecciones múltiples, permite una mayor adherencia a la terapia y flexibilidad en la alimentación, tanto en horario, tipo y cantidad de comida. El uso de bolos sin necesidad de colocar inyecciones extra también permite corregir hiperglicemia post-prandial e hiperglicemias aisladas, haciendo que los pacientes acepten administrar bolos de corrección entre las comidas. Diferentes estudios han demostrado que la mejoría del control metabólico se relaciona con el número de bolos diarios utilizados y con el uso del asistente o calculador de bolos10,11.
La bomba puede entregar bolos con diferentes formas, lo que permite entregar los aportes de insulina prandial de manera diferenciada según la composición nutricional de los alimentos y el tiempo estimado que paciente demorará en consumirlos (Figura 2).
4. Uso de basales temporales y facilidad para ajustar las dosis de insulina frente al ejercicio y en situaciones especiales. El uso de bomba permite ajustar en forma transitoria la dosis de insulina basal entregada, a través de una basal temporal, de duración programable, permitiendo aumentar o reducir en un porcentaje, también programado, la administración de insulina basal según sea la situación. Un ejemplo de su uso es durante el ejercicio. Las necesidades de disminución de aporte de insulina en relación a la actividad física, como estrategia de prevención de hipoglicemia, varían de persona a persona12⿿14.
Por otra parte la capacidad de ajustes rápidos en dosis basales y prandiales da facilidad para el manejo de situaciones especiales, tales como enfermedades agudas y viajes. En todo caso, el paciente debe estar atento al tratamiento y manejo de la bomba para lograr sacar provecho de la tecnología en este tipo de ocasiones.
6. Potencial mejoría en calidad de vida. El impacto en la calidad de vida con el uso de bombas de insulina versus terapia MDI no siempre es analizado en los ensayos clínicos o bien es un desenlace secundario dentro de los mismos. Los meta análisis más recientes muestran en general un impacto positivo sobre la calidad de vida de los usuario de bomba de insulina versus aquellos en terapia MDI, no obstante el poder de la evidencia es bajo4⿿6. A pesar de lo anterior existe un porcentaje (2-11%) que decide suspender el CSII y volver a tratamiento con inyecciones15,16.
EFECTOS ADVERSOS Y PROBLEMAS POTENCIALES DEL USO DE BOMBA DE INSULINASi bien la severidad de los eventos adversos con el uso de bombas modernas es menor que antaño, actualmente siguen siendo frecuentes, afectado a más del 40% de usuarios por año17. Según su naturaleza pueden dividirse en complicaciones metabólicas y no metabólicas. Dentro de las primeras las más importantes, por la consecuencia que trae a los pacientes, son la cetoacidosis diabética (CAD) y la hipoglicemia severa (HS). No metabólicos podemos encontrar: complicación con el sitio o set de infusión, falla de la bomba y problemas cutáneos de diferente naturaleza, incluidas las infecciones.
1. Hiperglicemia, cetosis y cetoacidosis. El hecho que CSII entregue insulina ultrarrápida en forma continua y en baja cantidad y que no haya una insulina basal de larga duración como en esquemas de MDI, explica que exista riesgo de CAD si se produce una interrupción de su aporte. Con más de 60 minutos de interrupción se produce elevación significativa de la glicemia, que de ser mantenida en el tiempo rápidamente lleva a la formación de cuerpos cetónicos, pudiendo llegar a CAD en pocas horas22,23. En el último tiempo se ha visto disminución de esta complicación con CSII y actualmente su incidencia no es mayor respecto a la reportada en los pacientes en terapia MDI24.
Como medida de seguridad, las bombas cuentan con una gráfica en la pantalla del equipo que muestra cuánta insulina queda en el reservorio y la carga de batería del dispositivo, además de alarmas que alertan al paciente ante la posibilidad de que se detenga el suministro de insulina.
2. Falla en el set de infusión. Los problemas relacionados a falla con el set de infusión pueden traer como consecuencia la interrupción del aporte de insulina lo que, puede llevar a desarrollo de CAD. Dentro de las posibles fallas podemos encontrar: oclusión o acodamiento del catéter, desplazamiento de la cánula fuera del espacio subcutáneo, filtración de insulina, formación de burbujas de aire en el catéter y acodamiento del catéter o cánula18.
3. Infección cutánea y otros eventos adversos cutáneos. La infección como evento adverso ha ido disminuyendo en los últimos años. En la década de los ochenta una publicación mostró esta complicación en el 29% de los usuarios de bomba19 versus un reporte reciente en que se observó infección en un 17% de los pacientes18, y en dos publicaciones pediátricas no se encontró ningún caso20,21. La infección del sitio de infusión tiene directa relación con la inadecuada preparación de la piel previa al cambio de set de infusión y/o a la mantención del mismo por más de los tres días recomendados.
La gravedad de estos cuadros varía, desde una celulitis, que se trata con cambio de sitio y set de infusión más terapia antibiótica con cobertura contra gram positivos, hasta abscesos. Esto último puede tener impacto sistémico variable, que además de una terapia antibiótica más prolongada y de mayor espectro, puede requerir drenaje quirúrgico.
También se han observado otros eventos adversos cutáneos como irritación y/o alergia a los adhesivos del set, cicatrices y lipodistrofias18.
4. Ganancia de peso en algunas personas que liberalizan la alimentación excesivamente. Algunos individuos pueden aumentar de peso, cuando aumentan el consumo de alimentos entre comidas ya que la insulina está siempre disponible para colocar bolos prandiales. A pesar de lo anterior, diversos estudios demuestran que el uso de la bomba per se no aumenta el peso25. Al contrario, en aquellas personas que quieren perder peso, la flexibilidad de la terapia insulínica con bomba permite disminuir la frecuencia de hipoglicemia y de alimentación como tratamiento de esta complicación, permitiendo disminuir las calorías totales ingeridas.
5. Costos. Los costos de la insulinoterapia con bomba son mayores que con terapia MDI, sin embargo estos pueden ser compensados con el mejor control metabólico, que lleva a la prevención del desarrollo de complicaciones crónicas y ahorro de los gastos asociados a ellas. Los costos de la terapia con bomba también se ven compensados por la reducción de hipoglicemias y la mejoría en la calidad de vida que ello conlleva. Múltiples estudios publicados avalan la costo efectividad de esta terapia26⿿30.
6. Consideraciones físicas y logísticas. Para algunas personas el usar bomba de insulina representa una desventaja o incomodidad, pues se sienten limitados al estar permanentemente ⿿conectados⿿ a un aparato. Esto los lleva a recordar continuamente su condición y los expone a que otras personas les pregunten sobre el dispositivo.
Por otra parte, desde el punto de vista logístico, el paciente que inicia el uso de una bomba de insulina requiere invertir tiempo considerable en entrenamiento, que debe ser contemplado, especialmente si vive lejos del centro de educación en diabetes.
MONITOREO CONTINUO DE GLUCOSA SUBCUTÿNEA (CGM)Dentro de los avances tecnológicos se cuenta con el monitoreo continuo de glucosa en el subcutáneo (CGM). Esta tecnología mide en forma continua la glucosa en el intersticio, a diferencia de los medidores de glicemia capilar de uso domiciliario habituales que determinan la concentración de glucosa en sangre capilar.
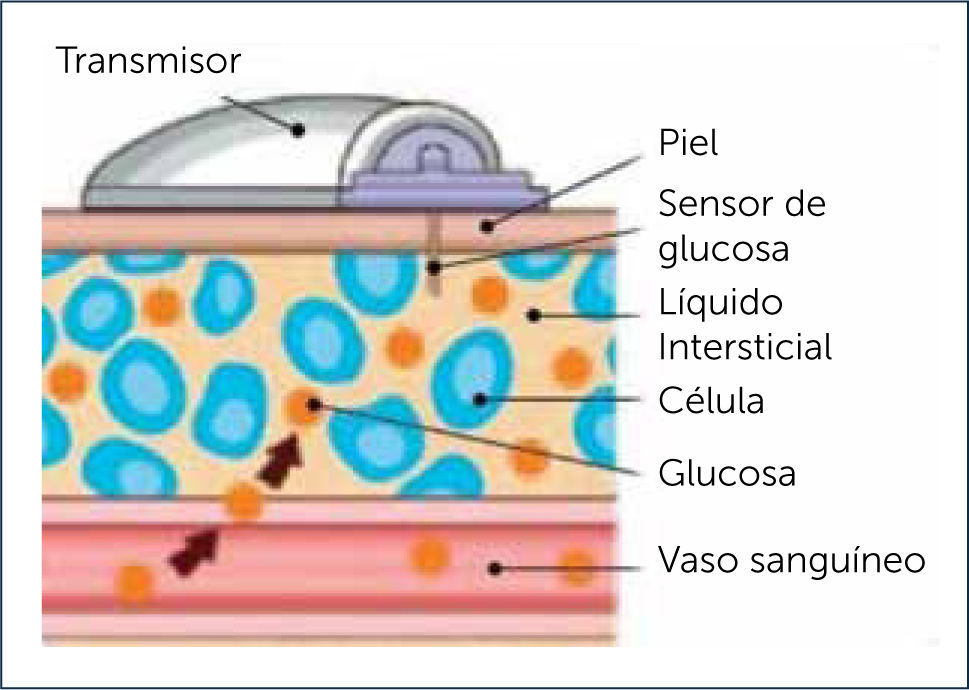
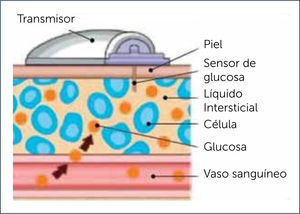
Descripción y funcionamiento del monitor continuo de glucosaEl CGM consta de 3 partes: 1) Sensor, 2) Transmisor y 3) Receptor. El sensor es un filamento que se inserta a través de la piel y es la pieza que mide los niveles de glucosa a nivel del espacio intersticial subcutáneo. El sensor está unido al transmisor, una pequeña pieza que queda por fuera de la piel, conectada al sensor. A su vez el transmisor informa en forma inalámbrica al receptor (Figura 3).
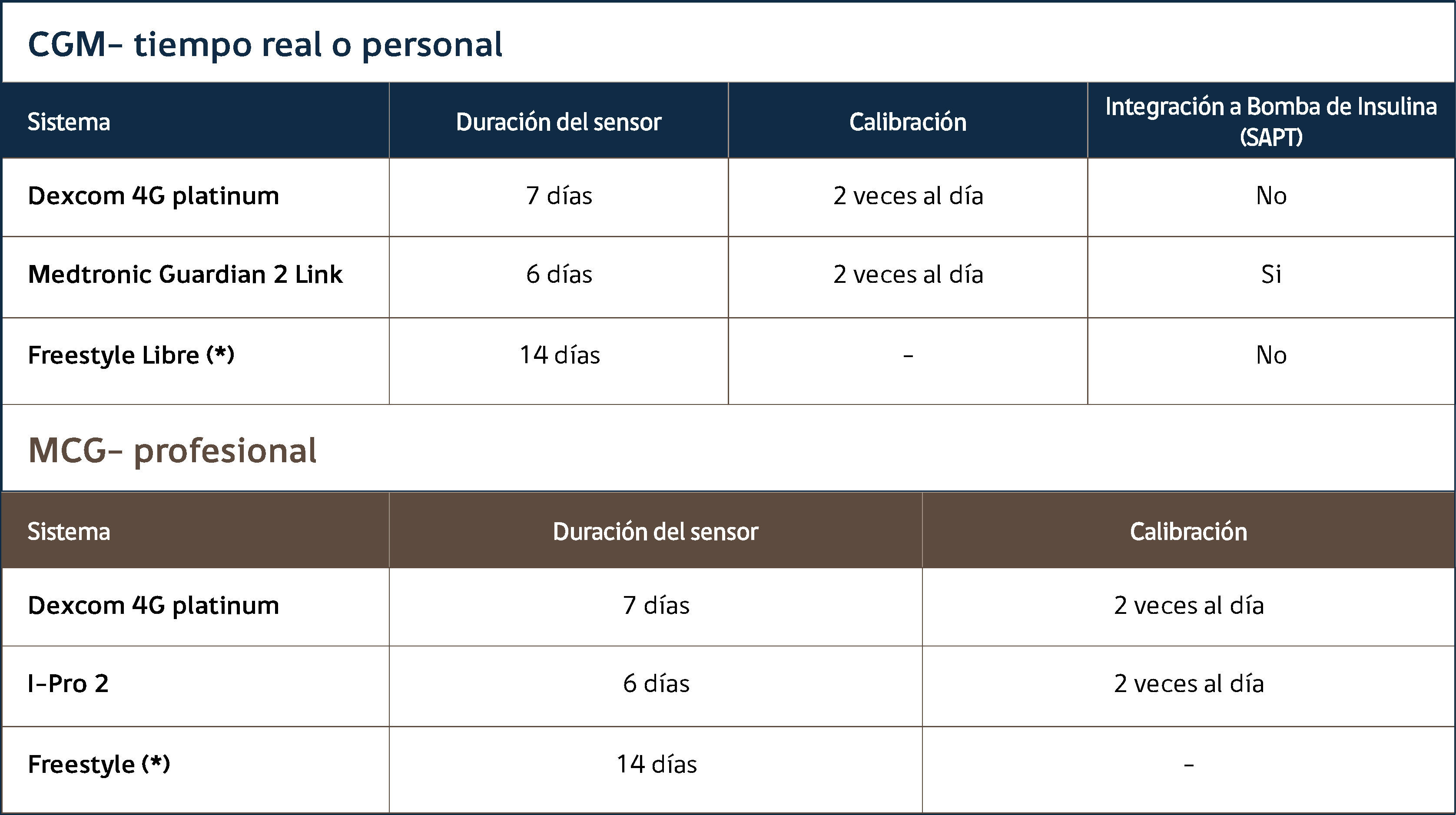
El sensor determina la glucosa intersticial cada 5 minutos, entregando así 288 mediciones en un día. El sensor contiene enzima glucosa oxidasa que por una reacción electroquímica dependiente de los niveles de glucosa informa una corriente eléctrica que es detectada por el transmisor. A su vez estas variaciones eléctricas son entregadas por el transmisor al receptor que las informa al usuario como glucosa en mg/dl31. La vida útil de los sensores varía de 3 a 14 días, dependiendo de la marca fabricante, de modo que debe ser reemplazado por uno nuevo una vez que su funcionamiento caduca.
Desfase o lag fisiológico y precisión del monitor continuo de glucosaEs importante destacar que al determinar glicemia intersticial el valor obtenido por el CGM tiene un desfase o ⿿lag⿿ fisiológico entre el valor observado en sangre capilar con respecto al medido por el CGM, y es en promedio de 5 a15 minutos. Este retraso o desfase, producto del tiempo que toma la glicemia en difundir y equipararse entre los dos compartimientos (Figura 3), es importante cuando hay cambios bruscos de glicemia, pero no cuando hay estabilidad en los niveles de glucosa. Por este motivo los CGM actualmente aprobados para uso en pacientes son considerados un complemento del automonitoreo con glicemias capilares.
La exactitud de los CGM ha ido mejorando con la aparición de nuevas tecnologías. Actualmente los dispositivos más modernos tienen una diferencia media respecto a la glicemia capilar y/o plasmática del 11,4 a 13,9%32,33, la que es mucho mejor a la reportada con los primeros equipos de CGM34.
TIPOS DE MONITOR CONTINUO DE GLUCOSAExisten tres tipos de CGM: 1) profesional 2) en tiempo real (CGM-RT) o personal y 3) en tiempo real pero, con lectura de las glicemias a demanda.
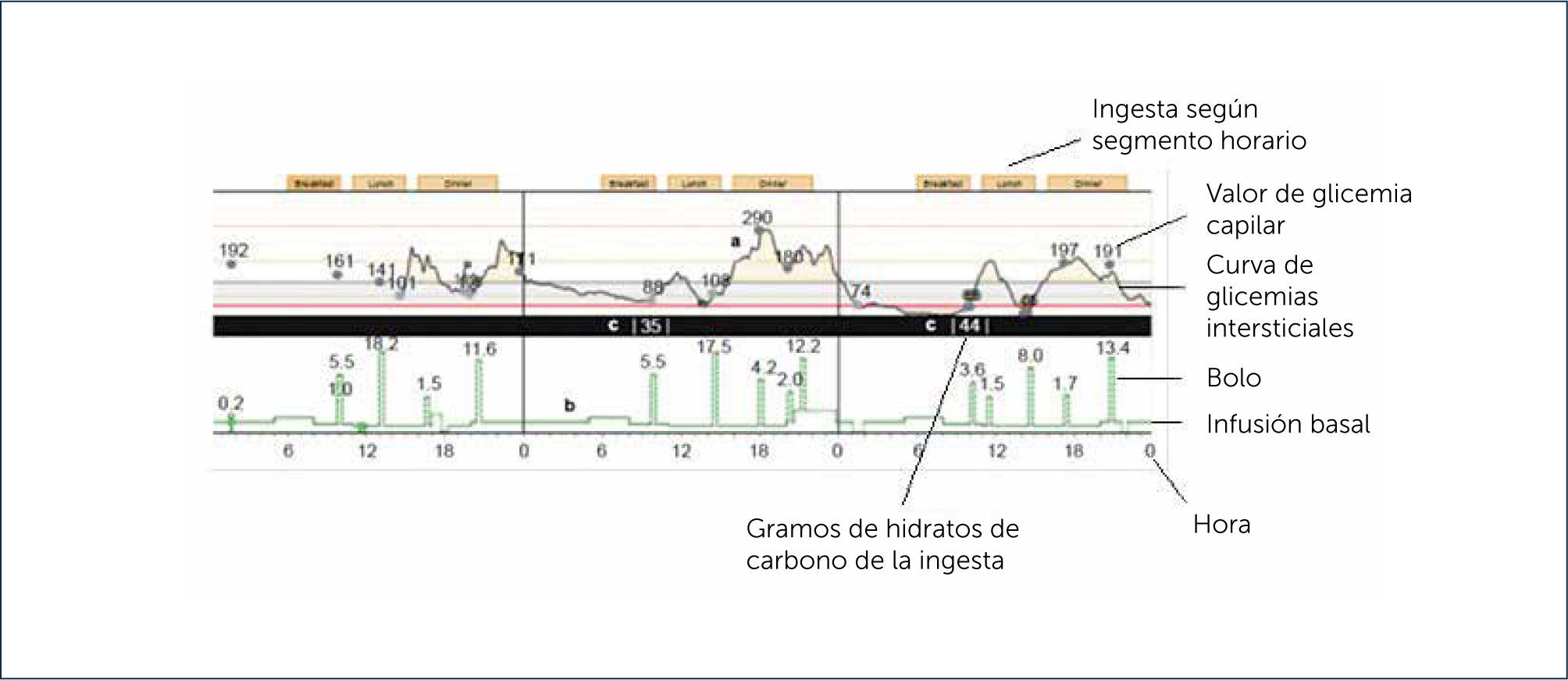
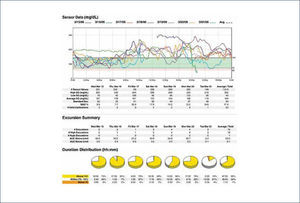
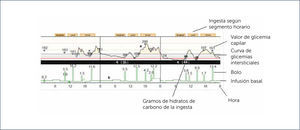
1) CGM profesional o ⿿holter de glicemia⿿ es ciego para el paciente, es decir, este no tiene acceso a las lecturas de glucosa. Las glicemias son obtenidas recién después de que el sensor es retirado del paciente y sus datos son analizados por un software específico que traducirá la información en un reporte con curvas y gráficos de glicemia (Figura 4). De este modo este tipo de CGM es retrospectivo y tiene como objetivo ser una herramienta para el médico especialista en el ajuste del tratamiento. Este tipo de monitoreo es solicitado por el médico como un examen de laboratorio.
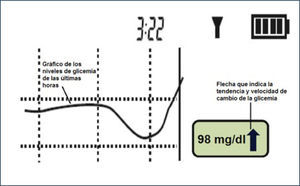
2) El CGM-RT o personal es de uso continuo por el paciente quien puede ver en forma constante las mediciones de glicemia, curvas y tendencias de ésta en una pantalla incorporada al receptor del monitor. Al entregar información gráfica en tiempo real (Figura 5) ésta puede ser usada por el paciente para hacer modificaciones en su tratamiento con el objetivo de lograr un mejor control metabólico y menor variabilidad glicémica. Inicialmente el CGM-RT fue usado por pacientes en tratamiento con CSII, pero se ha determinado su beneficio al ser usado en pacientes con tratamiento intensificado con MDI.
EJEMPLO DE GRÿFICA EN LA PANTALLA DEL RECEPTOR DE UN CGM-RT
Modificado de Tumminia A. et al. Patient Preference and Adherence 2015:9 1263⿿127035.
A diferencia del CGM profesional el CGM-RT requiere participación activa del paciente, quien debe ser entrenado de forma continua para ser capaz de interpretar la información que el dispositivo le entrega, y así pueda tomar decisiones eficientes y seguras respecto a su tratamiento. Parte de los beneficios de los CGM es que cuentan con alarmas que alertan al paciente de niveles altos o bajos de glicemia, y también frente a variaciones significativas en la velocidad de cambio de la glicemia.
3) Dentro de los CGM existe un nuevo tipo con lectura de glucosa intersticial en tiempo real pero con lecturas de los niveles de glicemia a demanda, es decir, que la información no se ve todo el tiempo en la pantalla del receptor, sino sólo cuando el paciente lee sus niveles de glucosa intersticial a demanda Está disponible en Europa y próximamente en Chile.
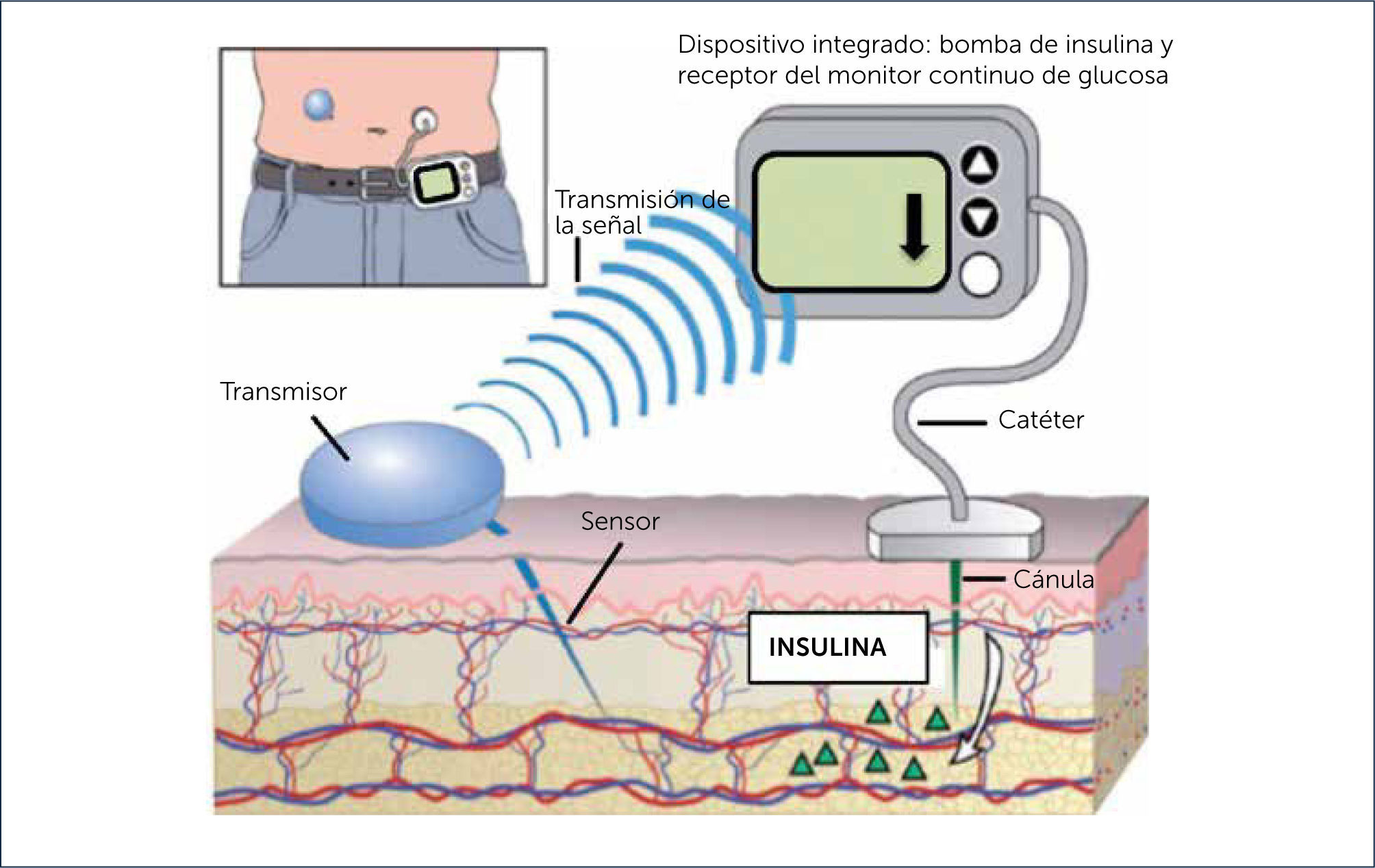
Actualmente se dispone de sistemas de CGM-RT incorporados a CSII en un mismo dispositivo (SAPT) (Figura 6). En los últimos años a estos sistemas integrados se les ha incorporado un software más sofisticado que permite además la detención de la infusión de insulina en caso de predicción de niveles bajos de glucosa intersticial.
TERAPIA INTEGRADA (SAPT, SENSOR AUGMENTED PUMP THERAPY): BOMBA DE INSULINA Y CGM-RT
Modificado de Tumminia A. et al. Patient Preference and Adherence 2015:9 1263⿿127035.
En la Tabla 5 se detallan los modelos disponibles en Chile.
El beneficio más evidente es que permite al paciente realizar ajustes más precisos de la dosis de insulina a administrar. El paciente obtiene información acerca de la tendencia en aumento o en disminución de la glicemia. Esta última se ve graficada en forma de curvas y flechas en la pantalla del CGM-RT (Figura 5).
El beneficio del uso de CGM-RT sobre el control metabólico depende del porcentaje de días efectivos usando el dispositivo, y de la edad del sujeto. Publicaciones en revistas de primer nivel han demostrado que la mejoría de la HbA1c es dependiente del tiempo que se utiliza el CGM, logrando beneficios de importancia si es usado más allá del 60-70% del tiempo36⿿40. En aquellos pacientes sin un buen nivel de adherencia al uso del sensor, como por ejemplo los adolescentes, no se ha observado este beneficio.
Otro de los posibles beneficios es el manejo oportuno de la hipoglicemia. Desgraciadamente, los ensayos clínicos no son concluyentes respecto a que la tasa de hipoglicemia leve efectivamente disminuya, pero si está objetivado su beneficio en la reducción de hipoglicemia severa cuando se usa SAPT con suspensión de la infusión de insulina en hipoglicemia8,9. A pesar de las dudas en la disminución de tasa de hipoglicemia, el uso de CGM ha sido recomendado como tratamiento de elección en casos de hipoglicemia severa a repetición, y en caso de insensibilidad a la hipoglicemia41,42.
Las desventajas del uso de CGM-RT se relacionan al costo, a fallas del sensor (como pérdida de señal), exceso de alertas, sobrecarga de información, necesidad de calibración y al desfase fisiológico entre sangre e intersticio. Estas desventajas hacen que en muchas oportunidades el uso del sensor resulte cansador para el paciente y solamente use este dispositivo en forma intermitente.
Factores predictores de éxito en el uso del monitor continuo de glucosaHabiendo revisado los beneficios y eficacia del uso del CGM-RT, se debe destacar la importancia de distinguir en los pacientes con indicación clínica de su uso, aquellos factores que predicen el éxito del tratamiento con este tipo de dispositivo, pues de lo contrario no se logrará alcanzar el beneficio real que el CGM-RT ofrece.
Software de reportesTanto CSII como los CGM cuentan con un software especializado que descarga la información del dispositivo a un computador, lo que permite analizar en forma retrospectiva el caso del paciente (Figura 7).
EJEMPLO DE REPORTE DESCARGADO A PARTIR DE UN DISPOSITIVO DE SAPT
Modificado de Tumminia A. et al. Patient Preference and Adherence 2015:9 1263⿿127035.
Esto representa una herramienta de valor incalculable para el médico tratante y el paciente, pues permite analizar la tendencia y comportamiento glicémico de forma más precisa y detallada de lo que permitiría hacerlo solo con el registro manual o cuaderno de glicemias capilares que el paciente pueda hacer. Además este software entrega una serie de información adicional como la adherencia al uso del sensor y al cambio de cánula, tiempos de suspensión de la infusión, ingesta de hidratos de carbono, proporción de insulina basal y bolos, entre otras. Estos reportes pueden ser enviados a través de internet, permitiendo ajustes a distancia si es necesario.
CONCLUSIÿNLas nuevas tecnologías representan una importante arma terapéutica para un grupo de pacientes con diabetes tipo 1, en especial para aquellos que pese a haber optimizado su terapia con múltiples dosis de inyecciones subcutáneas no logran un óptimo control terapéutico o sufren de hipoglicemia de difícil manejo. También es de gran ayuda en el tratamiento de pacientes de corta edad y en embarazadas. Considerando su elevado costo es fundamental que este grupo de pacientes sea tratado en centros de referencia, a cargo de médicos especialistas con experiencia en ese tipo de tecnologías.
Los Dr. Néstor Soto y Dra. Ethel Codner no tienen conflicto de interés en relación a este artículo. La Dra. Pamela Apablaza recibió ayuda de Medtronics para viajar a capacitación. La Dra. Rossana Román recibió apoyo de Medtronics para asistir a congreso.