La fibrilación auricular es la arritmia más frecuente y se relaciona con una alta tasa de accidente cerebrovascular y embolia sistéc)mica. La terapia establecida tanto para prevención primaria como secundaria es la anticoagulación con warfarina, antagonista de la vitamina K. Existen escalas que predicen el riesgo tromboembólico y la probabilidad de beneficiarse de terapia antitrombótica. El CHADS2ha sido la más simple y ampliamente utilizada, pero actualmente el CHA2DS2-VASc ha incorporado otros factores de riesgo, otorgando una mejor estratificación. El estrecho margen terapéc)utico de la warfarina y la interacción con fármacos y alimentos requiere controles seriados de la intensidad de la anticoagulación, limitando su uso clínico. Han aparecido nuevos anticoagulantes que ofrecen ventajas sobre los antagonistas de vitamina K. Estos actúan en dos sitios distintos de la cascada de la coagulación: inhibiendo directamente la trombina como el dabigatran, o el factor X activado como el rivaroxaban, apixaban, edoxaban y betrixaban. Estos nuevos fármacos han ido reemplazando a la warfarina y ya están incluidos en las guías de manejo de fibrilación auricular no valvular.
Atrial fibrillation is the most common arrhythmia and is a major risk factor for ischemic stroke and systemic embolism. The therapy for primary and secondary prevention is the anticoagulation with warfarin; antagonist of vitamin K. There are scores to predict the risk of thromboembolism and the benefit of the antitrombotic therapy. The CHADS2 score has been the easiest one and it has been used widely, but today the CHA2DS2-VASc score includes new risk factors and gives a better risk stratification. The narrow therapeutic. margin and the interaction with food and drugs requires frequents tests of intensity of anticoagulation limiting usefulness in clinical practice. There are new anticoagulants that offer advantages compared with warfarin. These drugs act in two different points of the cascade of anticoagulation; directly inhibiting thrombin like dabigatran or factor X activated like rivaroxaban, apixaban, edoxaban and betrixaban. These new agents are replacing warfarin and they are already included in the guidelines of atrial fibrillation.
La Fibrilación Auricular (FA) es la alteración más frecuente del ritmo cardíaco; uno de cada cuatro personas mayores de 40 años desarrollará FA a lo largo de su vida1. En el año 2007 se diagnosticó FA a 6,3 millones de personas en EE.UU., Japón, Alemania, Italia, España, Francia y el Reino Unido2. Debido al envejecimiento progresivo de la población se espera que esta cifra se duplique en 30 años3.
FIBRILACIÓN AURICULAR (FA) Y ACCIDENTE CEREBROVASCULAR (ACV)Los pacientes con FA tienen cinco veces más riesgo de presentar un ACV4. Aproximadamente 3 millones de personas sufren un ACV asociado a fibrilación auricular (FA) cada año en todo el mundo4,5. Un aspecto importante es que los pacientes con FA paroxística tienen el mismo riesgo de sufrir este evento que aquellos con FA permanente5,6. El ACV secundario a FA se asocia con una mortalidad de 25% a los 30 días7 y de un 50% al cabo de un año8. Afortunadamente dos tercios de estos ACV se pueden evitar con tratamiento anticoagulante adecuado.
Un meta-análisis de 29 estudios, publicado en JACC el año 20079 con 28.044 pacientes mostró que la administración de dosis ajustadas de warfarina reducía los ACV isquéc)micos en un 64% y la mortalidad total en un 26%. La anticoagulación oral con antagonistas de la vitamina K (AVK) ha sido utilizada hace más de 60 años para prevenir accidentes cerebrovasculares asociados a fibrilación auricular en pacientes con riesgo moderado y alto. Los AVK son altamente eficaces cuando los pacientes se mantienen dentro de un rango terapéc)utico adecuado (INR 2 a 3) durante la mayor parte del tiempo (60 - 70%), sin embargo, este porcentaje de cumplimiento con frecuencia es difícil de obtener.
ESTIMACIÓN DEL RIESGO DE ACV EN PACIENTES CON FIBRILACIÓN AURICULARNo todos los pacientes con FA tienen el mismo riesgo embólico, de tal manera que deben existir herramientas para diferenciarlos. El CHADS210 es un score de estratificación de riesgo de ACV isquéc)mico que considera 5 parámetros. Su nombre deriva de las iniciales de estos parámetros en ingléc)s (Tabla 1).
SCORE CHADS2
| ÍTEM | PUNTOS |
|---|---|
| Insuficiencia Cardiaca Congestiva | 1 |
| Hipertensión arterial | 1 |
| Edad ≥75 años | 1 |
| Diabetes mellitus | 1 |
| ACV/CIT | 2 |
ACV/CIT: Accidente Cerebrovascular / Crisis isquéc)mica transitoria Traducida de Gage, et al. Validation of clinical classification schemes for predicting stroke: results from the National Registry of Atrial Fibrillation. JAMA. 2001 Jun 13; 285(22):2864-70.
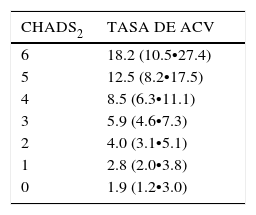
La probabilidad del score CHADS2 de predecir tasas de ACV isquéc)micos fue determinada en un grupo seleccionado de 1.733 pacientes, entre 65 y 95 años de edad, del Registro de FA, que fueron dados de alta sin tratamiento con Warfarina. El seguimiento de estos pacientes permitió determinar que, por cada punto que aumenta el score CHADS2 el riesgo de ACV se incrementa en 1,5% (95% CI 1.3•1.7)10 (Tabla 2).
Además del riesgo de embolia, en el tratamiento de estos pacientes tambiéc)n es importante estimar el riesgo de sangrado. Para esto, uno de los instrumentos más utilizados es el Score de Riesgo de Sangrado HAS BLED. En éc)l 1 punto representa un riesgo de 1.02%/año; 2 puntos: 1.88%/año y 3 puntos: 3.74%/ año (Tabla 3).
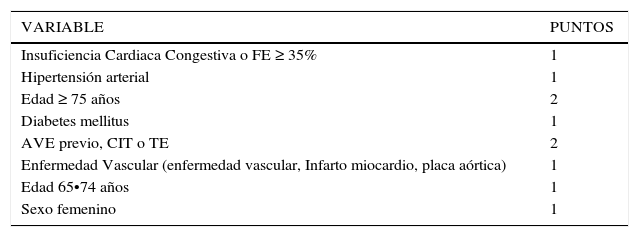
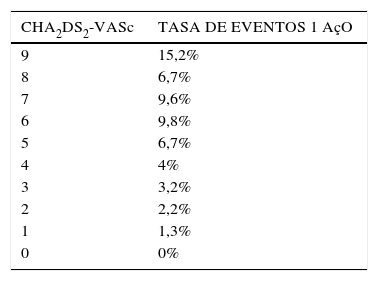
Si bien el CHADS2 es una herramienta muy útil, éc)sta no incluye otros factores reconocidos de riesgo de ACV como son el sexo femenino, la enfermedad vascular (Infarto agudo al miocardio, enfermedad arterial periféc)rica o placa aórtica) y la edad entre 65 y 75 años (ser mayor de 75 años no es un factor de riesgo dicotómico, sino más bien un factor continuo, aumentando el riesgo desde los 65 años en adelante). Esto puede llevar a subestimar el riesgo en algunos pacientes de mayor riesgo que así no recibirán terapia antitrombótica adecuada. En base a las consideraciones de estos otros factores de riesgo embólico, se generó el score CHA2DS2-VASc que corresponde a una adaptación del CHADS2 al que se han adicionado estos factores de riesgo y cuya validación fue efectuada con una cohorte de pacientes con FA, en la vida real, en Dinamarca11,12 (Tablas 4 y 5).
SCORE CHA2DS2-VASC
| VARIABLE | PUNTOS |
|---|---|
| Insuficiencia Cardiaca Congestiva o FE ≥ 35% | 1 |
| Hipertensión arterial | 1 |
| Edad ≥ 75 años | 2 |
| Diabetes mellitus | 1 |
| AVE previo, CIT o TE | 2 |
| Enfermedad Vascular (enfermedad vascular, Infarto miocardio, placa aórtica) | 1 |
| Edad 65•74 años | 1 |
| Sexo femenino | 1 |
Traducida de Olesen JB et al. BMJ 2011;342:d 124.Camm et al. Eur Heart J 2010, 31:2369-2429
Este score estratifica mejor el riesgo del paciente, generando sólo una pequeña proporción de pacientes que son categorizados como de riesgo intermedio, simplificando la selección de los pacientes para la anticoagulación. Comparado con el CHADS2 clásico, la incorporación del CHA2DS2-VASc aumenta la proporción de los pacientes en los cuales es recomendable el uso de anticoagulantes orales13.
LA PROBLEMÁTICA DE LA ANTICOAGULACIÓN CON WARFARINA EN FAEl tratamiento con AVK tiene varias limitaciones que lo hacen difícil de usar en la práctica clínica: respuesta impredecible, frecuente ajuste de dosis, ventana terapéc)utica estrecha (INR 2-3), numerosas interacciones con alimentos y fármacos, necesidad de monitorización sistemática de la coagulación, lento comienzo y desaparición del efecto, resistencia a la warfarina, etc. Debido a todas estas limitaciones de los AVK, se ha estimado que hasta un 50% de los pacientes elegibles para ser tratados no reciben tratamiento anticoagulante y de aquellos en tratamiento, sólo un 35% está en rango de INR terapéc)utico2-3; un 15% tendría un INR inferior a 2 y un 10% sobre 314. Por todo lo anterior se necesitaba un anticoagulante que ofreciera ventajas sobre los AVK como ser administración oral a dosis fija, rápido comienzo de acción, vida media corta, escasa interacción con fármacos o alimentos, eficacia y seguridad al menos como los AVK, efecto anticoagulante predecible y sin necesidad de monitorización sistemática.
Desde hace ya algunos años se están usando un grupo de anticoagulantes no vitamina K dependientes que cumplirían las condiciones previamente señaladas; dosificación simple y fija, sin restricciones de dieta, anticoagulación predecible y sin necesidad de monitorización rutinaria de la coagulación, menor interacción con alimentos y drogas, todo lo cual implica menos seguimiento intensivo, menos impacto en la calidad de vida y mejoría del cumplimiento lo que determina una reducción de costos administrativos mejor calidad de vida y mejoría de la eficacia y seguridad.
TIPOS DE ANTICOAGULANTES Y SU MECANISMO DE ACCIÓN1. Antagonistas de la vitamina K
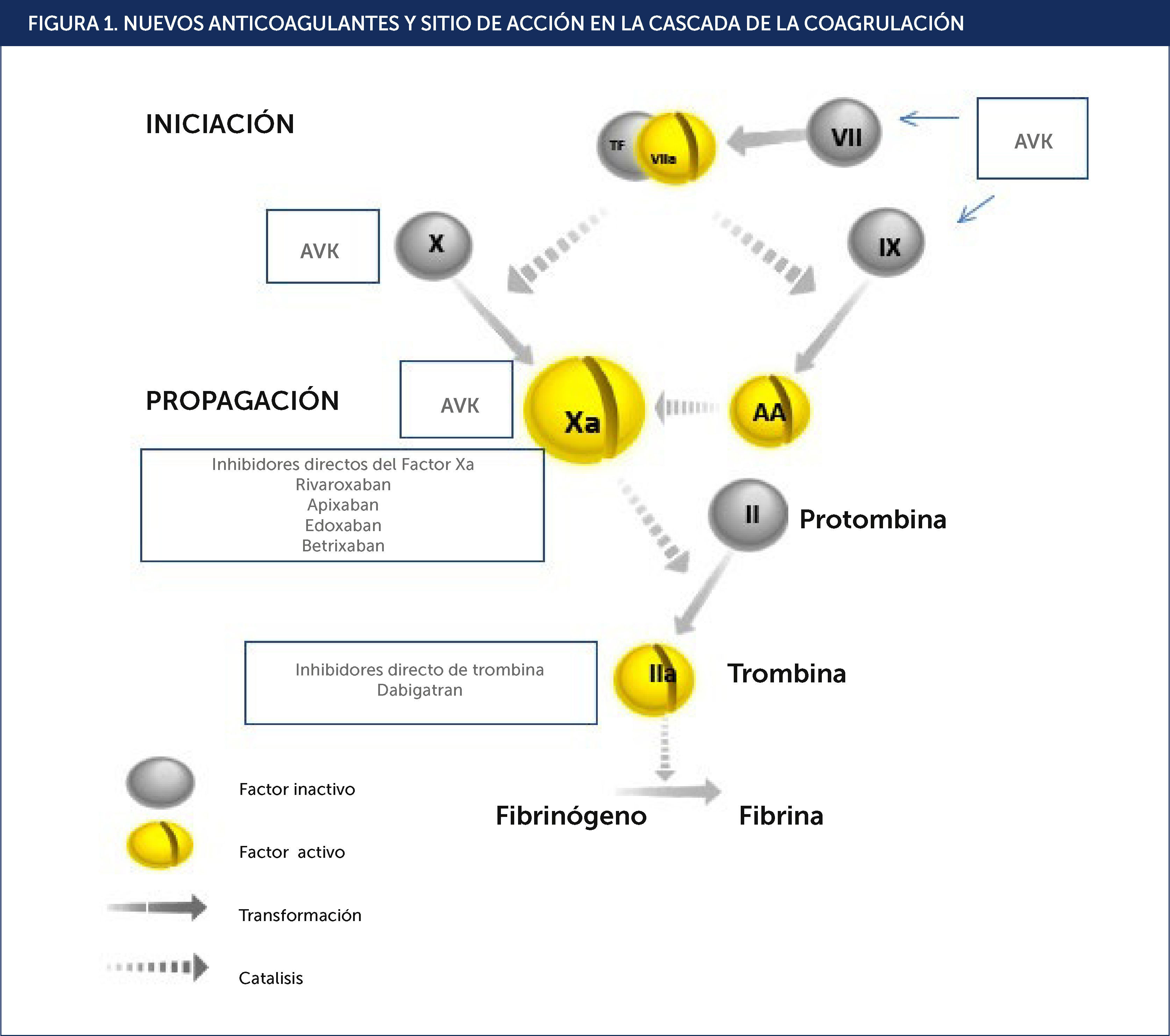
Estos fármacos, tales como la Warfarina o acenocumarol, actúan inhibiendo la carboxilación (dependiente de vitamina K) de los Factores II, VII, IX y X, produciendo una menor actividad coagulante15.
2. Inhibidores del Factor X activado (Xa)
El factor Xa juega un rol clave en el proceso de la coagulación, ya que es un paso limitante tanto de la vía intrínseca como extrínseca, sin Factor Xa no se puede generar trombina. Serían como formas “orales de heparina”. Existen varios fármacos con este mecanismo de acción que ya están aprobados o en vías de desarrollo: rivaroxaban, apixaban, edoxaban, betrixaban, darexaban, eribaxaban.
3. Inhibidores directos de la Trombina
La trombina convierte el fibrinógeno en fibrina, por lo que es fundamental en la formación del coágulo. Tambiéc)n es un potente inhibidor plaquetario. Estos fármacos pueden inhibir tanto la trombina libre como la unida al coágulo, bloqueando el paso final de la cascada. El Dabigatran es la única droga de este tipo actualmente disponible para la prevención de embolia sistéc)mica en pacientes con FA. El ximelagatran (actualmente descontinuado por toxicidad hepática en uso prolongado) mostró ya que era no inferior a warfarina en prevención de tromboembolismo (TE) en FA y además que no requerían monitoreo de rutina del efecto anticoagulante16 (Figura 1).
NUEVOS ANTICOAGULANTES ORALES (NACO)DabigatránEs una Prodroga que inhibe directamente la trombina, con acción reversible. Tiene un inicio de acción rápida y una vida media de 12-17hrs. Tiene un 6,5% de biodisponibilidad y es excretado en un 80% por vía renal. Tiene un efecto anticoagulante predecible y consistente, bajo riesgo de interacción con drogas, sin interacción con comidas y no requiere monitoreo rutinario de la coagulación17.
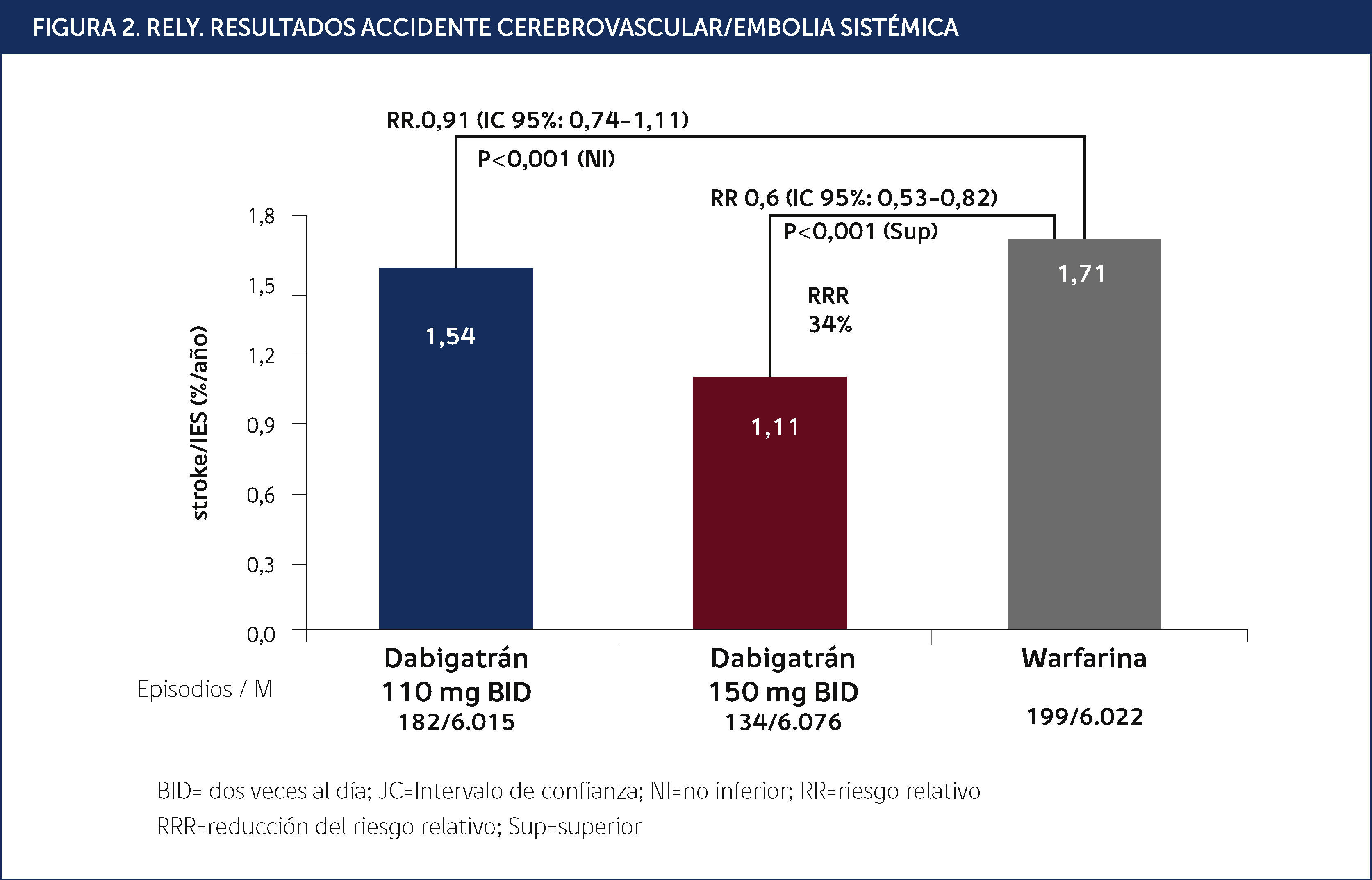
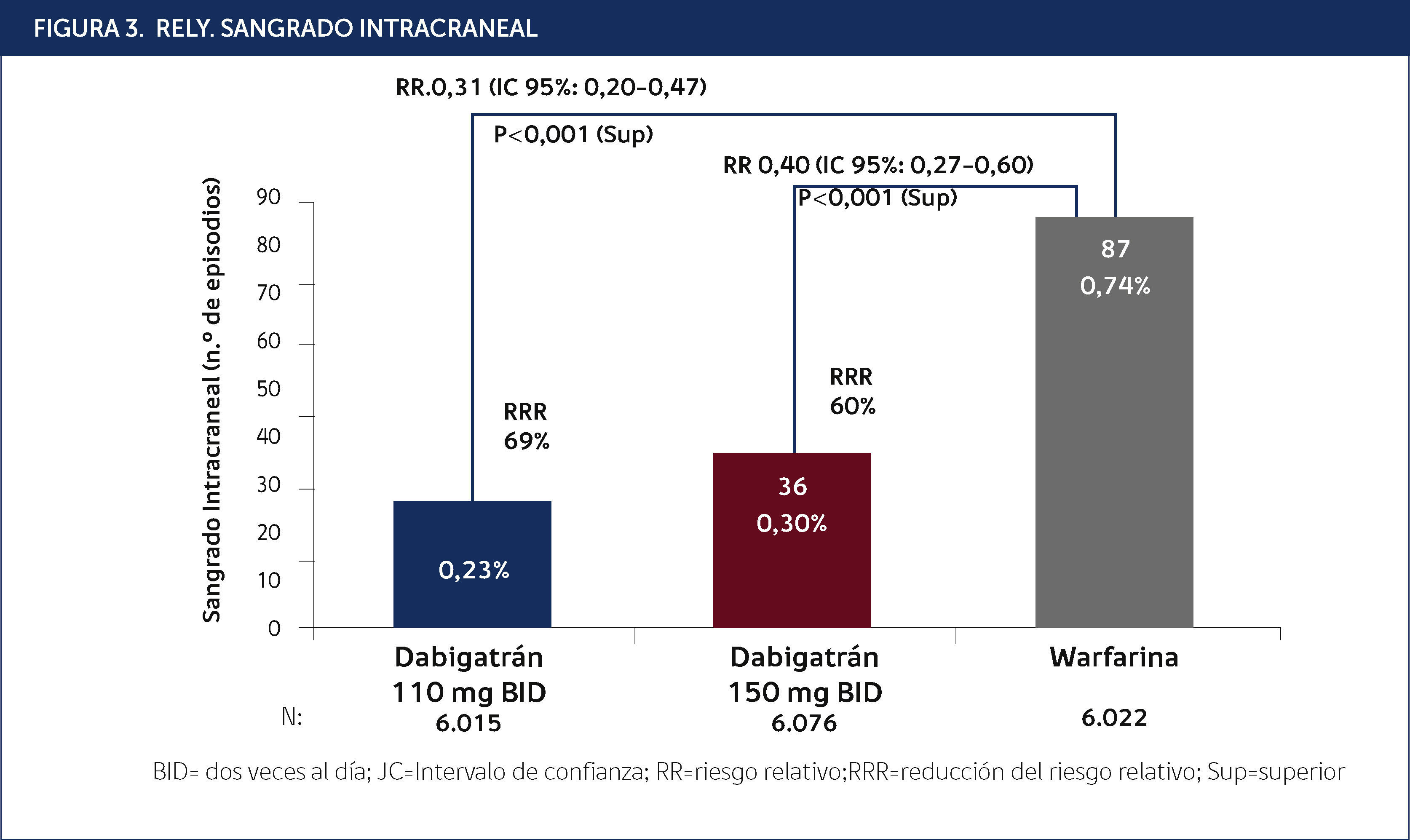
El Estudio RELY18 (Randomised Evaluation of Long term anticoagulant therapy) comparó Dabigatrán versus Warfarina en 18000 pacientes con Fibrilación Auricular no valvular y con 1 o más factores de riesgo, promedio CHADS2 de 2,1 randomizados a 3 ramas de 6000 pacientes cada una: warfarina (INR 2,0•3,0), dabigatrán etexilato 110mg dos veces al día y dabigatrán etexilato 150mg dos veces al día. Se siguieron por dos años en promedio. El objetivo principal del estudio fue establecer la no inferioridad de dabigatran frente a warfarina respecto de eficacia en la incidencia de ACV total (isquéc)mico + hemorrágico) y embolia sistéc)mica y respecto de seguridad con los eventos de hemorragia (mayor y menor). Los resultados de RELY mostraron que dabigatrán 110mg vs. warfarina tuvo tasas comparables de AVE/embolia sistéc)mica, comparado con warfarina, (1,53% vs 1,69%) (p 0,01 para no inferioridad) pero, su perfil de seguridad mostró una reducción estadísticamente significativa del stroke hemorrágico (0,12% vs 0,38% para warfarina (p 0,01), de las tasas de sangrado mayor (2,71 vs 3,36% para warfarina (p = 0,03), sangrados totales, sangrados potencialmente mortales (2,8% versus 3,57% (p=0,03) y sangrados intracraneales comparado con la AVK. La mortalidad fue de 3,75% versus 4,13% para warfarina (p =0,13). Con respecto a la dosis de dabigatrán 150mg vs. warfarina, éc)sta tuvo una reducción estadísticamente significativa del AVE/embolia sistéc)mica (1,11% vs 1,69% para warfarina (p 0,01 para superioridad) del stroke hemorrágico (0,1% vs 0,38% para warfarina (p 0,01) y mortalidad de 3,64% versus 4,13% para warfarina marginalmente significativa(p=0,051). Las tasas de sangrado grave fueron comparables (3,11% versus 3,36% (p = 0,3), sin embargo con el medicamento en estudio se obtuvo una reducción significativa de los sangrados totales, los sangrados potencialmente mortales y los sangrados intracraneales. Dabigatrán no se asoció con anormalidades en la función hepática más frecuente que warfarina, pero causó altas tasas de dispepsia (10%) que limitaron el tratamiento y se asoció con mayor tasa de sangrado gastrointestinal (posiblemente por circulación enterohepática de su metabolito). Los pacientes con dabigatrán tuvieron más infarto al miocardio, pero más que un efecto secundario del fármaco la explicación es que warfarina es mejor en reducir los eventos isquéc)micos coronarios que dabigatrán. El porcentaje promedio de INR en rango terapeútico (TTR) fue 64%.
En resumen este estudio mostró que dabigatrán 110mg dos veces por día produjo menos sangrado con similar eficacia y dabigatrán 150mg dos veces por día mostró eficacia superior con similar sangrado en el tratamiento de la prevención de TE en FA no valvular.
En consideración con esto las dosis menores beneficiarían a pacientes con mayor riesgo de sangrado, obviando la superioridad de la dosis más alta en la prevención de ACV y TE En Europa y Canadá las dosis disponibles son 110 y 150mg y en EE.UU. 150 y 75mg; esta última para pacientes con disfunción renal, pero no ha sido evaluada en trials.
Medición del efecto anticoagulante: Para esta droga no existe un test de laboratorio del efecto anticoagulante, pero se ve que el tiempo de protrombina, el TTPK, el tiempo de trombina (el más sensible) y el tiempo de coagulación con ecarina están prolongados. Actualmente no existe un antídoto probado, aunque los generadores de trombina como el concentrado de factor VII puede ser efectivo, así como su pobre unión a proteína lo hace fácilmente removible con diálisis. Está en estudio el Idarucizumab (BI 655075), anticuerpo para los inhibidores directos de trombina (Figuras 2 y 3).
El Estudio RELY-ABLE19 fue una extensión multicéc)ntrica del tratamiento con dabigatrán en pacientes con FA que completaron el estudio RELY. El objetivo fue estudiar la seguridad a largo plazo de dabigatrán. Fueron 5851 pacientes con un seguimiento de 28 meses. La Tasa de ACV/embolia fue 1,46% con dabigatrán 150mg y 1,6% con dabigatran 110 (HR 0,91). Las tasas de hemorragia mayor fueron 3,74 y 2,99% con dabigatrán 150 y 110 respectivamente (HR 1,26). Las tasas de ACV hemorrágico fueron 0,13 y 0,14% respectivamente y la tasa de mortalidad fue 3,02 y 3,1% (HR 0,97).
RivaroxabanEs un inhibidor directo, específico, competitivo del factor Xa, con una vida media de 5-13 horas, 1/3 se excreta por vía renal directa y 2/3 se metabolizan vía CYP 450. Se administra vía oral, dosis única diaria, sin necesidad de monitorización de la coagulación20,21.
El estudio ROCKET AF22 fue un estudio doble ciego con 14.000 pacientes con FA de alto riesgo con CHADS2 promedio de 3,5 randomizadosa Rivaroxaban 20 mgdía(o 15 mgparaclearance de Creatinina de 30-49ml/min) o a Warfarina con INR 2,5 (2,0-3,0 inclusive) con monitorización mensual. Se siguieron por 1,9 años en promedio. El Endpoint primario fue el ACV o la embolia sistéc)mica. Ambos grupos eran similares, especialmente destaca la proporción de pacientes con FA persistente. 5786 (81,1%) vs 5762 (80,8%), para rivaroxaban versus warfarina y antecedentes de stroke/accidente isquéc)mico transitorio o embolia sistéc)mica en 3916 (54,9%) vs 3895 (54,6%) para rivaroxaban versus warfarina.
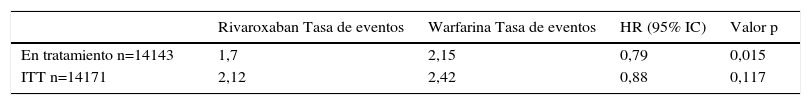
En téc)rminos de eficacia rivaroxaban fue no inferior a warfarina para prevención de stroke y embolia periféc)rica. Además hubo menos casos de stroke hemorrágico/año (0,3% vs 0,4%; p=0,02) respectivamente. La evaluación de seguridad mostró tasas similares de sangrado y eventos adversos, pero con rivaroxaban hubo menos sangrado intracerebral y sangrado fatal. La mortalidad fue de 1,9% versus 2,2% con warfarina (p=0,07). En este estudio el TTR fue 58% (Tablas 6 y 7).
ROCKET AF. RESULTADOS PRIMARIOS DE SEGURIDAD
| Parámetro | Rivaroxaban n=7111% año | Warfarina n=7125% año | HR | Valor p |
|---|---|---|---|---|
| End Point Primario de seguridad | 14,9 | 14,5 | 1,03 | 0,44 |
| Sangrado mayor | 3,6 | 3,4 | 1,04 | 0,58 |
| Tranfusión | 1,6 | 1,3 | 1,25 | 0,04 |
| Sangrado órgano crítico | 0,8 | 1,2 | 0,69 | 0,07 |
| Hemorragia intracraneal | 0,5 | 0,7 | 0,67 | 0,02 |
| Sangrado fatal | 0,2 | 0,5 | 0,5 | 0,003 |
Traducida de Patel MR et al. N Engl J Med 2011; 365:883•891
Es otro anticoagulante inhibidor del factor Xa23-25. Se absorbe rápidamente vía oral, alcanzando concentraciones máximas 3 a 4 horas despuéc)s. Se une a proteínas en un 87%, eliminación renal 27%, y la mayor parte digestiva, vida media de 12 horas.
El estudio AVERROES26 comparó el uso de Apixaban versus Aspirina en pacientes con FA no valvular en 3 ramas: Apixaban 5mg 2 veces al día, Apixaban 2,5mg 2 veces al día y Aspirina 81-324 mgs/día. Se siguieron por 1,1 años en promedio. El objetivo primario de eficacia fue Stroke compuesto (isquéc)mico o hemorrágico) o embolia sistéc)mica. Entre los pacientes con FA, para los que el tratamiento con AVK era inadecuado, o no lo deseaban, apixaban redujo el riesgo de embolia sistéc)mica frente a AAS (1,6% versus 3,7% 8 p 0,01). No aumentó el riesgo de hemorragia mayor (1,4% versus 1,2% (p = 0,57) o hemorragia intracraneal (11 casos versus 13). El estudio fue terminado precozmente por la mayor eficacia de Apixaban.
El estudio ARISTOTLE27,28 comparó Apixaban vs warfarina en pacientes con Fibrilación Auricular y al menos un factor de riesgo. Incluyó 18.000 pacientes con características similares, CHADS2 score promedio de 2.1 (+/- 1.1) en ambos grupos, randomizados a apixaban 5mg oral dos veces al día vs Warfarina (INR 2-3). El end point de eficacia fue Stroke o embolia sistéc)mica y como objetivo primario de seguridad el sangrado mayor (de acuerdo a la definición de la Sociedad Internacional de Trombosis y Hemostasia (ISTH) (baja de 2g de hemoglobina o transfusión de glóbulos gojos).
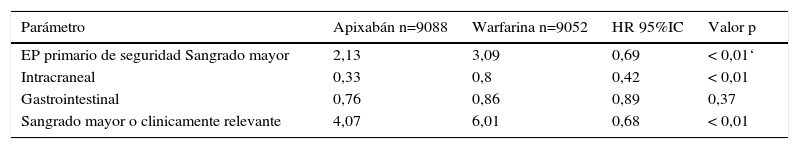
Apixaban comparado con warfarina, en pacientes con FA y al menos un factor adicional de riesgo para ACV, redujo el ACV y la embolia sistéc)mica en 21% (p=0.01), el sangrado mayor en 31% (p 0.001) y la mortalidad en 11% (p=0.047). En relación al sangrado, apixaban tuvo una incidencia significativamente menor, medido por diferentes escalas (GUSTO, TIMI) y localizaciones, excepto en el sangrado de origen gastrointestinal. La tasa de mortalidad total fue de 3,52% versus 3,94% para warfarina (0,047).
Estos resultados concluyen que el apixaban en pacientes con FA es superior a warfarina en prevenir el ACV o embolia, causando menos sangrado y resultando en menor mortalidad (Tablas 8 y 9).
ARISTOTLE TRIAL. END POINT DE EFICACIA
| Evento | Apixaban n=9120 Tasa eventos % año | Warfarina n=9081 Tasa eventos % año | HR (95% IC) | Valor p |
|---|---|---|---|---|
| ACV/Embolia sistéc)mica (ES) | 1,27 | 1,6 | 0,70 | 0,011 |
| ACV | 1,19 | 1,51 | 0,79 | 0,012 |
| ACV isquéc)mico o incierto | 0,97 | 1,05 | 0,92 | 0,42 |
| ACV hemorrágico | 0,24 | 0,47 | 0,51 | < 0,01 |
| Embolia Sistéc)mica | 0,09 | 0,1 | 0,87 | 0,7 |
| Mortalidad total | 3,52 | 3,94 | 0,89 | 0,047 |
| ACV, ES o mortalidad total | 4,49 | 5,04 | 0,89 | 0,019 |
| Infarto Miocardio | 0,53 | 0,61 | 0,88 | 0,37 |
Traducida de Granger C et al. Apixaban versus warfarin in patients with atrial fibrillation. NEJM 2011; 365: 981-992
ARIASTOTLE TRIAL. END POINT DE SEGURIDAD
| Parámetro | Apixabán n=9088 | Warfarina n=9052 | HR 95%IC | Valor p |
|---|---|---|---|---|
| EP primario de seguridad Sangrado mayor | 2,13 | 3,09 | 0,69 | < 0,01‘ |
| Intracraneal | 0,33 | 0,8 | 0,42 | < 0,01 |
| Gastrointestinal | 0,76 | 0,86 | 0,89 | 0,37 |
| Sangrado mayor o clinicamente relevante | 4,07 | 6,01 | 0,68 | < 0,01 |
Traducida de Granger C et al. Apixaban versus warfarin in patients with atrial fibrillation. NEJM 2011; 365: 981-992
Es otro inhibidor del factor Xa29,30.
El estudio ENGAGE AF-TIMI 4831 evaluó Edoxaban versus warfarina en pacientes con fibrilación auricular de moderado a alto riesgo (CHADS2 de2,8). Se randomizaron 21105 pacientes con FA a tres ramas: warfarina para INR de 2-3, edoxaban 30mg/día y edoxaban 60mg/día. Se siguieron por 2,8 años en promedio. Cada réc)gimen de edoxaban fue testeado para no inferioridad del end point primario de ACV/embolia sistéc)mica. El end point de seguridad fue el sangrado mayor. La tasa anual del end point primario fue 1,5% para warfarina, 1,18% para edoxaban alta dosis (p 0,001 para no inferioridad) y 1,61% para edoxaban baja dosis (p = 0,05 para no inferioridad). La tasa de eventos cerebrales isquéc)micos fue similar con dosis de 60mg, pero mayor con dosis de 30mg en comparación con warfarina, aumentando el riesgo en 40%. La tasa de sangrado mayor fue de 3,43% para warfarina, 2,75% con alta dosis de edoxaban (p 0,001) y 1,61 con baja dosis (p 0,001) y las otras tasas de sangrado fueron menores, excepto el gastrointestinal que fue mayor con la dosis alta, pero menor que warfarina con la dosis baja. Las tasas de mortalidad cardiovascular fueron 3,17% para warfarina, versus 2,74% para edoxaban 60mg (p =0,01) y 2,715 para edoxaban 30mg (p= 0,008). En conclusión, ambos regímenes de edoxaban fueron no inferior a warfarina bien manejada (68,4% de INR en rango terapéc)utico) para la prevención del ACV/embolia sistéc)mica. La tasa de ACV fue similar para warfarina y edoxaban 60mg, pero fue más alta con la dosis baja de edoxaban. La incidencia de ACV hemorrágico y la muerte cardiovascular fueron significativamente más bajos con ambas dosis de edoxaban.
En relación a medición de actividad de los inhibidores de factor Xa, permiten una aproximación el TTPK y tiempo de protrombina y el Hep Test, siendo más específico la medición de la actividad anti factor Xa. Existen algunos antídotos específicos para los inhibidores del factor Xa que están en estudio, Andexanet (PRT064445) que es una proteína recombinante que se une al sitio inhibidor del factor Xa y Aripazine (PER977), que es una moléc)cula sintéc)tica pequeña que se une directamente al anticoagulante. Este sería un antídoto para inhibidores del factor Xa, y tambiéc)n de inhibidores directos de trombina y heparinas de bajo peso molecular.
Estos nuevos anticoagulantes están ya en uso clínico pero llevan poco tiempo en el mercado. Es así como RELY apareció en agosto 2009, Dabigatran fue aprobado en EE.UU. en agosto del 2010, AVERROES apareció en febrero del 2011, ROCKET AF en agosto del 2011, Dabigatran fue aprobado en Europa en agosto del 2011, ARISTOTLE apareció en agosto 2011, Apixaban fue aprobado en Europa y EE.UU. en noviembre del 2012, ENGAGE AF publicado en noviembre del 2013, Edoxaban aún no aprobado.
RECOMENDACIONES ACTUALES: GUÍAS CLÍNICASConsiderando la evidencia aportada por estos estudios es que las sociedades científicas han incluido en sus guías para el manejo de la FA recomendaciones sobre la indicación de estos medicamentos.
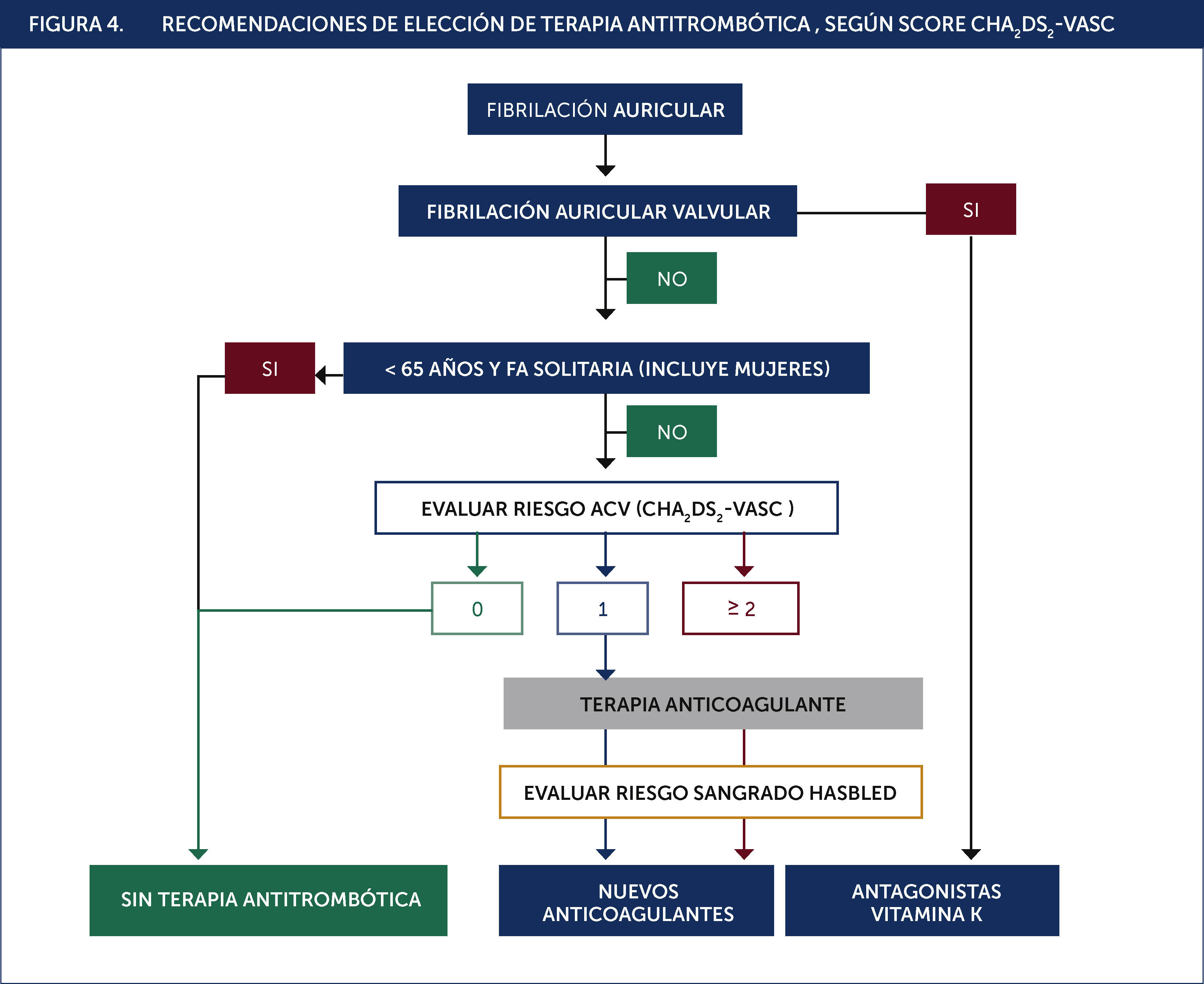
En el año 2012 la Sociedad Europea de Cardiología realizó una actualización de las Guías del año 2010 para manejo de la fibrilación auricular, en que sugiere la utilización del CHA2DS2-VASc en vez de CHADS2 para la estratificación de riesgo de estos pacientes, no usar terapia antitrombótica en CHA2DS2-VASc de 0 y usar terapia antitrombótica con anticoagulante en CHA2DS2-VASc de 1 y más mencionando a los nuevos anticoagulantes como alternativa equivalente a la warfarina32 (Figura 4).
Las Guías canadienses tambiéc)n sugieren el uso de los nuevos anticoagulantes, recomendando preferirlos sobre la warfarina33.
La American Heart Association/Sociedad Americana de Stroke34 recomienda el uso de cualquiera de los nuevos anticoagulantes o warfarina como primera elección para la prevención de tromboembolismo en FA no valvular. En la actualización 2014 para prevención secundaria se recomienda con nivel de evidencia A warfarina y apixaban sobre dabigatrán.
La AHA /ACC/HRS35 publicó en marzo del 2014 las nuevas Guías de Manejo de Fibrilación Auricular, que reemplazan a las del 2006 y actualizaciones del 2011. En ellas hay tres puntos importantes:
- 1)
Recomiendan el uso del score de CHA2DS2-VASc en vez de CHADS2 para la estratificación de riesgo (al igual que los europeos).
- 2)
A diferencia de los europeos para los pacientes con CHA2DS2-VASc de 1 recomiendan nada o Aspirina o terapia anticoagulante.
- 3)
Recomendación directa de uso de cualquiera de los nuevos anticoagulantes o warfarina (Tabla 10).
Tabla 10.ELECCIÓN DE TERAPIA ANTITROMBÓTICA SEGÚN SCORE CHA2DS2-VASc
CHA2DS2-VASc > 2 - Warfarina (A) - Dabigatran (B) - Rivaroxaban (B) - Apixaban (B) CHA2DS2-VASc = 1 - Sin terapia, aspirina o anticoagulante CHA2DS2-VASc = 0 - Sin terapia anticoagulante Traducido de January C, Wann S, Alpert J, Calkin H, ClevelanD J et al. 2014 AHA/ACC,/HRS Guideline for the management of patients with atrial fibrillation. Circulation, 2014; march 28.
En resumen, podemos decir que dabigatran 150mg dos veces al día disminuyó la tasa de ACV, incluyendo el isquéc)mico o no especificado, con una tasa similar de sangrado, aunque la tasa de sangrado gastrointestinal aumentó. La dosis de 110mg dos veces al día tuvo tasa de sangrado similar a warfarina pero con menor tasa de sangrado. Ambas dosis con menos sangrado intracraneal. Rivaroxaban fue no inferior a warfarina para prevenir ACV. Las tasas de hemorragia cerebral y fatal fueron menores, no así las otras. Apixaban mostró menos tasa de eventos y menos sangrado, además disminuyó el sangrado gastrointestinal, con menor tasa de infarto al miocardio y menor mortalidad. Edoxaban fue no inferior a warfarina, con menos tasa de sangrado y muerte cardiovascular.
Si bien todos los pacientes con FA no valvular se beneficiarían del uso de estos nuevos anticoagulante, los pacientes con FA no valvular en tratamiento con warfarina que se mantienen estables son los de baja prioridad en hacer el cambio a nuevos anticoagulantes, especialmente si el costo es una consideración. Sin embargo es importante no olvidar que los nuevos anticoagulantes tienen menor sangrado intracraneal. Existe un grupo sí con mayor beneficio potencial, que serían los pacientes que no estéc)n recibiendo anticoagulantes aún, los pacientes que hayan tenido un sangrado mayor y aquellos que hayan tenido un ACV isquéc)mico estando en terapia anticoagulante con antagonistas de vitamina K en rango terapéc)utico.
Finalmente, los nuevos anticoagulantes han mostrado al menos igual eficacia y mayor seguridad en comparación con warfarina para la prevención de ACV y embolia sistéc)mica en pacientes con FA no valvular. Su efecto predecible y la falta de monitorización rutinaria constituyen una gran ventaja. Hoy en día su uso se extiende cada vez más y habrá que esperar el paso del tiempo para saber si reemplazarán definitivamente a la warfarina.
La autora declara no tener conflictos de interéc)s, en relación a este artículo.