La circulación extracorpórea (CEC) es un componente esencial de la cirugía cardíaca dado que permite mantener soporte vital durante el paro cardíaco inducido necesario para realizar las intervenciones cardioquirúrgicas. Sin embargo, la CEC presenta efectos adversos a nivel local y sistémico debido a que sus componentes producen alteraciones a nivel de la macro y microcirculación, potencialmente llevando a una hipoperfusión. La técnica de perfusión dirigida por objetivos (GDP, por sus siglas en inglés), busca personalizar el manejo hemodinámico según metas predefinidas, optimizando de tal modo la oxigenación y perfusión tisular durante la CEC. Esto implica una monitorización constante de parámetros claves, con la finalidad de realizar cambios en tiempo real de las estrategias de perfusión. Durante los últimos 10 años, se han explorado los beneficios del uso de GDP y, visualizado su superioridad en relación al enfoque tradicional. El objetivo de este artículo es describir la práctica GDP en la monitorización durante la CEC. Nos enfocaremos en las variables ya existentes monitorizadas bajo el concepto de GDP, aplicándolas y manipulándolas para optimizar la perfusión tisular en tiempo real.
Extracorporeal circulation (ECC) is an essential component of cardiac surgery since it allows life support to be maintained during the induced cardiac arrest necessary to perform cardiosurgical interventions. However, CPB presents adverse effects at a local and systemic level because its components produce alterations at the macro- and microcirculation levels, potentially leading to hypoperfusion. The goal-directed perfusion (GDP) technique seeks to personalize hemodynamic management according to predefined goals, thereby optimizing tissue oxygenation and perfusion during CPB. This implies constant monitoring of key parameters, to make real-time changes to perfusion strategies. Over the past 10 years, the benefits of using GDP have been explored and its superiority over the traditional approach visualized. The objective of this article is to describe GDP practice in monitoring during CPB. We will focus on the existing variables monitored under the GDP concept, applying and manipulating them to optimize tissue perfusion in real-time.
La incorporación del bypass cardiopulmonar (BCP) o circulación extracorpórea (CEC) es un hito mayor dentro de la historia de la cirugía cardíaca. La primera cirugía con CEC se realizó en 1953. Los avances y desarrollo de esta técnica en los últimos 20 años han sido cruciales para avanzar en la optimización de dicho soporte, pasando en este periodo de actuar desde la experiencia clínica a la evaluación sistemática de la perfusión tisular.
La técnica de perfusión dirigida por objetivos (GDP, por sus siglas en inglés), busca personalizar el manejo hemodinámico según metas predefinidas, optimizando de tal modo la oxigenación y perfusión tisular durante la CEC. Esto implica una monitorización constante de parámetros claves, con la finalidad de realizar cambios en tiempo real de las estrategias de perfusión. Durante los últimos 10 años, se han explorado los beneficios del uso de GDP visualizándose su superioridad en relación al enfoque tradicional, sustentada principalmente en la experiencia clínica y al gasto cardíaco objetivo relacionado a índice cardíaco indexado1,2.
La CEC es un componente esencial de la cirugía cardíaca dado que permite mantener soporte vital durante la parada cardíaca electromecánica (paro cardíaco inducido) necesaria para realizar las intervenciones cardioquirúrgicas. Sin embargo, la CEC presenta efectos adversos a nivel local y sistémico debido a que sus componentes producen alteraciones a nivel de la macro y microcirculación, potencialmente llevando a una hipoperfusión3.
La GDP intenta mantener una perfusión óptima, en tiempo real, para disminuir el riesgo de una inadecuada perfusión tisular y alteraciones fisiológicas, que pudiesen llevar a efectos deletéreos tales como acidosis metabólica, hiperlactatemia, e isquemia de órganos1,2,4. Para lograr disminuir este impacto, la GDP identifica, cuantifica e interviene in situ los elementos que definen las variables fisiológicas tales como aporte de oxígeno (DO2), consumo de oxígeno (VO2) y extracción de oxígeno (ERO2)2–5.
Los inicios de la GDP se remontan a las décadas de 1970 y 1980, cuando los cirujanos y perfusionistas comenzaron a vislumbrar la importancia de mantener una perfusión adecuada durante la CEC1. En este periodo se enfatizaba la importancia de mantener la presión arterial y el flujo sanguíneo dentro de ciertos rangos para prevenir el daño de órganos y el síndrome de bajo gasto cardíaco (SBGC)2 (tabla 1), siendo estos dos parámetros los monitorizados en forma continua, sin evaluación final a nivel de microperfusión. A medida que avanzó la tecnología médica, y ya en la década de 1990, se marcó un paso importante en la monitorización y el ajuste de la perfusión: surgieron sistemas más sofisticados de monitoreo hemodinámico, con medición de multiparámetros en línea durante la CEC (actuales sistemas de monitorización en línea como Spectrum Medical Quantum M4, CDI 500, monitor GDP con SoftwareConnect, Landing, entre otros) que permitieron una evaluación dinámica, precisa y en tiempo real de los parámetros fisiológicos. Esta monitorización permitía ajustar la perfusión de manera individualizada para prevenir y/o responder a cambios en el medio interno, en miras a mantener la homeostasis6.
Parámetros CEC tradicionales vs. GDP2
| Parámetros globales actuales | Parámetros integrados (GDP) |
|---|---|
| SvO2>60–70% PAM≥65mmHg | Índice de suministro de oxígeno (DO2i; ≥ 260–272ml/min/m2) |
| PVO2>40mmHg | Índice de consumo de oxígeno (VO2; <60ml/min/m2) |
| pH: 7,35–7,45 | Índice de producción de dióxido de carbono (VCO2i; <60 ml/min/m2) |
| pCO2: 35–45mmHg | DO2i / VCO2i (>5) |
| Índice cardíaco: 2,2–2,6l/min/m2 | VO2i / DO2i (ERO2; <0,25) |
| Ácido láctico <2,0mmol/l | VCO2i / VO2i (cociente respiratorio; <1) |
El rol de la monitorización para actuar a tiempo en el manejo de estos pacientes es crucial, ya que el shock y el SBGC son condiciones potencialmente mortales. Se caracterizan por una insuficiencia del suministro de oxígeno (DO2) para el consumo de oxígeno (VO2), lo que conduciría a disfunción celular y falla de órganos5,7.
Una reducción del DO2 conducirá primero a un aumento en la proporción de la extracción de oxígeno (ERO2) para mantener estable el aporte de O2 a los tejidos. Como resultado, la saturación venosa central de oxígeno (SvcO2) disminuirá proporcionalmente a la reducción de DO2. La SvcO2 ofrece una imagen global del estado de extracción de oxígeno del paciente5,8. El papel de la SvcO2 como marcador, tanto del deterioro hemodinámico como de la respuesta clínica a los tratamientos, se ha estudiado ampliamente en pacientes adultos en Unidad de Cuidados Intensivos (UCI), siendo uno de los marcadores analizados durante la reanimación de un paciente y durante el bypass cardiopulmonar. En cirugía cardíaca, niveles de SvcO2 bajos se han asociado con deterioro hemodinámico progresivo y resultados clínicos desfavorables. Así también, y al igual que en otros pacientes críticos, el nivel de lactato sérico nos aporta información de una perfusión tisular inadecuada, dado que es uno de los marcadores más importantes de déficit de entrega de O2 y de inicio de metabolismo anaeróbico y eventual muerte celular9.
Por otra parte, los parámetros derivados de la producción de CO2 y su comportamiento como el delta CO2 (diferencia de CO2 venoso central y arterial, o ΔpCO2), son parámetros a seguir para posteriormente intervenir, dado que también muestran la perfusión de la microcirculación4,10.
Basados en estos fenómenos, la GDP toma los términos “convencionales” de perfusión óptima en CEC y agrega conceptos de microcirculación y perfusión/respiración celular. Durante la CEC, estos se “indexan”: Índice de suministro o aporte de oxígeno (DO2i), índice de consumo de oxígeno (VO2i), índice de producción de dióxido de carbono (VCO2i) y tasa de extracción de O2 (ERO2 o VO2/DO2). La importancia de supervisar y controlar estos valores, radica en las potenciales intervenciones derivadas del análisis de estos parámetros, con el fin de alcanzar una homeostasia del medio interno (Tabla 2)1,2,8.
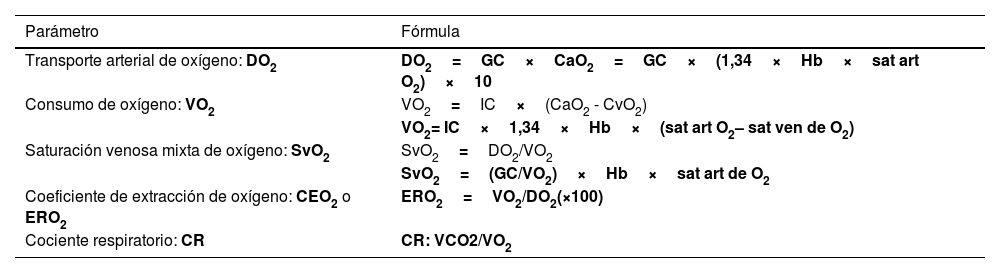
Convención de parámetros
| Parámetro | Fórmula |
|---|---|
| Transporte arterial de oxígeno: DO2 | DO2=GC×CaO2=GC×(1,34×Hb×sat art O2)×10 |
| Consumo de oxígeno: VO2 | VO2=IC×(CaO2 - CvO2) |
| VO2= IC×1,34×Hb×(sat art O2– sat ven de O2) | |
| Saturación venosa mixta de oxígeno: SvO2 | SvO2=DO2/VO2 |
| SvO2=(GC/VO2)×Hb×sat art de O2 | |
| Coeficiente de extracción de oxígeno: CEO2 o ERO2 | ERO2=VO2/DO2(×100) |
| Cociente respiratorio: CR | CR: VCO2/VO2 |
GC: gasto cardíaco; Hb: hemoglobina; IC: índice cardíaco; sat art: saturación arterial; sat ven: saturación venosa.
Por ejemplo, Ranucci, en revisiones del 2006 al 2015, se dedicó a explorar una serie de parámetros derivados del consumo de oxígeno y de la producción de CO2 y su asociación en la elevación del ácido láctico en CEC. Concluyó que los elementos que pronostican hiperlactatemia durante el bypass cardiopulmonar son una producción de CO2 (VCO2)>60ml/min/m2 y una relación DO2i/VCO2i<5:18,11,12. Además, con un estudio retrospectivo del 2011 (serie pequeña de 36 pacientes) Ranucci sostiene que las variables derivadas del oxígeno, saturación venosa de O2 (SvO2) y la tasa de extracción de oxígeno (ERO2) son mejores predictores que el valor de la hemoglobina a la hora de decidir la transfusión de glóbulos rojos durante la CEC8.
Estas observaciones son uno de los motivos principales que llevan a monitorizar lo referido, ya que permite tomar decisiones sobre que variables manipular para optimizar la perfusión durante la CEC.
La mayoría de los estudios publicados sobre GDP están relacionados con la lesión renal aguda9,13,14. Entre el 1% y 3% de los pacientes presenta insuficiencia renal aguda secundaria a CEC por inadecuado transporte15.
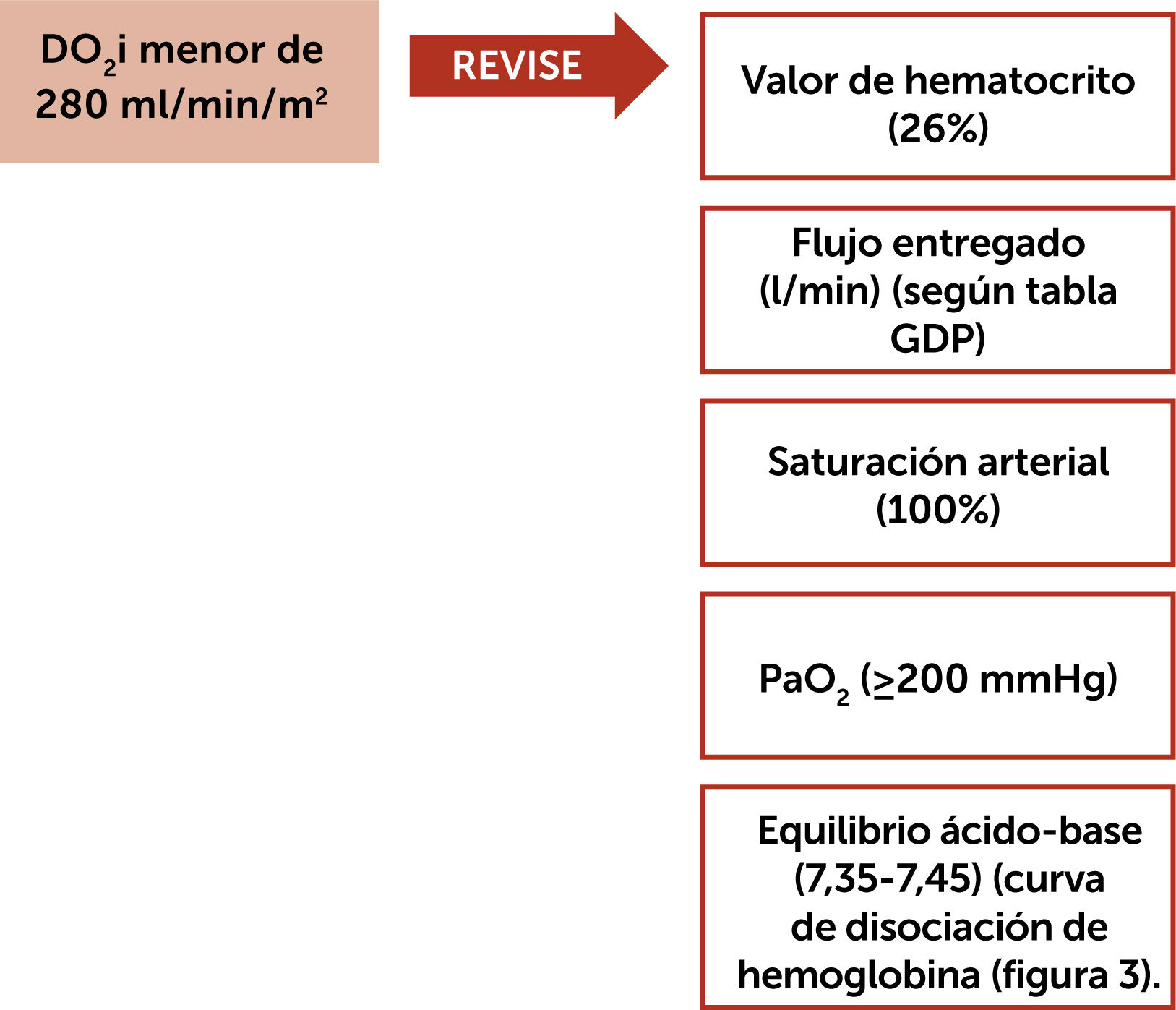
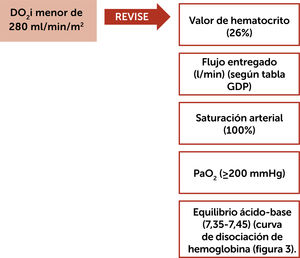
En otra serie pequeña del 2018, Ranucci demostró que la hemodilución durante la CEC y la injuria renal aguda (AKI, por su sigla en inglés) están relacionadas. Por cada disminución de 1% de hematocrito por debajo del 26%, la tasa de AKI aumentaba un 7%. Este estudio demostró que un hematocrito por debajo del 24% compromete el aporte de oxígeno al riñón, por lo tanto, el flujo de la bomba debe adaptarse al valor del hematocrito para mantener el suministro de O2 por encima del valor crítico descrito (260-272ml/min/m2) y no debe calcularse por superficie corporal y temperatura2,14. En relación a esto Ranucci y sus asociados en el ensayo Goal-Directed Perfusión Trial (GIFT)7 desarrollaron una herramienta de referencia (la cuál considera durante la CEC una PaO2 de ≥ 200mmHg y saturación de O2 de 100% (figura 1).
Fórmula de flujo sanguíneo. Modificado de Srey et al.7.
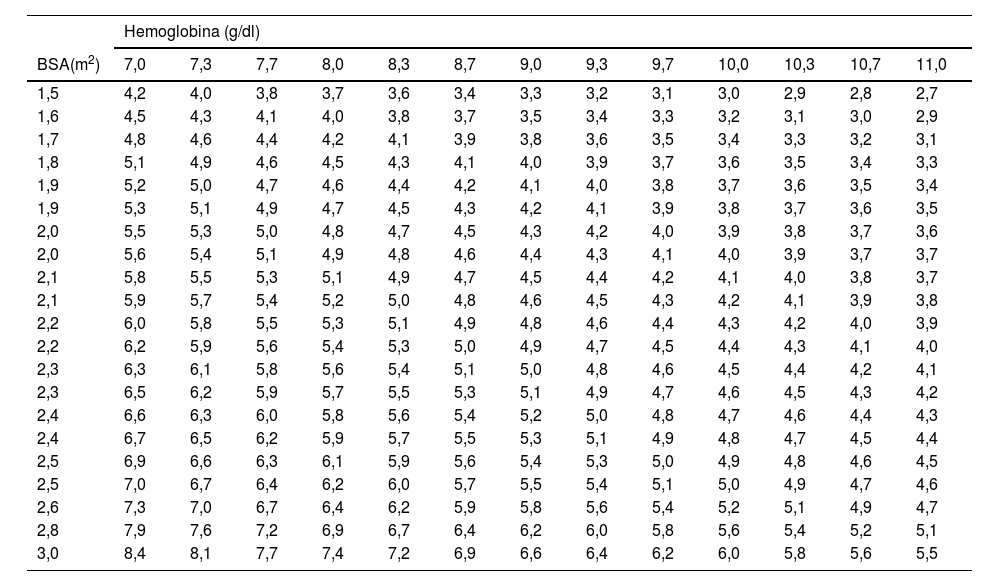
Esta herramienta permite determinar rápidamente el límite inferior del débito a proporcionar a un paciente de cualquier superficie corporal y asegurar un DO2 satisfactorio, permitiendo que cualquier centro de cirugía cardíaca adopte la técnica GDP, incluso en ausencia de monitoreo instantáneo de DO2 (Tabla 3).
Veterans Affairs Boston Healthcare System, guía de referencia rápida para uso en GDP
| Hemoglobina (g/dl) | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| BSA(m2) | 7,0 | 7,3 | 7,7 | 8,0 | 8,3 | 8,7 | 9,0 | 9,3 | 9,7 | 10,0 | 10,3 | 10,7 | 11,0 |
| 1,5 | 4,2 | 4,0 | 3,8 | 3,7 | 3,6 | 3,4 | 3,3 | 3,2 | 3,1 | 3,0 | 2,9 | 2,8 | 2,7 |
| 1,6 | 4,5 | 4,3 | 4,1 | 4,0 | 3,8 | 3,7 | 3,5 | 3,4 | 3,3 | 3,2 | 3,1 | 3,0 | 2,9 |
| 1,7 | 4,8 | 4,6 | 4,4 | 4,2 | 4,1 | 3,9 | 3,8 | 3,6 | 3,5 | 3,4 | 3,3 | 3,2 | 3,1 |
| 1,8 | 5,1 | 4,9 | 4,6 | 4,5 | 4,3 | 4,1 | 4,0 | 3,9 | 3,7 | 3,6 | 3,5 | 3,4 | 3,3 |
| 1,9 | 5,2 | 5,0 | 4,7 | 4,6 | 4,4 | 4,2 | 4,1 | 4,0 | 3,8 | 3,7 | 3,6 | 3,5 | 3,4 |
| 1,9 | 5,3 | 5,1 | 4,9 | 4,7 | 4,5 | 4,3 | 4,2 | 4,1 | 3,9 | 3,8 | 3,7 | 3,6 | 3,5 |
| 2,0 | 5,5 | 5,3 | 5,0 | 4,8 | 4,7 | 4,5 | 4,3 | 4,2 | 4,0 | 3,9 | 3,8 | 3,7 | 3,6 |
| 2,0 | 5,6 | 5,4 | 5,1 | 4,9 | 4,8 | 4,6 | 4,4 | 4,3 | 4,1 | 4,0 | 3,9 | 3,7 | 3,7 |
| 2,1 | 5,8 | 5,5 | 5,3 | 5,1 | 4,9 | 4,7 | 4,5 | 4,4 | 4,2 | 4,1 | 4,0 | 3,8 | 3,7 |
| 2,1 | 5,9 | 5,7 | 5,4 | 5,2 | 5,0 | 4,8 | 4,6 | 4,5 | 4,3 | 4,2 | 4,1 | 3,9 | 3,8 |
| 2,2 | 6,0 | 5,8 | 5,5 | 5,3 | 5,1 | 4,9 | 4,8 | 4,6 | 4,4 | 4,3 | 4,2 | 4,0 | 3,9 |
| 2,2 | 6,2 | 5,9 | 5,6 | 5,4 | 5,3 | 5,0 | 4,9 | 4,7 | 4,5 | 4,4 | 4,3 | 4,1 | 4,0 |
| 2,3 | 6,3 | 6,1 | 5,8 | 5,6 | 5,4 | 5,1 | 5,0 | 4,8 | 4,6 | 4,5 | 4,4 | 4,2 | 4,1 |
| 2,3 | 6,5 | 6,2 | 5,9 | 5,7 | 5,5 | 5,3 | 5,1 | 4,9 | 4,7 | 4,6 | 4,5 | 4,3 | 4,2 |
| 2,4 | 6,6 | 6,3 | 6,0 | 5,8 | 5,6 | 5,4 | 5,2 | 5,0 | 4,8 | 4,7 | 4,6 | 4,4 | 4,3 |
| 2,4 | 6,7 | 6,5 | 6,2 | 5,9 | 5,7 | 5,5 | 5,3 | 5,1 | 4,9 | 4,8 | 4,7 | 4,5 | 4,4 |
| 2,5 | 6,9 | 6,6 | 6,3 | 6,1 | 5,9 | 5,6 | 5,4 | 5,3 | 5,0 | 4,9 | 4,8 | 4,6 | 4,5 |
| 2,5 | 7,0 | 6,7 | 6,4 | 6,2 | 6,0 | 5,7 | 5,5 | 5,4 | 5,1 | 5,0 | 4,9 | 4,7 | 4,6 |
| 2,6 | 7,3 | 7,0 | 6,7 | 6,4 | 6,2 | 5,9 | 5,8 | 5,6 | 5,4 | 5,2 | 5,1 | 4,9 | 4,7 |
| 2,8 | 7,9 | 7,6 | 7,2 | 6,9 | 6,7 | 6,4 | 6,2 | 6,0 | 5,8 | 5,6 | 5,4 | 5,2 | 5,1 |
| 3,0 | 8,4 | 8,1 | 7,7 | 7,4 | 7,2 | 6,9 | 6,6 | 6,4 | 6,2 | 6,0 | 5,8 | 5,6 | 5,5 |
El flujo que se muestra (l/min) para una superficie de área corporal (BSA, por sus siglas en inglés) y hemoglobina determinadas es el mínimo requerido para lograr una DO2i de 280 ml/min/m2. Todos los valores asumen saturacion de 100% y una PaO2 de 200mmHg. Srey et al7.
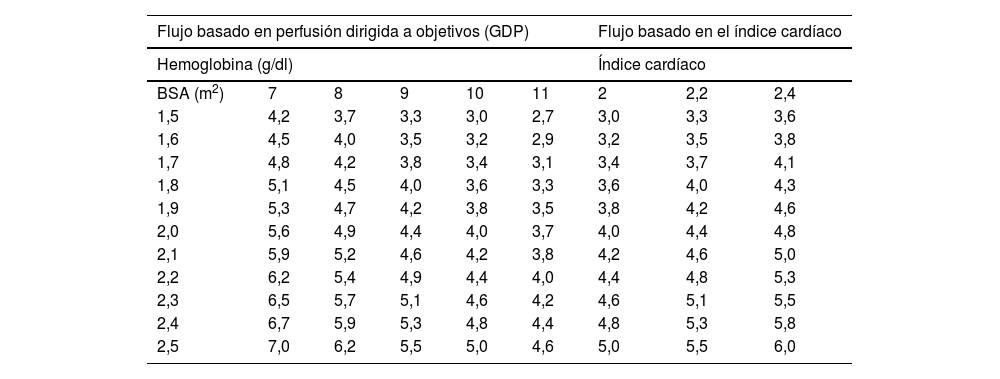
Los estudios han demostrado que los flujos sanguíneos en la CEC que no proporcionan un DO2 adecuados darán lugar a un mayor riesgo de lesión renal aguda e hiperlactatemia. Una comparación directa del flujo basado en el GDP con el flujo basado en el índice cardíaco muestra que los índices cardíacos comúnmente utilizados a menudo subestiman el flujo requerido para lograr un DO2 i de 280ml/min/m2 (tabla 4).
Comparación de flujo requerido (l/min) para determinar en GDP versus el flujo requerido basado en el tradicional índice cardíaco para pacientes con la misma superficie corporal
| Flujo basado en perfusión dirigida a objetivos (GDP) | Flujo basado en el índice cardíaco | |||||||
|---|---|---|---|---|---|---|---|---|
| Hemoglobina (g/dl) | Índice cardíaco | |||||||
| BSA (m2) | 7 | 8 | 9 | 10 | 11 | 2 | 2,2 | 2,4 |
| 1,5 | 4,2 | 3,7 | 3,3 | 3,0 | 2,7 | 3,0 | 3,3 | 3,6 |
| 1,6 | 4,5 | 4,0 | 3,5 | 3,2 | 2,9 | 3,2 | 3,5 | 3,8 |
| 1,7 | 4,8 | 4,2 | 3,8 | 3,4 | 3,1 | 3,4 | 3,7 | 4,1 |
| 1,8 | 5,1 | 4,5 | 4,0 | 3,6 | 3,3 | 3,6 | 4,0 | 4,3 |
| 1,9 | 5,3 | 4,7 | 4,2 | 3,8 | 3,5 | 3,8 | 4,2 | 4,6 |
| 2,0 | 5,6 | 4,9 | 4,4 | 4,0 | 3,7 | 4,0 | 4,4 | 4,8 |
| 2,1 | 5,9 | 5,2 | 4,6 | 4,2 | 3,8 | 4,2 | 4,6 | 5,0 |
| 2,2 | 6,2 | 5,4 | 4,9 | 4,4 | 4,0 | 4,4 | 4,8 | 5,3 |
| 2,3 | 6,5 | 5,7 | 5,1 | 4,6 | 4,2 | 4,6 | 5,1 | 5,5 |
| 2,4 | 6,7 | 5,9 | 5,3 | 4,8 | 4,4 | 4,8 | 5,3 | 5,8 |
| 2,5 | 7,0 | 6,2 | 5,5 | 5,0 | 4,6 | 5,0 | 5,5 | 6,0 |
BSA: superficie de área corporal. Srey et al.7.
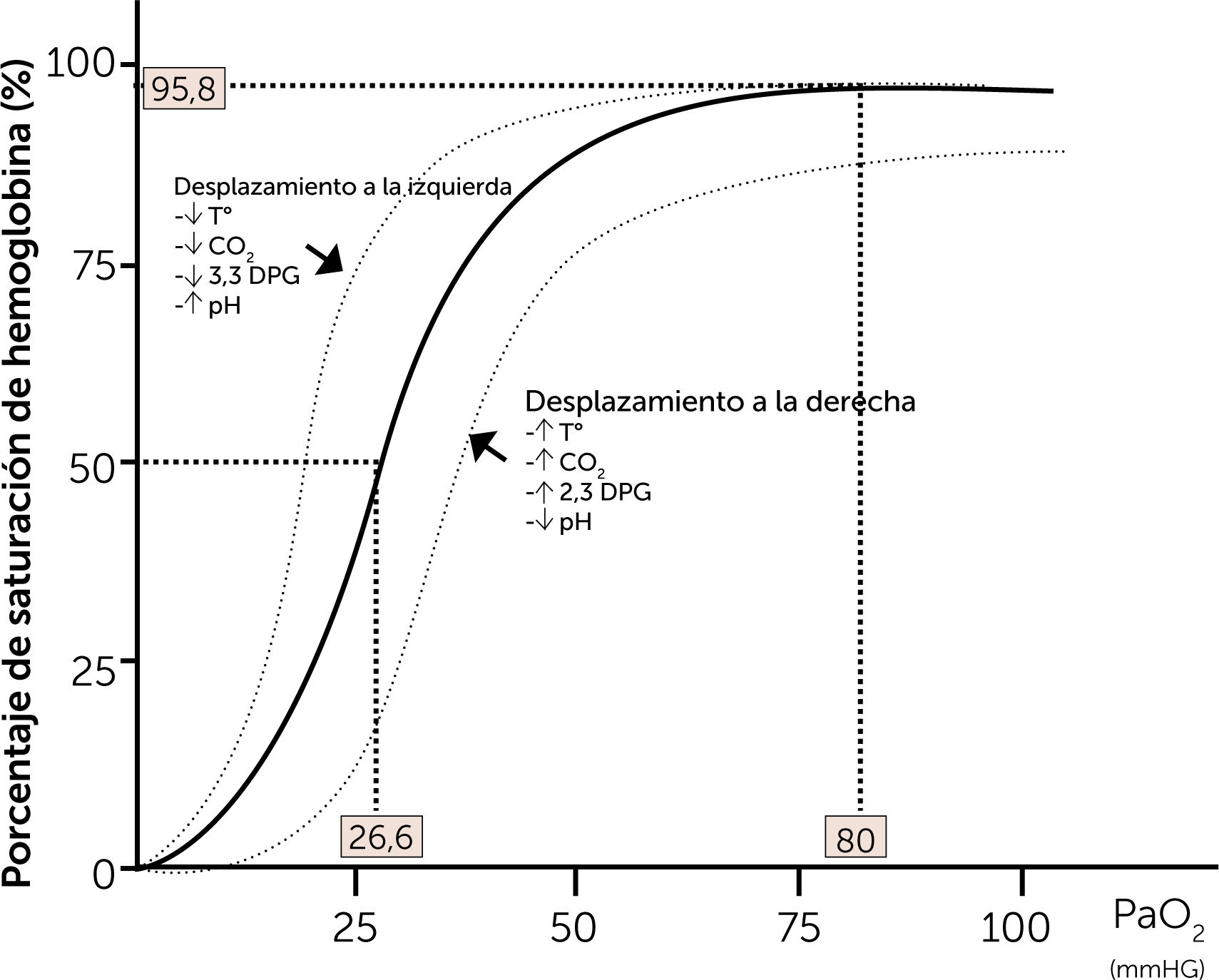
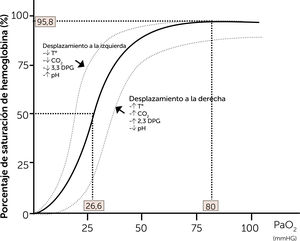
Durante la CEC se intervienen las variables ya descritas: hematocrito, equilibrio ácido-base, temperatura, aporte de O2, producción de CO2, flujo sanguíneo (l/min), que influirán en la entrega de oxígeno del paciente. La manipulación en cualquiera de estas variables debe estar dirigida a mantener un equilibrio del medio interno, para mantener constante el DO2 en 280ml/min/m2 y asegurar la perfusión optima en tiempo real (figuras 2 y 3).
Curva de disociación de la hemoglobina5.
En los últimos 10 años la técnica de GDP ha alcanzado avances significativos, demostrando su capacidad para obtener mejores resultados clínicos al optimizar la microperfusión durante la CEC. Los estudios descritos han demostrado consistentemente los beneficios de perfeccionar la perfusión durante el bypass cardiopulmonar, lo que nos ha llevado a una franca disminución de complicaciones y así, a mejores resultados. Sin embargo, la aplicación de GDP no está exenta de desafíos, ya que su implementación exitosa requiere una colaboración estrecha entre el equipo de cirujanos, anestesiólogos y perfusionistas para la recopilación y análisis de datos en tiempo real a través de sistemas de monitoreo avanzado y personal capacitado para interpretarlos1,3,16.
Aunque GDP muestre resultados prometedores, la falta de estandarización en los criterios de “perfusión óptima” es un desafío persistente. La variabilidad en la definición de objetivos y parámetros puede dificultar la comparación entre estudios y limitar la aplicabilidad clínica generalizada, por lo que se hace necesario establecer criterios de evaluación uniformes y realizar investigaciones sólidas para validar los beneficios clínicos de GDP.
Declaración de conflicto de interésLos autores declaran no tener conflictos de intereses