¿ Introducción
La incidencia del LNH se estima puede variar entre diez y doce veces, de acuerdo al país de que se trate. Así, se pueden documentar tasas de 1.6 a 17.1 por cada 100 000 personas por año entre la población masculina, y de 0.7 a 11.7 casos por 100 000 habitantes por año entre las mujeres.1 La incidencia estimada de LNH se ha incrementado a lo largo del tiempo en diferentes países en función de, género, edades y grupos étnicos. Las tasas de incremento en las décadas de los ochenta y noventa, se atribuyeron en parte a las mejoras de las técnicas diagnósticas, cambios en la clasificación de la enfermedad (nuevas entidades reconocidas como LNH y patología previamente catalogada como enfermedad de Hodgkin clasificada actualmente, como LNH), el incremento en el número de trasplantes de órganos sólidos y células progenitoras hematopoyéticas y la epidemia de SIDA.2 Con base en el registro de la Organización Mundial de la Salud (OMS) Globocan 2002, la tasa de incidencia de LNH en hombres a nivel mundial fue de 5.6 y la de mortalidad de 3.2.3 En una revisión del año 2000 al 2005 en el Hospital General de México, los LNH ocuparon el primer sitio de las neoplasias diagnosticadas en el servicio de Hematología, con un total de 616; que corresponde a 32.5% del total y a 82.6% de todos los linfomas. Se dio un promedio de 102.6 casos nuevos por año, con edades en el rango de 15 a 87 años, con una mediana de 48. En relación a la variedad histológica, el linfoma difuso de células grandes (LDCG) fue el más frecuente de los LNH (62.9%), seguido por el de linfocitos pequeños (4%) y los anaplásicos, T periféricos y foliculares (2% cada uno). El grupo de edad más afectado fue el de 70 años y mayores, el de menor incidencia el de 25 a 29 años.4
El tratamiento de primera línea actual para los linfomas más frecuentes (difusos de células grandes B), es el esquema CHOP-R (ciclofosfamida, vincristina, doxorrubicina, prednisona y rituximab).5-7 La tasa de respuesta completa con CHOP oscila entre 64% y 71% y la de respuesta parcial entre 21% y 36%.8,9 La supervivencia general con CHOP a tres años es de 50% a 65%6,8-10 y la supervivencia libre de evento, de 59% a tres años.6,7 En cuanto a los esquemas de segunda línea de tratamiento, hay diferencias en cuanto a los fármacos empleados, intensidad del tratamiento y costos.7,8 Con ellos la tasa de respuesta completa va de 22% a 53% y la parcial de 21% a 32%11-14 la supervivencia general a tres años presenta rangos de 25% a 31%, a cinco años alrededor de 30%12,15 y la supervivencia libre de evento a tres años con un esquema es de 26%.13
Ante el panorama expuesto, los objetivos de este estudio fue determinar la respuesta, la supervivencia general y la supervivencia libre de evento (progresión, recaída, muerte o última visita) asociadas a la aplicación de los esquemas de primera línea CHOP y de segunda línea DEP en pacientes con LNH en el HGM de 1992 a 2009, en enfermos quienes hubiesen completado el tratamiento.
¿ Métodos
Corresponde a un estudio de cohorte basado en el seguimiento de pacientes con diagnóstico de LNH que se encuentran en el archivo clínico del servicio de Hematología (unidad 103) del Hospital General de México. El periodo estudiado comprendió entre enero de 1992 a mayo de 2009.
Pacientes:
Criterios de inclusión: Enfermos con diagnóstico de LNH corroborado por medio de estudio histopatológico de una muestra obtenida por biopsia incisional revisada en el servicio de Patología del HGM; Mayores de 16 años; quienes hubieran completado el tratamiento con quimioterapia, incluidos de primera y segunda línea; y aquellos en los que se hubiera determinado la respuesta de acuerdo a International Workshop Criteria (IWC) 1999*. (*Para valorar el objetivo primario se toman en cuenta tratamientos completos para CHOP, los que incluyeran seis ciclos para estadios clínicos I a II y ocho ciclos para aquellos que tuvieran estadios III o IV; y para DEP cuatro ciclos).
Criterios de exclusión: Enfermos no diagnosticados por el servicio de Patología del HGM; y quienes hubiesen recibido tratamiento en otras unidades médicas.
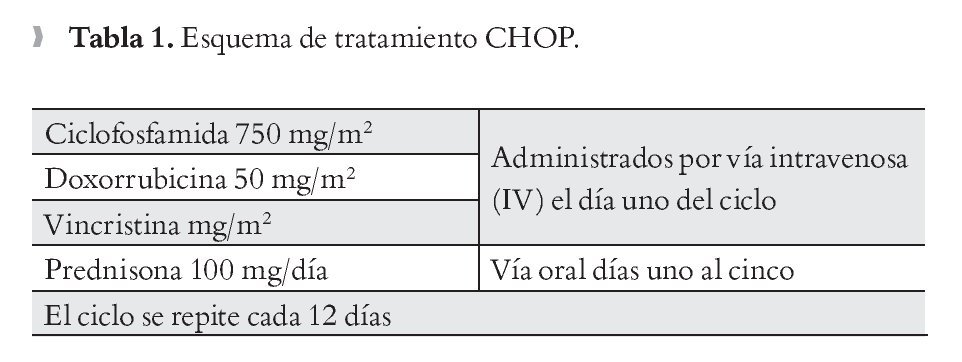
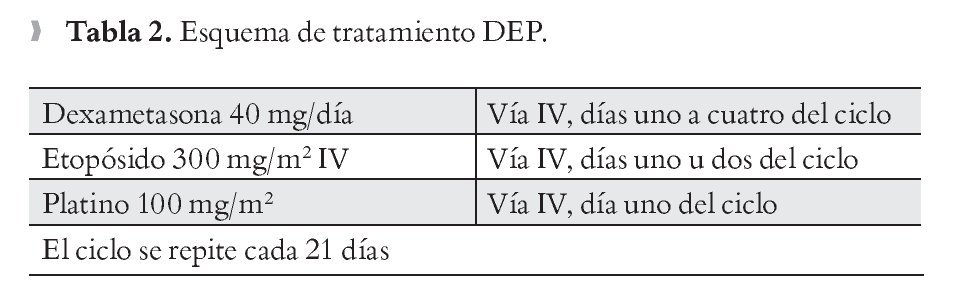
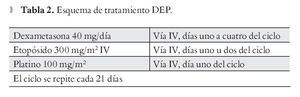
Esquemas de tratamiento: CHOP (Tabla 1), y DEP (Tabla 2).
Método estadístico: Se utilizó el software SPSS versión 17 para efectuar el análisis estadístico. Se utilizaron las medidas de tendencia central media y mediana; además de las pruebas Ji cuadrada y curvas de supervivencia de Kaplan Meier.
¿ Resultados
Se incluyó a 632 pacientes con el diagnóstico de LNH, los cuales tuvieron una media de edad de 52 años, con rango de 16 a 95. En cuanto al género, la relación hombre: mujer (H:M) fue de 1:1/1. La mayor parte de los linfomas correspondieron linfomas de células B, predominando el linfoma difuso de células grandes, seguido de linfomas indolentes. En el caso de linfomas de células T, los más frecuentes fueron: de células T periféricas y de células NK/T extranodal, de tipo nasal.
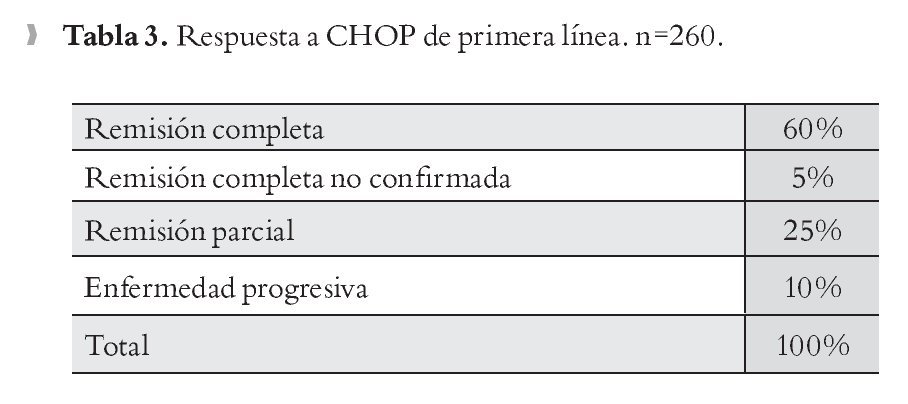
Tratamiento con CHOP de primera línea: Tras la quimioterapia de primera línea con CHOP, la mayor parte de las respuestas fueron completas (Tabla 3).
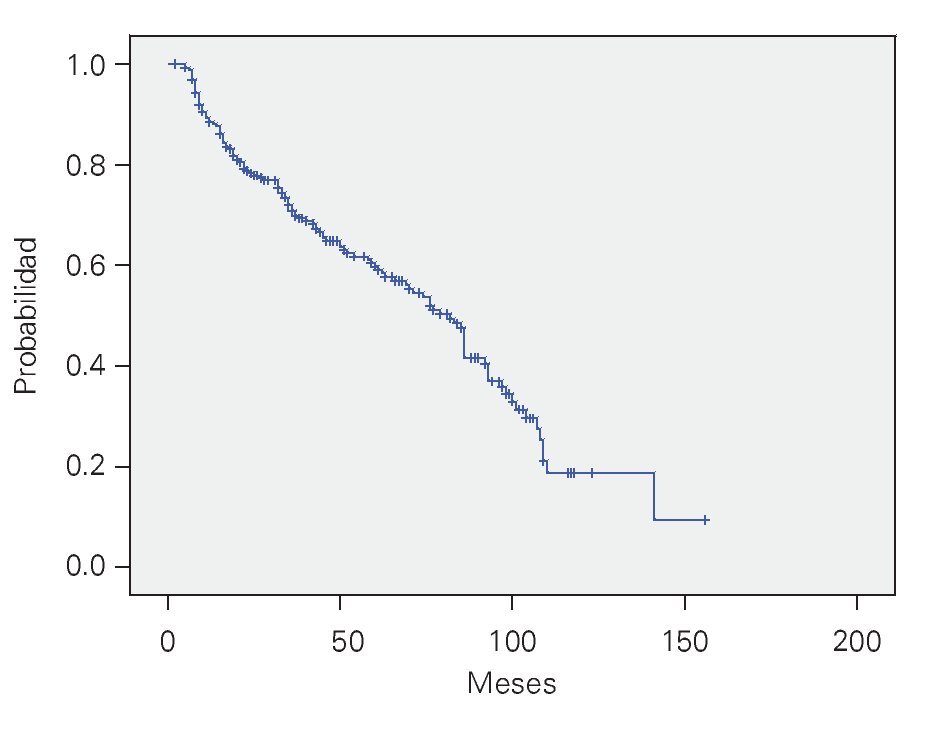
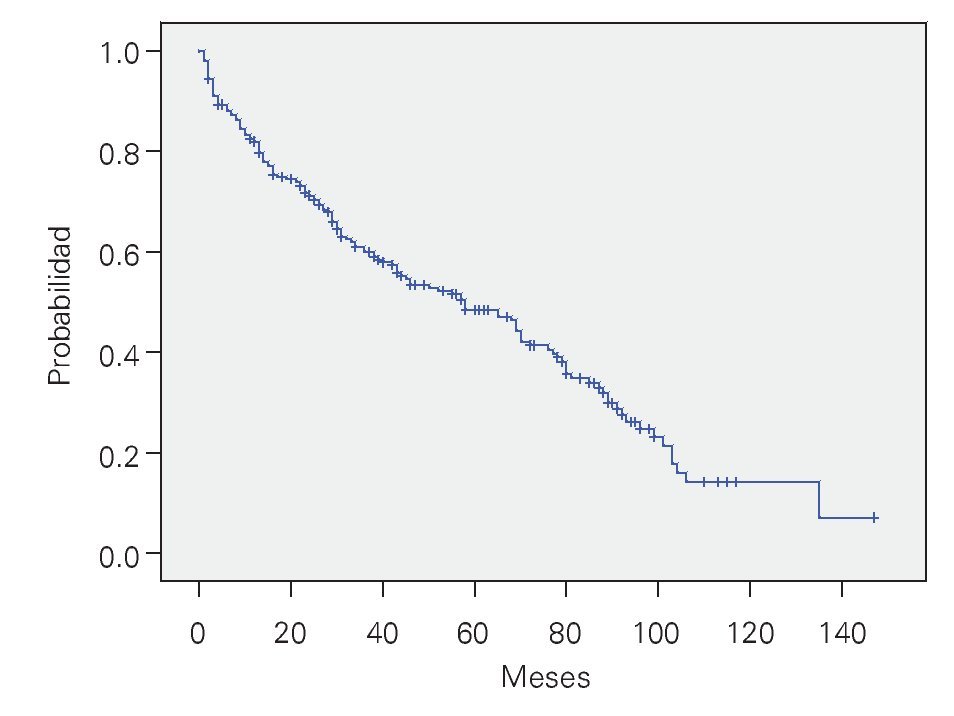
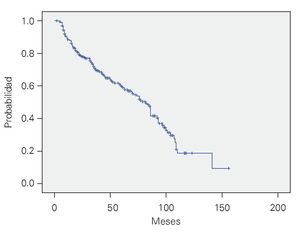
CHOP, supervivencia general (SG): Sólo 260 enfermos terminaron los ciclos planeados de quimioterapia. La SG fue de 66% a 36 meses y de 56% a 60 meses, con una mediana de 73 meses (Figura 1).
¿ Figura 1. Supervivencia general con CHOP. n = 260.
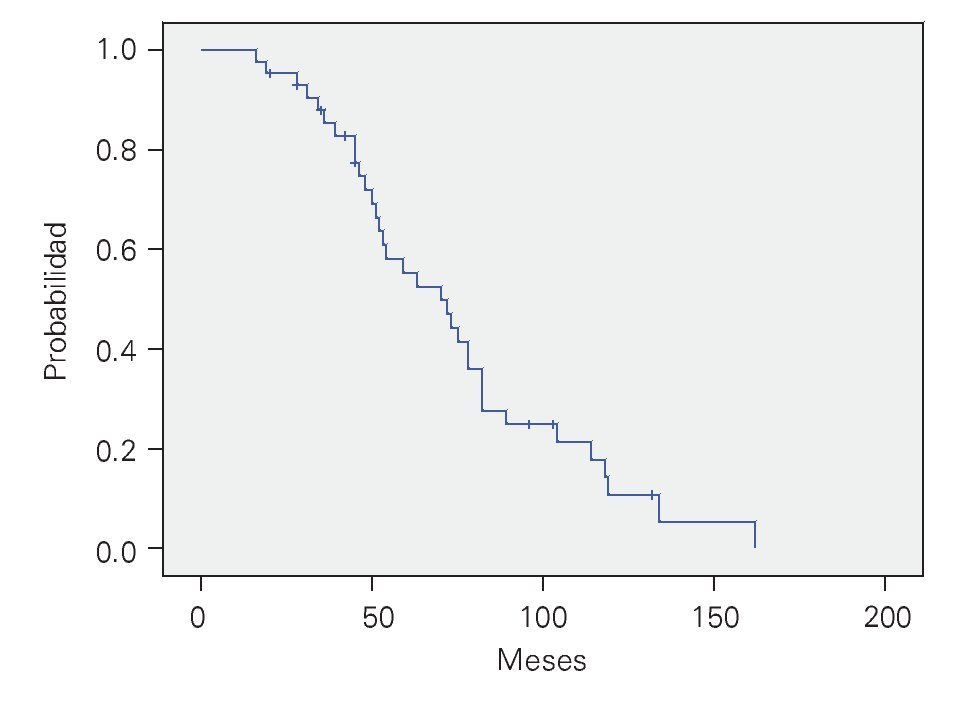
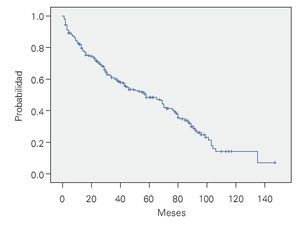
CHOP, supervivencia libre de evento (SLE): Se valoraron 260 enfermos, los cuales presentaron SLE de 59% y 46% a 36 y 60 meses, respectivamente, con mediana de 57 meses (Figura 2).
¿ Figura 2. Supervivencia libre de evento con CHOP. n = 234.
DEP de segunda línea: Casi la mitad de los pacientes, a pesar de que DEP es un tratamiento de segunda línea presentaron remisiones completas. Sin embargo, una quinta parte de los enfermos tuvieron enfermedad progresiva (Tabla 4).
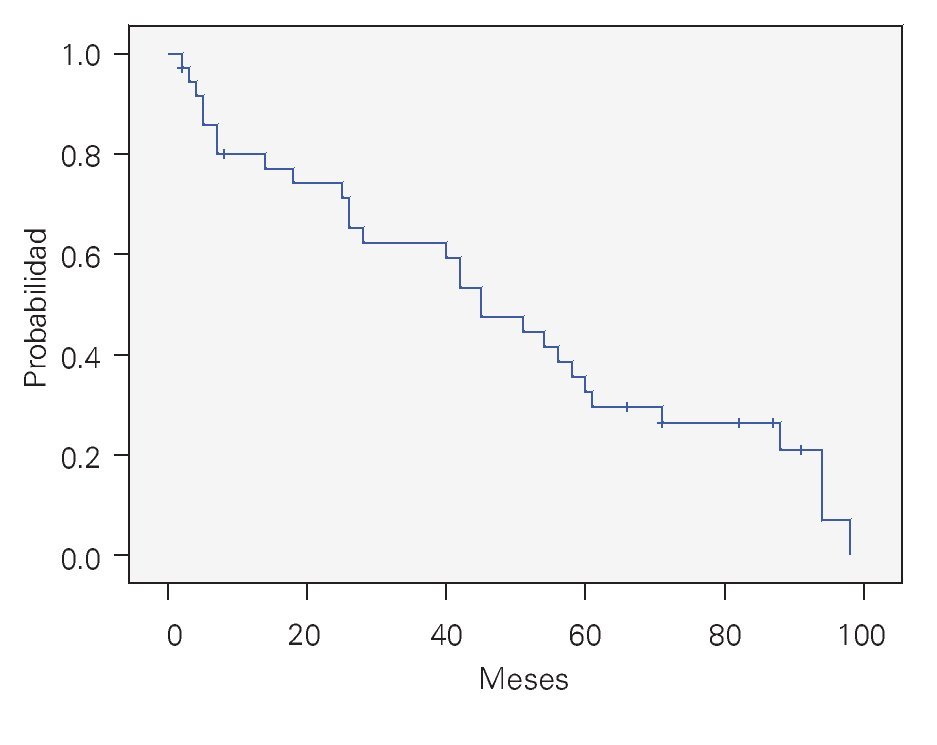
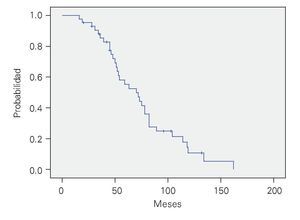
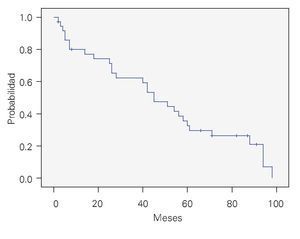
DEP, supervivencia general (SG): Se valoró en 43 pacientes. La SG a 36 meses fue de 56% y de 24% a cinco años, con una mediana de 45 meses. (Figura 3).
¿ Figura 3. Supervivencia general con DEP. n = 43.
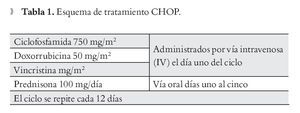
DEP, supervivencia libre de evento (SLE): Se analizaron los datos de 43 enfermos. La SLE fue de 27% y 7%, a 36 y 60 meses, respectivamente. La mediana fue de 21 meses (Figura 4).
¿ Figura 4. Supervivencia libre de eventos con DEP. n = 36.
¿ Discusión
Evaluación de CHOP en primera línea: Tipo de respuesta con CHOP. Habitualmente las respuestas en la literatura se miden en enfermos menores o mayores de 60 años. Dentro de las publicaciones que no hacen esta separación,8, 9 las tasas de remisiones completas y parciales (RC: 64% a 71% y RP: 21% a 36%) son semejantes a lo evidenciado en este estudio (RC: 60% y RP: 25%).
CHOP; supervivencia general (SG): Esta variable se midió desde la fecha del diagnóstico por biopsia hasta la muerte del enfermo por cualquier causa. La literatura médica internacional documenta porcentajes de SG a tres años que van desde 50% hasta 65%.7-10 Estos porcentajes son reproducibles en nuestra población (66% y 56% a tres y cinco años, respectivamente).
Lo previo establece de forma objetiva, que a pesar de los elementos adversos que presentan nuestros pacientes, la efectividad del tratamiento CHOP medida a través de la sobrevida es equiparable a lo que se ha establecido en otros centros.
CHOP, supervivencia libre de evento (SLE): Este parámetro estableció el tiempo que paso desde el diagnóstico por biopsia de la enfermedad hasta que se presentara algún evento (recaída, progresión, muerte o última visita). Lo documentado se compara con las tasas de protocolos de otros países (59% a tres años).10,11
DEP de segunda línea: Tipo de respuesta con DEP. El esquema de tratamiento DEP de forma general al compararse contra otros tratamientos de segunda línea para LNH logra equipararse en remisiones completas y parciales (RC: 44% y RP: 20%).
Los esquemas ESHAP,11 MINE,12 DHAP,14 ICE,16-19 y DICE,20,21 muestran resultados similares, en ese orden son: (RC: 37%, RP: 27%), (RC: 48%, RP: 21%), (RC: 34%, RP: 27%), (RC: 53%, RP: 27%) y (RC: 32%, RP: 32%). Además es superior a GDC22 (RC: 22%, RP: 21%).
DEP, Supervivencia general (SG) y supervivencia libre de evento (SLE): La supervivencia general a tres y cinco años fue de 56% y 24%, respectivamente. La supervivencia libre de evento a tres y cinco años fue de 27% y 7%. Esquemas como ESHAP11 y DHAP,14 documentan SG a 36 meses de 31% y 25%, por lo que en este punto DEP es superior. En relación a ICE19 la SLE a 2 años es equiparable (43% DEP vs. 42%), pero la SG a dos años es superior con DEP (78% vs. 65%), probablemente debido a que ICE es un régimen de mayor intensidad y por ende, toxicidad.
Si se compara contra mini-BEAM23 y DICE,20 los resultados de DEP son alentadores. La SG a cuatro años de miniBEAM es de 22% vs. 38% de DEP, la SG a tres años de DICE es de 43% vs. 56%.
En cuanto al EPOCH-R,24 la SLE a tres años es igual (26% vs. 26%), pero a menor costo. Y si lo compramos contra CEPPB25 la SG a cinco años de DEP es menor (24% vs. 30%).
¿ Conclusiones
Las tasas de respuesta objetiva (RC, RCNC y RP) con CHOP en este grupo, no mostraron diferencias con las informadas. Las tasas de supervivencia general y supervivencia libre de evento con CHOP a tres y cinco años fueron reproducibles y similares a las documentadas en protocolos de otros países. Sin embargo, aunque nuestros resultados son comparables con aquellos reportados para CHOP, no hay que dejar pasar por alto que este esquema terapeútico surgió desde los años 70 y que actualmente es el estándar de oro para el tratamiento de linfomas B, con marcador CD20+ que incluye al anticuerpo monoclonal anti CD20, denominado rituximab.
En aquellos pacientes refractarios o en recaída que recibieron DEP como segunda línea de tratamiento las tasas de respuesta objetiva, supervivencia global y supervivencia libre de evento fueron similares a las reportadas con otros esquemas de tratamiento más agresivos, costosos y tóxicos.
Correspondencia: Dr. Humberto Baldemar Castellanos Sinco.
Dr. Balmis N° 148 Unidad 103. Col. Doctores, 06426. México, D.F.
Correo electrónico: humbertosinco@hotmail.com