Alertar o pediatra sobre a ocorrência de hipertensão portal não cirrótica (HPNC) na faixa etária pediátrica, no sentido de evitar as consequências catastróficas dessa doença, como o sangramento de varizes de esôfago.
Descrição do casoPaciente de 13 anos, infectado pelo HIV por via vertical, recebia esquema antirretroviral com didanosina (ddI) havia 12 anos. Apesar do controle adequado da replicação viral, com carga viral do HIV indetectável havia 12 anos, passou a apresentar diminuição gradativa dos linfócitos TCD4+, trombocitopenia prolongada e fosfatase alcalina elevada. O exame físico detectou esplenomegalia, que desencadeou o processo de investigação e culminou no diagnóstico de fibrose hepática acentuada pela elastografia, por provável toxicidade hepática devido ao uso prolongado de ddI.
ComentáriosEste é o primeiro caso de HPNC em adolescente infectado pelo HIV descrito no Brasil. Embora seja entidade mórbida rara em pacientes soropositivos para o HIV na faixa etária pediátrica, deve ser investigada nos pacientes em uso prolongado de ddI ou que apresentem indicadores clínicos e/ou laboratoriais de hipertensão portal, como esplenomegalia, trombocitopenia e aumento de fosfatase alcalina.
To alert the pediatrician who is following up HIV‐infected patients about the possibility of non‐cirrhotic portal hypertension (NCPH) in this period of life, in order to avoid the catastrophic consequences of this disease as bleeding esophageal varices.
Case descriptionA 13 years old HIV‐infected patient by vertical route was receiving didanosine (ddI) for 12 years. Although the HIV viral load had been undetectable for 12 years, this patient showed gradual decrease of CD4+ T cells, prolonged thrombocytopenia and high alkaline phosphatase. Physical examination detected splenomegaly, which triggered the investigation that led to the diagnosis of severe liver fibrosis by transient elastography, probably due to hepatic toxicity by prolonged use of ddI.
CommentsThis is the first case of NCPH in HIV‐infected adolescent described in Brazil. Although, the NCPH is a rare disease entity in seropositive patients in the pediatric age group, it should be investigated in patients on long‐term ddI or presenting clinical and laboratories indicators of portal hypertension, as splenomegaly, thrombocytopenia and increased alkaline phosphatase.
Estima‐se que aproximadamente 718 mil indivíduos vivam com o HIV/Aids no Brasil, o que representa uma taxa de prevalência de 0,4% na população em geral. A taxa de detecção de Aids no Brasil sofreu uma elevação de cerca de 2% nos últimos 10 anos, sobretudo entre jovens de 15‐24 anos e adultos com 50 anos ou mais. No entanto, a taxa de detecção de casos de Aids em menores de cinco anos, indicador usado no Brasil para monitorar a transmissão vertical do HIV, teve redução de 35,8% em relação a 2003.1 A terapia antirretroviral combinada (TARVc) proporcionou uma queda acentuada na morbimortalidade das crianças e dos adolescentes infectados pelo HIV.2 Os inibidores da transcriptase reversa análogos de nucleosídeo foram os primeiros fármacos antirretrovirais oferecidos e não são raros os pacientes infectados pelo HIV em uso contínuo desses fármacos (isolados ou combinados com outras classes de antirretrovirais) há mais de 10 anos.
As doenças infecciosas (incluindo as infecções oportunistas) diminuíram progressivamente com o tratamento, mas as complicações não infecciosas, entre elas a doença hepática, tornaram‐se causas significantes de morbimortalidade em longo prazo nos sobreviventes. Um estudo retrospectivo, na América do Sul (Brasil, México, Argentina e Peru), que envolveu 6.000 pacientes adultos e soropositivos para o HIV, mostrou que a falência hepática terminal ou a cirrose foi a principal causa de morte, com 54/130 (42%) casos confirmados ou prováveis com base na avaliação clínica, laboratorial ou em achados histológicos.3 Rubio et al., em 2009, usaram procedimentos não invasivos para avaliar comprometimento hepático em 26 crianças cronicamente infectadas pelo HIV por via vertical e encontraram mais de 60% da população com sinais de alteração hepática em pelo menos um dos testes feitos.4
A hipertensão portal não cirrótica (HPNC) é uma das entidades clínicas que afetam os pacientes infectados pelo HIV. É uma patologia rara, ocorre em até 0,5% dos pacientes adultos soropositivos para o HIV.5 A ação direta do próprio HIV, o dano endotelial e mitocondrial, a hipercoagulabilidade e a translocação microbiana são fatores possivelmente implicados na sua patogênese.6‐8 O objetivo deste relato de caso é alertar o pediatra sobre a ocorrência de hipertensão portal não cirrótica (HPNC) na faixa etária pediátrica, no sentido de evitar as consequências catastróficas dessa doença, como o sangramento de varizes de esôfago.
Descrição do casoEste relato de caso foi aprovado pelo Comitê de Ética em Pesquisa da Unifesp (n° CAAE: 31701414.8.0000.5505) e termos de assentimento e consentimento foram assinados pelo paciente e seus responsáveis legais.
Paciente do sexo masculino, nascido por parto cesáreo, prematuro, com peso de nascimento de 1.250g, estatura de 36 centímetros e boletim de Apgar de 1° e 5° minutos de seis e oito, infectado pelo vírus da imunodeficiência humana (HIV) por transmissão vertical. A mãe era usuária de drogas ilícitas com uso irregular de zidovudina na gestação e recebeu profilaxia intraparto. A criança foi adotada aos seis meses de vida e iniciou o acompanhamento da infecção pelo HIV no Ambulatório da Disciplina de Infectologia Pediátrica da Unifesp/EPM (CEADIPe) com sete meses de idade, em dezembro de 2001, e apresentou carga viral do HIV de 1.100.000cópias/mL e linfócitos CD4+ de 819 células/mm3 (24,1%). Foi classificado como B2 e iniciou TARVc (zidovudina‐AZT+didanosina‐ddI+nelfinavir‐NFV) a seguir.
Houve boa adesão à terapia antirretroviral, com controle da replicação viral (carga viral do HIV indetectável) e normalização dos valores de linfócitos T CD4+. Histórico de duas hospitalizações (otite média aguda e pneumonia no início do acompanhamento com oito meses de idade e diarreia dois meses depois) e algumas intercorrências clínicas sem gravidade, como varicela e escarlatina durante o acompanhamento clínico. Recebeu o esquema vacinal completo recomendado para criança infectada pelo HIV. Manteve a mesma TARVc até junho de 2007, quando o NFV não estava mais disponível e foi substituído por nevirapina (AZT+ddI+nevirapina‐NVP). Houve controle da replicação viral e ausência de imunossupressão (CD4+ normal), com adequado desenvolvimento físico e neurológico, sem complicações da doença ou queixas clínicas até abril de 2009, quando passou a apresentar plaquetopenia (< 150.000 plaquetas/microlitro), sem sangramentos. Em março de 2013 começou a mostrar imunossupressão (queda de linfócitos T CD4+ abaixo de 500 células/mm3).
Em agosto de 2013, com 13 anos, apresentava‐se clinicamente bem, peso de 35,6kg; índice de massa corporal de 14,8 (entre 3 e 15 percentil); estatura de 155,5cm; E/I=111% (>97 percentil); pressão arterial 99×75mmHg; raros gânglios cervicais posteriores e inguinais (<0,5cm de diâmetro), fígado palpável a 3,5cm do rebordo costal direito e baço a 6cm do rebordo costal esquerdo (superfície lisa, indolor). Classificação de Tanner para Estágios da Puberdade G3P3 e exame neurológico normal.
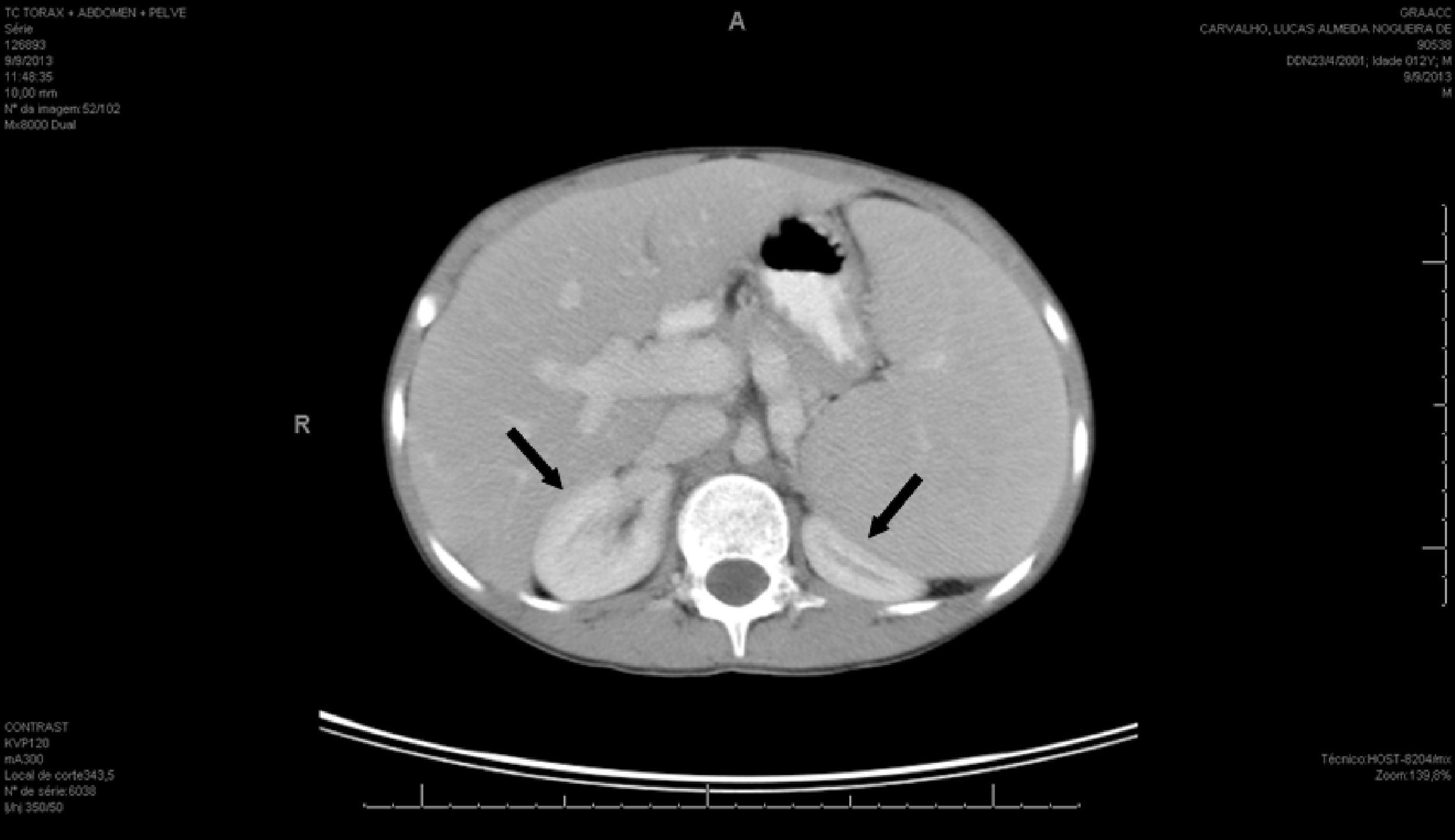
Foram investigadas e afastadas causas infecciosas e oncológicas para essa imunossupressão e hepatoesplenomegalia: imunidade para CMV, hepatite A e hepatite B; sorologias negativas para hepatite C, toxoplasmose, mononucleose. O ultrassom de abdome confirmou esplenomegalia; a tomografia computadorizada de tórax e abdome revelou exame do tórax dentro da normalidade, hepatoesplenomegalia homogênea, que comprimiu os rins posteriormente, e aumento das dimensões da veia porta (1,8cm) (fig. 1).
O mielograma sem células anômalas às da medula revelou relação G/E: 0,9/1 hiperplasia eritrocitária acentuada com maturação preservada; sinais discretos de diseritropoiese; normoplasia granulocítica, com maturação preservada. Presença de megaloblastose leve; normoplasia linfocitária e presença de plasmócitos. Normoplasia monocítica, aumento de macrófagos; normoplasia megacariocítica.
No hemograma apresentava: hemoglobina (Hb) 13,1 g/dL; hematócrito (Htc) 40,4%, plaquetas 63.000/uL, leucócitos 3.700/uL (bastonetes 7%, neutrófilos 64%, eosinófilos 1%, linfócitos 23%, monócitos 5%). Outros exames: proteína C reativa (PCR) 0,45mg/L, desidrogenase láctica (DHL) 163U/L, aspartato aminotransferase (AST) 40U/L, alanina aminotransferase (ALT) 36U/L, gama glutamil transferase (gamaGT) 68U/L, fosfatase alcalina (FA) 382U/L, proteínas totais 7,4g/dL, albumina 4,26g/dL. Índice APRI 1,11 (relação aspartato aminotransferase sobre plaquetas).
Diante desses exames laboratoriais, foi aventada a hipótese de hipertensão portal devido à toxicidade hepática medicamentosa pela didanosina (ddI). A TARVc foi modificada, com suspensão do ddI e troca de todo esquema anterior (abacavir‐ABC+lamivudina‐3TC+lopinavir e ritonavir‐LPV/r) e solicitadas elastografia hepática e endoscopia digestiva alta. A elastografia hepática revelou ausência de esteatose, índice E de 10,0kPa, com fibrose hepática acentuada (F2‐F3 de Metavir). A endoscopia digestiva alta revelou varizes de esôfago de fino calibre, gastropatia hipertensiva portal intensa, pólipos gástricos.
DiscussãoApenas dois outros casos de hipertensão portal não cirrótica (HPNC) em crianças e adolescentes infectados pelo HIV foram anteriormente descritos: uma criança de 10 anos na Itália9 e um adolescente de 15 anos nos Estados Unidos,10 ambos com exposição prolongada ao ddI e história de sangramento de varizes do esôfago. Não se identificaram outros casos descritos no Brasil. A investigação deste caso foi desencadeada porque o paciente, que apresentava controle da replicação viral do HIV (carga viral do HIV indetectável havia 12 anos), em uso de TARVc com ddI há 12 anos, sem sintomatologia clínica, apresentou plaquetopenia, queda progressiva de células T CD4+ e hepatoesplenomegalia.
Além das coinfecções pelos vírus da hepatite B e C, a infecção das células hepáticas pelo HIV pode contribuir para a progressão da doença hepática por mecanismos diretos e indiretos.11 O HIV pode infectar diretamente os hepatócitos, as células estreladas hepáticas (HSCs) e as células de Kupffer. A glicoproteína 120 (gp120) do HIV ligada ao correceptor CXCR4 pode induzir apoptose dos hepatócitos e ativação das HSCs. Ambas contribuem para a formação de fibrose hepática.11 Indiretamente, os inibidores da transcriptase reversa análogos de nucleosídeos e o próprio HIV (efeito via receptor ativado por proliferadores de peroxissoma – PPAR) podem contribuir para doença hepática por indução de síndrome metabólica. A infecção do trato gastrointestinal pelo HIV leva ao aumento de lipopolissacáride (LPS), que pode estimular os três tipos de células hepáticas a produzirem citocinas pró‐inflamatórias e quimiocinas, que atraem linfócitos ativados e monócitos para o fígado e aumentam mais a fibrose.11
Uma das apresentações clínicas de doença hepática em paciente monoinfectado pelo HIV é a hipertensão portal não cirrótica (HPNC), descrita inicialmente em adultos por Maida et al.12 Parikh et al.,13 em 2014, ao estudar adultos infectados pelo HIV com HPNC, verificaram que a maior parte deles apresentava esplenomegalia, trombocitopenia e fosfatase alcalina elevada. Maida et al., em 2006, ao avaliar um grupo de 17 adultos infectados pelo HIV com doença hepática criptogenética e compará‐lo a um grupo controle (pacientes infectados pelo HIV e sem doença hepática), encontraram o uso prolongado de ddI como único fator independente associado ao desenvolvimento de HPNC.12 O mesmo foi observado por Schouten et al.,14 em 2012. Eles demonstraram que os fatores de risco para o desenvolvimento de HPNC eram: exposição prolongada (11 anos) ao ddI isoladamente e/ou exposição em curto prazo (quatro anos) da combinação ddI+estavudina‐D4T ou ddI+tenofovir‐TDF.
Os antirretrovirais didanosina (ddI), estavudina (D4T) e zalcitabina são inibidores da DNA polimerase mitocondrial mais fortes do que zidovudina (AZT), lamivudina (3TC) e abacavir (ABC) e causam maior toxicidade mitocondrial. O esgotamento da DNA polimerase mitocondrial induzida por drogas é um mecanismo subjacente presumido de acidose láctica associada à esteatose, esteato‐hepatite e falência do fígado em indivíduos infectados pelo HIV. Associação entre hepatotoxicidade mitocondrial e HPNC também foi sugerida por Schouten et al., em 2012.14
Mais recentemente, Parikh et al., em 2014,13 com base na prevalência de fatores significantes em pacientes com HPNC, quando comparados com o grupo‐controle, propuseram um fluxograma para avaliar esse diagnóstico: a exposição ao ddI ou a esplenomegalia em um paciente soropositivo para o HIV sem doença hepática conhecida deveria desencadear avaliação para HPNC (excluindo pacientes com história de uso de álcool e hepatites virais detectadas por triagem sorológica). Diante da presença de trombocitopenia, AST maior do que 40U/L ou FA maior do que 115U/L, recomenda‐se encaminhar para hepatologista e iniciar a investigação.13
Considerando‐se que o comprometimento hepático pode ocorrer por longo período antes que as manifestações clínicas de hepatopatia sejam evidentes, e que as crianças infectadas pelo HIV por transmissão vertical estão sobrevivendo por maior tempo em uso contínuo de drogas antirretrovirais, é necessário buscar marcadores capazes de identificar lesão hepática precocemente.
Siberry et al., em 2014,15 avaliaram o índice APRI (razão aspartato aminotransferase/plaquetas) como preditor de fibrose hepática numa coorte de crianças infectadas pelo HIV por transmissão vertical na América Latina. O valor de corte para esse índice em crianças não está estabelecido, mas índices > 1,5 parecem ser bastante específicos, embora pouco sensíveis.15 O paciente estudado apresentou APRI de 1,11 no início da investigação da hepatoesplenomegalila, mas esse índice aumentou para 2 um mês depois.
A HPNC tem como consequência o sangramento de varizes de esôfago. No estudo de Parikh et al.,13 dos 34 casos com HPNC 55,9% apresentaram sangramento. Isso demonstra que a HPNC é subdiagnosticada, talvez devido à falta de um algoritmo para investigação. Foram identificadas varizes de esôfago em quase 90% do grupo com HPNC nesse estudo, prevalência maior do que a encontrada por outros investigadores: 15% no estudo de Mallet et al.,5 em 2007, e 69% no estudo de Maida et al.,6 em 2008. O paciente que descrevemos apresentava varizes esofágicas de fino calibre, sem sangramento. A substituição do ddI por outro antirretroviral neste caso teve a finalidade de interromper a progressão da fibrose hepática e diminuir os riscos de complicação da doença.
O propósito deste relato clínico é o de alertar os profissionais que atendem indivíduos que vivem com HIV/Aids, particularmente pediatras, para a possibilidade de HPNC em crianças e adolescentes infectados pelo HIV por transmissão vertical em uso prolongado de TARVc. Considerar como sinais de alerta a apresentação de plaquetopenia e hepatoesplenomegalia, independentemente da elevação de enzimas hepáticas. Investigar fibrose hepática nesses pacientes, além de identificar precocemente a doença, pode prevenir suas graves consequências, como o sangramento de varizes de esôfago.
FinanciamentoO estudo não recebeu financiamento.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.