La mamografía es la técnica habitual para el cribado poblacional del cáncer de mama. Sin embargo, la sensibilidad mamográfica disminuye mucho en las mamas densas, pudiendo ser de tan solo el 50%. En estos casos la ecografía complementaria puede jugar un papel importante al mejorar la sensibilidad, llegando a tasas de detección de cáncer de hasta el 0,3%. Sin embargo, la ecografía disminuye la especificidad y aumenta la tasa de rellamadas y de biopsias. La ecografía manual es operador dependiente, obliga a emplear mucho tiempo de radiólogo y no permite una revisión retrospectiva. La ecografía automatizada permite solventar varias de estas limitaciones, por lo que puede llegar a emplearse en el cribado como técnica adicional a la mamografía, especialmente en el caso de las mamas densas.
Mammography is routinely used for population-based breast cancer screening. However, the sensitivity of mammography is greatly reduced in dense breasts, and can be as low as 50%. In these cases, complementary ultrasound can play an important role in improving sensitivity, achieving cancer detection rates of up to 0.3%. Nevertheless, ultrasound reduces specificity and increases recall and biopsy rates. Manual ultrasound is operator dependent, is time consuming for the radiologist and does not allow a retrospective review. Automated ultrasound resolves several of these limitations and consequently could become used as an additional technique to mammography, especially in women with dense breasts.
Los programas de cribado basados en mamografía se encuentran instaurados en muchos países, contribuyendo a la disminución de la mortalidad por cáncer de mama1,2. No obstante, la mamografía tiene limitaciones, fundamentalmente en las mamas radiológicamente densas. El Colegio Americano de Radiología (ACR)3 clasifica la densidad mamaria mamográfica en 4 categorías (a-d), desde la mama completamente grasa a la extremadamente densa. En las mamas densas (patrones ACR c y d) la sensibilidad mamográfica puede disminuir de forma muy importante debido al ruido anatómico (enmascaramiento de cánceres no calcificados por el tejido denso circundante)4, a la ausencia de contraste radiológico entre la lesión y el tejido que lo rodea, o al patrón de crecimiento de la lesión (ausencia de masa tumoral o presencia de bordes definidos)5.
La mamografía digital ha supuesto la superación parcial de estas limitaciones debido a su amplio rango dinámico, su mayor resolución de contraste y la posibilidad de procesar las imágenes. El ensayo DMIST6 confirmó una mejoría estadísticamente significativa en la detección del cáncer de mama en mujeres con mamas densas, en la etapa pre- o perimenopáusica y con edad inferior a los 50 años. Aún así, la mamografía digital presenta limitaciones en su sensibilidad y especificidad, especialmente en las mamas densas. Por ello se han desarrollado otras estrategias diagnósticas complementarias, como la ecografía, la tomosíntesis o la resonancia magnética.
El objetivo del presente trabajo es revisar el papel de la ecografía complementaria a la mamografía en el cribado del cáncer de mama.
Equipos de ultrasonidoLa ecografía es una técnica de imagen basada en la detección y representación de la energía acústica reflejada por las diferentes interfases en el interior del organismo7. El estudio ecográfico de la mama ha evolucionado desde su introducción en los años 50 hasta convertirse en una técnica indispensable en el manejo de la patología mamaria.
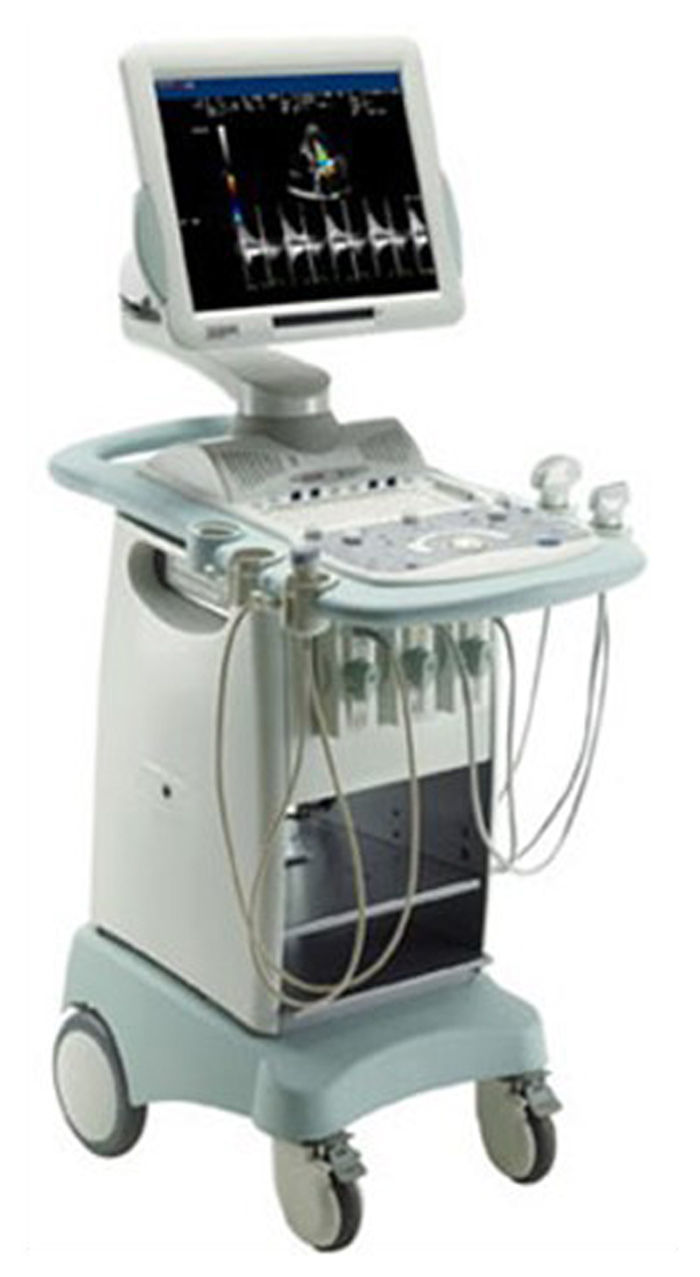
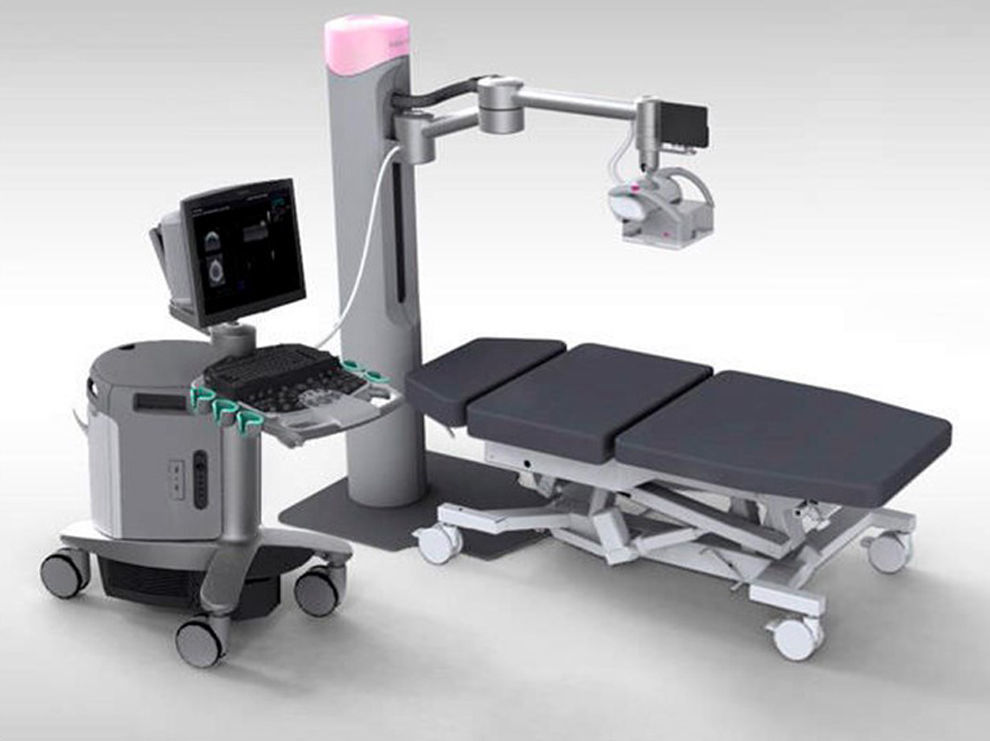
La técnica ecográfica incluye dos modalidades, la manual (fig. 1) y la recientemente introducida técnica automatizada o Automated Breast US (ABUS) (fig. 2).
En la ecografía manual, la exploración es realizada por el radiólogo o el técnico especializado, siendo explorador-dependiente. Se trata de una técnica escasamente reproducible que no queda almacenada en su totalidad, imposibilitando su revisión con fines diagnósticos o legales. No obstante, el diagnóstico ecográfico mamario puede ser extremadamente preciso.
La ecografía manual constituye un excelente método diagnóstico de la patología mamaria en el ámbito clínico tanto como técnica inicial como complementaria a la mamografía. El empleo de la ecografía manual se encuentra, no obstante, limitado por diversos factores tales como la calidad de los equipos ecográficos, el tamaño mamario, variabilidad y reproducibilidad de los estudios, habilidad, experiencia y destreza del examinador8 y tiempo consumido. La exploración ecográfica completa de ambas mamas requiere aproximadamente 20 min de tiempo de radiólogo9 un factor limitante añadido para su empleo en el cribado. Dado que el cribado mamario presenta importantes condicionantes económicos, debe existir una adecuada relación coste-beneficio.
Con el fin de superar las limitaciones de la ecografía mamaria manual se ha desarrollado la ecografía mamaria automatizada - ABUS, técnica que permite la exploración estandarizada de la mama y la valoración diferida de las imágenes en una estación de trabajo, minimizando el carácter operador-dependiente de la ecografía y mejorando la reproducibilidad. Las imágenes se adquieren con la paciente en posición supina con transductores de alta resolución. Debido a su carácter digital, cada plano seccional permite visualizar y almacenar un volumen mamario, que puede ser reconstruido posteriormente en múltiples planos. En concreto, el plano coronal (no posible mediante ecografía bidimensional) ofrece nueva información diagnóstica, ya que puede ser de utilidad en la distinción entre lesiones reales y áreas inhomogéneas10, y muestra mejor la distorsión asociada al cáncer de mama, sobre todo el lobulillar11–13. Esta capacidad multiplanar permite una mejor valoración del volumen tumoral, de gran importancia en la monitorización de la respuesta a los tratamientos de quimioterapia neoadyuvante. Además el almacenamiento completo de la exploración permite su posterior recuperación y reevaluación con fines médicos o forenses. Es posible comparar la localización de las diferentes imágenes y conocer la dirección y la distancia entre un área de interés y el pezón.
Referir, entre las limitaciones de esta técnica, la dificultad que presenta para explorar la región axilar así como para valorar la vascularización y la elasticidad de las lesiones mamarias. Se incluyen también entre las limitaciones la alta tasa de resultados falsos positivos y de rellamadas, común a la ecografía manual, la necesidad de realizar ecografía manual de hallazgos indeterminados, su dificultad en la valoración de mamas grandes y el tiempo requerido para revisar un gran número de imágenes.
El cribado ecográficoLa ecografía se presenta como una prueba de cribado atractiva, dado que es una técnica ampliamente disponible, bien tolerada por las pacientes y de un coste similar a la mamografía, que no requiere medios de contraste ni emplea radiación ionizante. La ecografía muestra, no obstante, algunas limitaciones, ya que no ha demostrado su eficacia como primera técnica diagnóstica en el cribado debido a su baja tasa de detección de microcalcificaciones (fundamental en el diagnóstico precoz del cáncer de mama), por tratarse de una técnica operador-dependiente en el caso de la ecografía manual (el mayor rendimiento diagnóstico de la técnica vendrá condicionado por la experiencia y la especialización del radiólogo), por requerir largos tiempos de exploración, en relación con la escasez de personal cualificado para realizar e interpretar los exámenes, la ausencia de protocolos de exploración estandarizados, así como por su elevado número de falsos positivos. Estas limitaciones han frenado el cribado ecográfico9.
Cribado ecográfico manual: estudios observacionalesLos trabajos efectuados en los años ochenta no demostraron la utilidad del cribado ecográfico, debido probablemente a las limitaciones técnicas de los equipos empleados14–18.
La llegada de mejoras en la tecnología ecográfica (con implementaciones en los transductores y en los circuitos, específicamente diseñados para realizar estudios mamarios permitiendo una mayor resolución espacial y de contraste) así como una mejor capacitación de los radiólogos han podido condicionar la detección de masas sólidas y cánceres más pequeños y más sutiles, imposibles de detectar previamente.
La contribución de la ecografía al cribado de mujeres con mamas mamográficamente densas ha sido examinada en múltiples estudios no randomizados19–27.
Se trata de series amplias, cuyo número de pacientes varía entre los 1.517 pacientes de la serie de Crystal20 y los 22.131 pacientes de la serie de Girardi19.
La mayoría de los trabajos20,22 se centraron fundamentalmente en el cribado ecográfico de mujeres con mamas mamográficamente densas (patrones ACR c y d), dado que el incluir patrones grasos probablemente no sería coste-efectivo. Sin embargo, algunos estudios incluyeron otros patrones19–21,23,24.
En la mayoría de las series las ecografías fueron realizadas por médicos radiólogos, aunque en otras las realizó un técnico de radiología22.
Todas las series valoraron el papel de la ecografía adicional a la mamografía en mujeres asintomáticas. La serie de Crystal20 sobre 1.517 mujeres incluyó un subgrupo de alto riesgo (318 mujeres con historia familiar de primer grado o historia personal de cáncer de mama). La serie de Kolb23 incluyó asimismo un grupo de mujeres de alto riesgo.
Las tasas de detección ecográfica mostraron valores similares en las series de Kaplan22 y Kolb23: 0,30%. La tasas de Corsetti25, Buchberger24 y Crystal20 fueron ligeramente superiores: 0,40, 0,41 y 0,46% respectivamente. En la serie de Crystal20 la tasa de detección ecográfica fue superior en el subgrupo de alto riesgo: 1,3% frente al 0,25% del subgrupo de riesgo basal.
Las tasas de procedimientos intervencionistas mostraron una mayor variabilidad, entre valores del 2,5% de la serie de Crystal20 dentro del rango admitido para el cribado mamográfico (1-3%) y el 5,2% de la serie de Kaplan22.
Finalmente, el VPP de las biopsias derivadas de las ecografías fue inferior al de las lesiones detectadas mamográficamente (28-30%), entre el 8,4% de la serie de Corsetti25 y el 16% de la serie de Gordon26. Limitar el número de biopsias derivadas de los hallazgos ecográficos es un factor determinante del éxito o fracaso del cribado ecográfico. El número de biopsias y el valor predictivo positivo de las biopsias deberían aproximarse a los del cribado mamográfico. Para ello, el cribado ecográfico debería ser supervisado por un radiólogo experimentado en mamografía y ecografía de mama, siendo esencial una adecuada correlación mamográfica de los hallazgos ecográficos.
El estadio precoz de los cánceres detectados exclusivamente por ecografía y la mayor contribución ecográfica a la detección de cáncer en el subgrupo de mujeres de 40-49 años (coincidente con el subgrupo de mayor incidencia proporcional de cánceres de intervalo) sugieren un potencial beneficio a largo plazo de la detección de cánceres adicionales mediante ecografía.
Cribado ecográfico manual: estudios randomizadosDos grandes estudios randomizados, el ACRIN 6666 y el J-START, se han centrado en la valoración del papel de la ecografía en el cribado mamario.
En el año 2003, Berg9 inició un ensayo prospectivo, multicéntrico, randomizado (ACRIN 6666) cuyo objetivo fue valorar el rendimiento diagnóstico del cribado combinado: mamografía y ecografía vs. mamografía en mujeres con riesgo intermedio y alto de cáncer de mama. En este ensayo de cribado ecográfico, la mamografía y la ecografía fueron realizadas y leídas independientemente, permitiendo el análisis detallado del rendimiento de cada modalidad de forma separada y conjunta. Dos mil ochocientas nueve mujeres con al menos tejido heterogéneamente denso en al menos un cuadrante fueron reclutadas y exploradas con mamografía y ecografía. El rendimiento diagnóstico de la mamografía fue de 7,6 cánceres/1.000 mujeres cribadas y se incrementó a 11,8 cánceres/1.000 para la combinación mamografía más ecografía. El rendimiento suplementario fue 4,2 cánceres/1 000 mujeres cribadas. El área bajo la curva de la mamografía fue 0,78 e incrementándose hasta 0,91 para mamografía más ecografía. De los 12 cánceres adicionales detectados solo por ecografía 11 fueron infiltrantes con un tamaño medio de 10mm (rango: 5-40mm). El valor predictivo positivo de la biopsia fue del 22,6% para la mamografía, 8,9% para la ecografía y 11,2% para mamografía más ecografía. El incremento en la tasa de detección de cáncer asociado al cribado ecográfico (4,2 cánceres/1.000 mujeres de alto riesgo cribadas) fue similar al de otras series que mostraron valores de entre 2,7 y 4,6 cánceres/1.000 mujeres cribadas. En esta población de riesgo elevado, enriquecida en mujeres con mamas densas, la sensibilidad mamográfica fue solo del 50% y la sensibilidad de la mamografía más ecografía fue del 77,5%.
Todos los cánceres detectados únicamente mediante ecografía excepto uno tuvieron ganglios negativos.
El cribado ecográfico aumentó los resultados falsos positivos: con la mamografía se realizaron biopsias innecesarias en 1/40 mujeres, mientras que con mamografía más ecografía las biopsias innecesarias ocurrieron en 1/10 mujeres. Asimismo la ecografía incrementó la tasa de lesiones BI-RADS 3, lo que genera ansiedad y morbilidad.
Las tasas de rellamadas de las exploraciones mamográficas estuvieron dentro de los rangos aceptados: 10,5%, siendo de 5,4% para la ecografía (un valor artificialmente bajo en probable relación según los autores con la realización de los estudios ecográficos por médicos radiólogos que podrían evaluar las lesiones en tiempo real). El VPP de las biopsias recomendadas por ecografía fue del 8,8-8,9%.
Concluyeron a la vista de sus resultados que añadir cribado ecográfico a la mamografía incrementaba el rendimiento diagnóstico en mujeres de alto riesgo pero incrementaba también sustancialmente el número de falsos positivos. Dada la cohorte seleccionada, los resultados no pueden ser aplicados a los programas de cribado de mujeres asintomáticas de entre 50 y 69 años.
Una limitación del ACRIN 6666 es que incluyó únicamente mujeres con riesgo elevado de cáncer de mama.
Otro ensayo randomizado comenzó en Japón en 2006, el Japan Strategic Anti-cancer Randomized Trial28. Su población diana fueron mujeres asintomáticas de entre 40 y 49 años. Se trató de un ensayo a gran escala (72.998 mujeres) que incluyó 36.859 mujeres con mamografía y ecografía y 36.139 mujeres control (con solo mamografía). Sus resultados, recientemente publicados, mostraron una sensibilidad significativamente mayor (91,1 vs. 77%) y una especificidad significativamente inferior (87,7 vs. 91,4%) en el grupo estudiado con mamografía y ecografía respecto del grupo control. La tasa de detección de cáncer fue superior en el grupo estudiado con ambas técnicas (67 cánceres adicionales detectados mediante ecografía) siendo más frecuentes en este grupo los estadios clínicos 0 y 1, la mayoría cánceres invasivos y con ganglios negativos. Un total de 18 cánceres de intervalo fueron detectados frente a los 35 del grupo control (p=0,034). Este ensayo concluyó que la ecografía complementaria incrementa la sensibilidad y la tasa de detección de cánceres de mama en estadio precoz.
ABUS como adjunto a la mamografíaDiversos estudios se han centrado en la valoración del papel de la ecografía automatizada complementaria a la mamografía.
Kelly et al.29 emplearon el ABUS adicional a la mamografía frente a la mamografía aislada en la evaluación de mujeres asintomáticas con mamas densas y/o riesgo elevado de cáncer de mama. Sobre 4.419 mujeres cribadas mamográficamente, la combinación mamografía y ABUS incrementó el rendimiento diagnóstico de 3,6 (mamografía aislada) a 7,2 cánceres/1.000 mujeres cribadas. No obstante, una de las limitaciones de este trabajo es que no aisló la densidad mamaria como factor de riesgo independiente para el desarrollo de cáncer de mama. El número de cánceres infiltrantes detectados de tamaño igual o inferior a 10mm se triplicó (pasó de 7 a 21) al añadir el ABUS a la mamografía. A la vista de sus resultados concluyeron que el ABUS incrementa significativamente la detección del cáncer de mama respecto a la mamografía. Este hecho, así como el menor tamaño de los cánceres infiltrantes detectados, podría justificar el empleo de esta técnica en mujeres con mamas densas y/o de alto riesgo para cáncer de mama.
En la misma línea, otros grupos de trabajo como el de Giuliano et al.30 valoraron la detección de cáncer de mama en mujeres asintomáticas con mamas densas empleando el ABUS. Realizaron estudio ABUS a 3.418 mujeres obteniendo una tasa de detección de 12,3 cánceres/1.000 mujeres cribadas (frente a una tasa de 4,6/1.000 del cribado mamográfico aislado). Incluyeron, no obstante, cánceres que también fueron detectados por mamografía. De particular relevancia fueron el pequeño tamaño (el tamaño tumoral medio fue de 14,3mm) y el estadio precoz de los cánceres detectados mediante esta técnica. Concluyeron que la posible justificación coste-beneficio de implementar la mamografía con ABUS en la población cribada (asintomática) portadora de mamas densas. Una de las principales limitaciones de su trabajo fue la ausencia de datos que soportasen una mejora de la mortalidad por cáncer de mama con la adición de la ABUS como modalidad de cribado.
La ABUS ha sido aprobada por la FDA en EE. UU. para el cribado de mujeres con parénquima mamario denso31.
ConclusiónDados los resultados de las diferentes series publicadas, la ecografía complementaria a la mamografía puede jugar un importante papel en el cribado de las mamas densas, aunque se encuentra limitado por su baja especificidad y su bajo valor predictivo positivo comparativamente con los del cribado mamográfico. Además el cribado ecográfico no ha demostrado a día de hoy en ensayos randomizados la reducción de la mortalidad por cáncer de mama. No obstante, la ecografía automatizada puede convertirse en una herramienta de cribado útil en mujeres con mamas densas.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Autoría/colaboradoresArlette Elizalde ha contribuido en la concepción, diseño y redacción del manuscrito.
Natalia Rodríguez-Spiteri ha contribuido en la redacción y supervisión del manuscrito.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.