Las vacunas son productos biológicos sintéticos diseñados para la prevención de enfermedades infecciosas. Después del agua potable, son la medida de salud pública más eficaz en reducir la mortalidad y las secuelas provocadas por las enfermedades inmunoprevenibles. En Chile, nos acompañan a lo largo del ciclo vital a través del Programa Nacional de Inmunización (PNI), creado en 1979 y constantemente sometido a modificaciones y avances para asegurar el acceso seguro y gratuito de la población general a vacunas.
Paralelamente, existen grupos de personas portadoras de ciertas condiciones clínicas que favorecen la adquisición y/o gravedad en la presentación de enfermedades inmunoprevenibles. Estas poblaciones especiales se encuentran en ascenso. En este contexto, el objetivo de esta revisión es entregar las directrices actuales que guían la inmunización de estos grupos particulares de pacientes.
Vaccines are synthetic biological products designed for the prevention of infectious diseases. After potable drinking water, they are the most effective public health measure in reducing mortality and other consequences caused by vaccine-preventable diseases. In Chile, they accompany us throughout our life cycle through the National Immunization Program (PNI), created in 1979 and constantly undergoing change and improvements in order to ensure safe and free access to vaccines to the general population. There are certain clinical conditions, however, that exacerbate the acquisition and/or severity of vaccine-preventable diseases. These special populations are on the rise. In this context, the objective of this review is to provide current guidelines for the immunization of these particular groups of patients.
Las vacunas, después del agua potable, son la medida de salud pública más eficaz en reducir la mortalidad y las secuelas provocadas por las enfermedades inmunoprevenibles1. Estas son productos biológicos sintéticos diseñados para la prevención de enfermedades infecciosas, su efecto protector se realiza estimulando la inmunidad adaptativa tras la inoculación. En base a su composición se pueden clasificar, en términos generales, de la siguiente manera2,3:
- 1.
Vacunas con agente infeccioso completo:
- -
Viva atenuada: patógeno vivo, debilitados bajo condiciones de laboratorio
- -
Inactivada: patógeno muerto
- 2.
Vacunas con subunidades: formadas con una porción antigénica del agente infeccioso. A su vez, pueden ser de carácter:
- -
Proteico
- -
Polisacárido
- -
Conjugado: Polisacárido unido a una proteína transportadora
- -
Vacunas mRNA
- -
- 3.
Vacunas con un producto extracelular del agente infeccioso (toxoides)
En Chile, las vacunas acompañan a la población a lo largo de su ciclo vital a través del Programa Nacional de Inmunización (PNI), nacido en 1979 del Programa Ampliado de Inmunización (PAI)4. Desde sus inicios el PNI se basó en disposiciones legales que establecían que el Ministerio de Salud debía garantizar acceso gratuito a vacunas frente a enfermedades transmisibles inmunoprevenibles para las poblaciones objetivo correspondientes. El Decreto Exento N°6 del año 2010 establece la vacunación obligatoria contra las siguientes enfermedades: tuberculosis, poliomielitis, tos convulsiva, difteria, tétanos, enfermedades infecciosas por H. influenzae tipo B, sarampión, paperas, rubéola, hepatitis B, enfermedad invasora por S. pneumoniae, influenza y rabia humana5. Dicho decreto también determina las poblaciones objetivo y establecimientos responsables de esta ejecución. Desde entonces se han realizados modificaciones al decreto N°6, agregando nuevas vacunas y modificando grupos objetivos.
En el año 2018, a raíz de un aumento en la solicitud de vacunas en circunstancias especiales procedentes de los distintos prestadores públicos y privados de salud, se elabora el documento “Recomendaciones Para la Vacunación de Pacientes con Necesidades Especiales por Patologías o Situaciones de Riesgo”, que viene a protocolizar y orientar a los profesionales de la salud y pacientes afectados por alguna condición clínica que determine, a través de diversos mecanismos, deficiencias en la respuesta inmunológica4,6.
El objetivo de este artículo es revisar las recomendaciones de inmunización en grupos poblacionales especiales, tales como:
- •
Personas con cánceres hematológicos y de tumores sólidos
- •
Personas con trasplante de órganos sólidos y precursores hematopoyéticos
- •
Personas en tratamientos inmunosupresores (corticoterapia y terapias biológicas)
- •
Personas viviendo con virus de la inmunodeficiencia humana (PVVIH)
- •
Personas con otras patologías crónicas: bronconeumopatías, cardiopatías, hepatopatías, enfermedad renal crónica (ERC), síndrome nefrótico, diabetes mellitus, afecciones neurológicas, fístula de líquido cefalorraquídeo (LCR) no resuelta e implante coclear.
- •
Personas mayores (adultos ≥ de 65 años)
- •
Embarazadas
Es fundamental el entendimiento de los mecanismos fisiopatológicos subyacentes que facilitan y/o determinan gravedad en la génesis y evolución de patologías infecciosas en los grupos especiales mencionados. En este sentido, se han observado alteraciones en la inmunidad innata y adaptativa (tanto humoral como celular); siendo frecuente la participación de trastornos de origen mixto en los que están involucrados ambos mecanismos.
Pacientes con cánceres hematológicos y tumores sólidosDe la mano con el envejecimiento de la población, la mortalidad por cáncer ha ido progresivamente en aumento. En Chile, en el año 2019, el cáncer sustituyó a las enfermedades cardiovasculares como la primera causa de mortalidad general7.
La patología oncológica, y sus terapias asociadas, conllevan alteraciones inmunológicas que afectan tanto a sus componentes humorales como celulares. En este contexto, las infecciones son una de las principales causas de morbimortalidad en estos pacientes7,8.
En este ítem abordaremos a aquellos pacientes con: leucemia, linfoma y tumores sólidos. En relación al tratamiento, se diferenciará en dos fases: inducción y remisión. La fase de inducción es aquella etapa inicial de quimioterapia de carácter agresivo cuyo propósito es la remisión de la patología neoplásica. Durante esta etapa de tratamiento se genera aplasia medular, lo que contraindica la administración de vacunas vivas atenuadas por seguridad y, en el caso de vacunas inactivadas, determina una menor respuesta inmunogénica con el riesgo concomitante de no otorgar una protección adecuada. De esta manera, en inducción solo se recomienda la inoculación de la vacuna contra la influenza (según la campaña respectiva).
Por otra parte, la fase de remisión se define como la desaparición de evidencia neoplásica en el examen empleado en su diagnóstico. En esta etapa se recomienda aplicar las vacunas inactivadas con el objetivo de lograr una mejor respuesta inmunogénica6. De acuerdo a lo anterior, en el caso de la vacuna contra la hepatitis B, se recomienda medir los anticuerpos antiantígeno de superficie del virus (anti-HBsAg) a los 30 días de la administración. En caso de obtenerse un valor <10mUI/ml, se volverá a vacunar con esquema inicial, realizando posteriormente una nueva medición de concentración de anticuerpos9.
En términos generales, en este grupo poblacional particular, durante la edad adulta la medición de infecciones inmunoprevenibles se centra en virus influenza, virus hepatitis B (VHB) y Streptococcus pneumoniae; desde los 50 años se amplía la recomendación para incluir herpes-zoster9,10 (tabla 1).
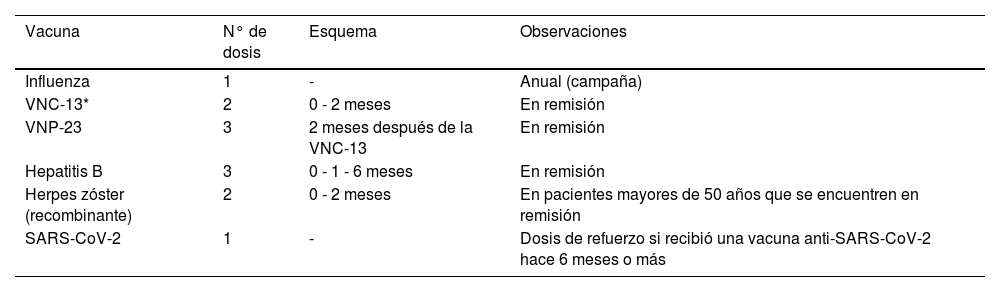
Recomendaciones de vacunas en adultos con cáncer hematológico o tumores sólidos
| Vacuna | N° de dosis | Esquema | Observaciones |
|---|---|---|---|
| Influenza | 1 | - | Anual (campaña) |
| VNC-13* | 2 | 0 - 2 meses | En remisión |
| VNP-23 | 3 | 2 meses después de la VNC-13 | En remisión |
| Hepatitis B | 3 | 0 - 1 - 6 meses | En remisión |
| Herpes zóster (recombinante) | 2 | 0 - 2 meses | En pacientes mayores de 50 años que se encuentren en remisión |
| SARS-CoV-2 | 1 | - | Dosis de refuerzo si recibió una vacuna anti-SARS-CoV-2 hace 6 meses o más |
VNC-13: vacuna neumocócica conjugada-13; VNP-23: vacuna neumocócica polisacárida-23; SARS-CoV-2: por sus siglas en inglés de Severe Acute Respiratory SyndromeCoronavirus-2.
Los pacientes trasplantados, tanto de órganos sólidos como de precursores hematopoyéticos, se encuentran en continuo aumento. Esto deriva de una mayor sobrevida y de la ampliación del espectro de indicaciones para ser receptor de un trasplante. Las infecciones, incluyendo las enfermedades inmunoprevenibles, constituyen una de las principales causas de muerte en este grupo11. En este contexto, a continuación, abordaremos las recomendaciones de vacunación en esta población:
Órganos sólidosEn Chile, en términos de frecuencia, el riñón lidera la lista de órganos sólidos trasplantados; seguido por el hígado y, menos frecuentemente, pulmón y corazón12. Los pacientes receptores de estos órganos, debido a su enfermedad de base y otras condiciones previas al trasplante, son más susceptibles a infecciones. Es por esto que en todos los candidatos a trasplante se recomiendan las siguientes vacunas (tabla 2): influenza anual, SARS-CoV-2, vacuna antihepatitis B, (en caso de tener anti-core total (-)) y, en pacientes portadores de hepatopatías, la administración de vacuna antihepatitis A si no existen antecedentes de haber presentado previamente la enfermedad6. La tabla 3 detalla las recomendaciones para la vacunación de trasplantados órganos sólidos.
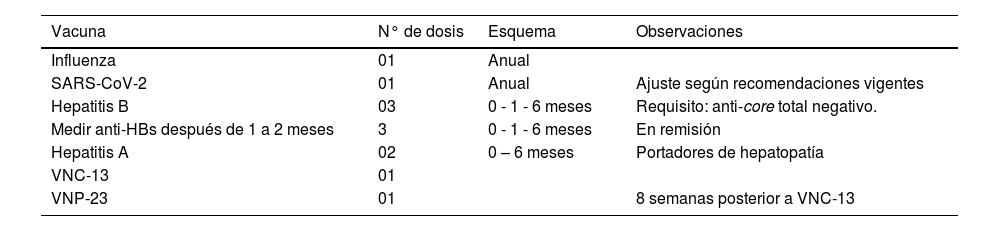
Recomendaciones para la vacunación en candidatos a trasplante
| Vacuna | N° de dosis | Esquema | Observaciones |
|---|---|---|---|
| Influenza | 01 | Anual | |
| SARS-CoV-2 | 01 | Anual | Ajuste según recomendaciones vigentes |
| Hepatitis B | 03 | 0 - 1 - 6 meses | Requisito: anti-core total negativo. |
| Medir anti-HBs después de 1 a 2 meses | 3 | 0 - 1 - 6 meses | En remisión |
| Hepatitis A | 02 | 0 – 6 meses | Portadores de hepatopatía |
| VNC-13 | 01 | ||
| VNP-23 | 01 | 8 semanas posterior a VNC-13 |
VNC-13: vacuna neumocócica conjugada-13; VNP-23: vacuna neumocócica polisacárida-23; SARS-CoV-2: por sus siglas en inglés de Severe Acute Respiratory Syndrome Coronavirus-2.
*En caso de disponer VNC-15, preferir esta por sobre VNC-13. En caso de disponer de VNC-20, preferir por sobre 13 y 15 valentes, considerar que VNC-20 no requiere refuerzo con VNP-23.
Recomendaciones para la vacunación de trasplantados órganos sólidos
| Vacunas | Administración | Observaciones |
|---|---|---|
| 6 meses post trasplante | [Inmunizaciones en el adulto: una mirada hacia las poblaciones especiales - Paulina Vergara-Pinto y col.] | |
| Influenza | Anual | |
| Otras vacunas inactivadas | Según riesgo epidemiológico | -Se administra VNC-13 si no la recibió pre-trasplante |
| -Dosis de refuerzo si recibió una vacuna anti-SARS-CoV-2 6 meses o más. | ||
| 12 meses post trasplante | ||
| Influenza | Anual | Independiente de estado de inmunosupresión |
| Vacuna hepatitis B | Según nivel anti-HBsAg | Dosis de refuerzo si nivel <10mUI/mL |
| Vacuna herpes zóster | 2 dosis | Vacuna recombinante. |
| No requiere serología varicela ni antecedente de enfermedad | ||
VNC-13: vacuna neumocócica conjugada-13; SARS-CoV-2: por sus siglas en inglés de Severe Acute Respiratory Syndrome Coronavirus-2; Anti-HBsAg: anticuerpos antiantígeno de superficie del virus hepatitis B.
En los 12 meses post trasplante, según estadio de inmunosupresión se pueden administrar dosis de refuerzo de vacunas inactivadas. Es importante considerar que algunas vacunas vivas se pueden administrar pasado 2 años desde el trasplante siempre y cuando no exista otra causa de inmunosupresión como el uso de fármacos inmunosupresores.
Precursores hematopoyéticosEl trasplante de células hematopoyéticas se puede clasificar según el tipo de donante en:
- -
Autólogo: las células madre hematopoyéticas (CMH) son obtenidas del propio paciente.
- -
Alogénico: las CMH provienen de otro individuo.
El compromiso inmunológico está presente antes de recibir el trasplante, tanto por la patología de base, como por la preparación previo a ella. Esto último es conocido como acondicionamiento medular, de intensidad variable, y cuyo propósito es suprimir la médula y el sistema inmunitario del paciente13. En este contexto, todo receptor CMH debe ser considerado como individuo “naive” ante las enfermedades inmunoprevenibles (virgen, no vacunado o no expuesto a la enfermedad), por lo que deben recibir todas las vacunas eficaces y disponibles a la fecha.
La etapa de reconstitución inmune posterior al trasplante está condicionada por múltiples factores, entre ellos: origen de las CMH, esquema de quimioterapia de acondicionamiento utilizado, fármacos empleados en la prevención de la enfermedad de injerto contra huésped (EICH o GVHD, por sus siglas en inglés de Graft-Versus-Host-Disease) y su presentación en el paciente, así como la aparición de infecciones oportunistas en el período de recuperación hematológica. La inmuno reconstitución suele completarse a los 6-12 meses posterior al trasplante, tras lo cual se aconseja iniciar la inmunización; lo anterior excluye a las vacunas vivas atenuadas, las que deben ser administradas tras un mínimo de 24 meses6,13 (tabla 4).
Recomendaciones de vacunación en receptores de trasplante de precursores hematopoyéticos
| Vacuna | Tiempo post trasplante | Esquema |
|---|---|---|
| dTpa + Hib + VPI + VHB | Desde 12 meses | 0 - 2 - 4 - 18 meses |
| VNC-13* | Desde 12 meses | 0 - 2 - 4 meses |
| Refuerzo a los 12 meses | Anual | Independiente de estado de inmunosupresión |
| VNP-23 | 12 meses después de la VNC-13 | 1 dosis |
| Meningocócica conjugada ACWY | Desde los 12 meses | 0 - 2 mesesDosis de refuerzo a los 3 años |
| Meningocócica conjugada B | Desde los 12 meses | 0 - 2 meses |
| Hepatitis A | 12 meses | 0 - 6 meses |
| Tres vírica | 12 meses | 0 - 1 mes |
| Varicela | 24 meses | 0 - 3 meses |
| Virus papiloma humano tetravalente | 12 meses | 0 - 2 - 6 meses |
| SARS-CoV-2 | 12 meses | 1 dosis |
| Herpes zóster (recombinante) | Desde los 12 meses | 0 - 2 meses |
dTpa: difteria, tétanos, pertussis acelular; Hib: Haemophilus influenzae tipo B; VPI: vacuna polio inactiva (virus inactivado); VHB: virus hepatitis B; VNC-13: vacuna neumocócica conjugada-13; VNP-23: vacuna neumocócica polisacárida-23; meningocócica conjugada ACWY: serogrupos A, C, W e Y; SARS-CoV-2: por sus siglas en inglés de Severe Acute Respiratory Syndrome Coronavirus-2.
Además de esta recomendación en términos de temporalidad, el paciente debe cumplir ciertas condiciones inmunológicas para iniciar la vacunación:
- 1.
Recuento absoluto de linfocitos T CD4(+): >400/mm3
- 2.
Recuento absoluto de linfocitos B CD19: >200/mm3
- 3.
Recuento absoluto de linfocitos: >1 000/mm3
- 4.
Concentraciones plasmáticas de Inmunoglobulina G (IgG) normales para la edad
Bajo ciertas situaciones epidemiológicas de riesgo particulares (brote de influenza, enfermedad meningocócica, riesgo de tétanos, entre otras) pueden aplicarse vacunas inactivadas desde los 3 a 6 meses post trasplante6,13.
Personas con tratamiento inmunosupresorCorticoidesLos corticoides son fármacos con potentes efectos antiinflamatorios, capaces de regular numerosas enfermedades inflamatorias e inmunomediadas. La prevalencia de su uso se encuentra en ascenso, aumentando con la edad. A través de varios mecanismos, la corticoterapia sistémica produce inmunosupresión de carácter celular y humoral. El grado de afectación inmunitaria suele estar relacionada con la dosis empleada como también la duración y potencia del tratamiento. Sin embargo, debido a los efectos inmunosupresores cuanti y cualitativos de estos fármacos, es complejo estimar con precisión la dosis y el tiempo de administración capaz de generar inmunosupresión significativa, condicionando una menor respuesta a la administración de vacunas o determinando un riesgo en términos de seguridad. En este contexto, se ha definido y establecido que esta dosis en adultos correspondería a prednisona 20mg/día (o dosis equivalente) a partir de los 7 días de uso14.
En estos pacientes se recomienda6,15:
- -
Administración de vacunas vivas atenuadas desde 1 a 3 meses desde finalizado el tratamiento corticoesteroidal. En relación con las vacunas inactivadas, posponer su administración hasta 1 mes post término de tratamiento.
- -
Si la duración de la terapia corticoidal es prolongada, se recomienda administrar las vacunas según calendario PNI y las respectivas campañas de influenza y anti-SARS-CoV-2, considerando que se producirá menor respuesta inmune.
- -
Se debe evaluar la posibilidad de vacunar en el momento en el que el paciente esté con la menor dosis posible de corticoide.
El uso de terapias biológicas ha ido en aumento, constituyendo un importante avance en el manejo de patologías autoinmunes y neoplásicas. Sin embargo, debido a su efecto en la modulación de la respuesta inmune y sus distintos mecanismos de acción, aumenta la susceptibilidad a infecciones en este grupo de pacientes. En ellos, la vacunación debiese realizarse preferentemente antes del inicio de la terapia biológica o en el momento de menor inmunosupresión con el objetivo de mejorar la respuesta inmunológica a la vacuna. Es importante tener en cuenta que las vacunas que contienen componentes vivos están contraindicadas en estados de inmunosupresión16.
Existe un aumento exponencial en la terapia biológica disponible, sin mayor evidencia en relación a las recomendaciones de inmunización en estos pacientes. Es por esto que muchas de las directrices que guían la administración de vacunas en esta población se basan en opinión de expertos.
En términos generales se recomienda lo siguiente en todos los pacientes: vacuna antiinfluenza anual, vacuna antineumocócica y contra SARS-CoV-2; tanto por su patología de base como por el uso de terapia biológica. Además, existen algunas particularidades según mecanismo de acción de la terapia biológica15–17 (tabla 5):
- -
Inhibidores de la función del complemento (eculizumab, ravulizumab, zilucoplan): al menos 2 semanas antes (sólo de ser posible), administrar la vacuna antimeningocócica tetravalente ACWY (para los serogrupos A, C, W e Y) conjugada, antimeningocócica serotipo B conjugada, esquema antineumocócico y Haemophilus influenzae tipo B.
- -
Antifactor de necrosis tumoral (anti-TNF-alfa) (adalimumab, infliximab, etanercept, certolizumab, golimumab, etc.): vacuna anti-VHB en aquellos pacientes sin evidencias de infección previa. Considerar la vacuna antiherpes zóster (VVZ) si son mayores de 18 años con serología positiva o antecedente de enfermedad previa.
- -
Anticuerpo monoclonal anti-CD52 (alemtuzumab): vacuna anti-VHB en aquellos sin evidencia de infección previa. Considerar, además la vacuna anti-VVZ si cumple las condiciones mencionadas anteriormente.
- -
Anticuerpo monoclonal anti-CD20 (rituximab, ocrelizumab): se recomienda vacuna anti-VHB en aquellos sin evidencia de infección previa.
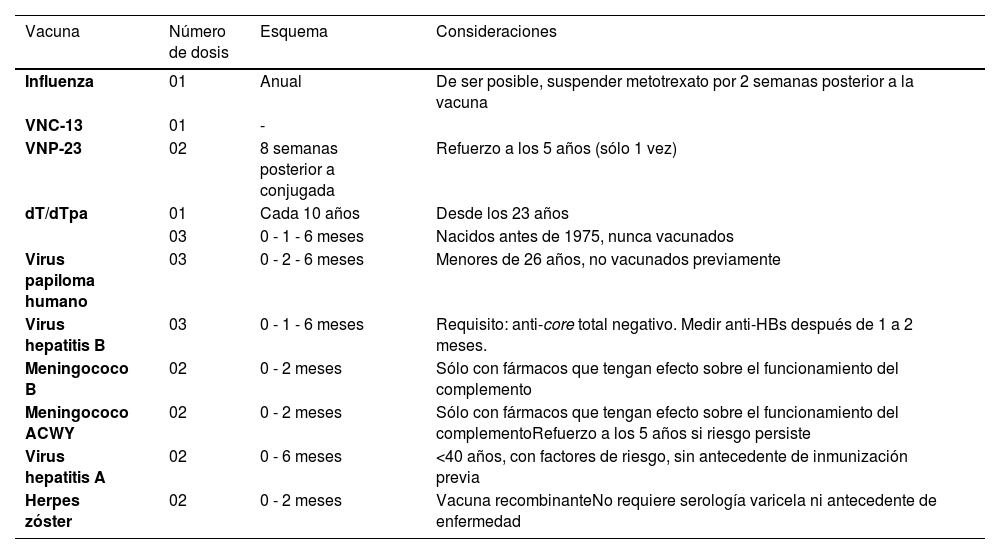
Recomendaciones vacunación en pacientes con inmunosupresión farmacológica
| Vacuna | Número de dosis | Esquema | Consideraciones |
|---|---|---|---|
| Influenza | 01 | Anual | De ser posible, suspender metotrexato por 2 semanas posterior a la vacuna |
| VNC-13 | 01 | - | |
| VNP-23 | 02 | 8 semanas posterior a conjugada | Refuerzo a los 5 años (sólo 1 vez) |
| dT/dTpa | 01 | Cada 10 años | Desde los 23 años |
| 03 | 0 - 1 - 6 meses | Nacidos antes de 1975, nunca vacunados | |
| Virus papiloma humano | 03 | 0 - 2 - 6 meses | Menores de 26 años, no vacunados previamente |
| Virus hepatitis B | 03 | 0 - 1 - 6 meses | Requisito: anti-core total negativo. Medir anti-HBs después de 1 a 2 meses. |
| Meningococo B | 02 | 0 - 2 meses | Sólo con fármacos que tengan efecto sobre el funcionamiento del complemento |
| Meningococo ACWY | 02 | 0 - 2 meses | Sólo con fármacos que tengan efecto sobre el funcionamiento del complementoRefuerzo a los 5 años si riesgo persiste |
| Virus hepatitis A | 02 | 0 - 6 meses | <40 años, con factores de riesgo, sin antecedente de inmunización previa |
| Herpes zóster | 02 | 0 - 2 meses | Vacuna recombinanteNo requiere serología varicela ni antecedente de enfermedad |
dT: difeteria, tétanos; dTpa: difteria, tétanos, pertussis acelular; VNC-13: vacuna neumocócica conjugada-13; VNP-23: vacuna neumocócica poli- sacárida-23; meningocócica conjugada ACWY: serogrupos A, C, W e Y;.
*En caso de disponer VNC-15, preferir esta por sobre VNC-13. En caso de disponer de VNC-20, preferir por sobre 13 y 15 valentes, considerar que VNC-20 no requiere refuerzo con VNP-23.
El inicio de la terapia antiretroviral (TAR) marca un antes y un después en la historia de esta enfermedad, logrando en muchos casos una esperanza de vida similar al de la población sin esta condición. De manera concomitante la transmisión del virus aún es frecuente, se estima que a nivel mundial durante el año 2021 cerca de 1,5 millones de personas se infectaron con el virus de inmunodeficiencia humana (VIH)18. Es debido a este importante aumento en el número de las PVVIH que se hace extremadamente relevante conocer las recomendaciones en relación a los esquemas de vacunación en estos pacientes6,18,19 (tabla 6).
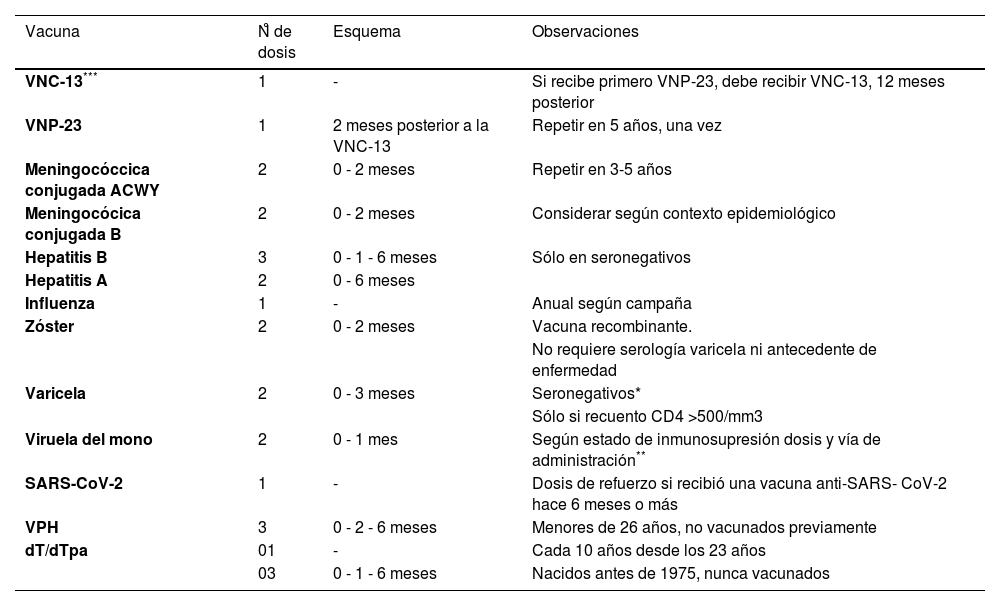
Recomendaciones de vacunas en adultos con infección por VIH
| Vacuna | N̊ de dosis | Esquema | Observaciones |
|---|---|---|---|
| VNC-13*** | 1 | - | Si recibe primero VNP-23, debe recibir VNC-13, 12 meses posterior |
| VNP-23 | 1 | 2 meses posterior a la VNC-13 | Repetir en 5 años, una vez |
| Meningocóccica conjugada ACWY | 2 | 0 - 2 meses | Repetir en 3-5 años |
| Meningocócica conjugada B | 2 | 0 - 2 meses | Considerar según contexto epidemiológico |
| Hepatitis B | 3 | 0 - 1 - 6 meses | Sólo en seronegativos |
| Hepatitis A | 2 | 0 - 6 meses | |
| Influenza | 1 | - | Anual según campaña |
| Zóster | 2 | 0 - 2 meses | Vacuna recombinante. |
| No requiere serología varicela ni antecedente de enfermedad | |||
| Varicela | 2 | 0 - 3 meses | Seronegativos* |
| Sólo si recuento CD4 >500/mm3 | |||
| Viruela del mono | 2 | 0 - 1 mes | Según estado de inmunosupresión dosis y vía de administración** |
| SARS-CoV-2 | 1 | - | Dosis de refuerzo si recibió una vacuna anti-SARS- CoV-2 hace 6 meses o más |
| VPH | 3 | 0 - 2 - 6 meses | Menores de 26 años, no vacunados previamente |
| dT/dTpa | 01 | - | Cada 10 años desde los 23 años |
| 03 | 0 - 1 - 6 meses | Nacidos antes de 1975, nunca vacunados |
VIH: virus de inmunodeficiencia humana; VNC-13: vacuna neumocócica conjugada-13; VNP-23: vacuna neumocócica polisacárida-23; LTCD4: linfoc- itos T CD4 (+); SARS-CoV-2: por sus siglas en inglés de Severe Acute Respiratory Syndrome Coronavirus-2; VPH: virus papiloma humano.
En términos fisiopatológicos, en la génesis de la infección por VIH se producen defectos en el sistema inmune tanto celular como humoral. Los mecanismos responsables de este deterioro a nivel inmunológico incluyen: infección y destrucción directa de los linfocitos T CD4, afectación cuanti y cualitativa de células Natural Killer (NK), defectos en la quimiotaxis y función de los monocitos y macrófagos y menor capacidad de respuesta imnunogénica de las células B, en comparación a la población sin VIH18.
Se debe considerar además que las PVVIH pueden estar expuestas a otras infecciones prevenibles asociadas a conductas sexuales de riesgo18,19.
Otras patologías crónicasExisten una amplia gama de patologías crónicas que condicionan mayor susceptibilidad y/o potencial gravedad en la presentación de infecciones inmunoprevenibles. Los mecanismos de disfunción inmunitaria asociados a estas enfermedades se centran en el estado inflamatorio crónico, con la desregulación inmunitaria que esto conlleva.
En esta sección abarcaremos: bronconeumopatías, cardiopatías, hepatopatías, afecciones renales (enfermedad renal crónica, síndrome nefrótico), diabetes mellitus, afecciones neurológicas, fístula de líquido céfalo-raquídeo no resuelta e implante coclear. Por fines prácticos, también incluiremos a los pacientes con asplenia o hiposplenia (asplenia funcional).
A continuación, mencionaremos algunos mecanismos fisiopatológicos que participan en el compromiso inmunológico en cada patología asociada6,14,15:
- -
Enfermedad pulmonar obstructiva crónica (EPOC): Deterioro en inmunidad celular con disminución de la citotoxicidad de las células NK y capacidad fagocítica reducida de monocitos, macrófagos y células polimorfonucleares (PMN). Se suma a lo anterior el compromiso inmunitario asociado al uso de corticoides sistémicos, ampliamente empleados en este grupo de pacientes (ver sección correspondiente en la presente revisión).
- -
Asma: Afectación principalmente de la inmunidad celular, con respuesta Th2 sobreactivada y Th1 disminuida. Se ha descrito además deterioro en la función de células inmunitarias, entre las que se incluye: células de Langerhans, células dendríticas, basófilos y mastocitos. También presentan respuestas inmunes innatas defectuosas y constituyen una población usuaria frecuente de corticoides sistémicos.
- -
Diabetes: Estos pacientes presentan trastornos inmunitarios tanto a nivel humoral como celular; además se ha descrito inmunidad innata disfuncional relacionado a la hiperglicemia persistente.
- -
Enfermedad renal crónica: Similar a lo observado en pacientes diabéticos, existe deterioro en la inmunidad innata y adaptativa (función celular y humoral). La necesidad de diálisis (peritoneal o hemodiálisis) aumenta la vulnerabilidad ante infecciones y se asocia a mayor compromiso inmunológico.
- -
Asplenia/Hipoesplenia: El bazo es un órgano fundamental en la fagocitosis, uno de los mecanismos principales contra bacterias encapsuladas. Es por esto que su ausencia o hipofunción constituyen factores de riesgo frente a infecciones bacterianas graves principalmente por Streptococcus pneumoniae, Haemophilus influenzae tipo B (Hib) y Neisseria meningitidis (serogupo B y serogrupos ACWY).
Las recomendaciones de inmunización para cada grupo de pacientes se describen en las tablas 7 and 8.
Recomendaciones de vacunas según patologías crónicas
| Patología | Vacunas |
|---|---|
| Bronco-neumopatías crónicas:EPOCAsmaBronquiectasiasNeumonitis alveolarEnfermedad respiratoria ocupacional o ambientalSarcoidosisFibrosis quísticaNeumonectomía parcial o total | Influenza anual (campaña)SARS-CoV-2VNC-13*+VNP-23**Haemophilus Influenzae tipo B (1 dosis)Hepatitis A (2 dosis/0 - 6 meses)Hepatitis B (3 dosis/0 - 1 - 6 meses)Anti varicela (2 dosis/0 - 3 meses)Herpes zóster (2 dosis/0 - 2 meses)dT/dTpa (1 dosis cada 10 años, vacunados previo) |
| Cardiopatía crónica:Insuficiencia cardíacaMiocardiopatíaHipertensión arterial | Influenza anual (campaña)SARS-CoV-2VNC-13*+VNP-23**Herpes zóster (2 dosis/0 - 2 meses)dT/dTpa (1 dosis cada 10 años, vacunados previo) |
| Hepatopatía crónica | Influenza anual (campaña)SARS-CoV-2VNC-13*+VNP-23**Hepatitis A (2 dosis/0 - 6 meses)Hepatitis B (3 dosis/0 - 1 - 6 meses)Meningocócica conjugada ACWY (1 dosis)Herpes zóster (2 dosis/0 - 2 meses)dT/dTpa (1 dosis cada 10 años, vacunados previo) |
| Nefropatía crónica | Influenza anual (campaña)SARS-CoV-2VNC-13*+VNP-23**Meningocócica conjugada ACWY (1 dosis)Haemophilus Influenzae tipo B (1 dosis)Hepatitis B (3 dosis/0 - 1 - 6 meses)Antivaricela (2 dosis/0 - 3 meses)Herpes zóster (2 dosis/0 - 2 meses)dT/dTpa (1 dosis cada 10 años, vacunados previo) |
| Enfermedades neurológicas:Accidente cerebrovascular secueladoParkinsonParálisis cerebral | Influenza anual (campaña)SARS-CoV-2VNC-13*+VNP-23**Haemophilus Influenzae tipo B (1 dosis)Herpes zóster (2 dosis/0 - 2 meses)dT/dTpa (1 dosis cada 10 años, vacunados previo) |
| Diabetes Mellitus | Influenza anual (campaña)SARS-CoV-2VNC-13*+VNP-23**Haemophilus Influenzae tipo B (1 dosis)Hepatitis A (2 dosis/0 - 6 meses)Hepatitis B (3 dosis/0 - 1 - 6 meses)Meningocócica conjugada ACWY (1 dosis)Antivaricela (2 dosis/0 - 3 meses)Herpes zóster (2 dosis/0 - 2 meses)dT/dTpa (1 dosis cada 10 años, vacunados previo) |
| Fístula LCR/Implante coclear | Influenza anual (campaña)SARS-CoV-2VNC-13*+VNP-23**Haemophilus Influenzae tipo B (1 dosis)Meningocóccica conjugada ACWY (1 dosis)Herpes zóster (2 dosis/0 - 2 meses)dT/dTpa (1 dosis cada 10 años, vacunados previo) |
EPOC: enfermedad pulmonar obstructiva crónica; SARS-CoV-2: por sus siglas en inglés de Severe Acute Respiratory Syndrome Coronavirus-2; VNC-13: vacuna neumocócica conjugada-13; VNP-23: vacuna neumocócica polisacárida-23; meningocócica conjugada ACWY: serogrupos A, C, W e Y.
Recomendaciones de vacunas pacientes esplenectomizados
| Vacuna | Dosis | Observaciones |
|---|---|---|
| VNC-13 | 1 | 2 semanas antes de la cirugía |
| VNP-23 | 1 | 2 meses posterior a VNC-13. Revacunar por una sola vez a los 5 años |
| Haemophilus influenzae tipo B (conjugada) | 1 | |
| Meningocócica conjugada ACWY | 2 | Revacunar en 3 - 5 años(0 - 2 meses) |
| Meningocócica conjugada B | 2 | (0 - 2 meses) |
| Influenza | 1 | Anual (campaña) |
| SARS-CoV-2 | 1 | Dosis de refuerzo si recibió una vacuna anti-SARS-CoV-2 hace 6 meses o más |
| Herpes zóster | 2 | Vacuna recombinanteNo requiere serología varicela ni antecedente de enfermedad |
| dT/dTpa | 0103 | Cada 10 años desde los 23 añosNacidos antes de 1975, nunca vacunados |
VNC-13:vacuna neumocócica conjugada-13; VNP-23: vacuna neumocócica polisacárida-23; SARS-CoV-2: por sus siglas en inglés de Severe Acute Respiratory Syndrome Coronavirus 2; Meningocócica conjugada ACWY: serogrupos A, C, W e Y.
El envejecimiento del sistema inmune o inmunosenescencia afecta la respuesta inmune humoral y celular. Hacen de esta población un grupo más expuesto a enfermedades inmunoprevenibles.
Alteraciones como desbalance entre mecanismos pro y antiinflamatorios, menor producción y diversificación de linfocitos T, disminución de la síntesis de anticuerpos, entre otros, son los mecanismos responsables20,21.
En estos pacientes, en relación al riesgo de neumonía neumocócica, este se incrementa con la edad y con la presencia de comorbilidades22. Además, al igual que con las infecciones por influenza, en caso de enfermedad, presentan cuadros más graves asociados a mayor mortalidad.
Ante este contexto, es relevante reforzar la importancia de la inmunización en estos pacientes (tabla 9).
Recomendaciones de vacunas personas mayores (65 años y más)
| Vacunas | Dosis | Observaciones |
|---|---|---|
| VNP-23 | 1 dosis | Revacunación a los 5 años según patologías crónicas |
| Influenza | 1 dosis | Campaña anual |
| SARS-CoV-2 | 1 dosis | Dosis de refuerzo si recibió una vacuna anti-SARS-CoV-2 hace 12 meses o más |
| Herpes zóster | 2 dosis | Vacuna recombinante Considerar en >50 años. No requiere serología varicela ni antecedente de enfermedad |
| Virus respiratorio sincicial | 1 dosis | Para todos los mayores de 75 años Considerar en >60 años con comorbilidades o institucionalizados |
VNP-23: vacuna antineumocócica polisacárida 2; SARS-CoV-2: por sus siglas en inglés de Severe Acute Respiratory Syndrome Coronavirus 2.
Durante la gestación los diversos cambios fisiológicos hormonales provocan variaciones en la respuesta inmunitaria; el aumento en las concentraciones de estradiol induce mayor actividad de las respuestas tipo Th2 y disminución de las Th1. Otros componentes de la respuesta inmunitaria, como la actividad fagocítica, se mantienen e, incluso, se pueden elevar durante el segundo y tercer trimestre del embarazo. La alteración en la inmunidad celular explica la respuesta subóptima a ciertas infecciones virales, como la influenza. Es por esto que las embarazadas tienen mayor riesgo de sufrir complicaciones graves relacionadas con la influenza, e infección por SARS-CoV-2, en comparación a las mujeres no embarazadas23.
Además, la vacunación durante el embarazo, es una forma efectiva de disminuir la morbimortalidad en los recién nacidos y lactantes menores a través del traspaso de anticuerpos placentarios al feto, protegiéndolo en sus primeros meses de enfermedades con alta letalidad, como el coqueluche grave. Esto es conocido como la estrategia capullo, implementada en Chile durante el 2012-201324. A continuación, se exponen las vacunas recomendadas en todas las embarazadas (tabla 10).
Recomendaciones de vacunas en embarazadas
| Vacunas | Dosis | Observaciones |
|---|---|---|
| dTpa | 1 dosis | A partir de la semana 28 de gestación, hasta el puerperio inmediato |
| Influenza | 1 dosis | Desde cualquier mes de gestación |
| SARS-CoV-2 | 1 dosis | Desde cualquier mes de gestación |
dTpa: Difteria, tétanos, tos ferina; SARS-CoV-2: por sus siglas en inglés de Severe Acute Respiratory Syndrome Coronavirus 2.
Existen situaciones especiales en el embarazo donde según la evaluación riesgo/beneficio se recomendarán vacunas adicionales a las recién mencionadas. Situaciones como: viajes donde exista alguna enfermedad endémica (fiebre amarilla, fiebre tifoidea, poliomielitis), o en determinadas situaciones de riesgo, en donde se requerirá la administración de vacunas contra: hepatitis A, hepatitis B, neumococos (conjugada y polisacárida), meningococos (conjugada y polisacárida) o rabia25,26.
ConclusionesLas vacunas son una medida eficaz para la reducción de la mortalidad y las secuelas relacionadas a las enfermedades inmunoprevenibles. En Chile contamos con el PNI, constantemente modificado a modo de asegurar el acceso seguro y gratuito a la población general, determinado un impacto significativo, indiscutible, a nivel de salud pública del país.
Las poblaciones especiales portadoras de condiciones clínicas que determinan deficiencias en su respuesta inmunológica han presentado un aumento constante, apoyado en el aumento de la expectativa de vida. Lo anterior determina la necesidad de conocer las bases a modo de otorgar un enfoque personalizado y específico en términos de la prevención y manejo oportuno de un número cada vez mayor de enfermedades inmunoprevenibles.
Declaración de conflictos de intereses:Los autores declaran que el Dr. Herrera ha recibido honorarios por parte de GSK para actividades (charlas y asesorías) de vacunas en el adulto.