The aim of the present study is to examine the possible effect de dexmedetomidine on the development of morphine tolerance in rats including nociception, morphine analgesia, apoptosis, oxidative stress, and tumour necrosis factor (TNF)/ interleukin-1 (IL-1) pathways.
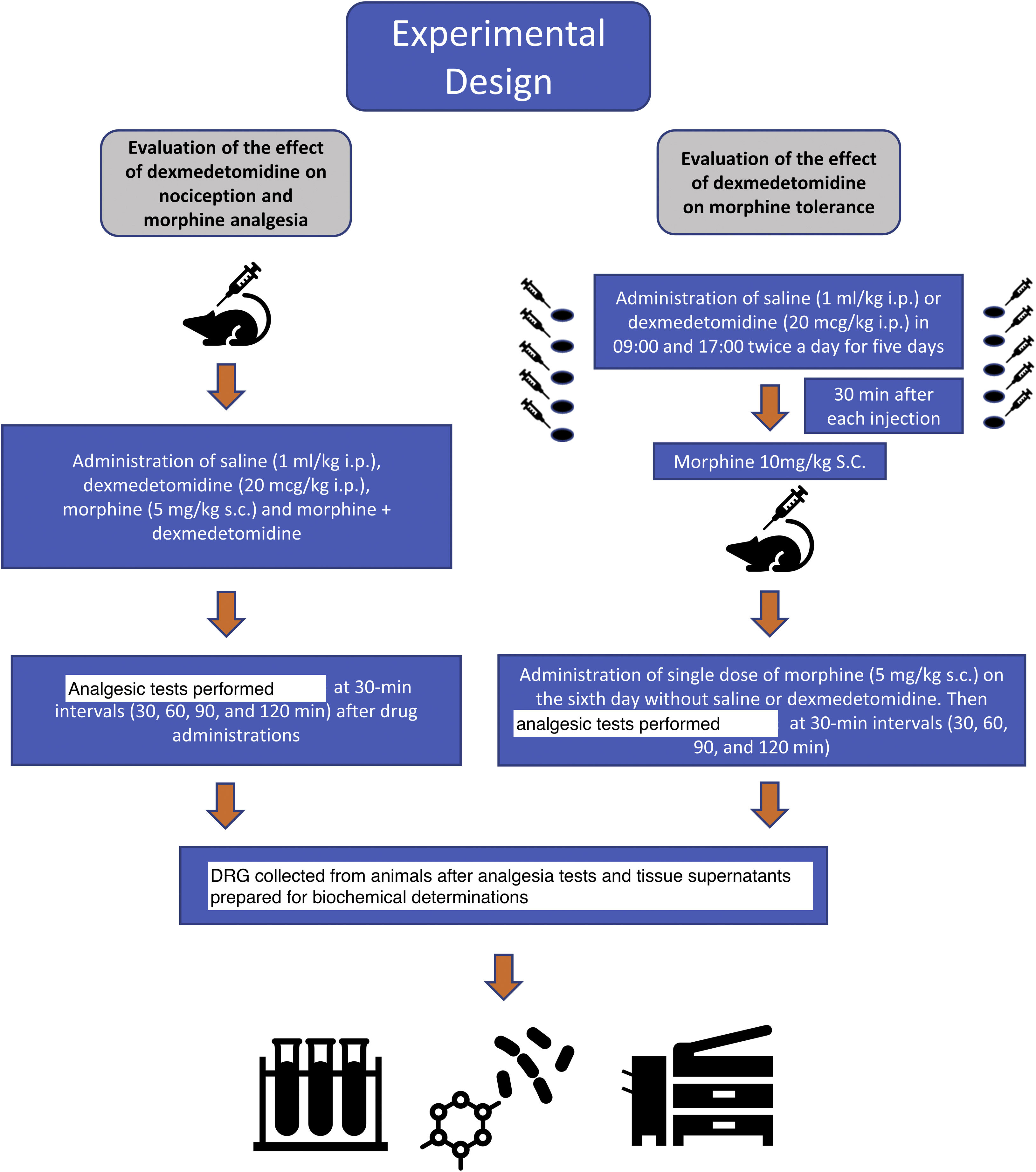
Materials and methodsIn this study, 36 Wistar Albino (225–245 g) rats were used. Animals were divided into 6 groups: saline (S), 20 mcg/kg dexmedetomidine (D), 5 mg/kg morphine (M), M + D, morphine tolerance (MT), and MT + D. The analgesic effect was measured with hot plate and tail-flick analgesia tests. After the analgesia tests, the dorsal root ganglia (DRG) tissues were excised. Oxidative stress parameters [total antioxidant status (TAS), total oxidant status (TOS)], TNF, IL-1 and apoptosis enzymes (Caspase-3, Caspase-9), were measured in DRG tissues.
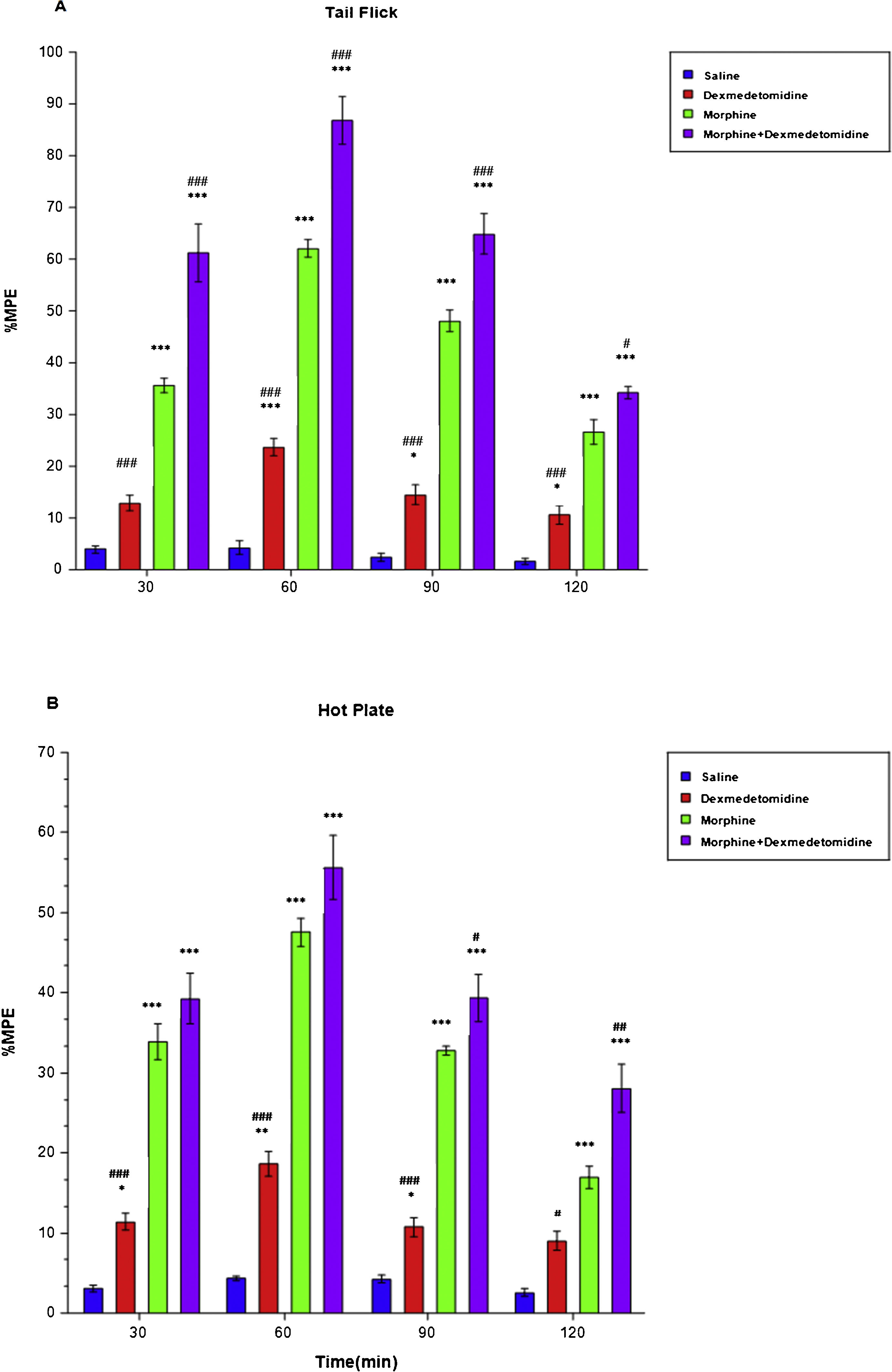
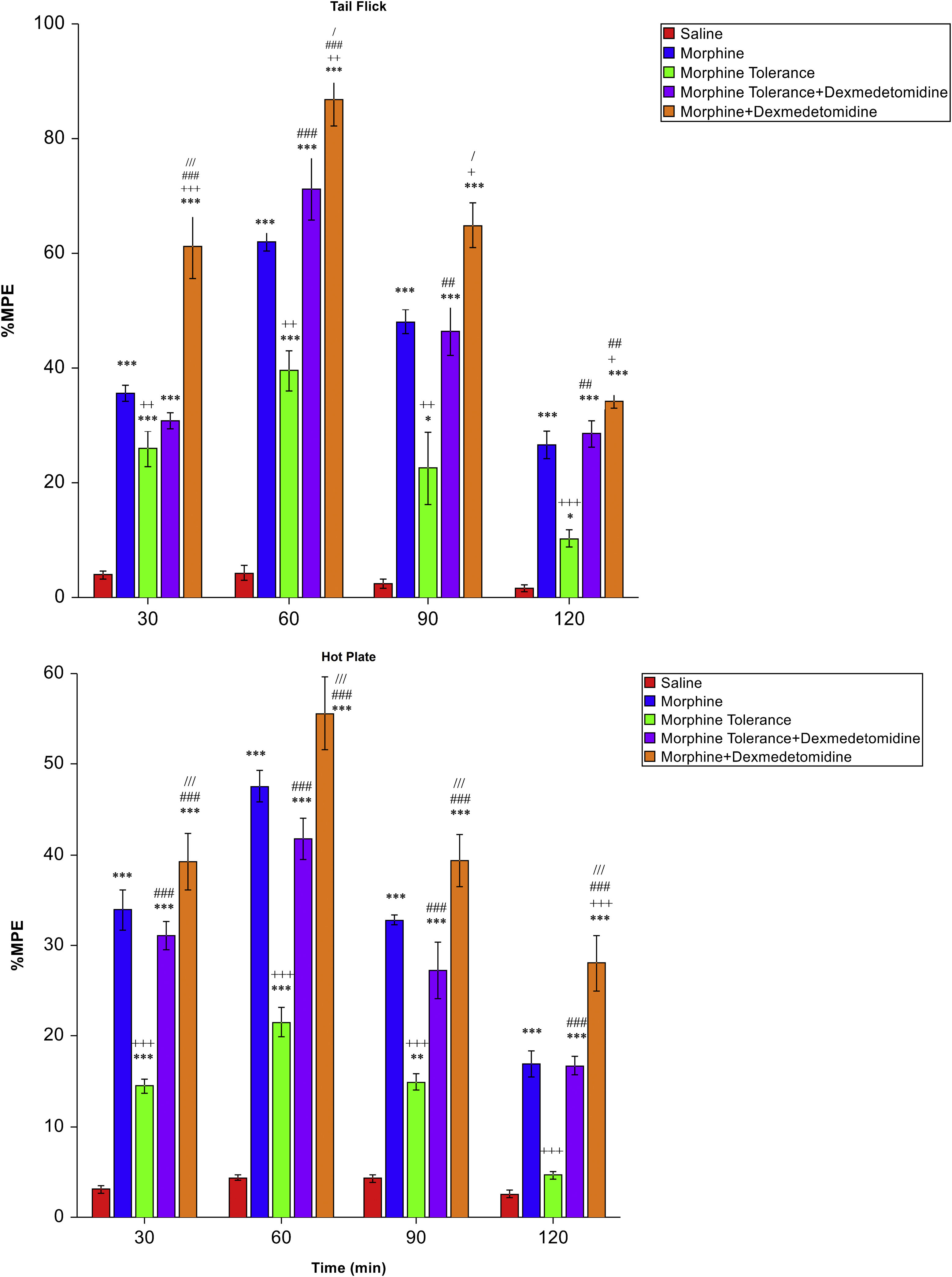
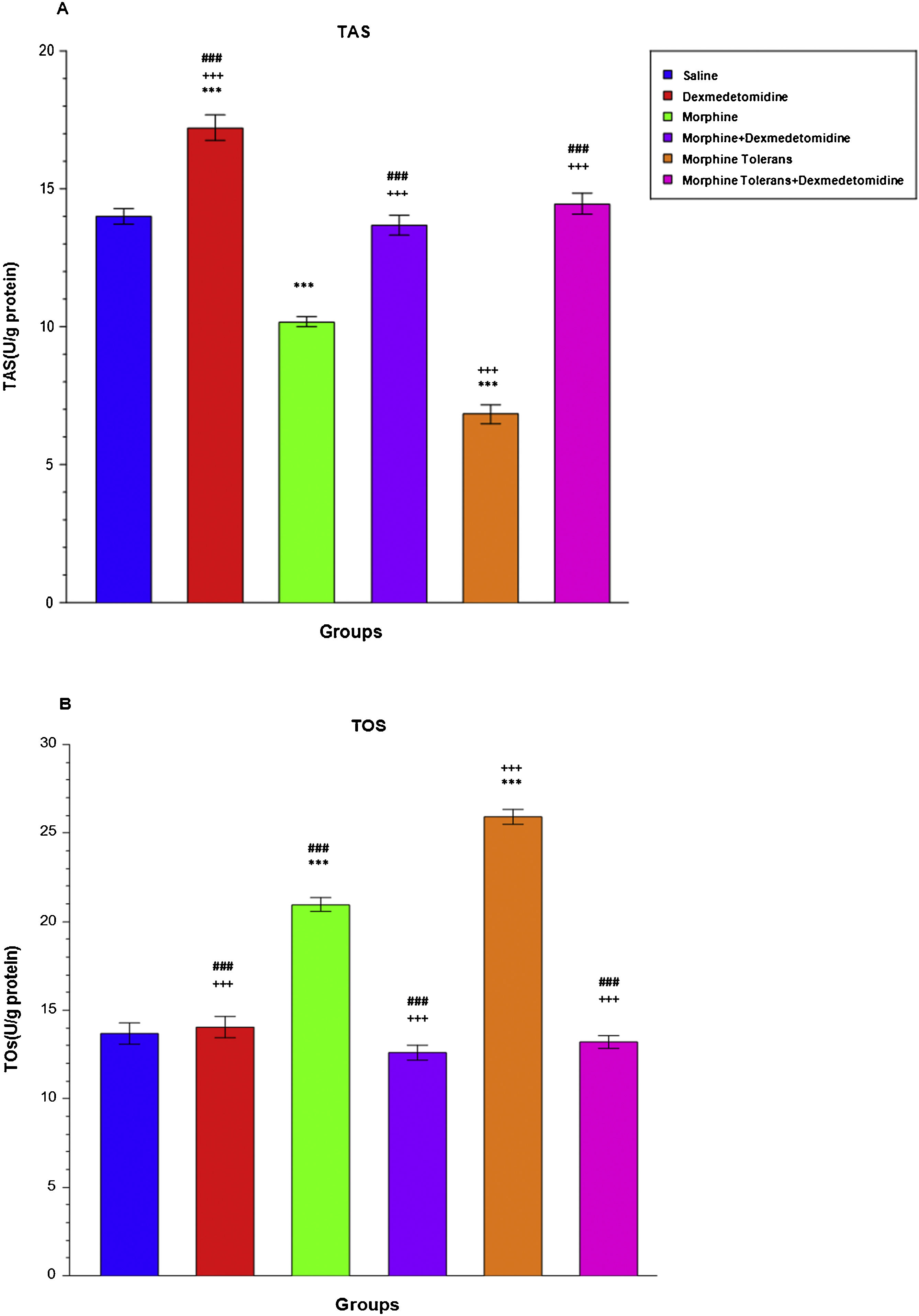
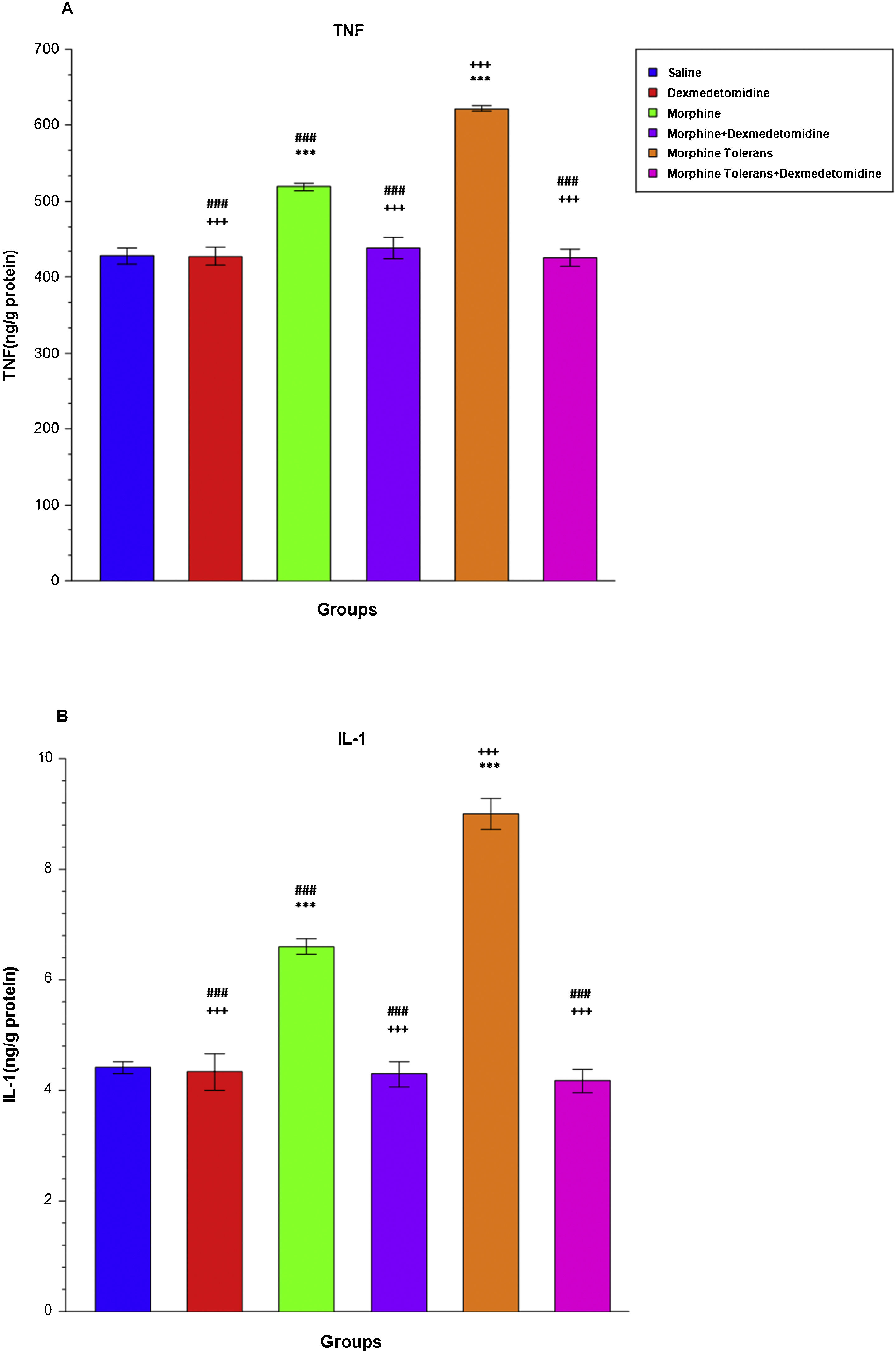
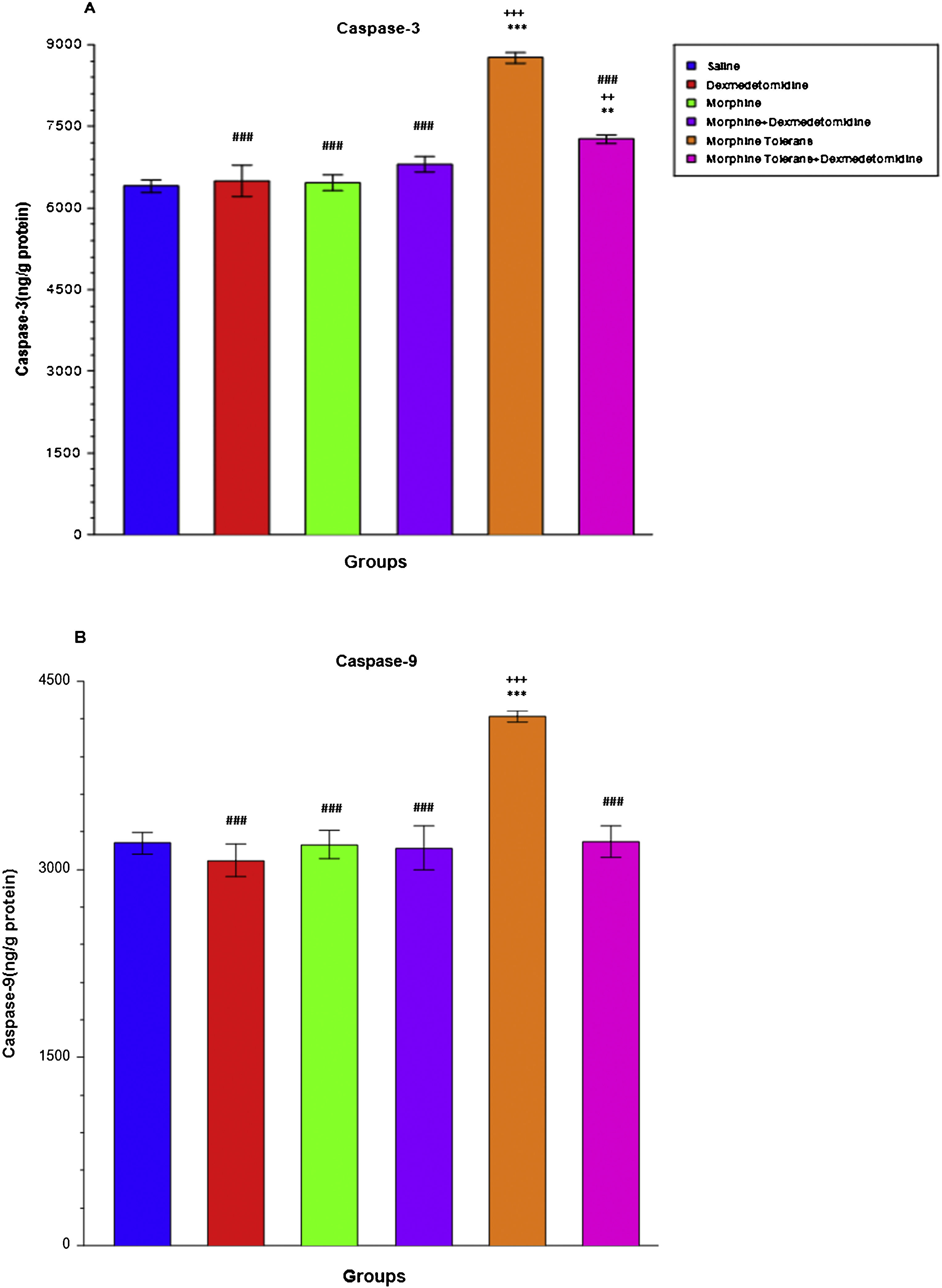
ResultsDexmedetomidine showed an antinociceptive effect when given alone (p < 0.05 to p < 0.001). In addition, dexmedetomidine increased the analgesic effect of morphine (p < 0.001), and also decreased the tolerance to morphine at a significant level (p < 0.01 to p < 0.001). Moreover, it decreased oxidative stress (p < 0.001) and TNF/IL-1 levels when given as an additional drug of single-dose morphine and morphine tolerance group (p < 0.001). Furthermore, dexmedetomidine decreased Caspase-3 and Caspase-9 levels after tolerance development (p < 0.001).
ConclusionDexmedetomidine has antinociceptive properties, and it increases the analgesic effect of morphine and also prevents tolerance development. These effects probably occur by the modulation of oxidative stress, inflammation and apoptosis.
El objetivo del presente estudio es examinar el posible efecto de dexmedetomidina en el desarrollo de tolerancia a la morfina en ratas, incluyendo nocicepción, analgesia con morfina, apoptosis, estrés oxidativo, y las vías del factor de necrosis tumoral (TNF)/ interleucina-1 (IL-1).
Materiales y métodosEn este estudio, se utilizaron 36 ratas Wistar Albino (225–245 g) dividiéndose a los animales en 6 grupos: solución salina (S), 20 mcg/kg de dexmedetomidina (D), 5 mg/kg de morfina (M), M + D, tolerancia a la morfina (MT), y MT + D. El efecto analgésico se midió mediante las pruebas analgésicas de placa caliente (hot plate) y de retirada de la cola (tail flick). Tras dichas pruebas, se extirparon los ganglios de la raíz dorsal (GRD), y se midieron en los tejidos de los mismos los parámetros del estrés oxidativo [estado antioxidante total (TAS), estado oxidante total (TOS)], TNF, IL-1 y enzimas de la apoptosis (Caspasa-3, Caspasa-9).
ResultadosDexmedetomidina reflejó un efecto antinociceptivo al administrarse en solitario (p < 0,05 a p < 0,001). Además, dexmedetomidina incrementó el efecto analgésico de la morfina (p < 0,001), y también redujo la tolerancia a la morfina a un nivel significativo (p < 0,01 a p < 0,001), reduciendo también los niveles de estrés oxidativo (p < 0,001) y TNF/IL-1 al administrarse como fármaco adicional al grupo de dosis única de morfina y tolerancia a la morfina (p < 0,001). Además, dexmedetomidina redujo los niveles de Caspasa-3 y Caspasa-9 tras el desarrollo de tolerancia (p < 0,001).
ConclusiónDexmedetomidina tiene propiedades antinociceptivas, e incrementa el efecto analgésico de la morfina, previniendo también el desarrollo de tolerancia. Estos efectos se producen probablemente debido a la modulación del estrés oxidativo, la inflamación y la apoptosis.