Las tasas de mortalidad por intoxicación con cianuro son significativamente altas debido a los efectos devastadores que esta sustancia química puede desencadenar en el organismo, comprometiendo rápidamente funciones vitales. Actualmente, dentro de las estrategias de tratamiento, se destaca el soporte circulatorio y ventilatorio, junto con la administración de antídotos específicos, los cuales son de difícil acceso y no suelen estar disponibles en la mayoría de los hospitales.
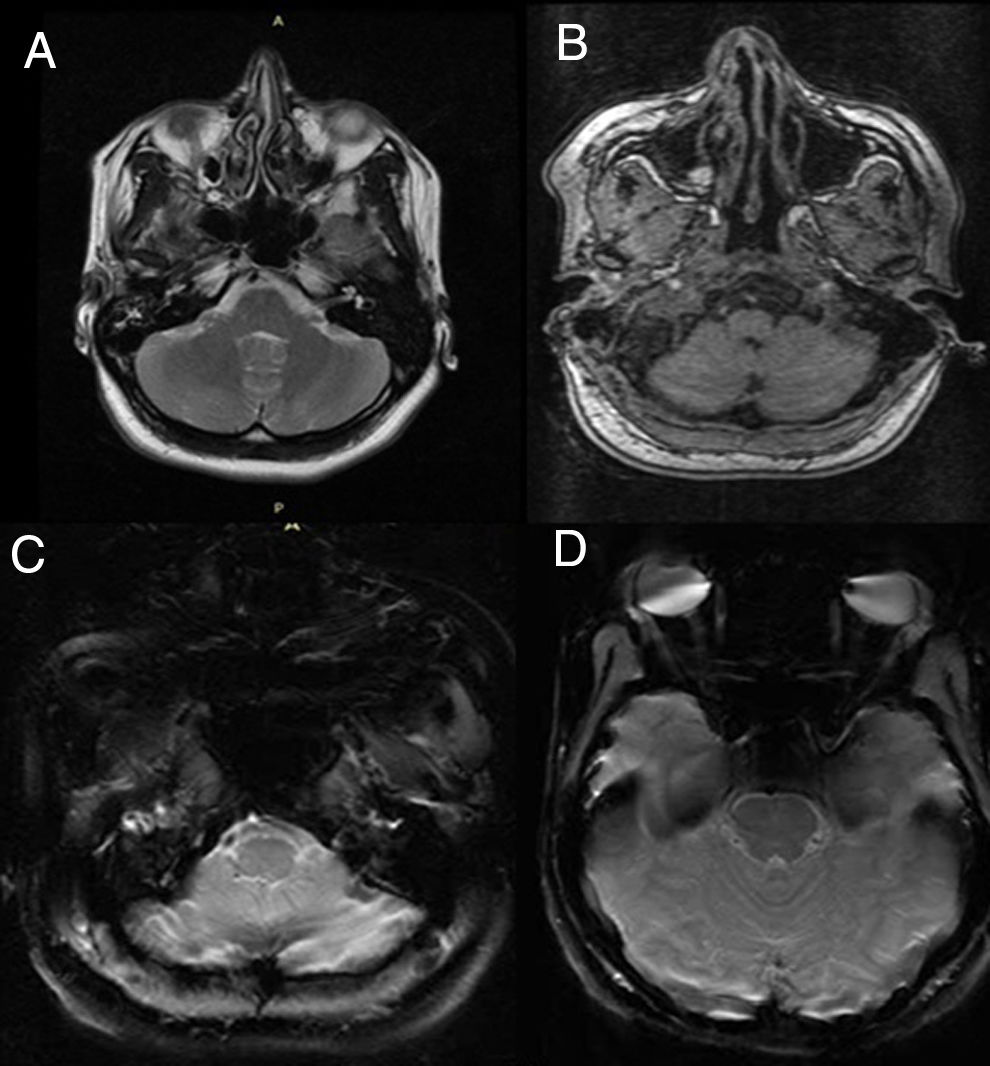
A pesar de que el azul de metileno ha sido considerado durante mucho tiempo como una opción para contrarrestar los efectos de la intoxicación por cianuro, la investigación sobre sus mecanismos de acción y eficacia ha sido limitada durante décadas, dejando de lado sus efectos protectores y propiedades únicas redox en complejos mitocondriales y el ciclo de Krebs. Se presenta un caso clínico de una paciente con intoxicación aguda por cianuro de potasio que respondió al tratamiento antidotal con azul de metileno; no obstante, desarrolló un accidente cerebrovascular cerebeloso) como consecuencia de la intoxicación, sin presentar repercusiones clínicas aparentes.
Mortality rates from cyanide poisoning are significantly high due to the devastating effects that this chemical substance can trigger in the body, quickly compromising vital functions. Currently, within the treatment strategies, circulatory and ventilatory support stands out, along with the administration of specific antidotes, which are difficult to access and are not usually available in most hospitals.
Although methylene blue has long been considered an option to counteract the effects of cyanide poisoning, research on its mechanisms of action and effectiveness has been limited for decades, leaving aside its protective effects and properties. unique redox in mitochondrial complexes and the Krebs cycle. A clinical case is presented of a patient with acute potassium cyanide poisoning who responded to antidotal treatment with methylene blue; However, she developed a cerebellar stroke as a consequence of the poisoning, despite having no apparent clinical manifestations.
Artículo
Socios de la Asociación de Medicina Crítica y Cuidado Intensivo
Para acceder a la revista
Es necesario que lo haga desde la zona privada de la web de la AMCI, clique aquí
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora