El envejecimiento de la población ha aumentado el número de cirugías sobre la válvula aórtica. Durante los últimos 20años la técnica quirúrgica ha evolucionado hacia una menor agresión corporal, apareciendo nuevos tipos de cirugía aórtica mínimamente invasiva (CMIAo). De todas estas técnicas, la hemiesternotomía superior (HES), o miniesternotomía, se ha convertido en la más utilizada, seguida por la minitoracotomía anterior derecha (MTA). Ambas, comparadas con la cirugía convencional, han demostrado una recuperación más rápida, mejor resultado cosmético, menor estancia hospitalaria y en UCI, mejor función respiratoria, menor pérdida de sangre y transfusiones, e incluso menor mortalidad precoz y tardía. A pesar de estos avances, su uso no se ha extendido definitivamente debido a un incremento en los tiempos de isquemia y de circulación extracorpórea (CEC) necesarios en estos procedimientos más complejos. La aparición de las prótesis sin sutura «Sutureless» de nueva generación puede solventar este contratiempo al reducir hasta en un 43% los tiempos de isquemia y CEC, y permitir que la CMIAo se expanda y sea una alternativa real a las válvulas transcatéter (TAVI) en los pacientes de alto riesgo operables. A pesar de que son recomendables ensayos clínicos prospectivos aleatorizados para confirmar estos datos, existe suficiente evidencia disponible como para considerar la CMIAo (sobre todo la HES) como el gold standard actual para la sustitución valvular aórtica aislada.
The aging of the population has led to an increase in the number of surgeries on the aortic valve. During the past 20years the surgical technique has progressed to less aggressive techniques, with new types of minimally invasive aortic valve surgery (MIAVR) emerging. Of these techniques, the upper hemi-sternotomy (UHS) or mini-sternotomy has become the most commonly used, followed by the right anterior thoracotomy (RAT). Compared with conventional surgery, both have shown a faster recovery, better cosmetic results, shorter hospital and ICU stay, better respiratory function, reduced blood loss and transfusions, as well as lower early and late mortality. Despite these advances, their use has not been definitively extended, due to an increase in the ischaemia and cardiopulmonary bypass (CPB) times needed in these more complex procedures. The emergence of new generation sutureless prosthesis can overcome this setback by reducing the ischemic and CPB by up to 43%, and allows MIAVR to expand and become a real alternative to the transcatheter valves (TAVI) in high risk operable patients. Although prospective randomised controlled trials are required to confirm these data, there is sufficient available evidence to consider MIAVR (especially UHS) as the current reference method for isolated aortic valve replacement.
Durante las últimas 2décadas, como consecuencia del envejecimiento progresivo de la población, el número de cirugías sobre la válvula aórtica debido a enfermedad degenerativa se ha multiplicado1, a la vez que ha disminuido la mortalidad como consecuencia en las mejoras técnicas2. La cirugía convencional (CC) a través de esternotomía media para implantar prótesis biológicas o mecánicas representa hoy en día el gold standard en el tratamiento de esta valvulopatía. A pesar de estas mejoras, se ha producido un gran desarrollo durante estos 20años hacia la utilización de incisiones más pequeñas y nuevas tecnologías (válvulas transcatéter [TAVI], Heart Port, válvulas Sutureless) para minimizar la agresión quirúrgica y mejorar los resultados en pacientes de alto riesgo, reduciendo los tiempos de isquemia y de circulación extracorpórea (CEC), mejorando la morbimortalidad, reduciendo costes y respondiendo a las exigencias y expectativas de pacientes y cardiólogos.
En 2008, una declaración científica de la American Heart Association3 definió la cirugía mínimamente invasiva cardíaca (CMI) como «una pequeña incisión en el tórax que no incluya una esternotomía media completa convencional». Así, la CMI no debe asociarse a un único procedimiento, sino que se trata de un «concepto o nueva filosofía» que requiere un entrenamiento y una estrategia específica para disminuir la agresión del acto quirúrgico4 pero manteniendo como mínimo una eficacia, una calidad y una seguridad similar a la CC.
Repaso históricoLa primera CMI sobre la válvula aórtica (CMIAo) se realizó en 1996, mediante acceso paraesternal derecho de unos 10cm, en la Cleveland Clinic por los doctores Cosgrove y Sabik5, con desarticulación de cartílagos 3.° y 4.°, ligadura del paquete mamario derecho y canulación periférica. Fue abandonada progresivamente debido al alto número de herniaciones pulmonares.
En 1997, el mismo doctor Cosgrove introdujo la esternotomía transversa por 2.° espacio intercostal, técnica adoptada por algunos grupos en España y que fue progresivamente abandonada, ya que requería ligadura bilateral de ambos paquetes mamarios y podía provocar inestabilidad esternal residual6,7.
En este mismo año, los doctores Cohn8 y Svensson9 introdujeron la CMIAo a través de hemiesternotomía parcial superior (HES o miniesternotomía) en T invertida y J, respectivamente, ampliando por 3.er o 4.° espacio intercostal, con canulación central o periférica, demostrando la seguridad de estos procedimientos respecto a la CC.
A finales de 1997 también se publicó CMIAo a través de minitoracotomía anterior derecha (MTA) con videoscopia (Dr. Benetti, Buenos Aires)10, si bien la primera publicación al respecto fue realizada por cirujanos del Texas Heart Center en 1993 (Drs Rao y Kumar)11, aunque con incisiones de toracotomía derecha muy superiores en longitud a las realizadas a partir de 1997 como para considerarlo CMI.
De todas estas técnicas aparecidas en los últimos 20años, la HES se ha convertido en la más utilizada (en sus numerosas variantes en T, J, por 3.er o 4.° espacio intercostal derecho [EICD], etc.), seguida por la MTA. Ambas, comparadas con la CC, han demostrado una recuperación más rápida, mejor resultado cosmético, menor estancia hospitalaria y en UCI, mayor estabilidad esternal, mejor función respiratoria y menor pérdida de sangre, transfusiones e infecciones, como veremos más adelante.
Miniesternotomía y minitoracotomía. ¿Para qué complicarse la vida?La HES, o miniesternotomía, es en la actualidad la CMIAo más frecuentemente utilizada. Existen diferentes técnicas, si bien la más utilizada es mediante apertura en J por 3.er o 4.° EICD, canulación central en aorta y AD o cava superior, con unos 8-10cm de incisión en piel.
Existen infinidad de artículos —la mayoría retrospectivos— y múltiples revisiones que demuestran la seguridad de la HES versus la CC. Ante la imposibilidad de comentarlos todos, expondremos los más relevantes12-16.
En nuestro medio, la evidencia publicada del grupo del Hospital General de Valencia12 mediante un estudio retrospectivo aprecia menor estancia en UCI (un día) y hospitalaria (2días), menos complicaciones respiratorias y menos mortalidad, si bien advierten con cautela de estos resultados al ser una muestra pequeña de 83HES vs 532CC. Sorprendentemente es el único estudio en donde el grupo HES presenta menores tiempos de CEC e isquemia que el grupo CC.
En un metaanálisis de 4.586 pacientes (2.054HES vs 2.532CC de 28 estudios diferentes [4 trials]), Brown et al.13 demostraron menor tiempo de ventilación mecánica (2h menos), clara tendencia a una menor mortalidad a pesar de la no significación estadística (p=0,06; IC95%: 0,5-1,02), menor estancia en UCI (12h) y hospitalaria (un día), así como menor pérdida de sangre durante las primeras 24h en favor del grupo HES, a expensas de un mayor tiempo de CEC e isquemia (12 y 8min de media, respectivamente).
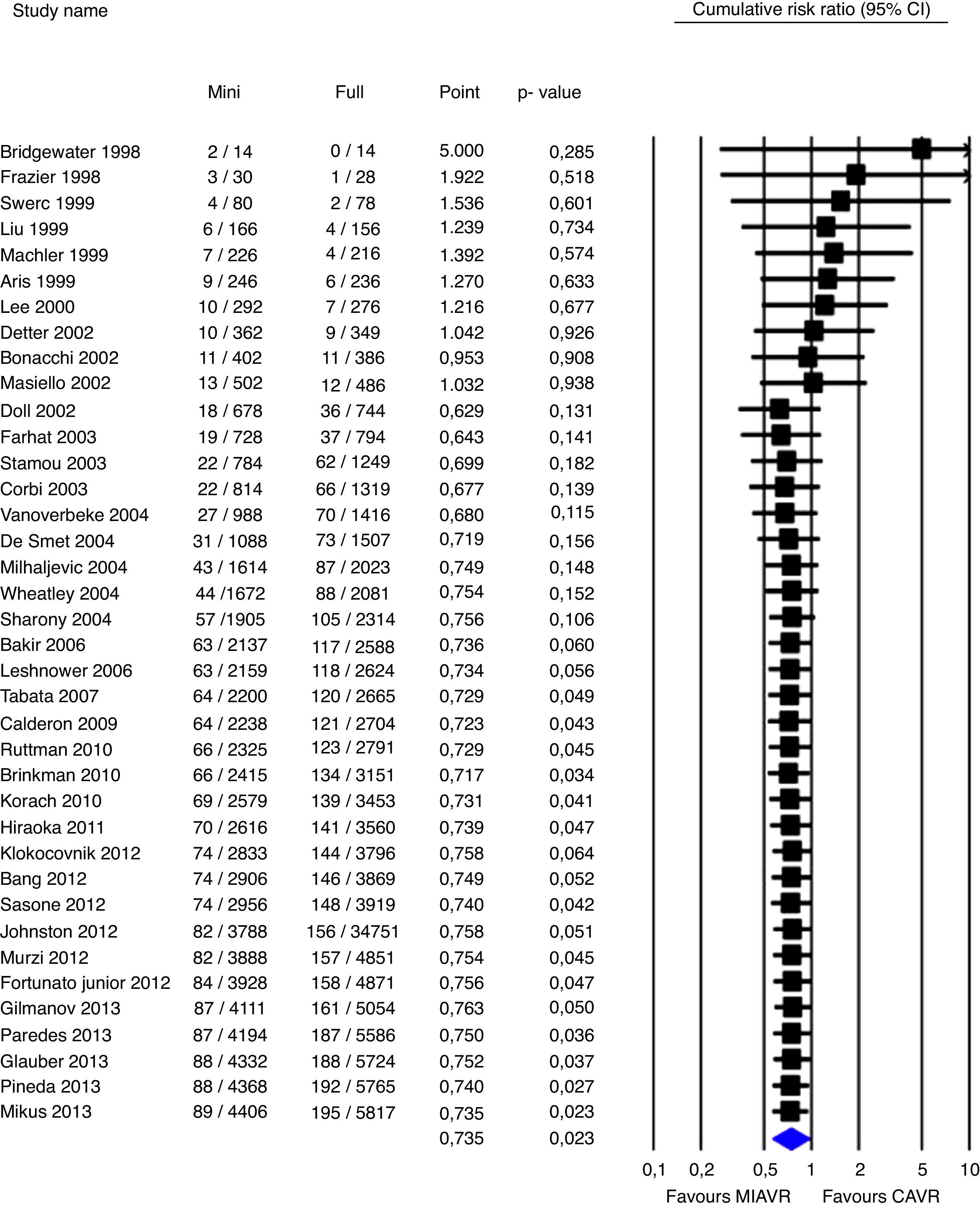
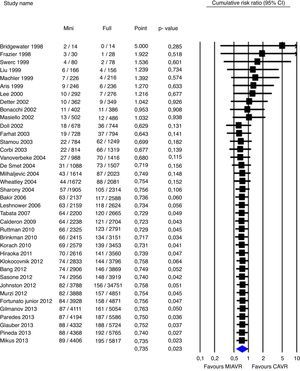
En 2014, Kevin Phan publicó un nuevo metaanálisis14 que incluye 50 estudios con 7 trials, 8 estudios con puntuación de propensión y 35 retrospectivos, de 5.162CMIAo (90%HES) vs 7.624 CC. Sin presentar diferencias preoperatorias entre grupos, dicho estudio apreció menor mortalidad en el grupo HES (1,9%) vs CC (3,3%) (p<0,05 global), menos transfusiones, menor estancia en UCI (0,6días) y hospitalaria (1,3días), similar frecuencia de infarto cerebral, fallo renal y fallo respiratorio. Como contrapartida fueron precisos 8min más de isquemia y 10 de CEC. En la figura 1 podemos apreciar como desde el año 2002 existe una reducción de la mortalidad constante a favor del grupo CMIAo, probablemente debido a la estandarización de la técnica y mejora de cuidados postoperatorios.
Mortalidad perioperatoria acumulada en pacientes de CMIAo vs CC. Los cuadrados sólidos denotan el riesgo relativo acumulado y son proporcionales a su peso en el estudio del metaanálisis. Las líneas horizontales representan los intervalos de confianza al 95%. El diamante azul expresa el RR ponderado, siendo sus puntas laterales los límites de intervalo de confianza al 95%.
Adaptado de Phan et al.14, con permiso de Elsevier®.
En 2015, el grupo de M. Borger15, en un estudio de 477 pares de pacientes pareados mediante puntuación de propensión, encontró una mayor supervivencia estadísticamente significativa tanto precoz (0,4% HES vs 2,3% CC, p=0,013) como tardía a 8años (HES 77,7±4,7% vs 72,8±3,1% CC, p=0,034), siendo la HES un factor independiente de supervivencia a largo plazo (OR=0,47; IC95%: 0,26-0,87), a expensas de solo 3-5min extra de tiempos de isquemia y CEC.
Estos hallazgos han fomentado progresivamente la adopción de estas técnicas de CMIAo, sobre todo de la HES, como técnica de elección en muchos centros de nuestro país debido a su relativamente corta curva de aprendizaje, seguridad, simpleza y fácil reconversión en caso de complicación. Sin embargo, aún son pocos los centros que utilizan la MTA como técnica de elección en la CMIAo. Esta técnica presenta una mayor curva de aprendizaje y gasto inicial debido a la necesidad de material quirúrgico específico. El grupo de Massa, con M. Glauber a la cabeza, tiene publicados resultados excelentes a 10años16, con 484 pacientes, tiempos medios de isquemia y CEC de 81 y 116min, 2% de reconversiones a CC, 6días de estancia media y 95% de supervivencia a 27meses, con amplia satisfacción por parte de los pacientes.
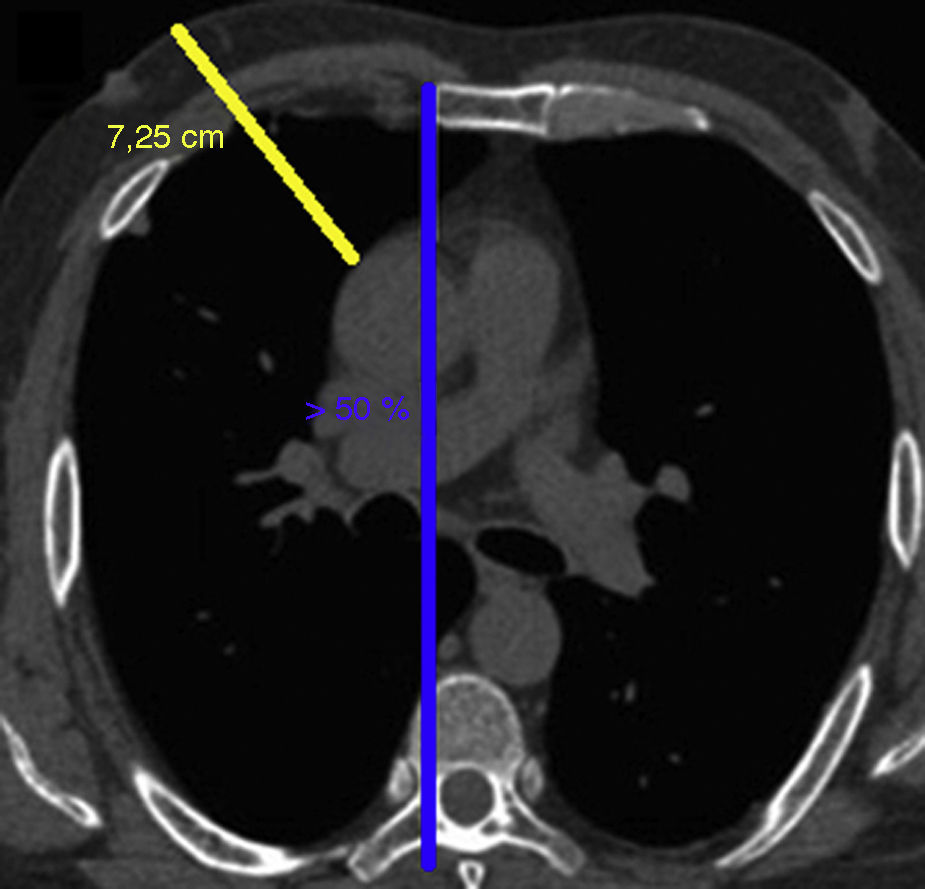
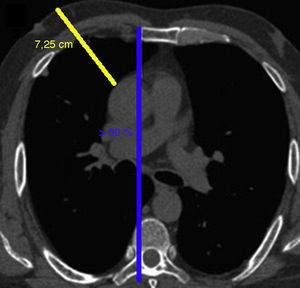
En este tipo de cirugía MTA es imprescindible realizar una tomografía computarizada (TC) sin contraste para evaluar una serie de relaciones anatómicas y mediciones para ver la factibilidad del procedimiento (fig. 2). Pueden intervenirse mediante MTA los pacientes en los que:
- a)
Si >50% de la aorta excede el borde esternal derecho, medida a nivel de la bifurcación de la arteria pulmonar.
- b)
La distancia desde la piel hasta la aorta es <10cm
- c)
El ángulo entre el eje de la aorta y su línea vertical es mayor de 45 grados, para evitar aortas verticalizadas.
- d)
No presenten otra contraindicación, como cirugía cardíaca previa, adherencias pleurales por cirugía pulmonar derecha previa, dilatación aórtica (>40-45mm), tórax profundos, deformidades torácicas o calcificaciones aórticas.
A día de hoy únicamente existen 2 estudios comparativos específicos sobre este tema. Uno es del grupo de Glauber17, que aprecia pequeñas diferencias comparando 251MTA y 155HES, presentando la primera menos FA postoperatoria (19,5% vs 34,2%; p<0,01), ventilación mecánica, estancia en UCI y hospitalaria (un día). Concluye que la MTA provoca menor morbimortalidad y se asocia a menor estancia hospitalaria, sin diferencias en los tiempos de CEC e isquemia.
El otro gran trabajo sobre este aspecto es un metaanálisis bayesiano, del Dr. Phan18, que utiliza este ardid estadístico para realizar una comparación entre grupos de manera indirecta, a partir de los datos recopilados de un metaanálisis anterior. Este trabajo concluye que no existen diferencias entre grupos, excepto mayores tiempos de CEC e isquemia en el grupo MTA (p<0,05). Serían precisos estudios aleatorizados para comprobar la supuesta superioridad en cuanto a menor morbimortalidad de la MTA, tal y como predican algunos grupos.
¿Válvulas transcatéter o cirugía miniinvasiva aórtica?Estos últimos años se han introducido en el mercado 3 tipos de válvulas de nueva generación, denominadas Sutureless o rapid deployment aortic valves (RDV): la Enable® (Medtronic, recientemente retirada del mercado), la Perceval® (Sorin Biomedica Cardio Srl, Sallugia, Italia; Sutureless) y la Edwards Intuity® (Edwards Lifesciences, Irvine, CA, EE.UU.; RDV).
El uso de estas válvulas ha mejorado los resultados quirúrgicos tanto de la CC como de la CMIAo19,20. Se redujeron los tiempos de CEC e isquemia en cerca de un 43% para MTA y de un 35% para HES, lo que puede facilitar y estandarizar la técnica de CMIAo, con solo un 1,8% de aparición de leaks perivalvulares, los cuales se asocian a un aumento del riesgo de mortalidad tardía.
En un reciente studio de Santarpino et al.21, el único que compara TAVI vs HES-Sutureless (HES-S), de 244 pacientes obtiene una muestra pareada mediante puntuación de propensión de 37 parejas. La mortalidad a 30días fue del 0% HES-S vs 8% TAVI, y la presencia de leak periprotésico significativo fue del 13,5% en el grupo TAVI y 0% en el HES-S. Con un seguimiento medio de 19meses, existen diferencias significativas en cuanto a supervivencia en favor del grupo HES-S (97,3% vs 86,5%; p=0,01), sobre todo a expensas de los pacientes con leak perivalvular en el grupo TAVI. Este trabajo sugiere que la CMIAo, junto con el uso de estas nuevas válvulas Sutureless o RDV, pueden convertirse en tratamiento de primera línea para pacientes de alto riesgo que se encuentren en la «zona gris» entre TAVI y CC. Estos datos requieren para su confirmación ensayos clínicos bien diseñados en un futuro.
Objeciones al uso de cirugía miniinvasiva aórticaA pesar que la CMIAo ha mostrado excelentes resultados, aún existe cierta crítica por parte de algunos cirujanos. En primer lugar, algunos piensan que solo se consigue un mejor efecto cosmético, sin repercusiones clínicas. Esto es debido a que la mayoría de publicaciones son estudios retrospectivos, mientras que los ensayos clínicos hasta la fecha no han demostrado diferencias significativas. Sin embargo, esto se debe a que estos ensayos han sido estadísticamente mal diseñados, con un bajo poder estadístico, y no basados en cohortes actuales de pacientes22. Ensayos futuros son muy difíciles de diseñar, debido a la baja frecuencia del principal endpoint (mortalidad), lo que requiere muchos pacientes, y a que se ha demostrado una técnica no inferior a CC, menos invasiva y con resultados cosméticos mejores, preferida por los pacientes.
En segundo lugar, están los costes asociados a nuevo instrumental, sobre todo en MTA, y a la curva de aprendizaje, ya que es una cirugía más compleja, con un campo operatorio más profundo y con menor maniobrabilidad. Para iniciar un programa de CMIAo es recomendable empezar por HES, ya que es más reproducible, el cirujano se siente en terreno seguro y su reconversión a CC es muy rápida en caso de complicaciones, aparte de que puede realizarse con material convencional sin gasto adicional.
En tercer lugar, muchos todavía piensan que las mejoras clínicas se ven reducidas por el hecho de aumentar los tiempos de CEC e isquemia. Si bien este aumento es moderado y de entre unos 10min extra de tiempo de isquemia y unos 15min de CEC, la aparición de las nuevas válvulas Sutureless o RVD, al reducir los tiempos entre un 35-45%, van a permitir la estandarización de la técnica y su adopción por más centros.
¿Cómo realizar una miniesternotomía?Existen múltiples opciones quirúrgicas para realizar una HES, ampliamente publicadas en la literatura8,9,12. Sin embargo, dada la gran variabilidad existente, expondremos cómo creemos que es más sencillo realizar una HES:
- -
Paciente en decúbito supino, posición habitual.
- -
Colocación de palas externas de desfibrilador.
- -
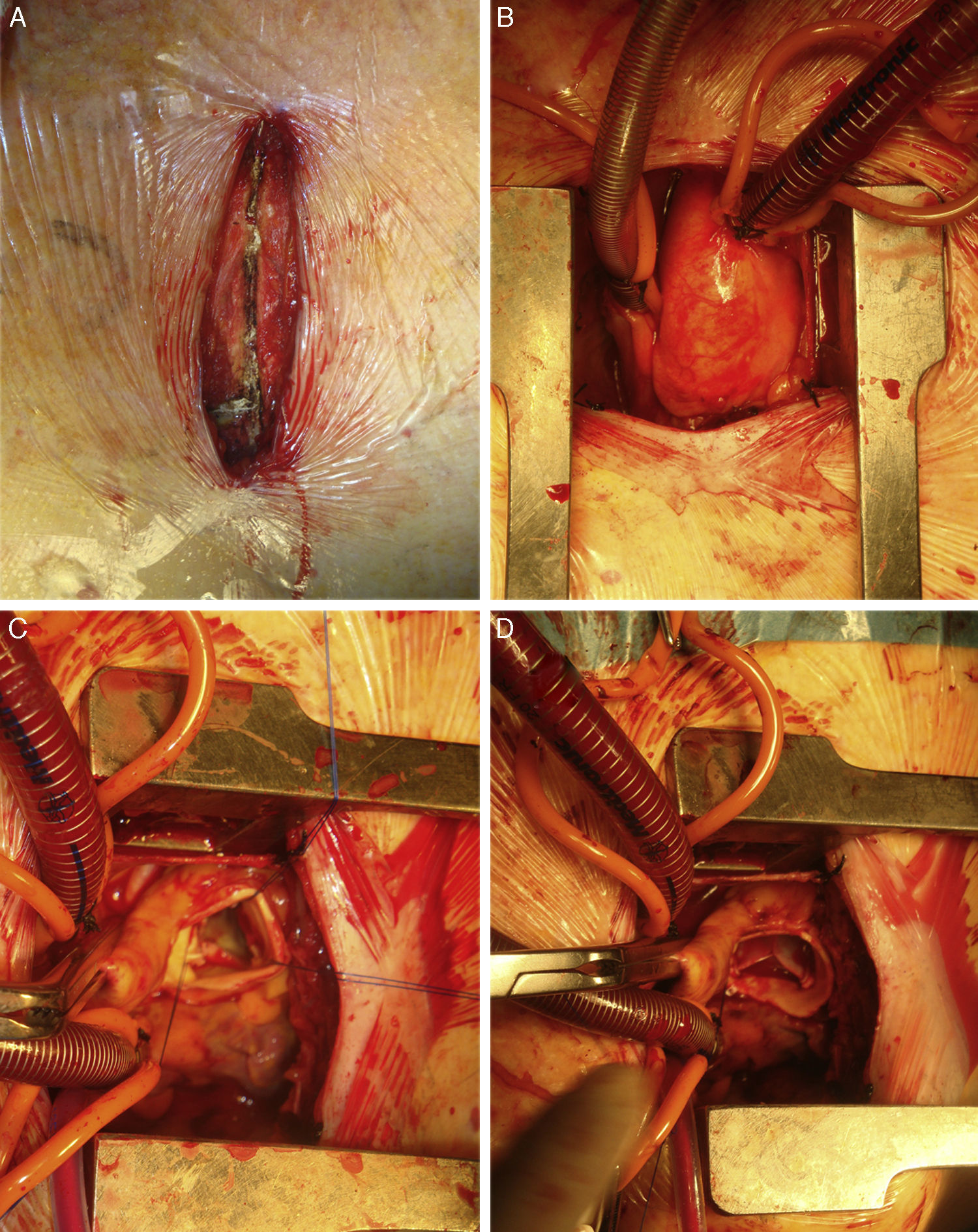
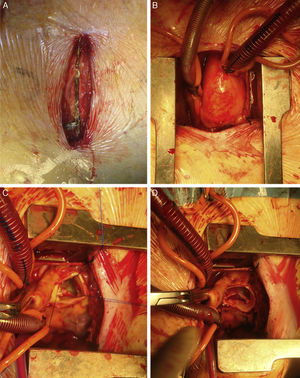
Apertura en piel de 8-10cm empezando en el ángulo de Louis esternal. HES en J por 4.° EICD con sierra normal/oscilante (fig. 3A). Si el esternón es muy pequeño, por 3.er EICD.
- -
Colocación de drenaje subxifoideo tipo Blake de 21mm. Uso de CO2 a través del mismo.
- -
Canulación central en aorta ascendente y AD. Si la AD es de difícil acceso o se prefiere abrir por 3.er EICD, canulación de cava superior con cánula triple puerto 29:29:29, con drenaje venoso activo. Vent en vena pulmonar superior derecha o transaórtico si esta es de difícil acceso (fig. 3B).
- -
Cardioplejía anterógrada hemática/cristaloide por raíz u ostia coronarios.
- -
Aortotomía transversa y sustitución valvular habitual (fig. 3C-D).
- -
Colocación de marcapasos transitorio antes de despinzar.
- -
Cierre con 3-4 alambres simples o cruzados.
Exactamente igual que en la HES, para realizar una MTA existen diferentes escuelas: las que prefieren el uso del endoclam23 y las que prefieren un clampaje directo4, con o sin videoasistencia, con diferentes tipos de clamps (de Glauber, de Chitwood…), canulación central o periférica, etc. Sin embargo, la parte más importante es la relativa a la selección de pacientes que cumplan los requisitos de TC previamente comentados.
En resumen, y como describe la Cleveland Clinic24, creemos que la forma más sencilla de realizar una MTA en los inicios es:
- -
Decúbito supino, palas externas de desfibrilador.
- -
Intubación selectiva con tubo endotraqueal doble luz.
- -
6-7cm herida a 2cm borde esternal derecho en 2° o 3.er EICD (selección del espacio tras evaluar TC). La mamaria derecha se puede ligar o no, al igual que desarticular el cartílago de la 3.a costilla si la visión es subóptima.
- -
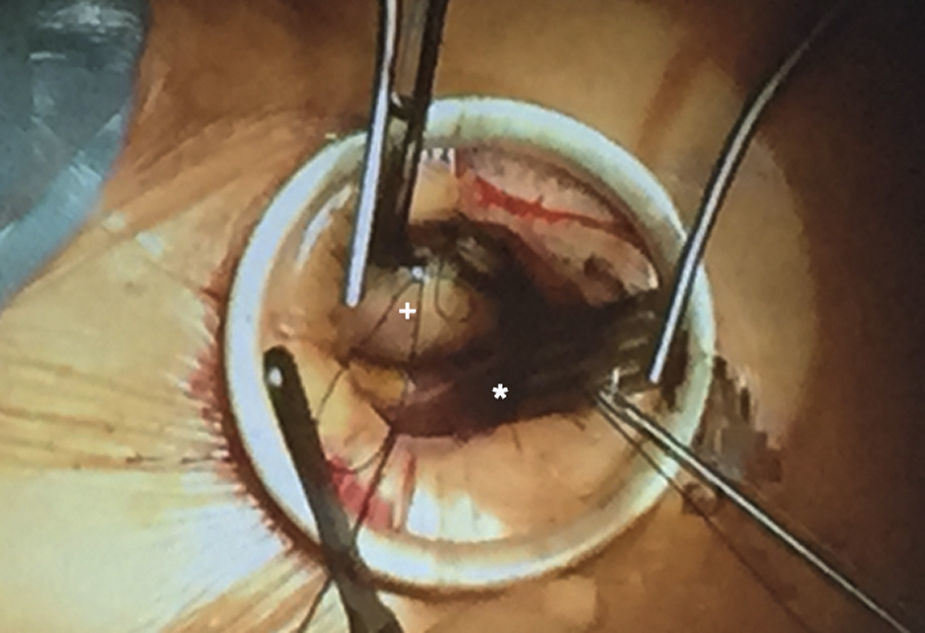
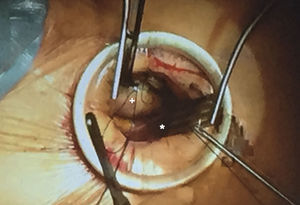
Recomendable retractor partes blandas y costal (fig. 4, visión operatoria). CO2 a través de orificio de drenaje en 5.° EICD. Se puede utilizar o no toracoscopia por otro puerto.
- -
Canulación periférica femoral arteriovenosa en los inicios. Posteriormente se recomienda central aórtica para evitar ictus y complicaciones vasculares. Vent vena pulmonar superior derecha.
- -
Clamp Chitwood/Glauber. Cardioplejía hemática/cristaloide por raíz o/y ostia. Actualmente la cardioplejía de Del Nido está en auge debido a que con una dosis se logran hasta 90min de protección miocárdica25.
- -
Aortotomía transversa. SVAo. Necesidad de material específico de cirugía miniinvasiva.
- -
Marcapasos antes de despinzar y salir de CEC. Um drenaje pleural tipo Blake (5.° EICD, el que utilizamos para CO2).
- -
Cierre costal. Cierre herida.
Las técnicas más comunes en la CMIAo son la HES y la MTA. Comparadas con la CC, han demostrado reducir la morbimortalidad postoperatoria precoz, permitiendo una recuperación rápida, con menor estancia hospitalaria, menor mortalidad temprana y tardía y mejor resultado cosmético, con el consecuente ahorro. A pesar de estas ventajas, el aumento de los tiempos de isquemia y CEC provoca cierto reparo a la hora de intervenir a pacientes mayores frágiles o de alto riesgo. Sin embargo, con la reciente introducción de las válvulas Sutureless (Perceval®, Sorin Group) o RDV (Intuity®, Edwards Lifesciences), los tiempos de CEC se han reducido en hasta un 43%. Atendiendo a estos resultados, la CMIAo con Sutureless o RDV puede ser la alternativa real a TAVI en pacientes de alto y mediano riesgo. Su implementación en el arsenal terapéutico es imprescindible para la evolución de nuestra especialidad y para responder a las exigencias de pacientes y cardiólogos. A pesar de que son recomendables ensayos clínicos prospectivos aleatorizados para confirmar estos datos, existe suficiente evidencia disponible como para considerar la CMIAo (sobre todo la HES) como el gold standard actual para la sustitución valvular aórtica aislada.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener conflictos de intereses.
XX Reunión Anual de Médicos Internos Residentes: Cirugía Valvular.