La transposición congénitamente corregida de las grandes arterias es una cardiopatía rara caracterizada por la doble discordancia entre las aurículas y los ventrículos, así como entre los ventrículos y las grandes arterias. En el siguiente manuscrito comentaremos la anatomía y fisiopatología de esta malformación y las distintas opciones de manejo quirúrgico, desde el cerclaje pulmonar hasta el doble intercambio.
Congenitally corrected transposition of the great arteries constitutes a rare heart disease featured by a double discordance, between the atria and the ventricles as well as between the ventricles and great arteries. In the next manuscript we’ll comment on the anatomy of pathophysiology of this malformation, and on the different options of surgical management, from pulmonary artery banding to double switch operation.
La transposición de grandes arterias congénitamente corregida (cc-TGA), también llamada aislada inversión ventricular, doble discordancia, transposición fisiológicamente corregida o L-transposición, es una cardiopatía muy compleja, que fue descrita por primera vez por von Rokitansky y representa menos del 1% de todas las cardiopatías congénitas. Se caracteriza por existir una doble discordancia entre la conexión de las aurículas con los ventrículos y los ventrículos con las grandes arterias.
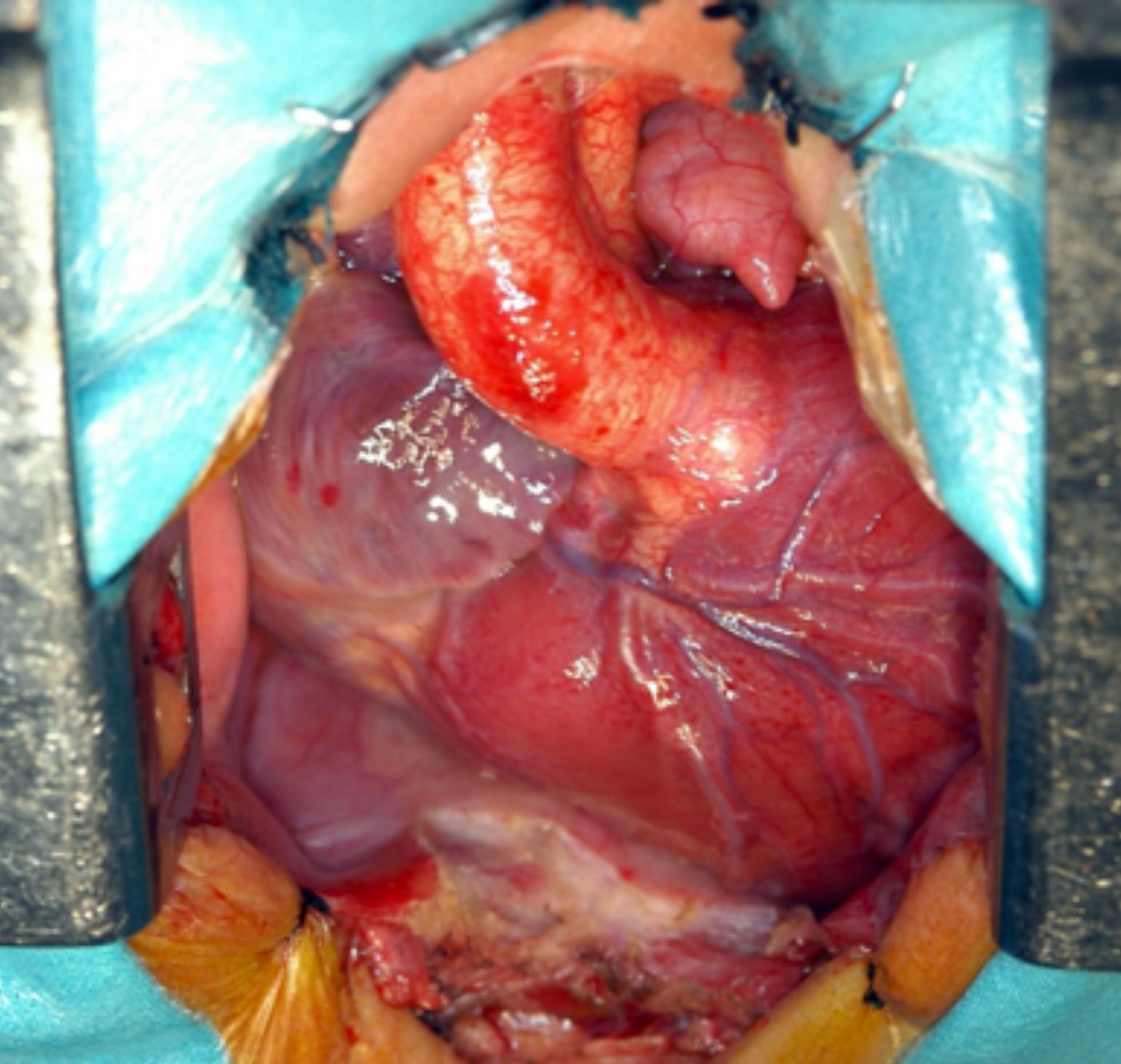
El retorno venoso sistémico desemboca en la aurícula morfológicamente derecha. Esta aurícula está conectada a través de la válvula mitral con el ventrículo morfológicamente izquierdo (VI), el cual conecta de modo discordante con la arteria pulmonar. La aurícula izquierda recibe el retorno venoso pulmonar y se conecta a través de la válvula tricúspide con el ventrículo morfológicamente derecho (VD), el cual se conecta a la aorta. Así, el camino de la sangre venosa sistémica regresa al corazón, que lo dirige a la arteria pulmonar, y el retorno venoso pulmonar es dirigido a la aorta (fig. 1).
Inicialmente Rokitansky usó el término «corregida» para denominar esta patología. Pero fue Schiebler quien modificó la denominación añadiendo «congénitamente» al término «corregida» para diferenciarla de las quirúrgicamente corregidas.
Embriología y anatomíaEn fases tempranas del desarrollo embriológico, el tubo cardiaco primitivo gira a la izquierda (L-asa), en vez de a la derecha (D-asa), como es habitual. Este giro anormal hace que el VI se sitúe a la derecha y, viceversa, que el VD se sitúe a la izquierda. El septo interventricular tiende a una posición más sagital y horizontal, lo que da lugar a una «malalineación» del septo auricular, lo que desviaría en grado variable al septo ventricular. Este concepto de «malalineación» de ambos septos influye en el tamaño del defecto interventricular, la morfología del tracto de salida ventricular y el sistema de conducción. Por esto, en un 80% de los pacientes se asocia a comunicación interventricular (CIV), que suele ser grande y perimembranosa, aunque puede localizarse en cualquier posición del septo interventricular.
La válvula auriculoventricular (AV) situada a la derecha tiene las características de la válvula mitral, con 2 músculos papilares sin inserción en el septo interventricular. La válvula AV situada a la izquierda tiene las características de la válvula tricúspide. Esta válvula es frecuentemente anormal: el velo septal cae bien en una posición anterior en el tracto de salida, bien posteriormente en relación con la comunicación. La aorta anterior e izquierda está soportada por un infundíbulo muscular y no existe continuidad con la válvula AV.
Se caracteriza porque los tractos de salida de las arterias principales adquieren una disposición en paralelo y no cruzados como un corazón normal. Este hecho condiciona una posición de los ventrículos uno al lado del otro. El tracto de salida subpulmonar se encuentra entre las válvulas mitral y tricúspide, y el anillo pulmonar puede situarse sobre el septo interventricular. Es por eso que es frecuente el hallar una obstrucción al tracto de salida del ventrículo morfológicamente izquierdo; ocurre hasta en un 40% de los pacientes, sobre todo los que presentan CIV.
Debido a la posición anatómica, tanto la válvula morfológicamente tricúspide como, en ocasiones, la mitral pueden cabalgar sobre el septo interventricular y se produce una displasia valvular, con o sin desplazamiento del velo septal o posterior. La insuficiencia se produce en el 30% de los pacientes.
En la mayoría de estos pacientes se presenta en situs solitus, pero hasta un 5% asocia situs inversus, y entre un 25% y un 50% asocia dextrocardia.
La terminología utilizada para la denominación de esta patología se ha unificado según la clasificación de van Praagh:
- -
(S, L, L) cc-TGA: solitus, L-asa, aorta la izquierda de la arteria pulmonar.
- -
(I, D, D) cc-TGA: inversus, D-asa, aorta a la derecha de la arteria pulmonar.
Según la clasificación por segmentos:
- -
Conexión AV: discordancia AV.
- -
Conexión VA: discordancia ventriculoarterial.
- -
Situs: solitus o inversus.
Las arterias coronarias se originan de los senos de la válvula aórtica y muestran una orientación invertida con un flujo adecuado a la distribución de sus ventrículos.
En la posición (S, L, L) la arteria coronaria derecha se origina del seno coronario derecho posterior y da origen a la arteria descendente anterior y circunfleja. Mientras que la arteria coronaria situada a la izquierda va por el surco AV y da ramas infundibulares y marginales. Adquieren por tanto una imagen en espejo. En la posición (I, D, D) la anatomía coronaria es normal.
El patrón coronario proximal en la raíz aórtica depende de la rotación aortopulmonar, y el patrón coronario periférico depende del situs auricular y de la posición apical determinada por el asa ventricular.
La anatomía coronaria es crucial en la posible alternativa quirúrgica mediante la técnica de doble intercambio.
Sistema de conducciónEl sistema de conducción en los pacientes con cc-TGA (S,L, L) es anormal debido al giro anómalo del corazón que produce una «malalineación» de los septos auricular y ventricular. En el caso de cc-TGA (I, D, D) el sistema de conducción es normal. Se describen clásicamente 2 nodos AV:
- -
Un nodo normal posterior e hipoplásico, localizado en el ápex del triángulo de Koch, el cual raramente está conectado con la masa ventricular a través de un haz posterior.
- -
Un nodo anormal AV anterior-derecho y lateral a la continuidad mitro/pulmonar, debajo del origen de la orejuela derecha, con un haz de His que tiene un curso superficial y anterior en el tracto de salida subpulmonar y por la pared superior del VI. Fue descrito por primera vez por Monckeberg en 1913.
En los casos de septos ventriculares malalineados el desarrollo de un haz de His desde un nodo AV normal es anatómicamente difícil. El grado de «malalineación» está relacionado con el tamaño del tracto de salida del VI y del tronco pulmonar. Los pacientes con un sistema de conducción normal presentan atresia pulmonar o estenosis significativa pulmonar, lo que resulta en un menor grado de «malalineación» septal.
El bloqueo AV congénito puede presentarse también en pacientes con cc-TGA, debido a una falta de continuidad entre la aurícula y el sistema de conducción especializado. Ocurre en alrededor del 5-10% de los casos, y el bloqueo AV adquirido se produce con una incidencia del 2% por año.
Las taquiarritmias aparecen en el 12-38% de los pacientes, y el mecanismo habitual es la reentrada AV utilizando una vía accesoria (pueden existir múltiples vías anómalas). Cuando la válvula AV es displásica (Ebstein-like), la fibrilación puede constituir un problema, a pesar del reemplazo de la válvula tricúspide.
DiagnósticoLos pacientes con cc-TGA no suelen presentar síntomas hasta la vida adulta. Los síntomas son en general reflejo de las lesiones asociadas.
La bradicardia (con o sin insuficiencia cardiaca) secundaria al grado de bloqueo AV puede ser el síntoma de comienzo en estos pacientes y la taquiarritmia reflejaría alteraciones del sistema de conducción. Aproximadamente un 5% de estos pacientes nacen con alteraciones del ritmo cardiaco.
La cianosis se produce por un flujo pulmonar insuficiente secundario a la obstrucción subpulmonar.
La insuficiencia cardiaca congestiva es secundaria a arritmia, o más frecuentemente a un gran defecto interventricular, o bien a la displasia de la válvula morfológicamente tricúspide situada a la izquierda con insuficiencia en grados variables, o bien a anomalías obstructivas del arco aórtico o un combinado de estas anomalías.
Tratamiento quirúrgicoTécnicas paliativasLos pacientes con cc-TGA raramente requieren de técnicas paliativas a menos de que exista una severa hipoplasia de uno de los ventrículos que impida una cirugía correctora o que el paciente padezca una cianosis grave en el periodo neonatal. En estos casos se tratarán quirúrgicamente mediante una fístula sistemicopulmonar. Nosotros preferimos realizar una fístula de Blalock-Taussig modificada desde la arteria subclavia a la arteria pulmonar usando un injerto de politetrafluoroetileno de 3,5 a 4mm de diámetro según el peso del paciente.
Es frecuente que estos pacientes asocien una obstrucción pulmonar subvalvular, valvular o supravalvular; por este motivo no suelen requerir la realización de un cerclaje pulmonar. Además se ha comprobado que la realización de un cerclaje pulmonar predispone a la dilatación de la raíz aortica, produciendo una insuficiencia aórtica que pondrá en peligro la realización de intercambio arterial posterior. El cerclaje de la arteria pulmonar puede ser necesario únicamente en el caso de que se plantee realizar un doble intercambio, especialmente en niños mayores, en los que la presión del VI es menos de 2 terceras partes de la presión del VD, y se necesita un cerclaje pulmonar para preparar al ventrículo izquierdo para soportar la presión sistémica.
Corrección fisiológicaEl abordaje clásico o la corrección fisiológica se centran en solucionar los problemas o anomalías asociados a la cc-TGA (como la presencia de CIV, de comunicación interauricular, obstrucción pulmonar, insuficiencia tricuspidea, arritmias), dejando el ventrículo y la válvula AV morfológicamente derechos como sistémicos. La mortalidad operatoria es baja (aunque depende mucho del defecto asociado que se quiera corregir), pero muchos autores rechazan este abordaje debido a los problemas que pueden desencadenar a medio y largo plazo un ventrículo y una válvula AV morfológicamente derechos en posición sistémica. Además, la insurgencia de un bloqueo AV completo espontáneo, que se verifica hasta en el 30% de los pacientes, deteriora mucho más la función de un ventrículo sistémico de morfología derecha, con respecto a uno de morfología izquierda.
Generalmente, se acepta este abordaje (que incluye el no hacer nada en pacientes sin lesiones asociadas) en pacientes asintomáticos sin lesiones asociadas o cuando las lesiones asociadas impiden o aumentan mucho el riesgo del doble intercambio (VI pequeño o disfuncionante, EP compleja o no directamente resecable o sin posibilidad de tunelizar la CIV a la aorta, anomalías en la válvula AV sistémica).
Cierre de la comunicación interventricularLa localización más frecuente de la CIV es conoventricular o en el septo membranoso. Normalmente existe una «malalineación» donde la válvula pulmonar cabalga el septo.
La dificultad para el cierre de la CIV radica en la variabilidad del tejido de conducción de estos pacientes. Lo más común es que se cierre la CIV mediante abordaje auricular derecho, desplazando la válvula mitral. Los puntos han de darse con cuidado apoyándose en el ventrículo morfológicamente derecho, especialmente en el ángulo anterosuperior.
Reparación de la obstrucción subpulmonarAl menos un 30-50% de los pacientes con cc-TGA muestran una obstrucción pulmonar o subpulmonar. Si la obstrucción es debida a una estenosis valvular suele ser posible dilatar la válvula realizando una valvuloplastia previa a la intervención. En el caso de que exista una obstrucción subvalvular suele ser por exceso de tejido debido a la existencia de una membrana fibrosa, por tejido accesorio mitral o por un aneurisma del septo membranoso…; en estos casos es precisa la resección del tejido para aliviar la obstrucción.
Reparación de la válvula auriculoventricular izquierdaLa insuficiencia de la válvula tricúspide en posición sistémica es una complicación frecuente en este tipo de pacientes. En ocasiones es suficiente con realizar una anuloplastia, aunque la dilatación suele evolucionar y es frecuente que requieran una sustitución valvular.
Reparación univentricularCuando no sea posible completar una reparación biventricular se puede realizar una operación de Glenn bidireccional. En un segundo tiempo se completará la circulación de Fontan construyendo un túnel con politetrafluoroetileno.
Otra opción quirúrgica para los pacientes con una función deprimida del ventrículo de la circulación pulmonar es el abordaje «uno y medio». Billingsley describió esta técnica quirúrgica que consiste en combinar una fístula de Glenn bidireccional con la corrección ventricular.
En todos los casos siempre, que sea posible, es preferible una corrección anatómica.
Corrección anatómicaLa corrección anatómica de la cc-TGA se centra en restaurar el VI y la válvula mitral como estructuras sistémicas. Este abordaje conlleva un riesgo operatorio mucho más alto y no siempre es realizable (según las anomalías asociadas), pero la función cardiaca es mejor preservada a medio y largo plazo, debido a la normal morfología (izquierda) del ventrículo y de la válvula AV sistémicos.
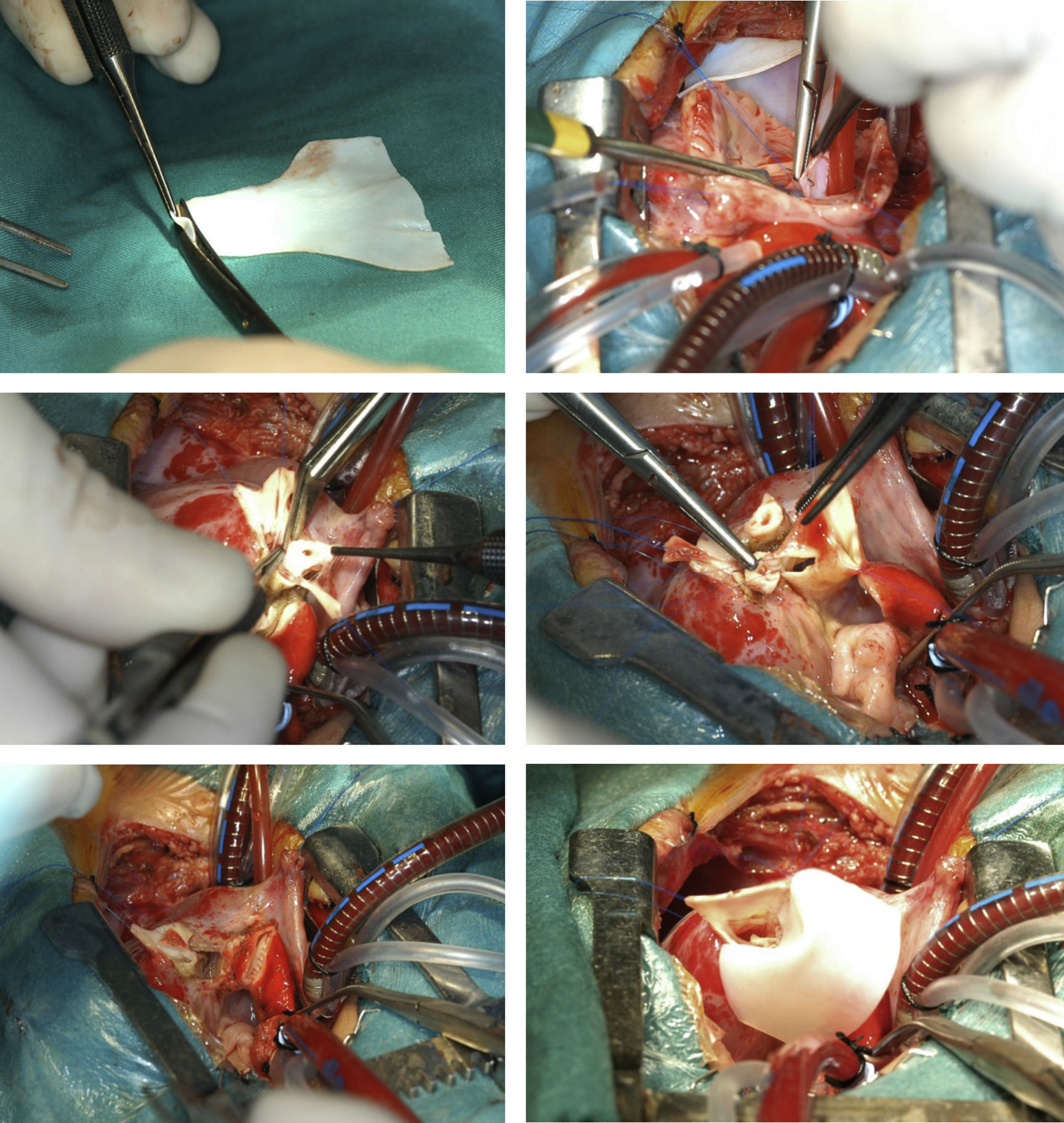
Técnica del doble intercambioLa técnica quirúrgica de los casos sin obstrucción compleja subpulmonar/valvular pulmonar es el doble intercambio, que asocia la operación de Senning o Mustard (intercambio auricular) a la operación de Jatene (intercambio arterial).
Principalmente la técnica quirúrgica consiste en realizar primero el intercambio de las grandes arterias con la translocación de las arterias coronarias y la anteroposición de las ramas pulmonares por delante de la aorta según la técnica de Jatene.
Posteriormente mediante atriotomía derecha se reseca parte del septo auricular y se abre el techo del seno coronario. Mediante un parche de pericardio heterólogo de completa el intercambio auricular con la técnica de Mustard o Senning, ambos con los mismos resultados (fig. 2).
Si existe CIV asociada se cierra con parche de pericardio heterólogo.
Senning o Mustard con operación de RastelliEn casos con EP compleja y CIV tunelizable a la aorta, se realiza primero el intercambio auricular, luego se tuneliza la CIV a la aorta y, por último, se reconstruye la continuidad VD-arteria pulmonar con un conducto preferiblemente homoinjerto valvulado. En algunas ocasiones es posible asociar al doble intercambio la operación de Glenn, para disminuir el riesgo de obstrucción de la vena cava superior con el intercambio auricular.
El intercambio auricular se lleva a cabo según la técnica ya descrita. En este caso, el cierre de la CIV se realiza mediante ventriculotomía derecha, cierre de la CIV con parche de pericardio heterólogo e interposición de conducto valvulado desde el VD a la arteria pulmonar. En ocasiones la CIV requiere que se aumente de tamaño para impedir que se produzca una obstrucción entre el VI y la aorta con el consiguiente riesgo de bloqueo AV.
Senning o Mustard con operación de NikaidohEn algunos casos en los que la anatomía no permite realizar la operación de Rastelli es posible asociar al intercambio auricular la técnica de Nikaidoh, que consiste en la desinserción de la raíz aórtica y pulmonar, translocación de las grandes arterias, movilización de las arterias coronarias implantándolas en la arteria aorta y cierre de la CIV.
ResultadosCorrección «clásica» y corrección univentricularSeries iniciales comprobaron que los pacientes con cc-TGA sin otras lesiones, no intervenidos, desarrollaban en un 35% fallo cardiaco congestivo a la edad de 40 años.
El grupo de Boston mostró en 2005 una serie de pacientes con cc-TGA a los que les habían realizado una corrección clásica en 96 casos o una operación de Fontan en 17 casos, mostrando una supervivencia global a los 5 años del 75%, a 10 años del 70% y a los 15 años del 60%. El grupo intervenido según la técnica de Fontan mostraba una supervivencia del 100%
La mortalidad media a los 10 años de los supervivientes a una intervención quirúrgica por el método fisiológico es del 25-30% con una tasa de reoperaciones a los 10 años del 41%.
Reparación anatómicaLos resultados del doble intercambio en pacientes por encima de la primera década de la vida, con ventrículos previamente reacondicionados, están lejos de lo ideal, no siendo en muchos casos posible el reacondicionamiento de dicho ventrículo.
Por todo ello, pacientes jóvenes asintomáticos con insuficiencia tricuspidea, deben ser evaluados para la realización de un reentrenamiento del VI, en preparación para el doble intercambio, ya que la historia natural de los pacientes con regurgitación tricuspidea se ha mostrado muy limitada, incluso cuando la función del VD permanece conservada.
La cirugía de doble intercambio mediante Senning y Rastelli ha sido durante los últimos años el proceder más utilizado, buscando una corrección anatómica con restitución del ventrículo anatómicamente izquierdo a la circulación sistémica.
Este proceder tiene todas las limitaciones del proceder de Rastelli, especialmente en lo que respecta a la realización de una ventriculotomía derecha y la colocación de un conducto valvulado excesivamente largo para conectar el ventrículo anatómico derecho con la circulación pulmonar. Es por esto que la doble translocación de raíz aórtica y pulmonar (Nikaidoh modificado) es altamente atractiva a pesar de su alta complejidad ya que supone una reconstrucción anatómica de ambos tractos de salida con tejidos autógenos y capacidad de crecimiento.
Los pacientes intervenidos según las técnicas anatómicas muestran unos resultados a los 10-58 meses muy favorecedores. Todos los supervivientes se encuentran en clase funcional i-ii de la NYHA. Un 90% con índices de función de VD normal en reposo. No muestran alteraciones de la función del VI o de la válvula mitral. El grado de insuficiencia tricuspidea desciende de media de 3/4 a 1/4. Muestra una tasa de reintervenciones del 4-6% con una supervivencia global del 92% (incluida la mortalidad hospitalaria) sin existir en nuestra serie mortalidad tardía.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.