Las cardiopatías congénitas son las malformaciones congénitas mayores más comunes. Generan importantes efectos deletéreos en términos de morbimortalidad neonatal y durante la edad temprana.
La transposición de grandes arterias representa el 5-7% de las cardiopatías congénitas. Hasta 1976 la única estrategia terapéutica disponible para tratar la transposición de grandes arterias era la corrección fisiológica, conocida también como switch auricular (cirugía de Mustard o Senning). Posteriormente, el profesor Adib Jatene haría pública su experiencia con la cirugía de corrección anatómica o switch arterial, convirtiéndose en el gold standard en el tratamiento de la mayor parte de los casos de transposición de grandes arterias.
A pesar del inmenso esfuerzo de grandes cirujanos, cardiólogos y magníficos equipos sanitarios, el switch arterial no está exento de complicaciones a corto, medio y largo plazo, entre otras, obstrucción al flujo coronario, obstrucción al flujo pulmonar e insuficiencia de la válvula neoaórtica secundaria la mayor parte del tiempo a dilatación de la neorraíz aórtica.
Con la intención de compartir nuestra experiencia en el tratamiento de la insuficiencia de la válvula neoaórtica luego de la cirugía de switch arterial, presentamos el siguiente caso clínico. El consentimiento informado fue obtenido de los padres de la paciente para realizar esta publicación.
Congenital heart defects are the most common major congenital malformations causing a significant effect on neonatal mortality and morbidity.
Transposition of the great arteries represents approximately 5-7% of all congenital heart defects. Until 1976, the only therapeutic strategy available to treat transposition of the great arteries was the atrial switch (Mustard or Senning surgery), also known as physiological repair. Later on, Professor Adib Jatene published his experience with anatomical repair known as arterial switch operation, this surgery will become the gold standard of care for patients with transposition of the great arteries.
Despite the effort of great surgeons, cardiologists and magnificent health teams, the arterial switch operation is related with some complications during short, medium and long term follow up, among these complications, obstruction to coronary flow, obstruction to pulmonary flow and neo-aortic valve regurgitation due in most cases to dilation of the neo-aortic root.
We would like to share our experience treating neo-aortic valve regurgitation after switch operation. Informed consent was obtained from the parents of the patient in order to publish the case.
Presentamos el caso de una paciente con diagnóstico tardío de dextrotransposición de grandes arterias realizado a los 3 meses de edad. La ecocardiografía mostraba los datos característicos de una dextrotransposición de grandes arterias junto con una gran comunicación interauricular no restrictiva de tipo ostium secundum. Destacaba una dilatación de la arteria pulmonar con un diámetro máximo a nivel de los senos de Valsalva de aproximadamente 14mm (z score: +2), se acompañaba de una insuficiencia valvular ligera central, el anillo aórtico medía 9mm (z score: 0,34) y 12mm a nivel de los senos de Valsalva (z score: 0,23). Con el fin de realizar una corrección anatómica de su cardiopatía se diseñó una estrategia terapéutica quirúrgica por estadios.
El primer estadio consistió en el reentrenamiento ventricular izquierdo a través de un cerclaje de la arteria pulmonar, al que se añadió una fístula sistémico-pulmonar de Blalock-Taussig de 4mm para mantener un adecuado flujo pulmonar.
Luego de 16 semanas de la primera intervención quirúrgica, y una vez confirmada la readaptación del ventrículo izquierdo mediante ecocardiografía y resonancia magnética que mostraban el aumento de la masa miocárdica, se procedió a la corrección anatómica mediante cirugía de switch arterial (SA).
Con 7 meses de edad y 8,3kg de peso se realizó la cirugía de SA, que consistió en transponer los grandes vasos, retirar el cerclaje de la arteria pulmonar, realizar la maniobra de Lecompte, reimplantar las arterias coronarias utilizando la técnica de trap-door y cerrar la comunicación interauricular; la disposición coronaria fue 1R-2LCx.
Luego de la corrección anatómica, la paciente fue dada de alta sin incidencias. En el estudio ecocardiográfico destacaba una insuficiencia ligera central de la válvula neoaórtica (VNA).
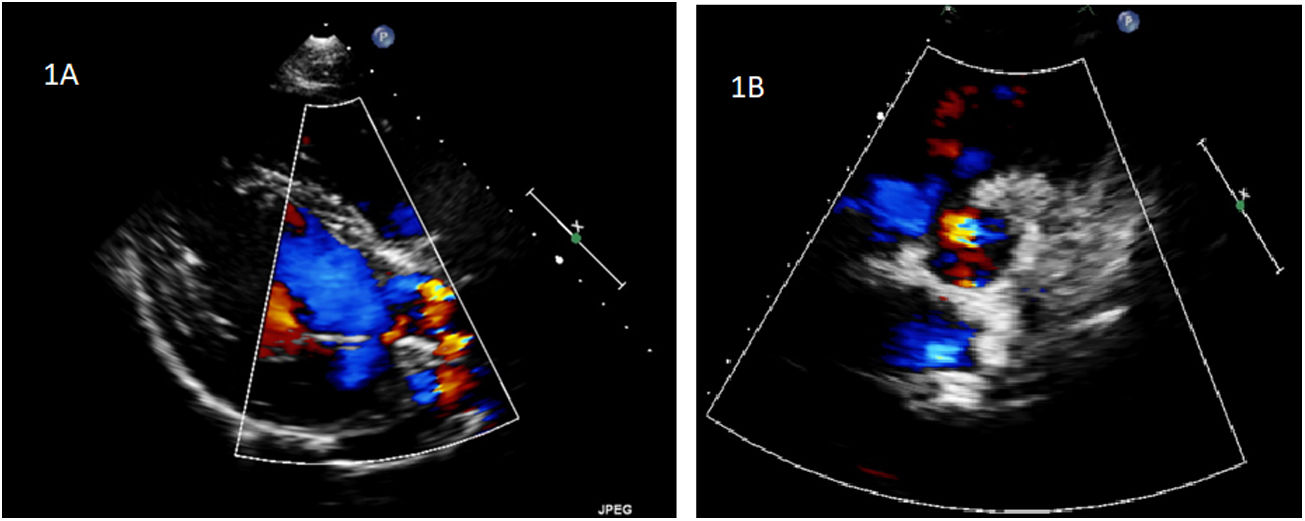
El seguimiento posterior mostró una paulatina dilatación de la neorraíz aórtica (NRA), un empeoramiento de la insuficiencia valvular, dilatación del ventrículo izquierdo y deterioro de la contractilidad ventricular. Con 10 años de edad y 30kg de peso, el último estudio ecocardiográfico mostraba una NRA de 20mm a nivel basal (z score: +2,56), 29mm a nivel de los senos de Valsalva (z score: +3,2) y 20mm a nivel de la unión sinotubular (z score: +1,8). El estudio mostraba una insuficiencia severa producida por 2 jets, uno excéntrico y otro central, el diámetro telediastólico del ventrículo izquierdo era de 48mm (z score: +1,9) y la contractilidad era del 45% (fig. 1 a y b). La ecocardiografía no mostraba segmentarismos y el estudio electrocardiográfico descartó lesiones indicativas de isquemia miocárdica. Dados estos hallazgos y la evolución de la paciente, se decidió una reintervención quirúrgica para reparar o sustituir la VNA.
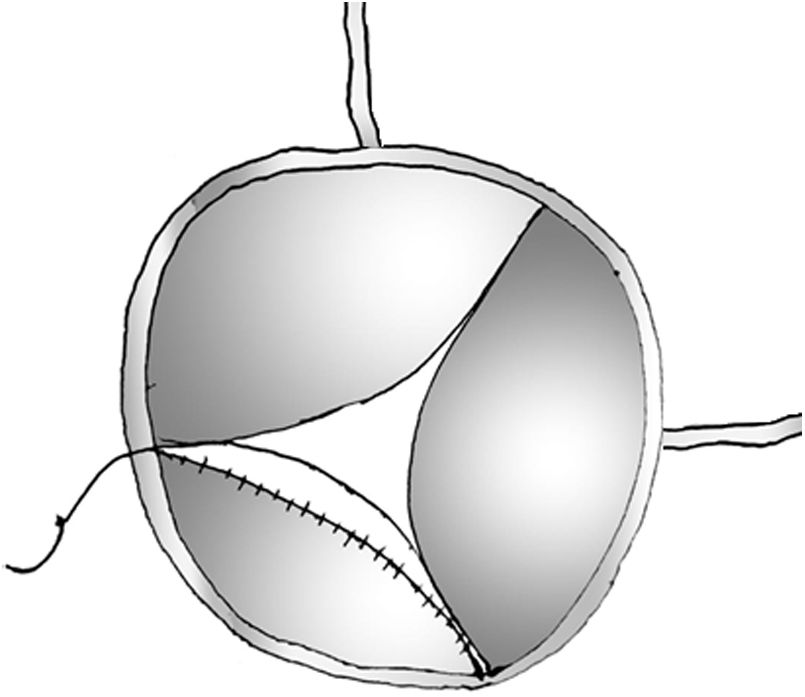
Técnica quirúrgicaLa reparación quirúrgica se realizó mediante reesternotomía media y con circulación extracorpórea. Luego de la reapertura esternal, manteniendo especial atención en evitar lesionar la arteria pulmonar anteriorizada por la maniobra de Lecompte, se procedió a la disección y movilización de la neoaorta. Se apreciaba una importante dilatación de la NRA, cuyo diámetro máximo se encontraba a nivel de los senos de Valsalva. La canulación arterial se realizó sobre la aorta ascendente a nivel del nacimiento de los troncos supraaórticos y el drenaje venoso se realizó mediante una cánula central venosa única. Se drenaron las cavidades izquierdas mediante un vent ventricular izquierdo colocado a través de la vena pulmonar superior derecha. Se utilizó cardioplejía anterógrada hipotérmica hemática intermitente (cada 20min) a través de los ostiums coronarios. Se realizó una arteriotomía aórtica transversa total a nivel de la línea de sutura de la cirugía previa, aproximadamente a nivel de la unión sinotubular. Se colocaron 3 puntos de exposición sobre cada una de las comisuras, intentando mantener la forma geométrica habitual de la NRA. Se exploró de forma minuciosa la NRA y la VNA. Se apreciaba un defecto de coaptación producido por la dilatación del anillo valvular, además de una degeneración leve con engrosamiento del borde libre de los velos correspondientes a los senos coronarios derecho e izquierdo. El velo no coronario presentaba un marcado acortamiento distal con importante engrosamiento de su borde libre. Dadas las características de la paciente y la necesidad de aplicar técnicas quirúrgicas que no impidan el crecimiento natural del anillo valvular, se decidió aumentar el área de coaptación actuando sobre las comisuras valvulares. Se utilizaron 3 suturas horizontales subcomisurales de Cabrol en forma de «U» con Prolene® 6/0 bajo cada comisura, teniendo en cuenta que la altura de cada sutura determinaría el aumento del área de coaptación y la disminución del área valvular efectiva. Esta maniobra permitió aumentar el área de coaptación en aproximadamente 2-3mm (fig. 2). Posteriormente, se revaloró la extensión de cada velo desde su nadir hasta su borde libre. Se apreciaba asimetría del velo correspondiente al seno en el que no se implantó ninguna arteria coronaria durante el SA; este velo presentaba una retracción de su borde libre en aproximadamente 2-3mm. Se realizó una resección parcial del borde engrosado manteniendo una zona firme para apoyar un parche de ampliación. La ampliación del velo se realizó utilizando un parche heterólogo de pericardio bovino de aproximadamente 3-4mm de altura y de longitud similar a toda la extensión del velo. Se procedió a suturar el mismo con una sutura continua de Prolene® 7/0 (fig. 3). Se suspendió el soporte circulatorio de circulación extracorpórea sin incidencias y el estudio ecocardiográfico postoperatorio no mostró ningún defecto residual.
Luego de una estancia hospitalaria total de 7 días sin incidencias la paciente fue dada de alta a su domicilio.
Con un seguimiento de 6 años, en el último control ecocardiográfico se evidenció una insuficiencia valvular ligera, central, sin repercusión sobre la función ventricular. La paciente se encontraba asintomática y con una clase funcional normal (NYHA I).
ConclusionesLa cirugía de SA se considera el procedimiento estándar para la corrección de transposición de grandes arterias. Durante las últimas décadas se ha demostrado que puede ser realizado y reproducido con buenos resultados. Sin embargo, una pequeña proporción de pacientes requerirá reintervención por una de las siguientes razones: obstrucción al flujo pulmonar, obstrucción del tracto de salida del ventrículo izquierdo, alteraciones en el flujo coronario, dilatación de la NRA e insuficiencia de la VNA.
Algunos reportes han demostrado la aparición de algún grado de insuficiencia valvular en la NRA secundaria a su dilatación en la mayoría de los pacientes (70-80%) luego de la cirugía de SA; sin embargo, únicamente en un 4% de los casos la insuficiencia será significativa y precisará reintervención quirúrgica1,2.
Es importante entender la raíz aórtica como una compleja unidad funcional tridimensional y dinámica que depende del correcto funcionamiento de todos sus componentes. La evolución de la cirugía de reparación valvular aórtica en el adulto durante las últimas décadas ha permitido una profunda comprensión de la raíz aórtica. En este sentido, cualquier evento fisiopatológico que altere la armonía que se produce entre los diámetros anulares y sinotubulares, la altura efectiva de coaptación, la altura geométrica, la altura propia de los velos, etc., puede generar un mal funcionamiento de la raíz y su válvula3.
Teniendo estos detalles claros es fácil comprender que la cirugía de SA altera varios de los factores mencionados previamente.
Algunas publicaciones han demostrado que, al nacimiento en este grupo de pacientes, el diámetro de la raíz pulmonar nativa es mayor que el diámetro de la raíz aórtica nativa, especialmente en presencia de defectos del septo ventricular. Esta asimetría entre la raíz respecto a su unión sinotubular luego de la cirugía de SA altera la capacidad de deformación circunferencial y longitudinal de la raíz durante el ciclo cardíaco. Este efecto disminuye la capacidad propia de la raíz de disipar el estrés parietal, producto de la energía cinética del flujo sanguíneo desde el ventrículo hacia la circulación sistémica, y favorece la degeneración de la raíz4.
Han sido reportadas, además, diferencias histológicas al nacimiento entre la válvula pulmonar y la válvula aórtica que contribuyen a la degeneración paulatina de la válvula pulmonar expuesta a presiones sistémicas. Lalezari et al. reportaron la presencia de menos tejido fibroso de soporte al nacimiento en la válvula pulmonar respecto a la válvula aórtica5.
Por último, se han reportado otros factores que pueden aumentar el riesgo de dilatación de la NRA y de deterioro de la función valvular: la coexistencia de coartación aórtica y gradientes residuales luego de su reparación quirúrgica, la insuficiencia valvular pulmonar nativa previa a la cirugía de SA y el cerclaje de la arteria pulmonar durante el reentrenamiento ventricular.
Desde el punto de vista quirúrgico, todas las técnicas utilizadas para realizar una reparación valvular deberán cumplir la premisa de no alterar la propiedad de crecimiento de las estructuras en donde se apliquen.
Una reparación exitosa de la VNA inicia con un análisis minucioso y sustancial del evento fisiopatológico que la origina. En el caso de la insuficiencia valvular luego de la cirugía de SA, el mecanismo más frecuentemente reportado es la dilatación de la NRA.
Respecto a la paciente citada en este caso, la causa de la insuficiencia valvular es evidentemente multifactorial. La necesidad de realizar un cerclaje arterial sobre una raíz pulmonar nativa dilatada, junto con una importante discrepancia de tamaños entre la raíz aórtica y pulmonar nativa, afectó el funcionamiento de varias estructuras de la raíz arterial luego del SA. Creemos que la insuficiencia central estaba relacionada con la dilatación del anillo, mientras que el jet excéntrico era producto de la afección de una de las unidades velo-seno de Valsalva secundaria al cerclaje de la arteria pulmonar.
En términos de durabilidad se ha demostrado que la estabilización del anillo valvular mediante anuloplastia es la técnica quirúrgica de preferencia; sin embargo, es poco útil en pacientes en etapa de desarrollo. En nuestra experiencia y opinión, una opción razonable es la sutura subcomisural descrita por Cabrol en 1966. Esta técnica permite aumentar el área de coaptación entre los velos, al disminuir el área valvular efectiva sin actuar directamente sobre el anillo valvular. Por supuesto, su punto débil es la durabilidad. La estabilización del anillo mediante anuloplastia interna utilizando una sutura absorbible ha sido publicada; sin embargo, la estabilización del anillo es efectiva mientras la sutura sea capaz de mantener la tensión aplicada de forma inicial6.
Cuando el defecto reside sobre los velos, varias técnicas han sido descritas. La ampliación del velo desde su borde libre, utilizando material protésico, en nuestra experiencia puede ser una buena opción tomando en cuenta, como es lógico, la inevitable degeneración natural del material utilizado7,8.
Por otro lado, cuando el defecto reside sobre el diámetro de la raíz aórtica, manteniendo los velos valvulares íntegros y en función de las características del paciente, se podrá considerar el remplazo de la raíz aórtica con preservación de la válvula9.
En caso de prolapso de uno de los velos se puede optar por utilizar una sutura subcomisural en las comisuras correspondientes al velo comprometido, junto con la plicatura del borde libre del velo de forma simétrica, plicando similar cantidad de tejido a ambos lados del nódulo de Arancio/Morgagni.
Respecto a la técnica de traslocación arterial, existen algunos reportes que evidencian que la técnica de trap-door clásica respecto a la técnica de inclusión puede representar un factor de riesgo añadido en la dilatación de la NRA; sin embargo, los hallazgos no son homogéneos entre autores.
Las técnicas de reparación valvular en la población pediátrica se encuentran limitadas por las características inherentes a estos pacientes. Es de trascendental importancia el análisis individual de cada paciente basado en la estructura de la compresión de la raíz valvular aórtica o neoaórtica como una unidad funcional, con el fin de buscar el mayor éxito en términos de competencia valvular y durabilidad posible.
Consideraciones éticasEl consentimiento informado fue obtenido de los padres de la paciente para realizar esta publicación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.