La naturaleza heterogénea de la válvula aórtica bicúspide (VAB) y su asociación con la dilatación de la aorta ascendente ha sido reconocida en muchos estudios observacionales. El objetivo de nuestro estudio es valorar la asociación que tiene el patrón de aortopatía con la morfología y lesión valvular primaria de esta valvulopatía.
MétodosDesde febrero del 2007 hasta noviembre del 2013, 107 pacientes con VAB y aneurisma de aorta ascendente fueron derivados a cirugía. Identificamos la morfología valvular intraoperatoriamente y la lesión valvular primaria por ecocardiografia. Con la tomografía preoperatoria realizamos mediciones en varios sectores de la aorta ascendente.
ResultadosLa edad media al momento de la cirugía fue significativamente menor en enfermos con insuficiencia frente a estenosis aórtica (51 vs. 64 años, p<0,001). La raíz aórtica fue significativamente mayor en enfermos con insuficiencia (N=24) comparado con estenosis aórtica (N=39) (45mm vs. 38mm, p<0,001). La fusión comisural derecho-no coronariano (N=10) presentó diámetros de arco aórtico proximal, medio y distal significativamente mayores que la fusión comisural izquierdo-derecho (N= 53), p<0,05.
ConclusionesLos pacientes con VAB que tienen insuficiencia aórtica como lesión predominante presentan criterios de intervención a edades más tempranas y se asocian a aneurisma de raíz aórtica. El patrón de fusión comisural derecho-no coronariano dilata más el arco aórtico que el resto de morfologías valvulares. Estos resultados nos corroboran que el lugar de mayor dilatación de la aorta ascendente en estos pacientes podría estar relacionado directamente con la morfología y la lesión valvular predominante.
The heterogeneous nature of the bicuspid aortic valve and its association with the ascending aortic aneurysm has been recognized in many observational studies. The main aim in this study is to evaluate the existing association of the pattern of aortic disease with the morphology and primary valvular lesion of the bicuspid aortic valve.
MethodsA total of 107 patients with bicuspid aortic valve underwent surgery between February 2007 and November 2013. The valvular morphology and the primary valve lesion with was identified using echocardiography. The aorta was measured at different levels using the pre-operative computed tomography.
ResultsThe mean age at the time of surgery was significantly lower in patients with insufficiency than those with aortic stenosis (51 vs. 64 years old, P<.001). The aortic root was significantly higher amongst those with insufficiency (N=24) compared to aortic stenosis patients (N=39) (45mm vs. 38mm, P<.001). The right non-coronary leaflet fusion (N=10) showed diameters for proximal, median and distal arch significantly higher than left-right leaflet fusion (N=54), P<.05.
ConclusionsBicuspid aortic valve patients with aortic insufficiency as main lesion have surgical criteria at younger ages and are associated with aortic root aneurysms. The Right-Non coronary leaflet fusion has more prevalence of aortic arch aneurysm than the rest of the valvular morphologies. These results corroborate that in patients with bicuspid aortic valve, the area of aortic aneurysm can be linked directly with the morphology and the predominant valve lesion.
La válvula aórtica bicúspide (VAB) es la anomalía cardíaca más frecuente, con una prevalencia entorno al 1-2% de la población mundial. Aunque algunos estudios previos indican que hasta el 80% de los pacientes con VAB desarrollan aneurismas de aorta ascendente, con un riesgo de disección 9 veces mayor que la población general1, series más recientes con un volumen considerable de pacientes nos indican que este tipo de complicaciones no son tan frecuentes, situando el desarrollo de aneurismas de aorta ascendente en pacientes portadores de VAB en torno al 4,8 y el 9,9%, respectivamente2,3. Clásicamente, se han barajado 2 teorías para explicar la asociación entre aneurismas de aorta ascendente y VAB: 1) la teoría genética, donde se sugiere que existe una alteración estructural de la pared aórtica causada por desórdenes genéticos, y 2) la teoría hemodinámica, la cual postula que la etiología de la dilatación son las anomalías en el flujo sobre la aorta ascendente proximal debidas a la alteración morfológica valvular, dado que la VAB, aun siendo «normofuncionante», es por su especial configuración una válvula estenótica4. No obstante, cada vez hay mayor evidencia de que la VAB es una entidad con una enorme heterogeneidad e implicaciones clínicas y pronósticas muy diferentes. En efecto, aunque la tendencia actual es a tratar agresivamente la aorta de pacientes con VAB debido a la creencia extendida de una historia natural desfavorable, con presentación precoz de la enfermedad, el riesgo aumentado de complicaciones aórticas, como la disección y la posible herencia poligénica en algunas familias, lo cierto es que la mayoría de los pacientes con VAB tienen un curso clínico mucho más favorable3. Podemos, por tanto, decir que no hay suficiente nivel de evidencia para justificar un «tratamiento profiláctico» de la aorta en todos los casos de aortopatía asociada a VAB. La VAB presenta muchas variantes morfológicas o fenotipos, en función de la fusión de las comisuras, presencia o no de rafe, orientación comisural, etc., y además puede presentarse clínicamente con estenosis, insuficiencia o doble lesión. La asociación entre esta gran heterogeneidad de la VAB y los distintos patrones de aortopatía ha sido discutida por muchos autores en los últimos años, aunque con resultados discordantes.
La tendencia actual va dirigida hacia individualizar el enfoque y el manejo de estos pacientes, debido a lo cual es fundamental establecer una estratificación de grupos de riesgo que diferencie entre aquellos pacientes con un bajo riesgo de dilatación y de complicaciones aórticas y los que presentarán un curso más grave de la enfermedad aórtica y que, por tanto, precisarán de una intervención más precoz y más agresiva. Se trata, por tanto, de correlacionar cada variante anatómica de la VAB con el desarrollo de un determinado patrón de aortopatía, determinar qué pacientes tienen más riesgo de complicaciones como la disección e identificar en qué enfermos la aortopatía se presenta de forma más severa y temprana.
El objetivo del presente estudio es valorar la asociación entre las distintas características anatómicas y funcionales (patrón de fusión comisural [PFC] y lesión valvular primaria [LVP]) de la VAB y los patrones de dilatación de aorta ascendente.
MétodosDesde febrero del 2007 hasta noviembre del 2013, 107 pacientes con diagnóstico de VAB fueron derivados a cirugía en nuestro centro, bien debido a criterios de valvulopatía aórtica, o bien por criterios de tamaño de la aorta ascendente. A todos los pacientes se le realizó una ecocardiografía transtorácica preoperatoria mediante la cual se determinó LVP y se hizo una primera aproximación para determinar el patrón de fusión comisural, el cual fue corroborado en la gran mayoría de los casos intraoperatoriamente. Como protocolo preoperatorio, a nuestros pacientes con esta alteración valvular se les realizó una tomografía de tórax preoperatoria para valorar los diámetros de aorta ascendente, así como las posibles limitaciones a la cirugía convencional.
VariablesEl estudio ecocardiográfico preoperatorio fue realizado por 3 ecocardiografistas expertos de nuestro centro. La LVP se determinó por distintos parámetros (área valvular aórtica, grado medio). La LVP la subdividimos de la siguiente forma: insuficiencia aórtica (IAo), estenosis aórtica (EAo) y doble lesión aórtica (DLAo, pacientes con EAo en los cuales la insuficiencia era al menos moderada). Con respecto a la morfología valvular, con la ecocardiografía se hizo un primer acercamiento diagnóstico, que fue corroborado intraoperatoriamente en el 74,7% de la muestra (80 pacientes).
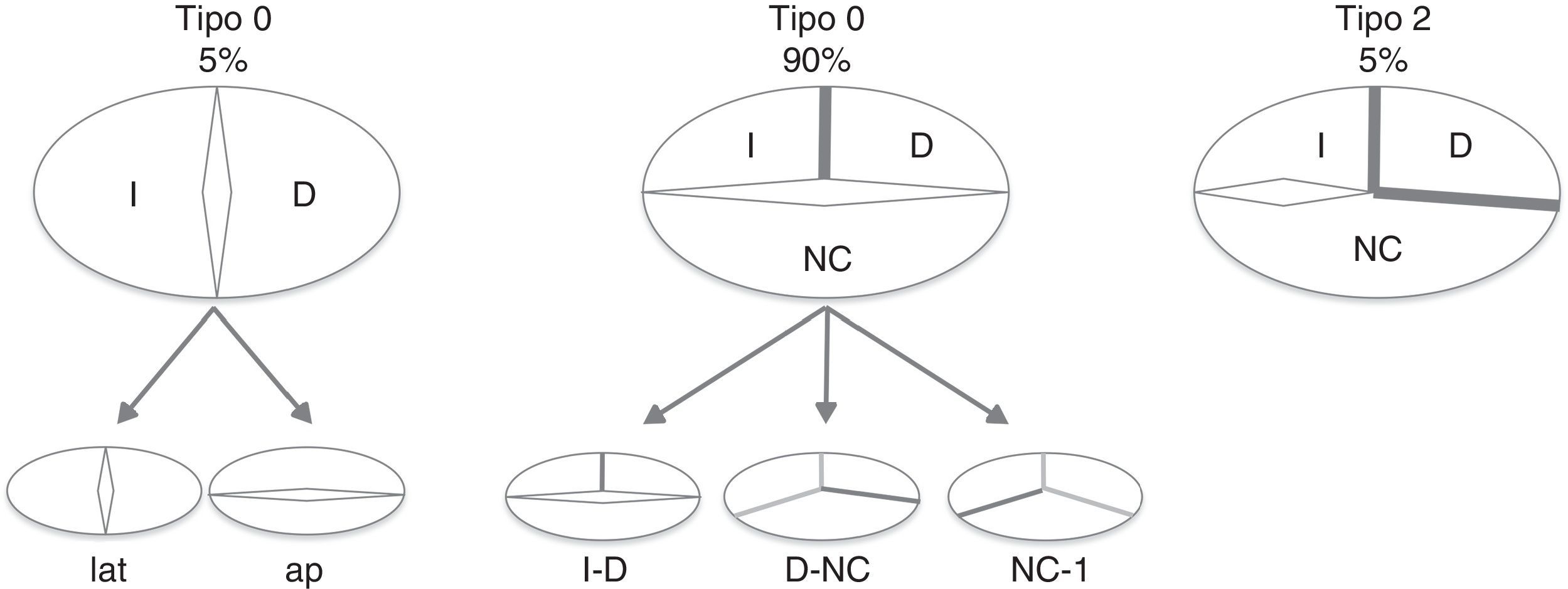
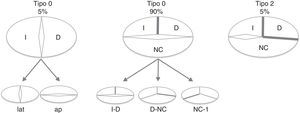
El PFC fue categorizado siguiendo la clasificación de Sievers (2007)5: a) tipo 0 (VAB pura, sin rafe); b) tipo 1 (morfología valvular más frecuente con un rafe entre los 2 velos), que se subdivide en: tipo 1 con fusión de velo aórtico izquierdo-derecho (tipo 1 I-D, el más frecuente), tipo 1 con fusión de velo derecho-velo no coronariano (tipo 1 D-NC, el segundo más frecuente), tipo 1 con fusión de velo izquierdo-no coronariano (tipo 1 I-NC, muy infrecuente), y por último, c) tipo 2 (con 2 rafes, monocúspide) (fig. 1).
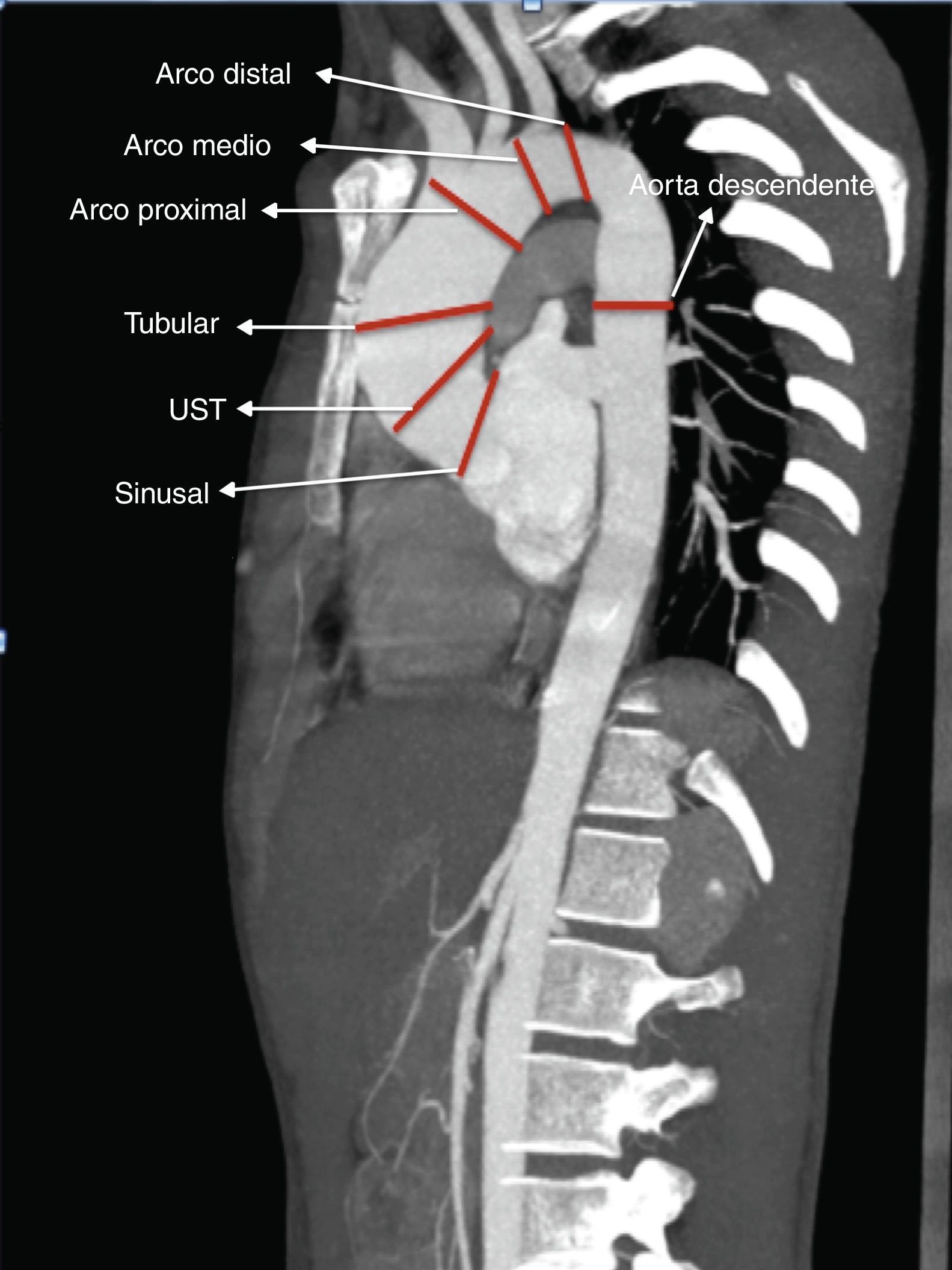
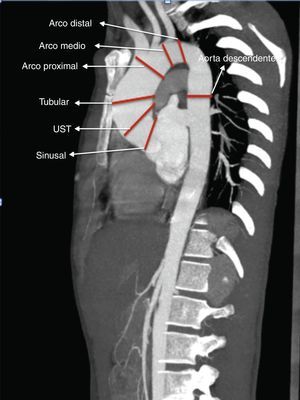
Con la tomografía de tórax preoperatoria realizamos mediciones de la aorta ascendente a varios niveles: sinusal, unión sino-tubular (UST), tubular, arco proximal (AP), arco medio (AM), arco distal (AD) y aorta torácica descendente (fig. 2).
Análisis estadísticoDespués de asegurar una distribución normal de la muestra, las variables continuas fueron comparadas con el t test y ANOVA. Las variables categóricas fueron presentadas como porcentajes y comparadas con la prueba de la χ2 y test de Fisher, siempre que fuese necesario.
ResultadosCiento siete pacientes fueron derivados a intervención. El 80,4% (86 pacientes) de la muestra total eran varones. Al evaluar la distribución de género con respecto a los distintos PFC evidenciamos que 90% (9 pacientes) del PFC D-NC y el 71% (38 pacientes) del PDC I-D eran varones. La distribución de género con respecto a la LVP no mostró diferencias significativas: el 79,5% (31 pacientes) de pacientes con EAo, el 75% (18 pacientes) de pacientes con IAo y el 83% (35 pacientes) de pacientes con DLAo eran varones (p=NS).
La edad media ± desviación estándar de la muestra total fue de 58±13 años. La edad media al momento de la intervención fue significativamente menor en enfermos con IAo comparado con EAo (51 vs. 64 años, p = 00,2) (tabla 1). Con respecto al patrón de fusión comisural, la edad no mostró diferencias estadísticamente significativas en los distintos subgrupos (tabla 2).
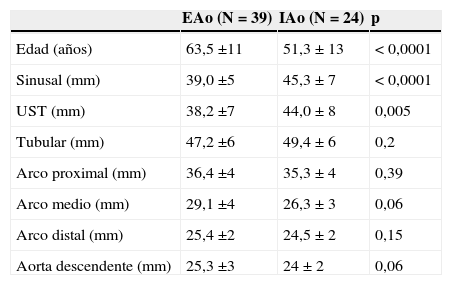
Comparación entre pacientes con válvula aórtica bicúspide que presentan estenosis aórtica e insuficiencia aórtica
| EAo (N = 39) | IAo (N = 24) | p | |
|---|---|---|---|
| Edad (años) | 63,5 ±11 | 51,3 ± 13 | < 0,0001 |
| Sinusal (mm) | 39,0 ±5 | 45,3 ± 7 | < 0,0001 |
| UST (mm) | 38,2 ±7 | 44,0 ± 8 | 0,005 |
| Tubular (mm) | 47,2 ±6 | 49,4 ± 6 | 0,2 |
| Arco proximal (mm) | 36,4 ±4 | 35,3 ± 4 | 0,39 |
| Arco medio (mm) | 29,1 ±4 | 26,3 ± 3 | 0,06 |
| Arco distal (mm) | 25,4 ±2 | 24,5 ± 2 | 0,15 |
| Aorta descendente (mm) | 25,3 ±3 | 24 ± 2 | 0,06 |
Se presenta la media ± desviación estándar.
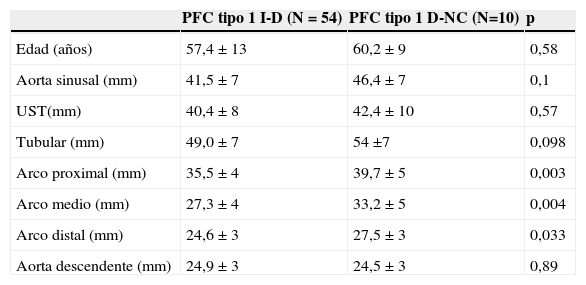
Comparación entre el patrón de fusión comisural I-D y patrón de fusión comisural D-NC
| PFC tipo 1 I-D (N = 54) | PFC tipo 1 D-NC (N=10) | p | |
|---|---|---|---|
| Edad (años) | 57,4 ± 13 | 60,2 ± 9 | 0,58 |
| Aorta sinusal (mm) | 41,5 ± 7 | 46,4 ± 7 | 0,1 |
| UST(mm) | 40,4 ± 8 | 42,4 ± 10 | 0,57 |
| Tubular (mm) | 49,0 ± 7 | 54 ±7 | 0,098 |
| Arco proximal (mm) | 35,5 ± 4 | 39,7 ± 5 | 0,003 |
| Arco medio (mm) | 27,3 ± 4 | 33,2 ± 5 | 0,004 |
| Arco distal (mm) | 24,6 ± 3 | 27,5 ± 3 | 0,033 |
| Aorta descendente (mm) | 24,9 ± 3 | 24,5 ± 3 | 0,89 |
Se presenta la media ± desviación estándar.
La LVP presentó la siguiente distribución: 36% (39 pacientes) de la muestra presentaban EAO, IAo en el 22,4% (24 pacientes) y DLAo en el 39% (42 pacientes); solo en 2 pacientes no se pudo determinar la LVP por ecocardiografía.
Al evaluar la distribución del PFC en la muestra global de pacientes, encontramos que el 49,5% de la muestra (53 pacientes) presentaban PFC tipo 1 I-D, el 9,3% (10 pacientes) presentaban PFC tipo 1 D-NC, ningún paciente presentaba PFC tipo 1 I-NC, el 11,2% (12 pacientes) presentaban PFC tipo O y el 4,6% (5 pacientes) presentaban PFC tipo ii. En el 254% de la muestra no obtuvimos información con respecto al PFC.
El diámetro medio de raíz aórtica fue a nivel sinusal de 41,4±6,5mm y en UST de 39,7±7,5mm. El 47% de la muestra total de pacientes presentaba diámetros de raíz aórtica>de 40mm. Estas mediciones fueron significativamente mayores en pacientes con IAo al compararlos tanto con enfermos con EAo (sinusal 45mm vs. 38mm y UST 44mm vs. 38mm, p<0,05) como con pacientes con DLAo (sinusal 45mm vs. 39mm y UST 44mm vs. 38mm, p<0,05). Los diámetros de raíz aórtica no mostraron diferencias estadísticamente significativas cuando comparamos los distintos patrones de fusión comisural (p = NS) (tabla 2).
El diámetro medio de la aorta tubular fue de 48,8±6,6mm; en este sector de la aorta ascendente ni el PFCPni la LVP de la BAV presentaron diferencias estadísticamente significativas, p=NS.
Al evaluar el arco aórtico en la muestra global, el diámetro medio del AP fue 36±4,8mm, AM de 28±4,5mm y AD 24±3,4mm. El 25,2% de la muestra presentaba diámetros de arco aórtico>40mm. El PFC D-NC presentaba diámetros de A), AM y AD significativamente mayores que el PFC I-D (AP 40mm vs. 35mm, AM 35mm vs. 27mm y AD 28mm vs. 24mm, p<0,05). No se encontraron diferencias significativas al comparar los diámetros de arco aórtico a todos los niveles entre los pacientes con PFC tipo 1 I-D (N=54) y PFC tipo 0 (N=12). Con respecto a la LVP, tampoco se encontraron diferencias significativas (tabla 1).
DiscusiónLa aortopatía asociada a VAB constituye una lesión frecuente cuyo correcto manejo no está claramente establecido, existiendo una gran disparidad de criterios de indicación y técnicas para su tratamiento, lo cual indica que en esta patología aún estamos bastante lejos de la evidencia y, por tanto, queda mucho por hacer. Las guías clínicas de manejo de la patología de aorta torácica publicadas en 20106 establecían unos criterios de indicación generales basados en el tamaño aórtico y/o la velocidad de crecimiento, recomendando el reemplazo aórtico para aortas mayores de 5cm o con un crecimiento superior a 0,5cm/año en el caso de la VAB. Sin embargo, la Guía Europea sobre manejo de valvulopatías publicada en 20127 y la más reciente de la Sociedad Americana de Valvulopatías8 establecen unas recomendaciones menos liberales para la cirugía de aorta en los pacientes con VAB, considerando el reemplazo aórtico para tamaños de más de 5cm solo en determinados subgrupos de riesgo, es decir, pacientes con historia familiar de disección de aorta o velocidad de crecimiento superior a 0,5cm/año (clase iia, nivel de evidencia C). El resto de los pacientes debería intervenirse en caso de diámetro de aorta mayor de 5,5cm, al igual que la población general (sin VAB). Por otro lado, el manejo en la práctica diaria muestra una escasa adherencia a las guías, con algunos grupos que intervienen de forma más agresiva realizando cirugía «preventiva» en aortas con dilatación muy ligera y otros que tratan exclusivamente la lesión valvular dejando sin tratar aortas que pueden medir entre 40 y 50mm. Existen trabajos en la literatura que apuntan hacia una estabilidad de la aorta tras cirugía de reemplazo valvular aislado2,9,10 y otros que describen una evolución menos favorable, con elevado riesgo de dilatación, rotura y reoperación con el tiempo11–13, por lo que recomiendan cirugía de aorta durante la corrección de la lesión valvular o en los casos de dilatación mayor de 45-50mm, sobre todo si hay coartación de aorta o antecedentes familiares de disección. En cuanto al tipo de técnica quirúrgica y la extensión de la reparación también hay diferencias, con grupos que sustituyen sistemáticamente la raíz aórtica y el arco aórtico junto con la aorta ascendente14-16 y otros que realizan técnicas de aortoplastia de reducción17,18, a pesar de tratarse de pacientes en general jóvenes y con una patología en la que no está claro el grado de participación que las alteraciones genéticas y moleculares tienen en la fragilidad de la pared aórtica. Algunos autores preconizan extender la reparación al arco aórtico19, dada la frecuencia de afectación del mismo en la VAB15. Sin embargo, dicha práctica probablemente es excesiva e innecesaria en los casos con dilatación leve a moderada del arco, ya que se ha demostrado ausencia de dilatación del arco con el tiempo en los pacientes con VAB20. Toda esta variabilidad en la toma de decisiones sobre cuándo intervenir a los pacientes, qué técnica utilizar y cuánto de aorta resecar deberá ir disminuyendo a medida que dispongamos de mayor información que permita una valoración más precisa e individualizada del riesgo de futuras complicaciones aórticas en el paciente con VAB. Para ello, uno de los primeros aspectos a dilucidar es si existe relación entre los fenotipos de VAB y patrones específicos de afectación aórtica, en cuanto a extensión y severidad de la misma. En 2008, Fazel et al.15 establecieron cuatro patrones o «clusters» de aortopatía en la VAB mediante el estudio con técnicas de imagen en una muestra de 64 pacientes. En este estudio, un 58% de los pacientes tenían afectación de la raíz y hasta un 73% afectación del AP. Los autores recomiendan extender la reparación quirúrgica con sustitución de raíz y técnica de península en el arco en todos los casos en los cuales la raíz y/o el arco presenten dilatación ligera o moderada. En cuanto a los diferentes fenotipos de VAB y los patrones de dilatación, Fazel et al.15 no encuentran resultados significativos, aunque se trata de una muestra muy pequeña en la que el 71% de los pacientes tenían un fenotipo 1 I-D (el más frecuente). Este estudio contrasta con el de Della Corte et al.21, que previamente habían publicado un trabajo en el que la dilatación aislada de la aorta ascendente era el patrón de aortopatía habitual, siendo la edad, la hipertensión y el grado de severidad de la EAo factores relacionados con el grado de dilatación. En esta serie la afectación de raíz aórtica solo se observó en un 13,6% de los pacientes, los cuales eran sobre todo varones y con IAo severa, siendo la estenosis un factor protector frente a la afectación de la raíz. Según esto, los autores concluyen que la cirugía de raíz solo es necesaria en un 10% de los pacientes.
En nuestro estudio hemos analizado a 107 pacientes con una distribución por sexos similar a la descrita en la literatura para la VAB y con una edad media en el momento de la cirugía menor a la de los pacientes con válvula aórtica tricúspide. En cuanto al tipo de lesión, la proporción de pacientes con IAo fue algo inferior a la de los pacientes con estenosis o doble lesión, siendo además más jóvenes los pacientes con insuficiencia valvular. El grado de afectación de la raíz fue del 47%, lo cual es similar al estudio de Della Corte et al.21 y claramente inferior al del grupo de Stanford15. En nuestro estudio, los pacientes con IAo presentaban diámetros medios de raíz aórtica significativamente mayores que aquellos pacientes que presentaban estenosis o DLAo como LVP; estos resultados están consonancia con los resultados de Della Corte et al.21,22 y con publicaciones previas23. Un aspecto importante que se debe resaltar de nuestro análisis es que no encontramos diferencias significativas al evaluar los diámetros de raíz aórtica con las distintas morfologías de la VAB, lo cual va en contradicción con publicaciones previas sobre las cuales se afirma que el PFC tipo 1 I-D presenta más prevalencia de dilatación de raíz aórtica24,25. Al analizar la aorta tubular, nuestro estudio no mostró resultados estadísticamente significativos con el tipo de lesión valvular y el patrón de fusión de las comisuras, a diferencia de lo reportado por Della Corte et al. Con respecto al arco aórtico, uno de los hallazgos de más relevancia de nuestro estudio es la asociación que existe entre la dilatación del arco aórtico y el PFC tipo 1 D-NC, si bien es sabido que los pacientes con VAB dilatan las porciones más proximales del arco aórtico15; previamente, en la literatura no se ha descrito la existencia de asociación entre aneurismas de arco aórtico y algún morfotipo particular de VAB.
Con los resultados de nuestro estudio podemos afirmar con mayor certeza que la mejor opción terapéutica quirúrgica para enfermos con VAB que presentan aneurismas de aorta ascendente debe ser individualizada teniendo en cuenta morfotipo valvular, la LVP y el lugar de la afección aneurismática. Podemos afirmar que la mayoría de los pacientes con VAB que presentan exclusivamente aneurismas de aorta tubular se pueden beneficiar de la sustitución aislada de este sector de la aorta, independientemente de la morfología valvular y la LVP de la VAB. En pacientes portadores de VAB que presentan aneurismas de raíz aórtica es bien conocida la asociación con IAo, género masculino y pacientes jóvenes, por lo tanto, pensamos que debería considerarse a este subtipo de aneurisma de aorta ascendente como una entidad patogénica independiente y que sería adecuado replantear las guías actuales por recomendaciones más agresivas debido a que se trata de un pequeño grupo de enfermos con mayor riesgo de complicaciones a largo plazo26. Con respecto a la cirugía de arco aórtico, sugerimos que se debe ser más agresivos en aquellos enfermos que presentan morfología valvular PFC tipo 1 D-NC dada la tendencia que presenta este grupo de enfermos a dilatar este sector en particular. En cuanto a aortoplastia, creemos que sería una alternativa solo en aquellos casos con raíz y arco normales, con dilatación moderada de aorta ascendente (< 45mm) y con riesgo elevado para un procedimiento más definitivo como la sustitución de aorta.
ConclusionesLa principal conclusión del análisis de nuestros resultados es que existen 2 factores que claramente determinan el lugar de la dilatación en la aorta ascendente en pacientes portadores de VAB: la LVP y el patrón de fusión comisural. Los pacientes portadores de VAB que presentan IAo como LVP tienen una clara asociación con aneurisma de raíz aórtico y también presentan criterios de intervención a edades más tempranas que pacientes con EAo. El PFCPtipo 1 D-NC se caracteriza por dilatar más el arco aórtico que el resto de morfotipos valvulares. El PFCPtipo 1 I-D se caracteriza por dilatar fundamentalmente la aorta tubular.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.