Los tumores cardiacos son infrecuentes con una sintomatología muy variable. Representan 0,2% de todas las neoplasias en general. El linfoma cardiaco primario representa 1,3% de los tumores cardiacos primarios y 0,5% de los linfomas extranodales. Se define como un linfoma no Hodgkin (LNH) que afecta solo al corazón y/o el pericardio. El linfoma no Hodgkin difuso de células B grandes es la variante histológica más frecuente. Se presenta un caso clínico de un paciente masculino de 57 años de edad, sin patología de base que fue hospitalizado en el servicio de cardiología con el diagnóstico de infarto agudo de miocardio sin elevación del segmento ST; en una ecocardiografía transtorácica se constata una masa intracardiaca en aurícula izquierda.
Cardiac tumors are infrequent with highly variable symptoms. They represent 0.2% of all neoplasms in general. Primary cardiac lymphoma represents 1.3% of primary cardiac tumors and 0.5% of extranodal lymphomas. It is defined as a non-Hodgkin's lymphoma (NHL) that affects only the heart and/or the pericardium. Diffuse large B-cell non-Hodgkin's lymphoma is the most common histological variant. A clinical case of a 57-year-old male patient is presented, with no underlying pathology who was hospitalized in the cardiology service with a diagnosis of non-ST-segment elevation acute myocardial infarction; A transthoracic echocardiogram revealed an intracardiac mass in the left atrium.
Los tumores cardiacos se dividen en primarios y secundarios; estos últimos son entre 20-40 veces más frecuentes. Dentro de los primarios, existen tumores benignos y malignos1.
Constituyen una enfermedad poco frecuente en la práctica clínica. La mayoría de las veces aparecen en adultos de 30 a 60 años de edad; 65% se produce en mujeres. Los mixomas son los tumores benignos más comunes del corazón y aproximadamente 75% de ellos se encuentra en la aurícula izquierda2 estas se desarrollan desde el borde de la fosa oval, ubicada en el septum interauricular3–5.
El tratamiento es, habitualmente quirúrgico, que debe ser oportuno para evitar futuras complicaciones y consiste en la resección completa del tumor intracardiaco2–4.
Historia clínicaAntecedentes y enfermedad actualSe presenta un paciente masculino de 57 años de edad, de procedencia urbana, niega patologías de base, niega hábito tabáquico, refiere ser bebedor social. Había sido intervenido quirúrgicamente por una colecistitis aguda hace 10 años. Ingresó con dolor en epigastrio de siete horas de evolución aproximadamente, con una intensidad 7/10 de carácter tipo opresivo y pesadez, no relacionado con los movimientos, que no irradia y no cede con el reposo. Se acompaña de náuseas y vómitos en dos oportunidades. A todo esto, se le agregó dificultad respiratoria. Había presentado cuadros similares anteriores de dolor en epigastrio hace 10 años aproximadamente.
Exploración físicaAl examen físico se observa mala tolerancia al decúbito dorsal, taquipneico (25 respiraciones por minuto) con tendencia a la desaturación de oxígeno (94%), por lo que requirió oxígeno suplementario; por mascarilla facial a tres litros por minuto. A la auscultación impresiona estertores crepitantes en ambas bases pulmonares. La frecuencia cardiaca era de 88 lpm y la tensión arterial de 110/70 mmHg. El resto de la exploración no presentó ninguna alteración.
Pruebas complementariasPrimeramente, se le realizó un electrocardiograma en donde se observaba un ritmo regular, sinusal, con una frecuencia cardiaca de 92 lpm, intervalo PR 200 ms, complejo QRS 120 ms, sin signos de hipertrofia ventricular, una extrasístole supraventricular en el tercer latido, segmento ST deprimido en derivaciones DII, DIII, aVF de 2 mV y V3, V4, V5 con 4 mV aproximadamente.
En la radiografía de tórax se evidencia una radiopacidad en pulmón derecho que abarca mayoritariamente el campo pulmonar medio, además signos de congestión en el tercio inferior de ambos campos pulmonares e hilios ingurgitados.
En los exámenes de laboratorio se evidenció leucocitosis a expensas de neutrofilia (13.400/91%), respectivamente, y ante la sospecha de un infarto agudo de miocardio se realizó dosaje de troponina; primer juego de troponina I ultrasensible de 0,20 ng/L, segundo juego de 11.377,6 ng/L y en el tercer juego 37.151,7 ng/L, cada uno de ellos con una diferencia de seis horas aproximadamente en la toma de muestra.
Con la impresión diagnóstica de un síndrome coronario agudo, se inició carga antiisquémica (clopidogrel 300 mg, ácido acetilsalicílico 325 mg y atorvastatina 80 mg), con posterior mejoría del cuadro.
Llama la atención en este paciente que luego de ocho horas aproximadamente del inicio del dolor en epigastrio se le realiza un segundo electrocardiograma en donde se observa normalización de los segmentos ST de las derivaciones afectadas en comparación con el electrocardiograma anterior.
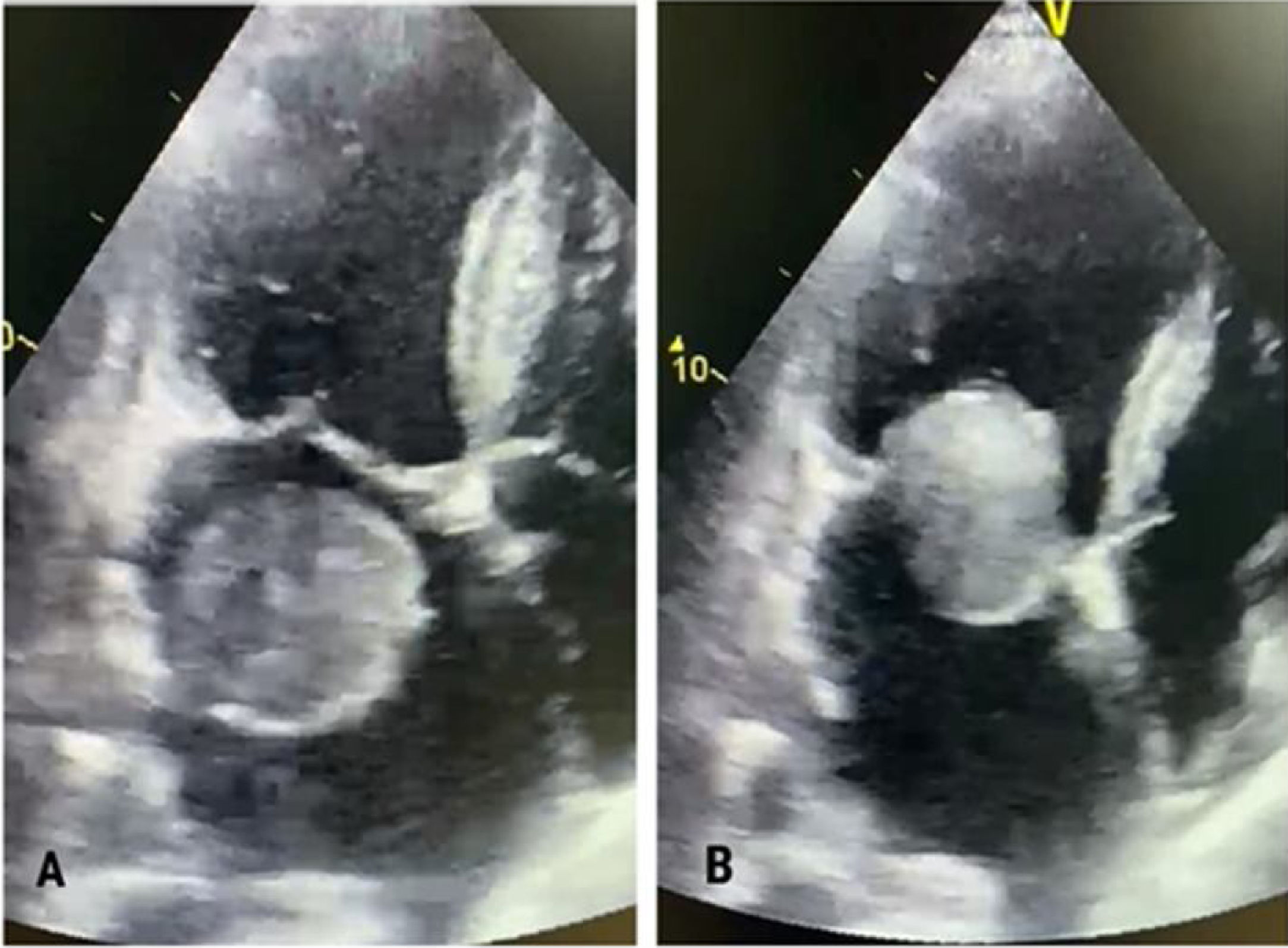
Por disponibilidad, tres días después se le realiza un ecocardiograma transtorácico en el que se observó una imagen ecogénica en aurícula izquierda de 60 x 49 mm, de bordes regulares, bien definidos, con una densidad acústica similar a las paredes miocárdicas, con base en la implantación en el tercio inferior del septum interauricular, de gran movilidad con desplazamiento hacia el anillo mitral y la cavidad ventricular izquierda durante la diástole, presentando características de un mixoma. Sin alteraciones valvulares a expensas de la válvula mitral que presentaba signos de esclerosis con una insuficiencia moderada. Aurícula izquierda dilatada con 57 mm. Fracción de eyección conservada. No se observan otras masas similares en las demás cámaras cardiacas (fig. 1).
Por las características de la masa intracardiaca y en el contexto preoperatorio se incluyó la cineangiocoronariografía diagnóstica. Este estudio arrojó las siguientes conclusiones:
- •
Tronco coronario izquierdo: con imagen radiolúcida en silla de montar sugerente de trombo con estenosis moderada.
- •
Arteria descendente anterior: con imagen radiolúcida ostioproximal sugerente de trombo con estenosis leve.
- •
Arteria circunfleja y la primera rama marginal de la arteria circunfleja: con imagen radiolúcida ostioproximal sugerente de trombo con estenosis severa.
En el contexto de este paciente se decidió exéresis del tumor intracardiaco más bypass coronario (la primera rama marginal de la arteria circunfleja) en el mismo acto operatorio. El paciente se mantuvo estable hasta el día de la cirugía, 13 días después de su ingreso.
EvoluciónEl paciente fue sometido a cirugía cardiaca mediante incisión esternal media longitudinal, infusión de heparina, canulación y entrada a circulación extracorpórea en hipotermia moderada, infusión de cardioplejia cristaloide por raíz de la aorta, atriotomía derecha, apertura del septum interauricular, resección de tumoración auricular izquierda de aproximadamente 6 cm de diámetro, consistencia sólida/elástica. Se procede a la rafia del septum y cierre de atriotomía derecha. Se realiza el bypass aortocoronario vena safena izquierda/primera rama marginal de la arteria circunfleja. Control de hemostasia sin particularidades. Tiempo de circulación extracorpórea: 75 min, tiempo de pinzamiento aórtico: 40 min.
Posteriormente fue ingresado a unidad de cuidados intensivos (UCI), en donde se le realiza una ecocardiografía transtorácica postoperatoria para evaluar el resultado quirúrgico, en donde se observó una dilatación leve de la aurícula izquierda, hipoquinesia septal, disfunción diastólica grado II, válvula mitral con insuficiencia leve (fig. 2B). En las primeras 24 h del procedimiento el paciente presentó una plejia facio-braquio-crural izquierda; se realiza una tomografía de cráneo simple en donde se constata una imagen hipodensa en región tálamo-capsular derecha, sin efecto de masa sobre las estructuras de la línea media (fig. 3). Se decide solo tratamiento con antiagregantes y estatinas, sin presentar criterios para fibrinólisis. No obstante, tuvo una evolución clínica favorable y se mantuvo tres días en UCI para luego pasar a sala común.
El material extirpado (fig. 2A) fue enviado a anatomía patológica para su estudio en donde se describió un tumor nodular hipocelular de abundante matriz mixoide conteniendo pequeños acúmulos, algunos de forma cordonal, en nidos y otros en estructuras anulares, incluso de aspecto pseudoglandular, constituidos por células de citoplasma eosinófilo y núcleos pequeños ovalados sin atipia, inmersos en un fondo laxo mixoide, compatibles con un mixoma cardiaco. El diagnóstico diferencial principal fue de linfoma no Hodgkin, ya que mostraba amplios sectores de necrosis y material fibrinoide y dentro de ésta se observaba un infiltrado de células de núcleos ovoides grandes, vesiculosos de escaso citoplasma, atipias, de aspecto linfoide, con presencia de numerosas mitosis y apoptosis la cual requería inmunohistoquímica para su diagnóstico. La inmunohistoquímica confirmó que además del mixoma se trataba también de un linfoma no Hodgkin de células grandes B (CD20+) de tipo activación (CD10-, BCL6+, MUM1+).
Confirmado el diagnóstico de linfoma, se le realizó una tomografía por emisión de positrones, en donde no se evidencia captación patológica del trazador 18-FDG, la cual excluye la afectación del linfoma a otro tejido, así también de las demás cámaras cardiacas. Con todos los datos requeridos se decide la realización de esquema R-CHOP con doxorrubicina liposomal en cuatro ciclos de forma ambulatoria. Fue dado de alta luego de 20 días desde su internación.
DiscusiónComo diagnóstico diferencial incluimos al fibroma, aunque este es más frecuente en niños también puede afectar a adultos y se localizan más a menudo en el ventrículo izquierdo y en el tabique interventricular, la clínica es muy similar a la del mixoma. También incluimos al rabdomiosarcoma por ser el más frecuente entre los sarcomas cardiacos2,3.
La frecuencia de aparición de los tumores cardiacos es muy baja y sus manifestaciones clínicas son muy variables, siendo considerado el «gran simulador». El diagnóstico temprano mediante un ecocardiograma transtorácico6 (sensibilidad de 94%) y el tratamiento quirúrgico oportuno reducen el riesgo de complicaciones y mejoran la sobrevida3.
La presencia del tumor de gran tamaño a nivel de la aurícula izquierda y su prolapso a través de la válvula mitral genera un mecanismo obstructivo al flujo sanguíneo3 y una dilatación de la aurícula izquierda en respuesta a la obstrucción mecánica4,5.
El tipo de mixoma polipoide y móvil está relacionado con una mayor frecuencia de embolismos5.
El accidente cerebrovascular perioperatorio es una de las complicaciones que pueden presentarse durante el proceder quirúrgico y hasta los 30 días posteriores al mismo, siendo la embolia la principal causa. Rara vez es reportado en cirugías de exéresis de tumores cardiacos4–7.
La aparición de un linfoma cardiaco es muy poco común y las cavidades derechas son las localizaciones más frecuentes del linfoma cardiaco primario (LCP). En 92% de los casos se encuentran comprometidas la aurícula derecha, esto contrasta con la afectación solitaria de lado izquierdo del corazón que solo es observada en 7%8.
No existe un tratamiento estándar de oro para el LCP. El pronóstico de supervivencia de estos pacientes es malo, con variaciones en la mediana de supervivencia global informada de siete meses, 12 meses y 63 meses, sin embargo, se reduce a un mes si la neoplasia compromete al ventrículo izquierdo8.
Por la ubicación de este tumor en la aurícula izquierda, como complicación perioperatoria se incluye el accidente cerebrovascular isquémico ya que el tumor cuando es móvil tiende a la formación de trombos que posteriormente embolizan al cerebro más frecuentemente. Los médicos deben considerar el LCP dentro de sus planteamientos etiológicos ante la identificación de un tumor en el curso de una insuficiencia cardiaca8.
Consideraciones éticasPara la presentación y posterior publicación de este caso clínico como aporte científico se consideró el consentimiento informado del paciente en cuestión, el cual nos autorizó el uso de los datos clínicos e imágenes y fue informado la intención franca de evitar perjudicarlo; que todo esto se utilizaría como objeto de investigación.
FinanciaciónNinguna.
Conflicto de interesesNinguno.