Investigar la supervivencia y las complicaciones mayores cardiovasculares a 10 años (muerte a 30 días, accidente cerebrovascular, reoperación protésica y sangrado mayor) en pacientes de 50 a 65 años tras sustitución valvular aórtica aislada con prótesis biológicas o mecánicas debido a estenosis aórtica severa.
Material y métodoEstudio analítico y retrospectivo de 721 pacientes procedentes de 5 centros con servicio de Cirugía Cardiovascular en Andalucía intervenidos entre los años 2000 y 2015. Como criterios de exclusión se encuentran: la cirugía concomitante, las reintervenciones y la endocarditis. Se realiza posteriormente un pareado por puntuación de propensión 1:1 para obtener 2 grupos de 181 pacientes para su comparación.
ResultadosEl 26% recibió bioprótesis (n=187), con un 35% de mujeres, y un EuroscoreI medio de 2,5% para las prótesis mecánicas versus un 2,9% para las biológicas (p=0,05). La supervivencia a 10 años fue del 70% para las biológicas versus el 78% para las mecánicas, con diferencias entre grupos (p=0,02) a favor de las mecánicas, que desaparecen tras el pareado (2 grupos de 181 pacientes, log-rank p=0,269). Las prótesis mecánicas presentaron más sangrado mayor (p=0,01), con mayor reintervención en las biológicas (p=0,01). No hubo diferencias en accidente cerebrovascular (p=0,660) ni en mortalidad a 30 días (p=0,08). El seguimiento medio fue de 6,7±4,3 años en el grupo mecánicas, y de 6,1±3,1 años en el grupo biológicas (p=0,03).
ConclusionesNo existen diferencias en supervivencia a 10 años. Las prótesis mecánicas presentaron mayor sangrado mayor, y las bioprótesis mayor necesidad de reintervención. Es preciso finalizar el estudio a 15 años para confirmar estos datos.
To investigate the survival and major cardiovascular complications at 10 years (30-day mortality, stroke, prosthetic valve reoperation and major bleeding) in middle-aged patients between 50 to 65 years undergoing isolated aortic valve replacement by severe aortic stenosis with biological or mechanical prostheses.
Material and methodRetrospective analytical study of 721 patients from 5 centers with Cardiovascular Surgery in Andalousia between the years 2000-2015. Exclusion criteria include concomitant surgery, reinterventions and infective endocarditis. Matching was performed by 1:1 propensity score to obtain two groups of 181 patients for comparison.
ResultsThe 26% of the sample received a bioprosthesis (n=187), 35% were women, with a mean EuroscoreI of 2.5% in mechanical prostheses versus 2.9% biological (P=.05). Ten-year survival was 70% biological versus 78% mechanical, with differences between groups (P=.02) in favor of mechanical group, which disappears after matching (log-rank P=.269). Mechanical prostheses presented more major bleeding (P=.01) versus greater re-intervention in biological ones (P=.01). There were no differences in stroke (P=.660) nor 30-day mortality (P=.08). Mean follow-up was 6.7±4.3 years in mechanical, versus 6.1±3.1 years in biological (P=.03).
ConclusionsThere are no differences in 10-year survival in the matched sample. Mechanical prostheses showed higher major bleeding, and bioprostheses showed increased need for reoperation. The study must be completed up to 15 years to confirm the data.
La sustitución valvular aórtica (SVA) es el tratamiento de elección en la actualidad para pacientes con valvulopatía aórtica severa. Se realiza en ∼280.000 pacientes en todo el mundo cada año1, y en ∼5.000 en España2. Las últimas guías clínicas de valvulopatías de 2017 de la Sociedad Europea de Cardiología/Asociación Europea de Cirugía Cardiotorácica (ESC/EACTS) sostienen que las bioprótesis deberían considerarse de elección en pacientes mayores de 65 años de edad3. En pacientes con edades comprendidas entre los 60-65 años, se considera como opciones aceptables tanto las prótesis mecánicas como las biológicas (indicación de clase IIa). Según la reciente actualización de 2017 de las guías clínicas americanas de la American Heart Association/American College of Cardiology (AHA/ACC)4, la elección de la válvula cardíaca protésica debe ser un proceso compartido de toma de decisiones entre médico y paciente, ampliándose el rango de edad de los 60-70 años a los 50-70 años para considerar como aceptable la elección de cualquier tipo de prótesis (indicación de clase IIa) en función de los deseos del paciente.
Actualmente existen datos contradictorios en cuanto a supervivencia a largo plazo en el grupo de pacientes de entre 50-65 años en función del tipo de prótesis implantada, biológica o mecánica. Chiang et al.5, en una cohorte estadounidense en 2014, publicaron que la bioprótesis podría considerarse para pacientes de hasta 50 años de edad, lo que es respaldado por otros estudios6. Glaser et al.7, en una cohorte sueca, concluyeron en 2016 que los pacientes de 50-69 años que recibieron válvulas mecánicas tenían una mejor supervivencia a largo plazo. El riesgo de accidente cerebrovascular (ACV) fue similar. Sin embargo, los pacientes con bioprótesis tuvieron un mayor riesgo de reoperación y un menor riesgo de hemorragia mayor en ambos estudios.
Posteriormente, en diciembre de 2017, Goldstone et al.8 publicaron el mayor estudio hasta la fecha sobre la materia, con más de 9.900 pacientes de entre 45-65 años. Apreciaron en una cohorte californiana (Estados Unidos) que no existieron diferencias significativas entre tipos de prótesis en cuanto a la supervivencia a 15 años en pacientes mayores de 55 años, con menos sangrado mayor y más reoperaciones en las biológicas.
A pesar de todo, la SVA biológica en pacientes de 50-65 años sigue siendo controvertida, ya que también depende de la durabilidad a largo plazo de la bioprótesis que se utilice. En estudios publicados con pacientes en este rango de edad se ha visto que hasta un 85% fallece antes de necesitar reintervención, con una durabilidad media de hasta 19 años y un 15% de riesgo de reoperación a 15 años en una cohorte de más de 500 pacientes9.
Las tasas de eventos esperados para complicaciones perioperatorias y relacionadas con la válvula a largo plazo no se han determinado claramente en este subgrupo de pacientes en una población mediterránea. Nuestro objetivo fue cuantificar la supervivencia a largo plazo (15 años) y la morbilidad mayor (tasas de ACV, reoperación valvular aórtica y eventos hemorrágicos mayores) en un grupo de pacientes de 50 a 65 años que recibieron una SVA primaria aislada con válvulas bioprotésicas o mecánicas debido a una estenosis aórtica severa entre los años 2000 y 2015.
MétodosEste estudio consiste en el análisis interino de datos del estudio ANDALVALVE (ANDALousian Aortic VALVE Multicentric Study [ClinicalTrials.gov ID: NCT03239509]) una vez alcanzado el 50% de los pacientes.
Diseño del estudioSe realizó un estudio analítico, retrospectivo y multicéntrico en el cual participaron todos los centros públicos con servicio de Cirugía Cardiovascular de Andalucía (España). Se analizó a todos los pacientes de entre 50 y 65 años con estenosis aórtica severa intervenidos mediante cirugía de SVA primaria aislada entre 2000-2015 como criterio de inclusión. El estudio fue aprobado por el Comité de Ética el 27 de abril de 2017 (Comité de Ética de la Investigación Provincial de Málaga, documento anexo).
Los datos del presente estudio son aquellos entregados con fecha 10 de enero de 2018, representando el 50% de la muestra total esperada (análisis interino de datos), con datos de 5 de los 7 centros participantes. La mayoría (>90%) de pacientes analizados en este análisis interino se intervinieron entre 2005 y 2015.
Los criterios de exclusión fueron: residencia fuera de Andalucía, necesidad de cirugía concomitante, cirugía cardíaca previa y endocarditis infecciosa. Se obtuvieron 721 pacientes divididos en 2 grupos: mecánico (n=534) y biológico (n=187).
Objetivos del estudioComo objetivos principales se consideraron la supervivencia a largo plazo (máximo 17 años) y la presencia de complicaciones mayores cardíacas y cerebrovasculares (MACCE), definidas como muerte de cualquier causa, ACV, reoperación sobre prótesis de cualquier causa y sangrado mayor según los criterios del Valve Academic Research Consortium 210. Las características preoperatorias, muertes y MACCE se identificaron utilizando el programa de registros médicos Diraya Atención Especializada ([DAE], Servicio Andaluz de Salud, España) y la base de datos local de cada departamento de Cirugía Cardiovascular, buscando en todas las admisiones hospitalarias y consultas ambulatorias o de urgencias cualquier complicación. Los datos se confirmaron por contacto telefónico directo con el paciente y/o familiares en caso de fallecimiento.
Método estadísticoPara ajustar las diferencias en las características preoperatorias iniciales y el sesgo de selección, se realizó un análisis en crudo de los datos y un análisis pareado mediante puntuación de propensión posterior. Se utilizó un protocolo de comparación 1:1 tipo «vecino más cercano» (nearest neighbour matching), sin reemplazo, y con una calibración máxima igual a 0,2 de la desviación estándar del logit de la puntuación de propensión. Se obtuvo un tamaño muestral final de 362 pacientes, 181 por cada grupo de estudio para su comparación.
Todos los análisis se realizaron con el paquete de software IBM SPSS Statistics 22.0 para Windows (IBM Corp., Armonk, NY, EE.UU.). Las variables continuas se expresan como media±desviación estándar. Las variables categóricas se expresan como frecuencias absolutas (n) y relativas (%). Las diferencias basales entre los pacientes que recibieron válvulas bioprotésicas o mecánicas se detectaron mediante la prueba t de Student y la prueba de Chi-cuadrado (χ2) para las variables categóricas. En los casos en que no se pudo aceptar la normalidad, se aplicó la prueba no paramétrica correspondiente.
Todas las características basales (edad, sexo, EuroscoreI logístico, índice de masa corporal, hipertensión, diabetes mellitus, fibrilación auricular, enfermedad pulmonar obstructiva crónica, dislipidemia, ACV previo, infarto de miocardio previo, enfermedad renal crónica, valor de creatinina preoperatorio, arteriopatía periférica, gradiente transaórtico medio y fracción de eyección del ventrículo izquierdo) se incluyeron como covariables en el modelo de la puntuación de propensión.
Se construyeron curvas de supervivencia de Kaplan-Meier para los grupos tras el pareado mediante puntuación de propensión. La diferencia en la supervivencia se evaluó con la prueba log-rank Mantel-Cox.
La degeneración estructural significativa (DES) se definió como fallo protésico que condiciona una insuficiencia aórtica severa, una estenosis aórtica severa con gradientes transaórticos>40mmHg, o un incremento>20mmHg respecto de los valores ecocardiográficos postoperatorios previos al alta.
ResultadosPoblación de estudioIdentificamos a todos los pacientes de 50 a 65 años que cumplían los criterios de inclusión y exclusión. Se detectaron un total de 758 pacientes con SVA primaria aislada hasta el 1 de enero de 2018.
El seguimiento fue completado en 721 pacientes (95%). En 534 (74%) de los pacientes se implantaron prótesis mecánicas y en 187 (26%) bioprótesis. Los tiempos de seguimiento medio y máximo fueron 6,5±4,5 y 17 años en la cohorte global, 6,7±4,3 y 17 años en el grupo de válvula mecánica, y 6,1±3,1 y 17 años en el grupo de válvula bioprotésica (p=0,03). El uso de bioprótesis aumentó del 13% de todas las SVA en 2000-2008 al 33% en 2009-2015, mientras que la edad media de los pacientes por año se mantuvo relativamente constante alrededor de los 60 años.
Las bioprótesis utilizadas fueron 82 (44%) Carpentier-Edwards Perimount (Edwards Lifesciences, Irvine, EE.UU.), 56 (30%) Mitroflow (Sorin Group, Saluggia, Italia), 17 (9%) de Stentless tipo Freedom 10 (5%) o Freedom Solo 7 (4%) (Sorin Group, Saluggia, Italia) y 6 (3%) Stentless Porcine Toronto (St Jude Medical, Inc, St Paul, MN, EE.UU.), siendo de otras marcas las 26 (14%) prótesis restantes. Entre las válvulas mecánicas hubo 268 (50%) Carbomedics/Pericarbon (Sorin Group, Saluggia, Italia), 197 (37%) ATS (Medtronic, MN, EE.UU.), y 69 (13%) correspondían a prótesis de otras marcas.
Características de los pacientesLas características basales de los pacientes en la cohorte global se muestran en la tabla 1. La edad media fue 58,8 años en los pacientes que habían recibido válvulas mecánicas (M) y 60,8 años en los que habían recibido válvulas bioprotésicas (B, p=0,001). En comparación con los pacientes que recibieron bioprótesis, los pacientes que habían recibido válvulas mecánicas eran 2 años más jóvenes y tenían más fibrilación auricular crónica preoperatoria (12% M vs. 6% B; p=0,02) y arteriopatía periférica (2,6% M vs. 6% B; p=0,03).
Características basales de toda la muestra (no ajustada)
| Todos (n=721) | Mecánicas (n=534) | Biológicas (n=187) | p | |
|---|---|---|---|---|
| Edad (años) | 59,3±4,3 | 58,8 (4,1) | 60,8 (3,7) | 0,0001 |
| Sexo femenino | 67 (33,5%) | 188 (35%) | 69 (36,8%) | 0,678 |
| Logistic Euroscore (%) | 2,6±2,3 | 2,5±1,7 | 2,9±1,6 | 0,090 |
| IMC (kg/m2) | 29,2±5 | 29,3±5,4 | 29,4±5,6 | 0,784 |
| Hipertensión | 454 (62%) | 326 (61%) | 125 (67%) | 0,200 |
| Diabetes mellitus | 166 (23%) | 112 (21%) | 48 (25,6%) | 0,933 |
| Fibrilación auricular | 77 (10,6%) | 63 (12%) | 11 (6,0%) | 0,020 |
| Enfermedad pulmonar obstructiva crónica | 90 (12,5%) | 59 (11%) | 30 (16%) | 0,080 |
| Hiperlipidemia | 314 (31%) | 233 (44%) | 84 (45%) | 0,823 |
| Ictus previo | 32 (4,4%) | 20 (3,7%) | 11 (6,0%) | 0,080 |
| Infarto miocardio previo | 49 (7%) | 34 (6%) | 15 (8%) | 0,324 |
| Insuficiencia renal crónica | 45 (6,8%) | 33 (6%) | 12 (6%) | 0,824 |
| Valor creatinina (mg/dL) | 1,06±0,9 | 1,02±1,3 | 0,99±0,3 | 0,307 |
| Arteriopatía periférica | 25 (3,7%) | 14 (2,6%) | 11 (6%) | 0,030 |
| Fumador | 132 (18%) | 106 (20%) | 26 (14%) | 0,183 |
| Hábito alcohólico | 23 (11,5%) | 53 (10%) | 22 (12%) | 0,428 |
| FEVI (%) | 59±12 | 58±13,6 | 60±10 | 0,091 |
| Gradiente máximo transaórtico (mmHg) | 77±24 | 75±24 | 79±25 | 0,690 |
| Gradiente medio transaórtico (mmHg) | 51±18 | 50±20 | 52±17 | 0,312 |
Las variables categóricas se expresan como n (%). Las variables continuas se expresan como media±desviación estándar.
FEVI: fracción de eyección ventrículo izquierdo; IMC: índice de masa corporal.
Negrita: valores estadísticamente significativos.
Tras el pareado por puntuación de propensión (se obtuvieron 2 grupos de 181 pacientes), se aprecia que todas las variables están equilibradas y no presentan diferencias (tabla 2).
Características basales de los pacientes tras el pareado
| Mecánicas (n=181) | Biológicas (n=181) | p | |
|---|---|---|---|
| Edad (años) | 60,9 (2,7) | 60,8 (3,7) | 0,670 |
| Sexo femenino | 59 (32,5%) | 67 (37%) | 0,377 |
| Logistic Euroscore (%) | 3 (2,2) | 2,8 (1,6) | 0,526 |
| IMC (kg/m2) | 29,6 (5,5) | 29,54(5,6) | 0,611 |
| Hipertensión | 118 (65%) | 121 (67%) | 0,739 |
| Diabetes mellitus | 43 (23,7%) | 46 (25,4%) | 0,714 |
| Fibrilación auricular | 11 (6%) | 11(6%) | 1,000 |
| Enfermedad Pulmonar Obstructiva crónica | 20 (11%) | 27 (15%) | 0,274 |
| Hiperlipidemia | 84 (46%) | 83 (46%) | 0,600 |
| Ictus previo | 9 (5%) | 13 (7%) | 0,379 |
| Infarto miocardio previo | 4 (3,4%) | 6 (7,2%) | 0,746 |
| Insuficiencia renal crónica | 14 (7,7%) | 12 (6,6%) | 0,591 |
| Valor creatinina (mg/dL) | 1,08±1,3 | 0,99±0,3 | 0,307 |
| Arteriopatía periférica | 7 (4%) | 10 (5,5%) | 0,156 |
| Fumador | 24 (13%) | 25 (14%) | 0,110 |
| Hábito alcohólico | 18 (10%) | 21 (11%) | 0,950 |
| FEVI (%) | 57±13 | 60±10 | 0,083 |
| Gradiente máximo transaórtico (mmHg) | 79±25 | 78,8±24 | 0,957 |
| Gradiente medio transaórtico (mmHg) | 48±20 | 52±17 | 0,319 |
Las variables categóricas se expresan como n (%). Las variables continuas se expresan como media±desviación estándar.
FEVI: fracción de eyección ventrículo izquierdo; IMC: índice de masa corporal.
La figura 1 muestra las curvas de supervivencia Kaplan-Meier para la supervivencia global en los pacientes no emparejados, existiendo diferencias significativas en favor del grupo de prótesis mecánicas; las curvas de supervivencia de la cohorte tras el pareado se muestran en la figura 2. Tras el pareado por puntuación de propensión no se observaron diferencias en la supervivencia a largo plazo (log-rank Mantel-Cox p=0,263): las bioprótesis obtuvieron una supervivencia del 88, 67 y 40% frente al 82, 65 y 25% obtenido por las prótesis mecánicas a los 5, 10 y 15 años, respectivamente. En la cohorte emparejada hubo 34 (19%) muertes en el grupo de bioprótesis y 42 (23%) muertes en el grupo de prótesis mecánicas durante un máximo de 17 años de seguimiento. El hazard ratio (HR) de muerte para el grupo de prótesis mecánicas frente al grupo de bioprótesis fue de 1,3 (IC 95%: 0,82-2,00; p=0,272).
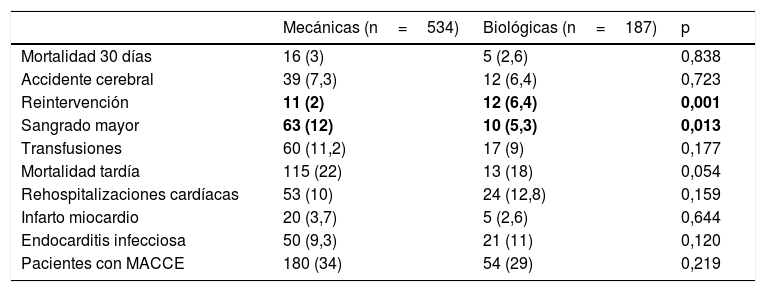
En la tabla 3 se resumen todas las MACCE de la cohorte global sin emparejar. El objetivo combinado MACCE de las 4 complicaciones principales (mortalidad a los 30 días, ACV, cualquier reoperación relacionada con prótesis y hemorragia mayor/transfusión) fue no significativo (p=0,219): grupo biológico, 54/187 (29%) frente a grupo mecánico, 180/534 (34%).
Eventos mayores cardiovasculares adversos (MACCE) en la muestra general (no ajustada)
| Mecánicas (n=534) | Biológicas (n=187) | p | |
|---|---|---|---|
| Mortalidad 30 días | 16 (3) | 5 (2,6) | 0,838 |
| Accidente cerebral | 39 (7,3) | 12 (6,4) | 0,723 |
| Reintervención | 11 (2) | 12 (6,4) | 0,001 |
| Sangrado mayor | 63 (12) | 10 (5,3) | 0,013 |
| Transfusiones | 60 (11,2) | 17 (9) | 0,177 |
| Mortalidad tardía | 115 (22) | 13 (18) | 0,054 |
| Rehospitalizaciones cardíacas | 53 (10) | 24 (12,8) | 0,159 |
| Infarto miocardio | 20 (3,7) | 5 (2,6) | 0,644 |
| Endocarditis infecciosa | 50 (9,3) | 21 (11) | 0,120 |
| Pacientes con MACCE | 180 (34) | 54 (29) | 0,219 |
Variables categóricas expresadas como n (%).
Negrita: valores estadísticamente significativos.
Después del emparejamiento (tabla 4), hubo 59 (32,5%) pacientes con MACCE en el grupo mecánico y 52 (28,7%) en el grupo biológico, sin alcanzar la significación estadística (p=0,425).
Eventos mayores cardiovasculares adversos (MACCE) en la muestra general pareada
| Mecánicas (n=181) | Biológicas (n=181) | p | |
|---|---|---|---|
| Mortalidad a 30 días | 10 (5,5) | 3 (1,6) | 0,086 |
| Accidente cerebral | 10 (5,5) | 11 (6) | 0,660 |
| Reintervención | 3 (2) | 12 (6,6) | 0,001 |
| Sangrado mayor | 22 (12) | 9 (5) | 0,015 |
| Transfusiones | 25 (14) | 16 (9) | 0,136 |
| Mortalidad tardía | 42 (23) | 34 (19) | 0,302 |
| Rehospitalizaciones | 11 (6) | 21 (12) | 0,094 |
| Infarto miocardio | 5 (3) | 5 (3) | 1,000 |
| Endocarditis infecciosa | 18 (10) | 28 (15) | 0,102 |
| Pacientes con MACCE | 59 (32,5) | 54 (29) | 0,425 |
Variables categóricas expresadas como n (%).
Negrita: valores estadísticamente significativos.
Analizando cada MACCE por separado (tabla 4, cohorte pareada), podemos apreciar que se evidencia mayor sangrado mayor en el grupo mecánico (12% M vs. 5% B; p=0,01) y mayor tasa de reoperación en el grupo biológico (2% M vs. 6,6% B; p=0,001), si bien por DES fue en solo 5 casos (2,7%); en el resto (n=8) fue debido a endocarditis infecciosa en 6 casos y a trombosis en otros 2. Hubo 2 trombosis y otras 2 prótesis con formación de pannus en el grupo mecánico (4 casos, 2%).
Tanto en tasa de ACV (5,5% M vs. 6% B; p=0,660) como en mortalidad precoz a 30 días (5,5% M vs. 2,1% B; p=0,07) no se apreciaron diferencias significativas.
No hubo diferencias significativas en aparición de endocarditis infecciosa.
DiscusiónLa elección actual del tipo de prótesis cardíaca debe ser una decisión compartida de acuerdo con el deseo del paciente, tras una correcta información. Las pautas existentes en las guías valvulares EACTS/ESC 2017 indican que cualquier elección es razonable en pacientes de 60 a 65 años, siendo una SVA mecánica razonable en pacientes menores de 60 años3. En la última actualización de las guías americanas de la AHA/ACC en 2017, se amplió el rango de edad hasta los 50-70 años para considerar como razonable la elección de cualquier prótesis4.
Estos límites de edad se establecen en el punto en el que el beneficio de la bioprótesis (ausencia de anticoagulación) supera el riesgo de reintervención por DES, ya que una menor edad está directamente asociada a la misma3,4,9. Este cambio en el valor de corte es compatible debido a que las bioprótesis actuales parecen tener tasas más bajas de DES, gracias a los nuevos tratamientos anticalcificación, que los utilizados durante los ensayos clínicos aleatorizados históricos11-13, con bioprótesis de primera generación. Por tanto, los hallazgos de estos estudios pueden no reflejar los resultados en la actualidad. Además, debido a que los riesgos de la reoperación han seguido disminuyendo con el tiempo, los pacientes jóvenes que reciben SVA son más reacios a aceptar las restricciones de actividad o dieta que conlleva la toma de anticoagulantes orales (NACO) en caso de portar válvulas mecánicas.
Los estudios previos no aleatorizados que investigaron la supervivencia y los resultados clínicos después de SVA con válvulas mecánicas o bioprotésicas en pacientes de mediana edad han obtenido resultados contradictorios. Algunos estudios obtuvieron mayor supervivencia a largo plazo en pacientes con válvulas mecánicas7,14,15, mientras que otros no observaron diferencias entre tipos valvulares5, sobre todo a partir de los 55 años8.
También en un gran metaanálisis de 32 artículos con seguimiento durante 10 años con 17.439 pacientes y 101.819 pacientes-año que recibieron SVA, no encontraron diferencias significativas en la mortalidad entre las válvulas mecánicas y las biológicas en todos los grupos de edad16; incluso en el grupo de menores de 60 años no se apreciaron diferencias en la supervivencia tras más de 20 años de seguimiento17.
Desde 2014, varios estudios observacionales (Chiang et al.5, Glaser et al.7, y Goldstone et al.8) presentaron resultados contradictorios. Los primeros, en 2014, no encontraron diferencias en la supervivencia (HR=0,97, IC 95%: 0,83-1,14; p=0,74), pero sí mayores tasas de hemorragia en las válvulas mecánicas (12% vs. 7%; p=0,001) y mayores reintervenciones en las válvulas biológicas (12% vs. 6%; p=0,001), con las mismas tasas de ACV (8%, p=0,84) a los 15 años. Los segundos, en 2016, encontraron una mayor supervivencia en el grupo mecánico (mortalidad en las biológicas: HR=1,34, IC 95%: 1,09-1,66; p=0,006), con resultados MACCE similares a los de Chiang et al.: mayores tasas de hemorragia en el grupo mecánico (16% vs. 8%; p=0,001) y más reintervenciones en las biológicas (8% vs. 4%; p=0,001), con las mismas tasas de ACV (12%, p=0,84) a los 15 años. Esta diferencia podría explicarse debido a la excelente calidad del control de anticoagulación realizado en Suecia, que ha demostrado repetidamente ser muy bueno18. Por lo tanto, esta calidad del manejo de la anticoagulación puede afectar favorablemente los resultados clínicos en pacientes con válvulas cardíacas mecánicas.
A finales de 2017 se publicó en el New England Journal of Medicine el estudio de Goldstone et al.8, el de mayor número de pacientes hasta la fecha, con más de 9.900 aórticos, que estudió mediante una base de datos poblacional del estado de California (EE.UU.) la supervivencia a largo plazo en función del tipo de prótesis implantada, estratificando por grupo de edad. Los resultados mostraron una mayor supervivencia en prótesis mecánicas entre los 45-55 años (mortalidad: 30,6% B vs. 26,4% M a 15 años; HR=1,23; IC 95%: 1,02-1,48; p=0,03, diferencia de 6 meses), mientras que entre los 55-65 años no se encontraron diferencias en cuanto a supervivencia (HR=1,04; IC 95%: 0,91-1,18; p=0,60). En el subgrupo de mayores de 55 años no hubo diferencias en ACV (HR=0,92; IC 95%: 0,73-1,13), mientras que sí las hubo en cuanto a sangrado mayor a favor de las biológicas (HR=0,66; IC 95%: 0,58-0,75) y en reoperación a favor de las mecánicas (HR=2,46; IC 95%: 1,93-3,20).
Tras analizar detenidamente estos estudios, decidimos realizar un estudio piloto en una población mediterránea, en cuyos pacientes las áreas de superficie corporal y los tamaños de las válvulas tienden a ser más pequeños que en las de otros países19. Se obtuvo una tendencia hacia el doble de complicaciones de MACCE en las mecánicas, con supervivencias similares a los 15 años, aunque sin alcanzar diferencias estadísticamente significativas, probablemente debido a un tamaño de muestra pequeño20.
A raíz de este trabajo surge la necesidad de una colaboración multicéntrica a nivel autonómico para incrementar el tamaño muestral en esta población tan particular, por lo cual se crea el estudio ANDALVALVE, con el objeto de que aúne a los 7 centros públicos con Cirugía Cardiovascular de Andalucía, inscribiéndose como Registro retrospectivo en la página web clinicaltrials.gov.
Nuestros resultados en MACCE tras el pareado de la muestra inicial son consistentes con los estudios más recientes, con tasas de ACV similares (5,5% M vs. 6% B; p=0,660), mayor número de hemorragias mayores en las prótesis mecánicas (12% M vs. 5% B; p=0,01) y más reoperaciones en el grupo de bioprótesis (2% M vs. 7% B; p=0,01), con tasas muy bajas de DES que requiera de reintervención, que fue solo de 5 casos (2,7%). La variabilidad de marcas de bioprótesis utilizadas, junto con el escaso número de pacientes en este grupo de edad, hacen no viable una comparativa entre válvulas debido a la escasa potencia estadística.
En cuanto a la durabilidad actual de las bioprótesis, Bourguignon et al.9 objetivaron que la esperanza de vida de los pacientes operados de estenosis aórtica severa era menor que la población general francesa a pesar de la SVA. Por encima de los 50 años, la estimación esperada de durabilidad de la válvula Carpentier-Edwards fue igual o superior a la esperanza de vida tras la cirugía en el 85% de los pacientes, con una mediana de durabilidad de la válvula de 19 años21. Otras prótesis también han demostrado excelentes resultados a largo plazo, como la Hancock II (Medtronic, MN, EE.UU.)22. A pesar de la preocupación generalizada sobre la durabilidad de la válvula Mitroflow por DES precoz, comunicada por determinados centros, antes de añadirse el nuevo tratamiento anticalcificación23, estudios recientes apreciaron ausencia de reoperación por DES a 10 años en un 96%24.
Incluso si se requiere una nueva intervención, las reoperaciones sobre prótesis aórticas se pueden realizar de forma segura. Los resultados actuales han mejorado, con tasas de mortalidad de alrededor del 5%25 o bajando incluso hasta el 2,5% con cirugía mínimamente invasiva26. Además, la generalización de los procedimientos transcatéter (TAVI) ha propiciado la aparición de la técnica valve in valve (ViV), que actualmente es considerada una alternativa a la reoperación para pacientes de alto riesgo27. Esta opción está cambiando la dinámica en cuanto a la discusión de las ventajas y desventajas entre las válvulas mecánicas y las bioprotésicas. A pesar de las expectativas generadas, no todas las bioprótesis son adecuadas para un futuro procedimiento ViV, que siempre requiere la inserción de una válvula más pequeña que la original, y el desajuste o mismatch prótesis-paciente podría ser un problema potencial.
También existe un cambio de paradigma tras la reciente introducción de inhibidores de trombina directos orales e inhibidores del factor Xa para el tratamiento de la fibrilación auricular como alternativa a la warfarina. Actualmente, estos nuevos NACO no están aprobados para las válvulas mecánicas28, pero los pacientes que han recibido una bioprótesis y que presenten fibrilación auricular pueden elegir entre la warfarina y los NACO, que son más fáciles de administrar, no presentan restricción dietética y no precisan análisis de sangre repetidos, además de ser más seguros29. Por lo tanto, es necesario reconsiderar el mito establecido de que un paciente con fibrilación auricular precisa una prótesis mecánica al estar ya anticoagulado.
La presencia de sangrado mayor en nuestro estudio ocurrió en el 12% de las prótesis mecánicas y en el 5% de las biológicas. La mortalidad a los 30 días después de un evento hemorrágico mayor en estudios recientes5 alcanza un 13,2%, por lo que el mejor perfil de seguridad de los NACO es un factor muy importante.
Un ensayo clínico que comparó los regímenes de anticoagulación automonitorizada de baja intensidad frente a anticoagulación estándar en pacientes con válvulas mecánicas no demostró una reducción significativa en eventos hemorrágicos mayores o tromboembólicos30. Estos resultados, junto con la insatisfacción del paciente frente a la perspectiva de una vida con anticoagulación, pueden explicar en parte el uso creciente de bioprótesis que observamos durante la última década1,2.
Creemos que la tecnología en evolución (nuevas prótesis diseñadas para un futuro ViV), tratamientos anticalcificantes nuevos30 y la evolución de las TAVI promoverán una disminución en el rango de edad para las tasas de implante de bioprótesis en los próximos años.
Limitaciones del estudioEste estudio consiste en el análisis interino de datos del estudio ANDALVALVE (ClinicalTrials.gov ID: NCT03239509) una vez alcanzado el 50% de los pacientes. Será preciso analizar la muestra global para confirmar los resultados.
Para evitar los sesgos de selección del presente estudio observacional, analítico y retrospectivo, se realizó un pareado mediante puntuación de propensión. Sin embargo, solo es posible emparejar las variables medidas y registradas previamente. Puede haber factores no medidos o desconocidos o ambos que no pudimos controlar (factores de confusión residual). Esto potencialmente podría introducir un sesgo a favor de las válvulas mecánicas porque los cirujanos clásicamente implantaban bioprótesis en este grupo de edad en aquellos pacientes que consideraban frágiles, con una esperanza de vida reducida o con contraindicación para anticoagulación.
El análisis de las complicaciones una vez completado el 100% del estudio se realizará mediante un análisis de riesgos competitivos, ya que la muerte puede limitar la aparición de dichas complicaciones MACCE.
Los datos ecocardiográficos de seguimiento no se obtuvieron en el mismo punto de tiempo durante el seguimiento. Las interpretaciones interpersonales de ecocardiogramas también podrían subestimar la tasa real de DES y el valor de los gradientes.
ConclusionesActualmente hay un uso cada vez mayor de bioprótesis tanto en Andalucía como a nivel mundial. Tras obtener el 50% de los datos y realizar el análisis interino, entre los pacientes pareados no hubo diferencias en la supervivencia a largo plazo entre válvulas mecánicas y válvulas biológicas. Las prótesis mecánicas presentaron mayor sangrado y las biológicas mayor reoperación, con una tendencia de más complicaciones en las válvulas mecánicas. Es imprescindible la colaboración multicéntrica para obtener resultados robustos y extrapolables en nuestro medio.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Este artículo ha sido aceptado para comunicación oral en el XXIV Congreso de la SECTCV, celebrado en Murcia del 30 mayo al 2 junio de 2018.