Introducción. El tratamiento laparoscópico de la enfermedad por reflujo gastroesofágico se acompaña de importantes ventajas clínicas, aunque existen algunos puntos controvertidos: una correcta indicación quirúrgica, el tipo de funduplicatura más apropiada en virtud de los estudios preoperatorios y el valor que tienen ciertos detalles técnicos.
Pacientes y método. Hemos practicado una funduplicatura a 176 pacientes, con un rango de edad entre 22 y 78 años. La indicación de cirugía incluyó: intratabilidad médica, pacientes jóvenes y hernia paraesofágica. La sintomatología predominante fue: reflujo (93%), disfagia (38%), dolor torácico (18%) y síntomas respiratorios (4%). Nuestra serie incluye 27 casos (15%) de enfermedad por reflujo gastroesofágico sin hernia asociada, 119 (67%) de hernia de hiato axial, 14 (8%) de hernia de hiato paraesofágica y 16 (9%) de hernia de hiato mixta. A todos los pacientes se les practicó un estudio baritado gastroduodenal, endoscopia en 88 (50%), pH-metría, en 140 (89%) y manometría en 146 (92%).
Resultados. Las técnicas utilizadas fueron: Nissen-Rosetti en 114 casos (65%), Toupet en 55 (31%) y Dor en 6 (3%). Se seccionaron los vasos cortos en 7 casos (4%). El índice de complicaciones intraoperatorias fue del 1,7%, la tasa de conversión del 1,7% y la tasa de reintervenciones del 1,1%. En todos los casos se controló la sintomatología de reflujo. El 60% de los pacientes no presentaron disfagia, el 29%, disfagia leve (< 4 semanas), el 10% moderada (> 4 semanas) y el 0,63% disfagia grave. Seis pacientes (3,41%) presentaron un síndrome de retención gaseosa.
Conclusión. La cirugía antirreflujo por vía laparoscópica ofrece resultados similares a los de la cirugía abierta, con las ventajas añadidas de este tipo de abordaje. Estos resultados dependen de una correcta indicación y de la elección de una técnica quirúrgica adecuada e individualizada para cada paciente.
Introduction. Laparoscopic treatment of gastroesophageal reflux disease (GERD) offers considerable clinical advantages, although there remain a number of controversial aspects, including the definition of the correct surgical indication, the most suitable type of fundoplication in accordance with preoperative studies and the value of certain technical details.
Patients and method. We performed fundoplication in 176 patients between the ages of 22 and 78 years. The surgical indication included refractoriness to medical treatment, young age and paraesophageal hernia. The predominant symptomatology was reflux (93%), dysphagia (38%), chest pain (18%) and respiratory symptoms (4%). Our series included 27 patients (15%) with GERD without hernia, 119 (67%) with axial hiatal hernia (HH), 14 (8%) with paraesophageal HH and 16 (9%) with mixed HH. All the patients underwent gastroduodenal barium study. Endoscopy was performed in 88 (50%), pH-metry in 140 (89%) and manometry in 146 (92%).
Results. The following fundoplications were carried out: Nissen-Rosetti in 114 patients (65%), Toupet in 55 (31%) and Dor in 6 (3%). The short gastric vessels were transected in 7 cases (4%). The incidence of intraoperative complications was 1.7%, the rate of conversion was 1.7% and the reoperation rate was 1.1%. Reflux symptoms were monitored in every case. Sixty percent of the patients presented no dysphagia, 29% had mild dysphagia (< 4 weeks), which was moderate (> 4 weeks) in 10% and severe in 0.63%. Six patients (3.41%) complained of gas bloat.
Conclusion. The outcome of laparoscopic antireflux surgery is similar to that of open surgery, plus the benefits of this approach. The results depend on the correct identification of the indication and the choice of the proper surgical technique for each patient.
Introducción
La enfermedad por reflujo gastroesofágico (ERGE) es uno de los trastornos gastrointestinales más comunes en los países occidentales. La mayoría de los pacientes presentan una sintomatología limitada que responde a cambios del estilo de vida y dieta, y a un tratamiento médico simple, por lo que no requieren una cirugía antirreflujo. De hecho, ampliar las indicaciones de la cirugía para incluir formas menores de la enfermedad sólo serviría para reducir la tasa global de éxitos. Uno de los puntos clave en el manejo de estos pacientes es la identificación de aquellos que presentan una ERGE y precisan una intervención quirúrgica y de los que presentan una ERGE progre siva.
El objetivo de la cirugía antirreflujo consiste en restablecer la competencia del cardias, mientras se preserva la capacidad de deglutir con normalidad, aliviar la distensión gaseosa y vomitar cuando es necesario. Existen actualmente pocas dudas sobre el tipo de abordaje para este tipo de intervención, tras los buenos resultados obtenidos con el abordaje laparoscópico desde que Dallemagne1 la describiera por primera vez. La controversia se mantiene en cuanto al análisis del tipo de funduplicatura más adecuada y de los detalles técnicos necesarios para obtener unos buenos resultados funcionales.
Actualmente, muchas de las respuestas a las dudas que persisten en el manejo de la ERGE pueden ser resueltas con el análisis de los resultados publicados y de nuestra serie, y así poder conocer de forma más precisa qué pacientes se beneficiarían de una cirugía antirreflujo y de la técnica más apropiada. A la vez, debe ser analizado, de una forma especial, el tratamiento quirúrgico de ciertas complicaciones de la ERGE, como el esófago de Barret o la estenosis esofágica y una entidad que, tal vez, debamos considerar aparte, como es la hernia de hiato paraesofágica.
Pacientes y método
Datos de los pacientes, indicaciones y estudios preoperatorios
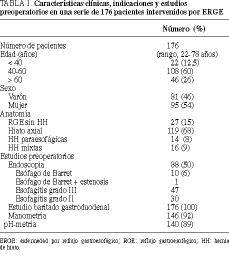
Las características clínicas y exploraciones complementarias de los pacientes se resumen en la tabla 1. Las indicaciones de cirugía fueron: intratabilidad médica, bien por rebeldía al mismo o por recidiva tras su retirada, pacientes jóvenes y enfermos con una hernia paraesofágica. La sintomatología predominante en los pacientes intervenidos fue: reflujo (93%), disfagia (38%), dolor torácico (18%) y sintomatología respiratoria (4%).
Técnica quirúrgica
El objetivo de la cirugía antirreflujo es restablecer la competencia del esfínter esofágico inferior para hacer desaparecer el reflujo, evitando una compresión excesiva que provoque disfagia o dificulte el vómito. Para llegar a obtener estos resultados es preciso seguir una serie de principios técnicos básicos.
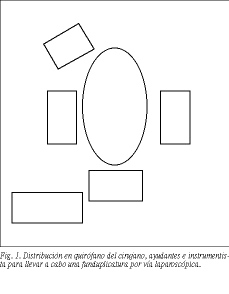
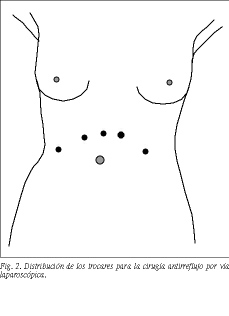
Se coloca al paciente en posición de litotomía modificada y el cirujano se sitúa entre las piernas; el ayudante que maneja la cámara y la pinza de tracción del estómago se coloca a la izquierda y en el lado derecho el asistente que sostiene el separador de hígado (fig. 1). Una vez creado el neumoperitoneo, se colocan los trocares (cuatro de 10 mm y uno de 5 mm) como se expone en la figura 2. Uno de los principios básicos del abordaje laparoscópico es la correcta exposición del hiato esofágico, que se facilita mediante la gravedad colocando al paciente en anti-Trendelenburg, y mediante la introducción del separador de hígado por el trocar situado en el flanco derecho y la tracción del estómago, que se realiza con una pinza atraumática por el trocar del flanco izquierdo. Al tensar el estómago hacia la izquierda del paciente se expone la membrana freno esofágica, observándose un triángulo, donde se inicia la disección, formado por el borde medial del hígado, el borde lateral derecho del esófago y el pilar derecho, y cuya base es la rama hepática del vago, la cual se debe respetar en todos los casos en los que sea posible.
Una vez abierta la membrana frenoesofágica, queda expuesto el pilar derecho del hiato y la cara anterolateral del esófago. Se continúa la disección del esófago hasta llegar al pilar izquierdo y se liberan las adherencias del fundus al pilar, para continuar su disección hasta la base en la zona de unión con el pilar derecho. Dicha maniobra se facilita mediante la tracción del estómago hacia la derecha del paciente.
A continuación se diseca la cara posterior del esófago, mediante disección roma, hasta visualizar el pilar izquierdo. Por la ventana que hemos creado introducimos, a través del canal de trabajo de la mano derecha del cirujano, un tractor curvo de esófago de izquierda-derecha (endoflex), el cual permite concluir la disección roma del espacio retroesofágico. Entonces se retira la pinza de tracción que maneja el ayudante, para introducir por dicho trocar el tractor curvo de esófago de derecha-izquierda, que permite elevar el esófago y exponer ambos pilares. Antes del cierre de pilares se calibra el esófago con una sonda de Fouchet. Utilizamos habitualmente el endostich para dar los puntos de sutura necesarios, que en el caso del cierre de pilares intentamos siempre que sean al menos dos. Una vez cerrados los pilares, introducimos por el canal de trabajo de la izquierda, una pinza con cabeza giratoria que pasa por detrás al esófago para coger el fundus libre y pasarlo por detrás, comprobando que no existe demasiada tensión. En los casos necesarios se procede a la sección de los vasos cortos, aunque si se ha liberado adecuadamente el pilar izquierdo del fundus no suele ser preciso. A continuación se retira la pinza retractora del esófago y, por el mismo canal de trabajo, se introduce la misma pinza con la que traccionábamos el estómago para sujetar el fundus y facilitar la realización de la funduplicatura, que se completa con tres puntos de sutura de fundus a fundus, incluyendo la cara anterior del esófago. Debemos garantizar una funduplicatura corta y que no cierre excesivamente el esófago, tutorizado por la sonda de Fouchet. Para concluir, damos un punto del fundus al pilar derecho para evitar la migración de la funduplicatura al tórax y la rotación de la misma.
En caso de efectuar una hemifunduplicatura tipo Toupet, se realizan las mismas maniobras, pero llevamos a cabo dos líneas de sutura de fundus a esófago, cada una de ella con tres puntos. La primera incluye el fundus que ha pasado por detrás del esófago a la cara anterolateral derecha del esófago, y una segunda línea de la cara anterolateral izquierda del esófago al fundus del otro lado. En la mayoría de los casos añadimos al menos dos puntos desde el fundus que ha pasado por detrás del esófago al pilar derecho diafragmático. No es necesario calibrar este tipo de funduplicatura, dado que la cara anterior del esófago queda libre.
Resultados
Las técnicas utilizadas en los 176 pacientes intervenidos fueron el Nissen-Rosetti en 114 casos (65%), Toupet en 55 casos (31%), hemifunduplicatura anterior en 6 pacientes (3,4%) y, en una paciente a la que se le efectuó una gastrorreducción con banda por obesidad mórbida, se realizó únicamente el cierre de pilares. Es de resaltar que en los últimos 76 casos la proporción de intervenciones tipo Toupet es mayor que de Nissen-Rossetti, por lo que se están progresivamente igualando los porcentajes de una técnica y otra (tabla 2). Las distintas variantes técnicas se fueron añadiendo progresivamente hasta estandarizarla del modo como se ha descrito y es como se ha efectuado en nuestros últimos 85 casos. La sección de los vasos cortos se ha realizado únicamente en 7 casos (4%). De forma simultánea se efectuaron 40 colecistectomías, 5 extirpaciones de quiste de ovario, 4 apendicectomías, 4 herniorrafias umbilicales, una vagotomía gástrica proximal, una gastrorreducción con banda y una extirpación de un divertículo de esófago distal.
Un 1,7% de los casos presentaron complicaciones intraoperatorias: una perforación gástrica y dos enfisemas subcutáneos importantes. La tasa de conversión fue del 1,7% y corresponde a los 3 casos descritos anteriormente. Fueron reoperados 2 pacientes (1,1%): un hemoperitoneo por hemorragia del lecho vesicular en un paciente al que se practicó una colecistectomía y otro, al año de la intervención, por recidiva de una hernia paraesofágica que desarrolló una incarceración gástrica. Fue reintervenido por laparoscopia, reduciéndose la hernia y cerrando los pilares con una malla de politetrafluoroetileno expandido. Un paciente desarrolló una hernia en el orificio del trocar epigástrico.
Respecto a los resultados funcionales, éstos han sido excelentes en cuanto al control de la sintomatología de reflujo, que ocurrió en el 100% de los casos. Al analizar la disfagia post operatoria distinguimos dos grupos: los primeros 18 casos, en los que no se realizaron pruebas funcionales preoperatorias ni se llevaron a cabo la mayoría de los detalles técnicos descritos previamente, en los que existió en todos los casos una disfagia leve o moderada; y los 158 casos restantes. En éstos, no presentaron disfagia 95 pacientes (60%), mientras 46 (29%) presentaron una disfagia leve (de menos de 4 semanas de duración), 16 pacientes (10%) una disfagia moderada (disfagia autolimitada de más de 4 semanas) y un paciente (0,63%) presentó una disfagia grave (que precisa dilataciones o reintervención), requiriendo una sola dilatación. Por otro lado, únicamente 6 pacientes (3,4%) presentaron un síndrome de retención gaseosa (tabla 3). Respecto a los pacientes intervenidos por esófago de Barret, el índice de remisión observado en las endoscopias de control fue del 90%.
Discusión
Como comenta Hunter2, ex presidente de la SAGES, los principios básicos de la cirugía antirreflujo por vía laparoscópica se resumen en una frase: "los buenos resultados de la cirugía antirreflujo se obtienen cuando la selección de los pacientes es adecuada, es realizada por cirujanos con una preparación adecuada y se lleva a cabo la técnica adecuada". Lógicamente, parece que sean los principios básicos para llevar a cabo cualquier intervención quirúrgica, sea por el abordaje que sea, pero es necesario resaltar estos pilares básicos de la cirugía en este tipo de intervenciones, ya que estamos realizando una cirugía funcional que precisa una indicación y una técnica depurada realizada por cirujanos bien preparados para obtener unos buenos resultados.
Selección de pacientes
Ha quedado demostrado en diversos estudios que la cirugía laparoscópica antirreflujo es un tratamiento efectivo para pacientes con ERGE ya que mejora su calidad de vida, tanto en los que no responden al tratamiento médico como en aquellos que lo hacen de manera adecuada a la medicación pero prefieren no estar sometidos a tratamiento médico de por vida2. Diversos estudios aleatorizados demuestran una mayor efectividad del tratamiento quirúrgico sobre el tratamiento médico en el control de la sintomatología y en la curación de la esofagitis en pacientes con reflujo severo3,4. Por todo ello, parece que no existen dudas sobre el valor de la cirugía en el tratamiento de la ERGE en pacientes con reflujo severo, al igual que van desapareciendo las dudas acerca del beneficio que supone la cirugía en aquellos pacientes en los que aparecen complicaciones derivadas de la existencia de reflujo5, como alteraciones de la motilidad esofágica o esofagitis grave, llegando hasta el esófago de Barret, donde se ha observado incluso su desaparición. Además, desde el punto de vista de coste-efectividad, cualquier paciente varón menor de 48 años o mujer menor de 55 que precise medicación de por vida es un candidato potencial a una cirugía antirreflujo4,6.
Pero al tratarse de una cirugía funcional, y dejando a un lado la indicación de cirugía por las complicaciones, lo ideal es identificar a aquellos pacientes que se beneficiarían de una cirugía antirreflujo por presentar un "reflujo progresivo", para lo cual es necesaria la realización de estudios funcionales precisos, que además de ayudarnos a la identificación de este grupo nos orientarán, como veremos más adelante, sobre el tipo de cirugía más apropiada para cada paciente.
Múltiples estudios han demostrado que la disminución de la resistencia del esfínter esofágico inferior es el factor predisponente más importante para la aparición de reflujo y de rebeldía al tratamiento médico7. La manometría es la exploración más importante para identificar a aquellos pacientes con "reflujo progresivo", debiendo lógicamente completar el estudio con una pH-metría de 24 h, ya que la simple existencia de síntomas no es un dato fiable de la presencia de la enfermedad8.
La indicación quirúrgica debe basarse en una serie de pruebas diagnósticas, que incluyen la endoscopia para evaluar las lesiones esofágicas, un estudio radiológico esofagogastroduodenal, para obtener una idea de la anatomía de la región y la manometría y la pH-metría comentada. Actualmente se considera que el estudio de vaciamiento gástrico es otro punto básico en el conjunto de pruebas diagnósticas, ya que nos ofrece una visión de las posibles alteraciones motoras de la zona9.
Análisis de la técnica quirúrgica
La técnica antirreflujo ideal es la que hace desaparecer la sintomatología de reflujo, permite deglutir sin dificultad y mantiene la capacidad de liberar la distensión gaseosa y vomitar. Para ello no existe una técnica quirúrgica ideal, sino diferentes tipos de técnicas antirreflujo que se pueden realizar de diversas formas y que deben individualizarse para cada paciente en virtud de las características de los mismos, según las pruebas funcionales preoperatorias y las variaciones anatómicas. Está bien establecida la superioridad de la funduplicatura sobre las demás técnicas antirreflujo tipo Belsey, Hill, cardiopexia o la prótesis de Angelchik10.
La funduplicatura de Nissen original se asociaba a una alta tasa de síntomas obstructivos por la funduplicatura de 360°11. El mejor conocimiento del funcionamiento de la funduplicatura ha obligado a modificar la técnica original para minimizar sus efectos indeseables. DeMeester y otros grupos han demostrado mejores resultados con una funduplicatura corta, de 2 cm o menos y sin tensión, utilizando la cara anterior del estómago y sobre un esófago tutorizado con una bujía de dilatación12. A estas variaciones técnicas se añaden otros gestos quirúrgicos más discutidos, como el cierre sistemático de pilares, la fijación de la funduplicatura a los pilares y la división rutinaria de los vasos cortos.
Los estudios de Allison, ya en 1951, demostraban la importancia de situar el esfínter esofágico inferior en el ambiente de la presión positiva de la cavidad abdominal13. Nosotros realizamos sistemáticamente el cierre posterior de los pilares y la fijación de la funduplicatura al pilar derecho, maniobras que no incrementan la morbilidad y que creemos necesarias para mantener la funduplicatura en la cavidad abdominal. En nuestra experiencia, cuando no realizábamos el cierre de pilares existía una emigración de la funduplicatura a la cavidad torácica en el 40% de los casos en el postoperatorio inmediato14 y que, según Soper et al, podría ser causante de ciertos síntomas postoperatorios (dolor epigástrico o torácico, recidiva de la sintomatología de reflujo o retención gaseosa)15. Por otro lado, la fijación de la funduplicatura al pilar derecho, además de evitar el desplazamiento a la cavidad torácica, evita la rotación del esófago distal como consecuencia de la tendencia natural del fundus a volver a su posición habitual, lo que podría ser la causa de la aparición de disfagia o retención gaseosa en el postoperatorio, aunque no existen estudios definitivos que justifiquen dicho gesto.
La sección de los vasos cortos es un punto mucho más controvertido que los anteriores dado que dicho gesto podría estar relacionado con la tensión en la funduplicatura, la aparición de disfagia en el postoperatorio y el aumento de complicaciones peroperatorias. La sección de los vasos cortos incrementa la morbilidad intraoperatoria (hemorragia), las tasas de conversión y el tiempo operatorio16. Sin embargo, no existen estudios fidedignos que demuestren que su sección se acompañe de menos disfagia17. Únicamente existe un estudio prospectivo aleatorizado en el que no se demuestra una menor incidencia de disfagia cuando se seccionan de manera sistemática18. En nuestra serie no realizamos la sección sistemática de los vasos cortos, llevándola a cabo únicamente cuando existe una excesiva tensión al paso del fundus por detrás del esófago (el 4% de nuestros pacientes). Por otro lado, creemos que es importante llevar a cabo una correcta disección del pilar izquierdo, seccionando las adherencias del mismo al fundus, lo cual reduce la tensión en la funduplicatura. Con estas maniobras, la incidencia de disfagia en nuestra serie es similar a la hallada en la bibliografía, con lo cual no consideramos necesaria la sección de los vasos cortos de forma rutinaria.
Existen otra serie de gestos quirúrgicos cuya influencia en los resultados funcionales de la funduplicatura es mucho más difícil de valorar, como el tamaño de la ventana posterior o la sección de la membrana frenoesofágica y que, hoy por hoy, se derivan de sensaciones del cirujano; y como algunos de los gestos descritos anteriormente serían precisos estudios prospectivos para validarlos con certeza.
Elección del tipo de funduplicatura
La idea más generalizada es que la disfagia aparece con mayor frecuencia tras una funduplicatura de 360°, mientras que los resultados a largo plazo demuestran que la recidiva del reflujo es más frecuente tras una funduplicatura de Toupet19, a pesar de que existen estudios que no demuestran este hecho tras 5 años de seguimiento20, y mucho mayor aún tras la realización de una hemifunduplicatura anterior tipo Dor21.
A pesar de que muchos estudios comparativos demuestran menos disfagia tras la la hemifunduplicatura posterior22, únicamente deberían tenerse en cuenta estudios prospectivos aleatorizados a la hora de determinar las ventajas de una u otra técnica. Los únicos estudios de este tipo existentes en la actualidad, tres tras cirugía abierta23-25 y uno tras cirugía laparoscópica26, han demostrado igual control de la sintomatología tras una técnica u otra, pero no han puesto de manifiesto una reducción significativa de la presencia de disfagia tras una funduplicatura parcial posterior, excepto el estudio de Lundell et al, en el que observaron una menor incidencia de disfagia tras el Toupet a los 3 meses de la intervención, siendo igual en el postoperatorio inmediato, a los 6 meses y a los 5 años del estudio23. Por todo ello no podemos asegurar que la hemifunduplicatura posterior ofrezca mejores resultados que la funduplicatura de 360°, a pesar de que series no aleatorizadas han demostrado las ventajas de la hemifunduplicatura posterior27. Por su parte, el único estudio prospectivo aleatorizado en el que se compara la técnica de Nissen con la hemifunduplicatura anterior por vía laparoscópica demuestra menos disfagia postoperatoria pero, a la vez, pone de manifiesto que es un procedimiento menos efectivo que la técnica de Nissen en el control del reflujo28, como ya ha quedado reflejado en otros estudios no aleatorizados21.
De esta forma, la técnica de elección en el ERGE es la funduplicatura de 360°, reservando la hemifunduplicatura posterior cuando existe una alteración de la motilidad del esófago, ya que crea una valva de menor presión que la funduplicatura completa, con lo que se facilita el vaciamiento esofágico y se evita la disfagia. A la vez, está demostrado que esta técnica mejora la motilidad del esófago distal29, ante la presencia de un esfínter esofágico inferior (EEI) normo o hipertónico, ya que la hipotonía del EEI ocurre en aproximadamente el 80% de los pacientes con síntomas de reflujo rebeldes o refractarios al tratamiento médico. En los pacientes con normo o hipertonía del esfínter podrían estar implicadas relajaciones transitorias del EEI no detectadas en la manometría u otros factores etiopatogénicos, por lo que no es conveniente aumentar la presión del EEI. También es recomendable la técnica de Toupet cuando no es posible la realización de la manometría, dado que no conocemos el tono del EEI ni las características de la motilidad esofágica. Por otra parte, hemos realizado una hemifunduplicatura anterior sólo en casos en los que no es posible la disección de la ventana posterior del esófago, habitualmente en grandes hernias de hiato paraesofágicas o en pacientes de edad avanzada con una hernia grande y sin sintomatología de reflujo o controlada médicamente en los que la indicación de la cirugía es otra diferente a la presencia de ERGE.
Existen otros aspectos controvertidos derivados de la patogenia multicausal de la ERGE que pueden requerir otros gestos quirúrgicos, pero cuando se detecta un retraso en el vaciamiento gástrico que pudiera tener relación con el reflujo no es necesario añadir ningún gesto quirúrgico, ya que dicho retraso se corrige tras la realización de una funduplicatura, que favorece el vaciamiento gástrico30.
Hernias paraesofágicas, ¿debemos considerarlas como una entidad independiente?
Las hernias paraesofágicas predisponen a la aparición de una ERGE y la resolución quirúrgica de las mismas es similar, pero existen una serie de peculiaridades que nos hacen considerarlas de forma independiente. El abordaje laparoscópico de la hernia de hiato paraesofágica incluye una serie de controversias independientes del tratamiento de la ERGE. La indicación quirúrgica es clara en todos los pacientes en los que se detecta una gran hernia paraesofágica debido al peligro de complicaciones. Por otro lado, existe controversia acerca de la necesidad de extirpación del saco herniario31,32, la sistematización del uso de una malla para el cierre de pilares diafragmáticos, la necesidad de una funduplicatura en los casos en los que la indicación no haya sido la existencia de reflujo, o la utilidad de fijar la pared anterior del estómago a la pared abdominal para evitar la volvulación del mismo33. La cirugía de la hernia paraesofágica se asocia a un mayor número de complicaciones peroperatorias y una elevación de la tasa de conversión, como se observa en nuestra serie.
Como conclusión, la cirugía antirreflujo por vía laparoscópica es una técnica que ofrece resultados similares a los de la cirugía abierta, con las ventajas añadidas de este tipo de abordaje. Los buenos resultados de la misma dependen de una correcta indicación y de la elección de una técnica quirúrgica adecuada e individualizada para cada paciente, llevándola a cabo de una forma depurada. Su instauración progresiva en los diferentes centros depende únicamente del entrenamiento adecuado para poder realizar este procedimiento.