El tratamiento de la enfermedad diseminada abdominal continúa siendo una de las fronteras en oncología1. Esta afectación regional de las enfermedades cancerosas ha sido tradicionalmente asociada con un mal pronóstico y casi uniformemente considerada como estadio terminal e incurable. El tratamiento de este tipo de pacientes ha variado desde laparotomías para la toma de biopsias hasta extensas resecciones de tumor, y luego los pacientes son remitidos a sus oncólogos para tratamiento con quimioterapia sistémica. La mayoría de estos pacientes sufren intensamente y en 9 meses de media mueren por obstrucción intestinal o caquexia terminal por inanición2,3. Debido a los pobres índices de supervivencia de estos pacientes, algunos cirujanos están a favor incluso de actitudes abstencionistas en casos seleccionados4. La carcinomatosis peritoneal es la causa más frecuente de muerte en pacientes con resecciones por cánceres intra-abdominales5,6. Según Sugarbaker7, la persistencia de células tumorales en la pelvis y en la cavidad abdominal es la causa de la muerte del 30 al 50% de los pacientes con estas enfermedades.
Desde 1982, Sugarbaker8 ha considerado la diseminación abdominal como un estadio locorregional de la enfermedad y ha desarrollado una nueva alternativa terapéutica basada en el tratamiento de la enfermedad macroscópica mediante cirugía citorreductora radical oncológica con técnicas de peritonectomías por él diseñadas9, seguido del tratamiento de la enfermedad microscópica residual con la aplicación directa de quimioterapia intraperitoneal de intensificación mediante quimioterapia intraperitoneal intraoperatoria hipertérmica (QIIH), y la posterior aplicación de quimioterapia intraperitoneal postoperatoria precoz.
La morbimortalidad asociada con este tratamiento combinado de cirugía citorreductora radical y quimioterapia de intensificación locorregional es alta. Si bien hay una gran variabilidad en la morbilidad y la mortalidad publicadas, con índices del 0-43% y el 0-20%, respectiva-mente10-15, los mejores resultados siguen siendo los del grupo de Sugarbaker con una morbilidad del 25% y una mortalidad del 1,5%16 en carcinomatosis de origen colorrectal, y más recientemente, otros grupos han mejorado sus resultados en carcinomatosis de otros orígenes17.
Las complicaciones pueden derivar directamente de la cirugía, la quimioterapia o la hipertermia o la suma de los tres factores. Es difícil separar las complicaciones secundarias a la cirugía de las relacionadas con la QIIH, tanto las relacionadas con la hipertermia como las relacionadas directamente con los citostáticos, pero la mayoría de las complicaciones descritas parecen relacionadas principalmente con la agresión quirúrgica.
El uso de esta nueva alternativa terapéutica, con cirugía citorreductora radical, en el tratamiento de los pacientes afectos de carcinomatosis peritoneal produce el peor de los escenarios posibles y representa un nuevo reto para los equipos multidisciplinarios encargados del seguimiento de estos pacientes, tanto en su evolución postoperatoria como en los cuidados requeridos, dado que además de ser diferente del de los pacientes convencionales, no ha sido completamente definido ni protocolizado.
La catastrófica situación abdominal encontrada durante las reintervenciones por complicaciones en el período postoperatorio en muchas ocasiones hace desaconsejable un cierre abdominal primario. La principal dificultad en el tratamiento de estos pacientes radica en conseguir la total eliminación del foco causante de la complicación, que obliga a un cierre abdominal temporal diferido.
Las características ideales que debiera cumplir un cierre abdominal diferido son: contención y protección de las vísceras; prevención de la contaminación de la cavidad abdominal; evacuación de los fluidos y contenidos tóxicos intraabdominales; prevención del síndrome compartimental abdominal; ser una técnica fácil y de rápida aplicación; permitir fáciles manejo y cuidado de enfermería; bajo coste y asegurar la preservación de la pared abdominal y, especialmente, evitar la retracción de los bordes faciales. Hemos elegido la técnica de abdomen abierto en vacío (AAV), descrita por Brock et al17 hace más de 10 años para el control temporal de estas difíciles situaciones, por cuanto cumple con todos los requisitos de la técnica ideal del cierre abdominal diferido.
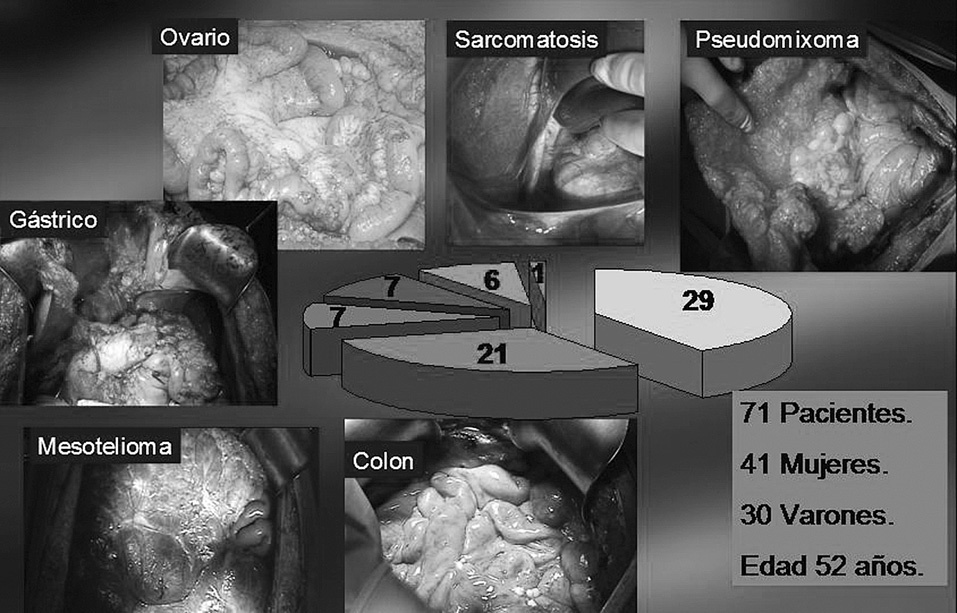
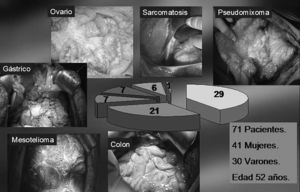
Material y métodoNos hemos basado en nuestra experiencia personal18 en el tratamiento de 110 citorreducciones realizadas entre febrero de 1997 y febrero de 2007 en 71 pacientes; 41 varones y 30 mujeres, afectos de carcinomatosis peritoneal difusa de diferente origen (fig. 1); 50 (70%) de los 71 pacientes sufrieron algún tipo de complicación durante su evolución postoperatoria, en 28 ocasiones precisaron alguna reintervención por complicaciones de grado III-IV19. La situación abdominal encontrada durante la reintervención hizo aconsejable un cierre abdominal diferido en 17 casos; se ha utilizado siempre la técnica del AAV para el cierre abdominal diferido.
Fig.1.Tipo de carcinomatosis según el tumor original.
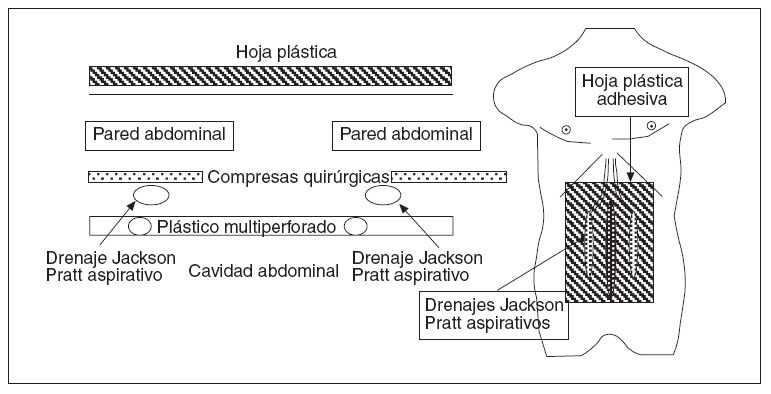
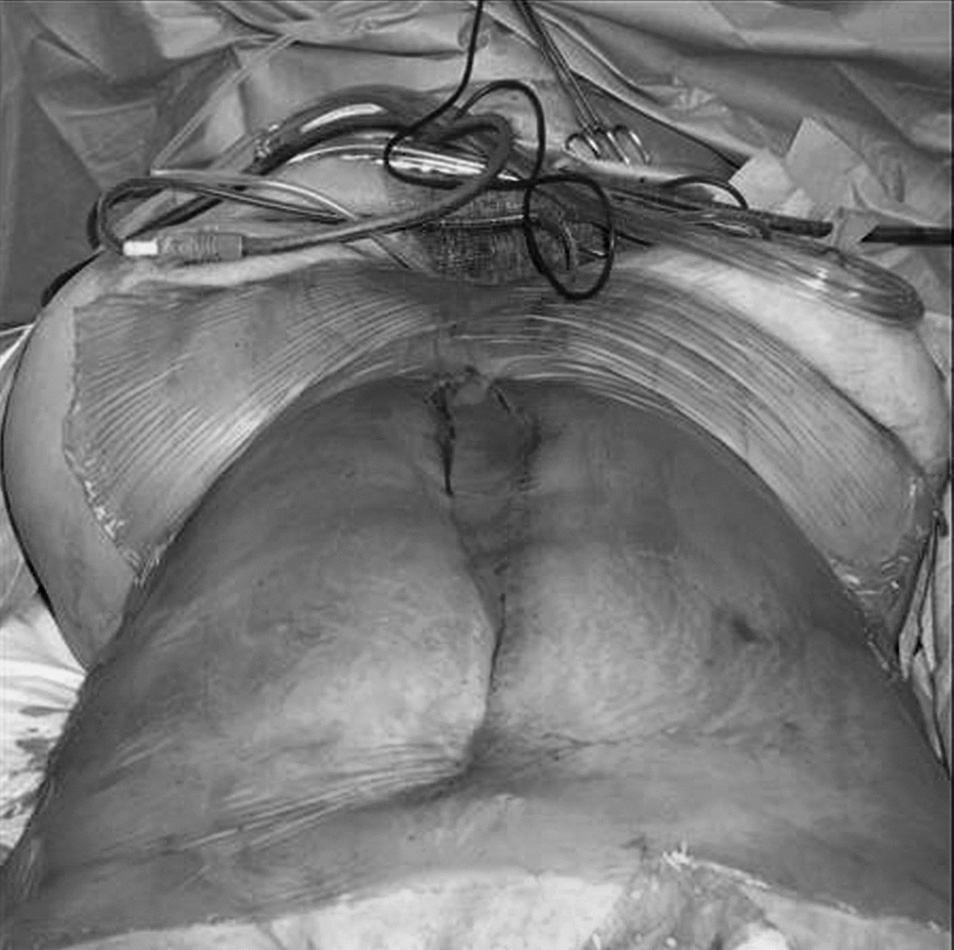
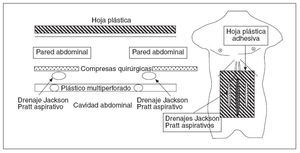
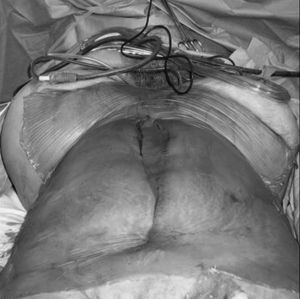
La técnica del AAV consiste en una cura oclusiva sin suturas de 3 capas estabilizada por la aplicación continua del vacío, como muestran los esquemas de las figuras 2 y 3. La capa más interna está constituida por una hoja fenestrada de polietileno colocada entre las vísceras y la pared abdominal. Dos drenajes aspirativos tipo Jackson Pratt, junto con 2 compresas estériles quirúrgicas, constituyen la capa intermedia que actúa de filtro del material exudado. La capa más externa está formada por una hoja adhesiva que cubre totalmente la pared abdominal (Ioban®, 3M). La aplicación continua de aspiración a los drenajes crea una compresión rígida producida por la presión negativa, similar a los paquetes de café al vacío, que facilita el drenaje de la cavidad abdominal. La cura oclusiva aplicada es firme, seca y estanca, y supone una barrera segura que permite movilizar a los pacientes en la cama e incluso llegar a levantarlos al sillón sin riesgo de evisceración. La aplicación de la técnica del AAV es relativamente simple y su ejecución lleva unos pocos minutos. Todas las revisiones de los AAV se llevan a cabo en el quirófano, con revisión completa de toda la cavidad abdominal, y así se puede proceder al cierre de la cavidad o a la práctica de un nuevo AAV, con una duración de 60 min de media en su ejecución, según nuestra experiencia.
Fig. 2. Esquema del abdomen abierto con la triple capa sin sutura, aspiración continua en vacío.
Fig.3. La cura oclusiva producida por el vacío, similar a los paquetes de café al vacío, es firme, seca y estanca, facilita el drenaje de la cavidad abdominal aplicada y supone una barrera segura. Ha permitido el cierre abdominal primario en el 66% de las ocasiones.
Se estudia esta serie de pacientes, en cuanto al tipo de tumor original, grado de enfermedad en el momento de la citorreducción, peritonectomías y resecciones viscerales necesarias realizadas, tipo de complicación postoperatoria y circunstancias que obligaron a un cierre abdominal diferido, y finalmente, se comunican los resultados con la aplicación y la evolución del AAV.
ResultadosGrado de enfermedad y citorreducción practicadaTodos nuestros pacientes, salvo 5 (7%), tenían una media de 1,6 (intervalo, 1-4) intervenciones previas por paciente, y en el 60% de las ocasiones habían recibido tratamiento citostático sistémico con una o más líneas de tratamiento (intervalo, 1-6).
El volumen y la extensión de la carcinomatosis se determinaron siempre con el índice de carcinomatosis peritoneal (ICP)20,21. El ICP medio de nuestros pacientes fue 20,5, lo que justifica que nuestro tiempo operatorio medio fuera de 9,5 h.
La citorreducción se obtuvo mediante la técnica de peritonectomías descrita por Sugarbaker22; se realizaron cuantas peritonectomías y resecciones viscerales fueran necesarias, siempre limitadas exclusivamente a zonas afectas por tumor evidente. El grado de citorreducción alcanzado al final de la cirugía también quedó registrado prospectivamente acorde al índice de citorreducción conseguida (ICC)23. A pesar de lo avanzado de la enfermedad, fuimos capaces de conseguir una citorreducción completa CC0-CC1 en el 83% de las ocasiones, si bien se precisaron 264 peritonectomías parietales (media, 3,6 peritonectomías parietales por paciente), junto con 350 resecciones viscerales (media, 3,4 órganos por paciente) y la práctica de 90 anastomosis digestivas (media, 1,3 por paciente), sin contar las rafias y/o los refuerzos parietales parciales que son necesarios en muchas ocasiones. Fue necesario realizar pelviperitonectomía en el 83% de los pacientes y peritonectomía diafragmática completa, izquierda o derecha, o ambas a la vez, al menos, en el 57% de las ocasiones. La enfermedad obligó a practicar omentectomía mayor en los pacientes que todavía tenían epiplón mayor (84%), con lo que se los priva de uno de los principales mecanismos de defensa intraabdominales.
Las resecciones viscerales pueden afectar a cualquiera de las vísceras macizas o huecas abdominales, digestivas y genitourinarias. Cada una de las resecciones viscerales por sí misma constituye una intervención quirúrgica en un paciente oncológico convencional; sin embargo, en estos pacientes sometidos a citorreducciones oncológicas radicales, se pueden precisar varias de estas resecciones viscerales simultáneamente.
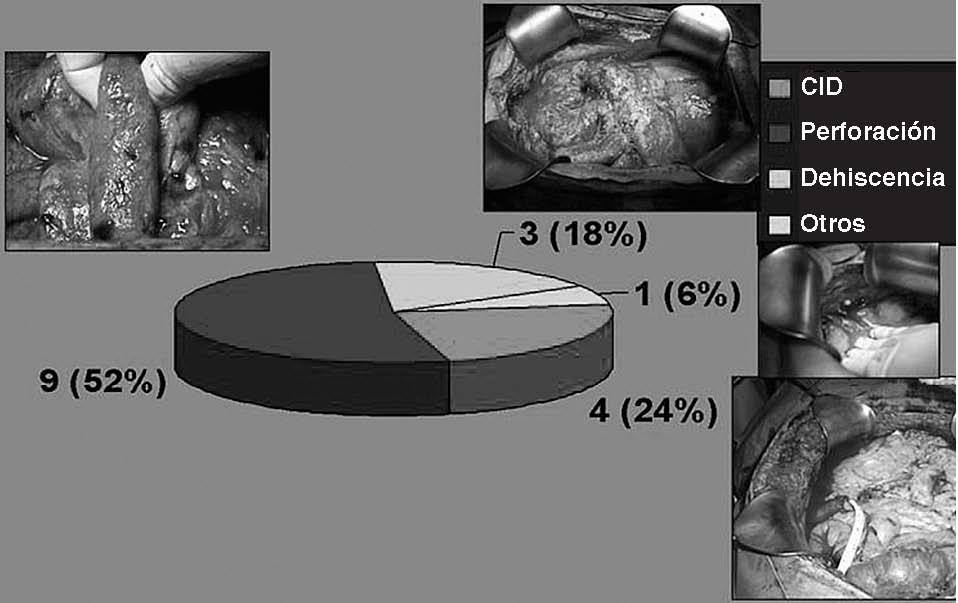
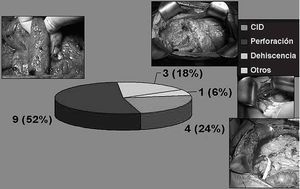
Tipo de complicación postoperatoria que obligó a un cierre abdominal diferidoDe los 71 pacientes, 50 (70%) sufrieron algún tipo de complicación durante su evolución postoperatoria, 28 de estos pacientes precisaron alguna reintervención por complicaciones de grado III-IV19. La catastrófica situación abdominal encontrada durante la reintervención hizo aconsejable el cierre abdominal diferido en 17 pacientes: 9 por peritonitis difusa secundaria a perforación intestinal por las electroevaporizaciones practicadas para el tratamiento de la enfermedad en el peritoneo visceral; 3 por peritonitis difusa secundaria a dehiscencia de anastomosis (2, colorrectal y 1, ileocólica); en 4 ocasiones fue por coagulopatía de consumo, y 1 paciente con un urinoma secundario a la perforación de la vejiga por la sonda vesical el día 18 del postoperatorio (fig. 4).
Fig.4.Tipo de complicación postoperatoria que obligó a un cierre abdominal diferido.CID:coagulación intravascular diseminada.
Tratamiento aplicado y evoluciónEn estos 17 pacientes fue necesario practicar la técnica del AAV en un total de 52 ocasiones (mediana, 2,8 por paciente; intervalo, 1-10), antes de que la complicación abdominal estuviera completamente bajo control.
Las coagulopatías aparecieron en los primeros 3 días postoperatorios, en todos los casos causadas por peritonectomía pelviana y/o peritonectomía diafragmática. Estos casos sólo precisaron un AAV para el control de la hemorragia, siempre se pudo cerrar la cavidad en la revisión practicada 24-48 h después, tras una cuidadosa y completa revisión de la situación hemostática de toda la cavidad abdominal.
En tres ocasiones sufrimos una peritonitis secundaria a una dehiscencia de anastomosis. También en estos pacientes la sepsis intraabdominal se pudo controlar tras la práctica de una o dos aplicaciones del AAV, dado que practicamos una ostomía derivativa a estos pacientes. Siempre pudimos cerrar la cavidad abdominal no más tarde de 48-96 h después de la reintervención.
La situación fue muy distinta en los casos de peritonitis secundaria a perforaciones diatérmicas intestinales por electroevaporización de implantes tumorales. La causa de esta complicación fue un adelgazamiento de la pared con escara diatérmica profunda inadvertido en la mayoría de los casos. Los problemas sépticos abdominales aparecieron más tarde, durante la segunda semana, días 8 a 14 postoperatorios. La sepsis abdominal normalmente se diagnosticó porque el contenido intestinal salía por los drenajes abdominales o por la propia herida quirúrgica. En estos pacientes, aunque suturamos las enterotomías primariamente, el edema, el íleo postoperatorio y los fenómenos de hiperpresión intraluminales hicieron que con frecuencia no se controlase el problema de entrada; uno de nuestros pacientes precisó la aplicación de la técnica del AAV hasta en 10 ocasiones antes de que pudiéramos cerrar la cavidad. Conseguimos un cierre primario del plano musculoaponeurótico completo en dos tercios de los casos (el 66,6% de los pacientes). Hemos observado solamente 2 fístulas intestinales relacionadas directamente con esta técnica, y todos los pacientes, salvo uno, abandonaron el hospital con buen estado general.
DiscusiónEste tipo de tratamiento con cirugía citorreductora oncológica produce el peor de los escenarios posibles, con alteración locorregional de la respuesta y desaparición de los signos y síntomas habituales de la peritonitis química y/o bacteriana; de tal forma que puede acontecer una dehiscencia de sutura o un vertido por perforación intestinal, sin las manifestaciones clásicas de peritonismo ni vientre en tabla; el paciente tiene un aceptable estado general y la única manifestación es la salida del contenido intestinal por los drenajes ambientales del circuito de quimioterapia postoperatoria, cuando todavía los tiene, o a través de la herida quirúrgica, o el progresivo establecimiento de un cuadro de sepsis.
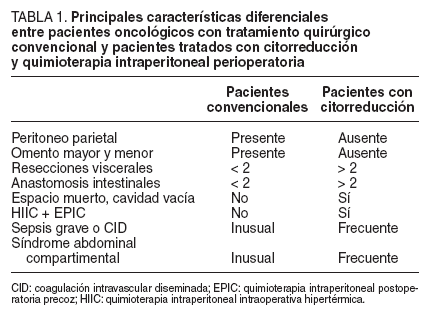
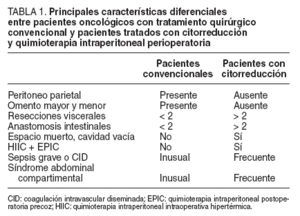
En estos pacientes, se produce una suma de factores de riesgo por la agresión quirúrgica y quimioterápica y los producidos por la hipertermia, junto con un déficit de mecanismos de defensa ante el estrés por la enfermedad y el tratamiento recibido. Las características diferenciales de estos pacientes respecto a los pacientes quirúgicos convencionales, incluso los oncológicos, quedan reflejadas en la tabla 1. Es de destacar que a nuestros pacientes se les ha privado de uno de los principales mecanismos de defensa intraabdominales, al no poder cubrir y proteger áreas adelgazadas o anastomosis endebles, por la omentectomía mayor realizada. Este desequilibrio defensivo frente a la agresión recibida justifica la aparición de un mayor índice de morbimortalidad que en los pacientes convencionales, e imposibilita la solución de la complicación abdominal en un tiempo, en muchas ocasiones; en nuestra experiencia, en 17 (60%) de los 28 pacientes reintervenidos por complicaciones postoperatorias tras este tratamiento.
TABLA 1. Principales características diferenciales entre pacientes oncológicos con tratamiento quirúrgico convencional y pacientes tratados con citorreducción y quimioterapia intraperitoneal perioperatoria
La complicación postoperatoria abdominal más frecuente sigue siendo la perforación intestinal causada por el traumatismo quirúrgico sobre la superficie intestinal durante la resección de los implantes viscerales, mediante la técnica de las eletroevaporizaciones, posiblemente agravado por la acción del calor y los fármacos citostáticos24. Sin embargo, Shido et al25 han demostrado que la hipertermia por sí sola no causa el daño visceral cuando se usa en procedimientos con QIIH.
La principal dificultad en el tratamiento de estos pacientes radica en que conseguir la total eliminación del foco causante de la complicación, tanto en el caso de hemorragia por coagulopatía como de infección abdominal por peritonitis, es un requisito indispensable antes del cierre de la cavidad abdominal, y que a menudo esta situación no se consigue con una sola reintervención. La técnica empleada de cierre abdominal diferido provisional temporal es un factor determinante en la supervivencia26.
Tal y como expresaban Castellanos et al27 en su revisión, las principales complicaciones de los cierres abdominales provisionales diferidos son las fístulas enterocutáneas y las eventraciones, estas últimas por falta de cuidado de la integridad de la pared abdominal.
La técnica del AAV elegida por nuestro grupo28 cumple con todos los requisitos exigibles al cierre temporal diferido de la cavidad abdominal ideal: garantiza la contención del contenido abdominal, protege el paquete visceral, asegura la evacuación de los fluidos, evita la contaminación, es fácil y rápida en su ejecución, previene del síndrome compartimental abdominal, preserva y mantiene la integridad completa de la pared abdominal, ya que limita la retracción de la fascia musculoaponeurótica, y es sumamente económica.
La práctica de la técnica del AAV nos ha permitido el control de estas difíciles complicaciones, asegurando el correcto control hemostático en los casos de coagulación intravascular diseminada (CID) por coagulopatia de consumo en 48 h, además del tratamiento de las peritonitis resultantes de las dehiscencias de sutura en 96 horas, o de perforaciones intestinales por diatermia de estos pacientes singulares, si bien en mayor plazo; en el 66% de las ocasiones se logró el cierre completo de la totalidad de la pared abdominal.
ConclusionesComo consecuencia de esta experiencia, en nuestra opinión, el AAV es la técnica de elección para cualquier cierre temporal de la cavidad abdominal, independientemente de la razón por la que se precise, incluso en el peor de los escenarios posibles, tal como hemos demostrado en el tratamiento de las complicaciones quirúrgicas tras citorreducciones y quimiohipertermia intraperitoneal.
Correspondencia: Dr. A. Gómez Portilla. Programa de Carcinomatosis Peritoneal. Hospital San José. Beato Tomás de Zumárraga, 10. 01008 Vitoria-Gasteiz. Álava. España. Correo electrónico: agomezpor@teleline.es
Manuscrito recibido el 25-2-2008 y aceptado el 20-5-2008.