Introducción
La investigación y el desarrollo de los biomateriales constituye un área en creciente expansión. La generalización de su uso en algunas aplicaciones, como en la reparación de los defectos herniarios1, ha ido condicionando modificaciones de éstos, con el fin de conseguir una prótesis de comportamiento óptimo en todas las interfaces. Esta prótesis por el momento no existe.
Por otro lado, el futuro desarrollo de biomateriales de segunda y tercera generación2, que cuentan con el propio receptor y su biología para mejorar su integración y sirven de soportes o scaffolds, hacen de este campo una indudable y atractiva área de investigación.
Desde un punto de vista clínico y para el cirujano, es necesario familiarizarnos con los diferentes tipos existentes de materiales protésicos, y saber con qué fin y para qué se han diseñado, así como conocer cuál es su mejor ubicación tisular.
La clasificación propuesta por Amid3 en 1997, aunque básicamente marcó las directrices de aplicación de los diferentes materiales protésicos, ha quedado actualmente relegada, debido a la aparición de las prótesis de última generación. Éstas persiguen alcanzar la mejor integración posible en los tejidos, mejorar su comportamiento en todas las intefaces y evitar la aparición de complicaciones.
Cambios y modificaciones de los biomateriales clásicos
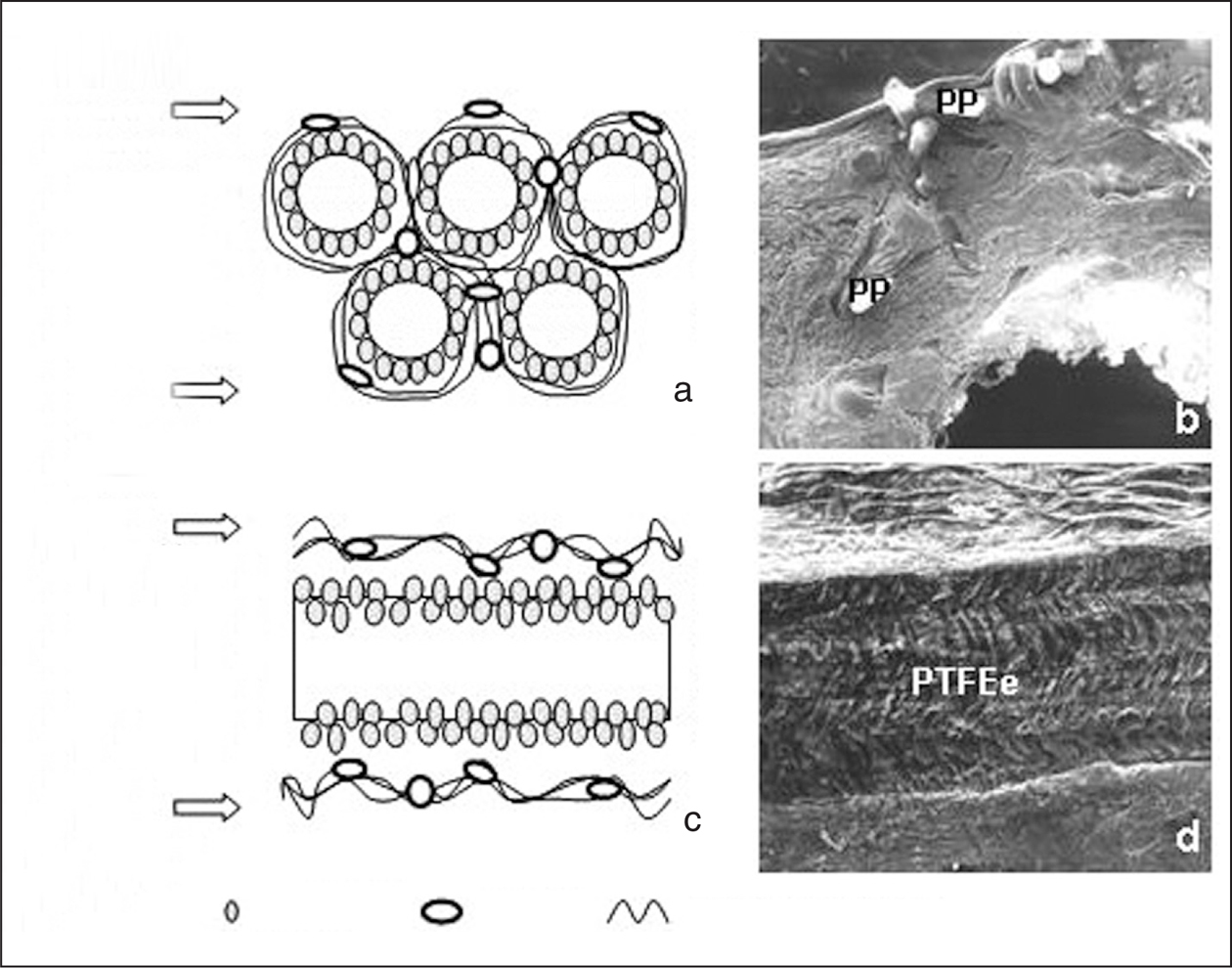
A partir de los biomateriales clásicos: polipropileno (PP), poliéster (PL) y politetrafluoroetileno expandido (PTFEe), en los últimos años se han llevado a cabo modificaciones. Muchas de estas modificaciones no han aportado nada, especialmente aquellas que han afectado al PP (fig. 1a y b).
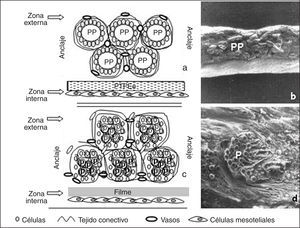
Fig. 1. a) Representación esquemática del proceso de integración de las prótesis reticulares; b) imagen a microscopia electrónica de barrido del implante de una prótesis reticular de polipropileno (x 50); c) proceso de integración en las prótesis de tipo laminar; d) aspecto del politetrafluoroetileno expandido (PTFEe) una vez implantado (MEB x 200). PP: polipropileno.
Sin embargo, muy recientemente las prótesis reticulares se han visto modificadas en el sentido de crear prótesis con menor cantidad de biomaterial, a base de crear poros más amplios y una menor reordenación espacial de los filamentos. En la terminología empleada por el grupo de Schumpelick4, serían prótesis de polipropileno de poro amplio y baja densidad, también denominadas lightweight. Estas prótesis tienen un comportamiento similar en cuanto a integración tisular que las clásicas prótesis de polipropileno tipo Marlex®. Nuestro grupo, antes de la aparición de estas prótesis demostró que la resistencia biomecánica no cambiaba5, ni estaba en relación con el tamaño de poro empleado, siempre y cuando el mismo no pasara de 3 mm. Estas prótesis lightweight, que se integran lo mismo que las prótesis convencionales de PP, provocan menor reacción de cuerpo extraño, pues llevan menos cantidad de biomaterial y además después del implante mantienen la elasticidad del tejido receptor. Esta última propiedad ha sido ampliamente discutida. En algunos pacientes se ha observado una cierta "contractura" o "incomodidad" en la pared abdominal después de implantes de polipropileno con poro de 1 mm. Probablemente, y de acuerdo con algunos autores6, todo ello depende de una reacción individualizada de respuesta biológica a la cicatrización para cada implante.
Las prótesis lightweight podrían ir formadas no solamente por material no absorbible (PP en este caso) sino también por material absorbible. De esta forma se generan prótesis híbridas.
¿Qué objetivos tratan de conseguir estas prótesis?
Fundamentalmente dos: en primer lugar, reducir la cantidad de material extraño que queda ubicado en el huésped y, en segundo lugar, dejar una menor fibrosis en el tejido receptor.
Aunque inicialmente la reacción a cuerpo extraño es mayor que en las prótesis totalmente no absorbibles, no cabe duda de que la ventaja de reducir la cantidad final de material extraño en el organismo receptor debería ser ventajosa, de una forma especial en los implantes efectuados en pacientes muy jóvenes. Obviamente, en estos pacientes el biomaterial ha de permanecer a veces largo tiempo incluido en los tejidos, y todavía no se sabe la reacción o los cambios últimos que éstos pueden generar después de muchos años de haber efectuado el implante.
Estudios preliminares de nuestro grupo (resultados pendientes de publicación) demuestran que la integración y la resistencia biomecánica de estas prótesis híbridas es similar a la de las prótesis reticulares convencionales formadas sólo por PP. Además, algunas de ellas incorporan polímeros biodegradables a tiempos largos (poliglecaprona 25), hecho que desde el punto de vista cicatrizal aporta grandes ventajas al proceso general reparativo.
Estas prótesis híbridas finalmente generan una menor reacción fibrosa que, igual que comentábamos con las prótesis de PP de amplio poro, evitan la aparición de "rigideces" en los implantes que pueden aparecer a medio/largo plazo en algunos pacientes.
Dentro de las prótesis laminares, el PTFEe también se ha visto sometido a cambios en su estructura (fig. 1c y d). Si inicialmente era un parche (Soft Tissue Match®), después evolucionó hacia un parche multiperforado (MicroMesh®), con la finalidad de obtener una mejor resistencia biomecánica, sin conseguirlo7. Finalmente, en la última generación de PTFEe surgió una prótesis laminar (DualMesh®), en la que no existía integración celular por la vertiente peritoneal, y solamente se llevaba a cabo por la vertiente superficial8. Para incrementar esta integración se creó una superficie rugosa en ésta. A pesar de ello, la resistencia mecánica no cambió respecto a los diseños iniciales. Algo importante en cuanto a las modificaciones de estas prótesis fue la impregnación de éstas con una solución argéntica para impedir la adhesión bacteriana en los primeros momentos postimplante. Estudios efectuados con esta modificación han constatado el beneficio aportado por este pretratamiento en este tipo de biomaterial9.
También, en el contexto de las prótesis laminares, hay que resaltar los diseños efectuados con materiales totalmente absorbibles, fundamentalmente derivados de submucosa porcina (Surgisis®)10,11. Son prótesis naturales, entendiendo por éstas aquellas procedentes de tejidos extirpados de su medio natural y que, con o sin modificaciones, servirán como soporte para la colonización celular en los tejidos receptores al implante.
Estos tipos de prótesis naturales requieren unos controles muy estrictos, dada su procedencia animal de diversas especies (bovino, porcino) y que no están, por ello, exentas de posibles transmisiones de enfermedades como ya ha ocurrido con prótesis de duramadre liofilizada.
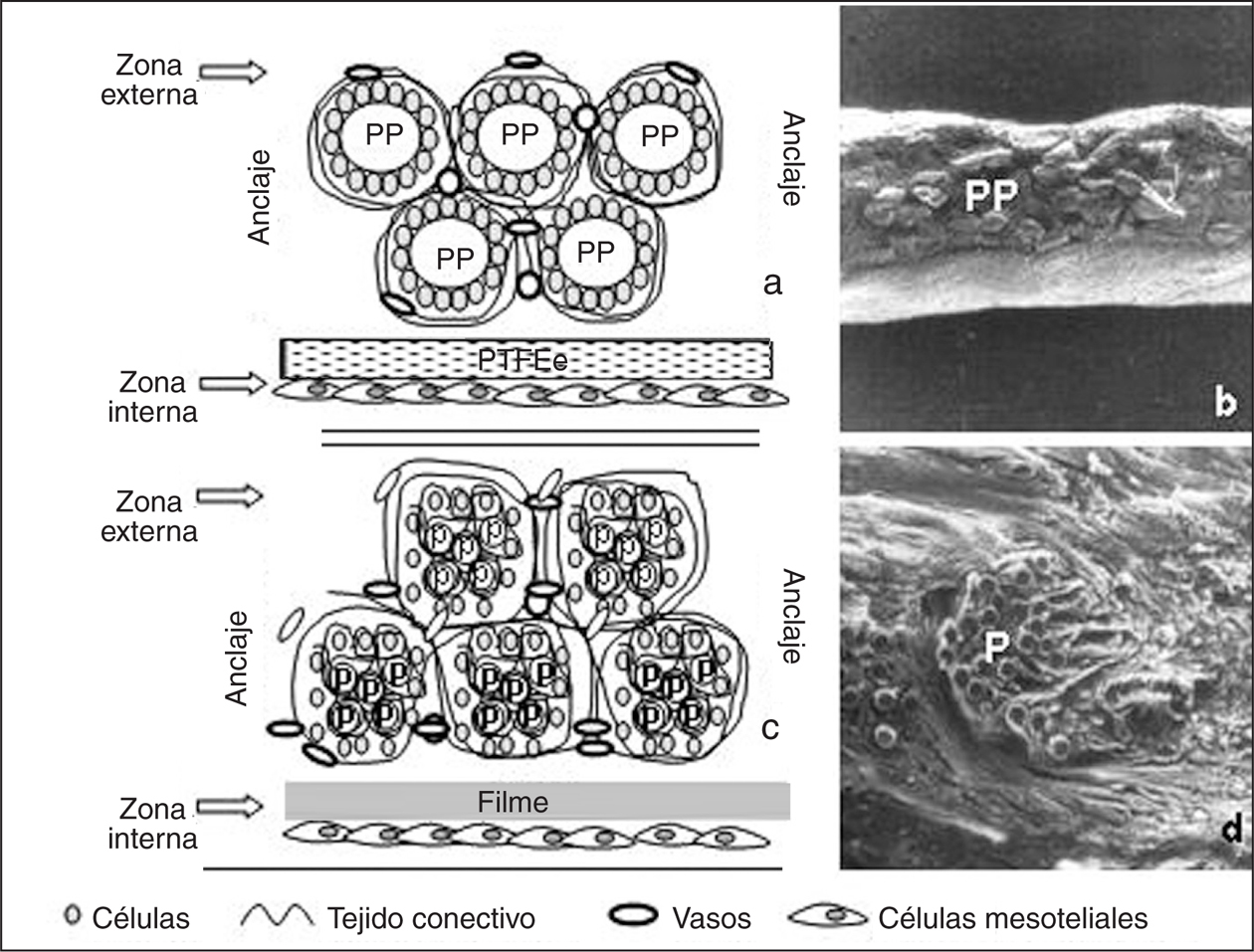
Finalmente, en el campo de la reparación de grandes defectos herniarios, en los que básicamente hay que llevar a cabo una reconstrucción de la pared abdominal, en los que no hay soporte prácticamente de tejido, y el biomaterial tiene que quedar ubicado en contacto con el peritoneo visceral, las prótesis tipo compuesto o composite han abierto un amplio abanico de posibilidades en la reparación de grandes defectos (fig. 2)12.
Fig. 2. Integración de 2 prótesis compuestas con el tejido receptor: a) prótesis cuyos 2 componentes no son absorbibles; b) panorámica a microscopia electrónica de barrido del tipo de prótesis anterior (x 15); c) esquema de la integración tisular de una prótesis, que contiene un componente absorbible (filme de polietilenglicol); d) visión de la prótesis integrada a microscopia electrónica de barrido (x 200). PP: polipropileno; PTFEe: politetrafluoroetileno expandido; P: poliéster.
Por ello, el objetivo primordial de estas prótesis es mejorar el comportamiento en relación con la interfaz visceral. Además, con éstas se trata de evitar la aparición de algunas complicaciones como la aparición de cuadros de obstrucción intestinal y/o fístula enterocutánea, generada la mayoría de las veces por el contacto entre el intestino y el material protésico.
Las prótesis composite tienen 2 componentes: uno puede ser el biomaterial principal (primer componente), al que se puede añadir otro, que cumple la función especifica que no puede llevar a cabo el primero (segundo componente). De esta forma el diseño de estas prótesis va dirigido a que el biomaterial que constituye el primer componente asuma el papel de integración tisular, y el segundo quede ubicado en contacto directo con el peritoneo visceral y module el comportamiento en esta interfaz. Ambos componentes suelen estar unidos mediante pegamentos acrílicos, termosellado e incluso sutura.
Los biomateriales que forman el primer componente suelen ser prótesis de tipo reticular, bien polipropileno o poliéster. El segundo componente suele ser de tipo laminar y puede ser absorbible o no absorbible. Debido a las características de este segundo componente, en la terminología fundamentalmente anglosajona se habla de prótesis con "barreras físicas y/o químicas". Las primeras son aquellas en las que el segundo componente es no absorbible, y las segundas, en que es absorbible.
¿Qué barrera tiene un mejor comportamiento?
Realmente no hay muchas diferencias. Las físicas parecen más estables, aunque tienen el inconveniente de que queda más material extraño en el organismo receptor.
Propuesta de clasificación
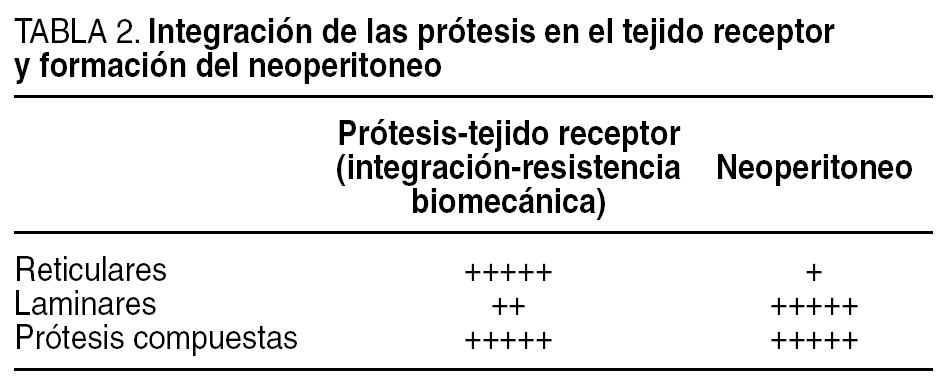
Nuestra clasificación propone dividir a las prótesis en 3 grandes grupos: reticulares, laminares y compuestas. Los subtipos de prótesis en esta clasificación dependen de si el biomaterial es absorbible o no (tabla 1). Además, para una mejor comprensión de éstas y de su utilidad práctica, se ha diseñado una correlación entre la estructura, y el comportamiento biológico y biomecánico de integración a los tejidos receptores.
Siguiendo a los distintos grupos de prótesis (tabla 2), las prótesis reticulares, estructuralmente y desde un punto de vista biomecánico, son óptimas para su colocación en una interfaz tejido-tejido. Las prótesis laminares deben emplearse para colocarse en contacto directo con el peritoneo visceral. Finalmente, las prótesis compuestas pueden ubicarse en todas las interfaces, aunque su diseño está ideado con la finalidad de ser colocadas en una interfaz de tejido y a su vez en una interfaz de peritoneo visceral.
El presente trabajo ha sido realizado con una Ayuda de Investigación GR/MAT0917/2004.