Las duplicaciones del tracto gastrointestinal son anomalías congénitas muy infrecuentes que pueden afectar a cualquier segmento del tubo digestivo1–5. Sanger en 1880, publicó por primera vez un paciente con un quiste de duplicación duodenal (QDD)2. Desde entonces se han publicado aproximadamente unos 120 casos2. Presentamos una paciente con un QDD sintomático y debatimos la etiología, las pruebas diagnósticas y sus opciones terapéuticas.
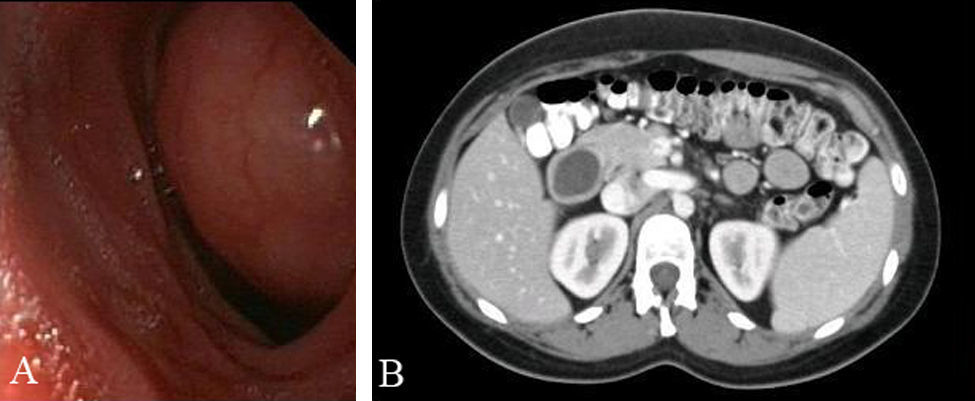
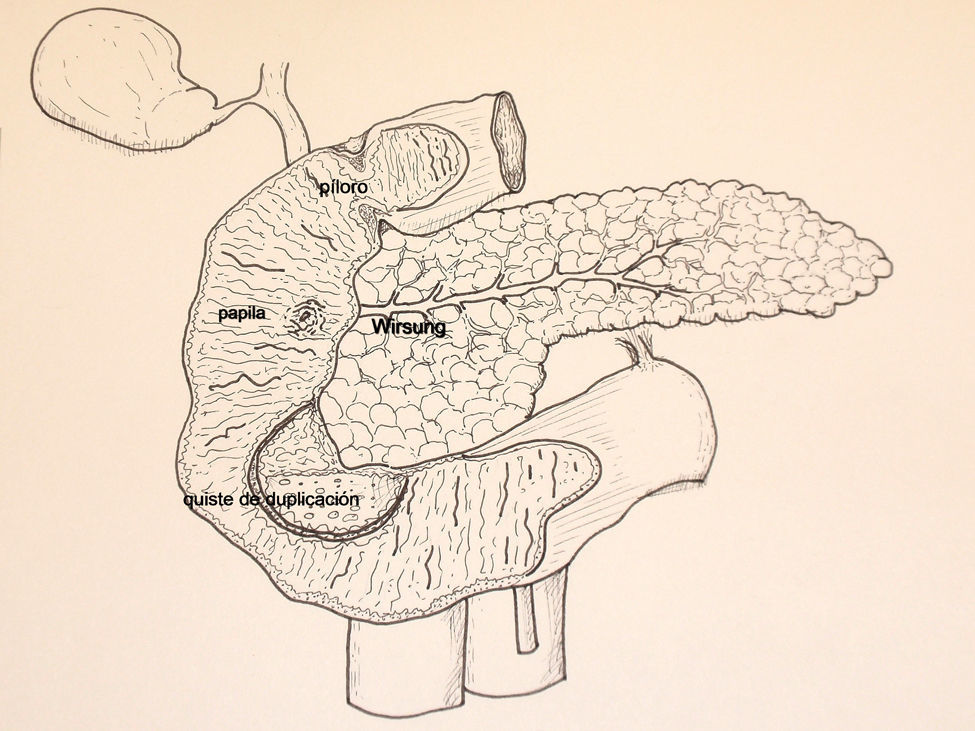
Mujer de 26 años que consultó por vómitos de repetición y dolor abdominal de dos meses de evolución. Todas las analíticas realizadas fueron normales. La endoscopia digestiva alta y la ecoendoscopia detectaron, en la pared posterior de la primera porción duodenal, una lesión submucosa que ocupaba casi toda la luz aunque permitía el paso del endoscopio (fig. 1A). Durante la exploración endoscópica no se puncionó la lesión por intolerancia de la paciente. La tomografía computerizada (TC) abdominal mostró una imagen redondeada, quística, homogénea, de 30mm de diámetro y de pared fina sin calcificaciones, dependiente de la pared lateral del duodeno (fig. 1B). Se intervino quirúrgicamente mediante incisión subcostal derecha, apreciando el QDD en el borde mesénterico duodenal. Se practicó colecistectomía y duodenotomía transversa sobre la lesión. Se comprobó la relación entre la papila y el QDD, mediante la colocación de un catéter de colangiografía en la vía biliar, observando que la papila estaba muy cercana al QDD pero no incluida en la lesión (fig. 2). Se puncionó el quiste y se tomaron muestras para citología y bioquímica, cuyos resultados obtenidos en el periodo postoperatorio fueron: amilasa 3578UI/l, CEA: 121.9UI/l, CA19.9: 29.8UI/l, citología benigna y cultivo positivo para E Coli. Se procedió a su apertura comprobando que la pared posterior del QDD estaba fusionada a la pared duodenal y a la cabeza pancreática por lo que practicamos una resección casi total (>90%) del QDD, dejando una mínima zona de la pared posterior unida firmemente a la cabeza pancreática. Se cerró la duodenotomia y se colocó un tubo de Kehr. En el periodo postoperatorio presentó pancreatitis aguda con colecciones peripancreáticas, derrame pleural bilateral, y, fuga biliar por extracción accidental del tubo de Kehr, que fue recolocado por el radiólogo intervencionista. Ante la existencia de algún vómito aislado, se realizó transito intestinal que demostró buen paso del contraste a través del duodeno. El estudio histológico confirmó el diagnostico de QDD. En la mucosa se apreció alguna área de tejido pancreático aislado. Actualmente la paciente se encuentra asintomática y con buena tolerancia oral.
Los QDD representan un 5% del total de duplicaciones gastrointestinales1–5. Su incidencia es inferior a 1 caso por cada 100000 nacimientos2. Habitualmente son quistes esféricos, que se localizan en la primera ó segunda porción duodenal, en el lado mesentérico de la pared anterior, y que no se comunican con el tubo digestivo aunque, también, pueden ser tubulares y tener una comunicación2–5. Normalmente están tapizados por mucosa duodenal pero también puede detectarse mucosa gástrica (15% de QDD), intestinal, o tejido pancreático2,5. El segmento final de la vía biliar y pancreática puede estar incluido en el QDD5. Existen varias teorías sobre el origen del QDD, todas basadas en un defecto en el desarrollo embriológico aunque, la etiología concreta aún no está aclarada3,5. Habitualmente se diagnostican en la infancia por lo síntomas que causan, aunque en un tercio de los pacientes se manifiesta bruscamente en la edad adulta1,2,5.
A nivel clínico causan dolor abdominal, obstrucción intestinal y, en ocasiones, una masa abdominal palpable. Pueden también producir invaginación duodenoyeyunal, pancreatitis recurrente, ictericia o hemorragía1–3,5,6. La pancreatitis se produce por compresión directa de la papila por el QDD o por obstrucción del árbol biliopancreático por material del QDD1,6. Otras complicaciones menos frecuentes son: litiasis intraquistica, infección, infarto, perforación, comunicación transdiafragmática o malignización que se ha descrito en 3 ocasiones2.
En los estudios baritados se observa una masa que comprime la rodilla duodenal. La TC y la resonancia magnética (RM) proporcionan información sobre el tamaño, la localización y la naturaleza quística de la lesión3–5. En la ecoendoscopia, se observa la gut signature: la submucosa forma una capa interna hiperecoica y la capa muscular una externa hipoecoica3, y además, permite la punción de la lesión. La endoscopia valora el grado de obstrucción, la localización y la relación con la papila. Los posibles diagnósticos diferenciales son: tumores duodenales intramurales, quiste de colédoco, coledocele, pseudoquiste pancreático y tumores quísticos pancreáticos2,4.
Merrot et al distinguen histológicamente dos tipos de QDD: 1) pared común formada por dos mucosas separadas con su muscularis mucosae y una capa de tejido conectivo entre ambas y 2) pared común con capas musculares y dos capas mucosas que incluye ductos biliares o pancreáticos5. Los niveles de CA19-9 y CEA intraquísticos pueden estar elevados2.
El tratamiento de elección es la escisión quirúrgica completa del quiste3,5. Pero no siempre es factible, ya que sólo es aplicable en QDD sin comunicación con la vía biliar o ducto pancreático y con doble capa (duodenal y del quiste)5. La resección subtotal o derivaciones digestivas externas e internas se han realizado en los casos que por localización o tamaño no permiten la exéresis total3,5. Se recomienda la exéresis casi completa del QDD dejando sólo la zona adherida al páncreas3,5. En nuestro caso, sólo la duodenopancreatectomía cefálica habría conseguido la resección completa. La resección endoscópica del QDD, como alternativa terapéutica, fue realizada por primera vez en 1984, y consiste en la fenestración endoscópica del quiste1,6. Existen varios instrumentos endoscópicos para realizarla1,2,6. La dificultad técnica y el riesgo de malignización ha dificultado la aceptación de la resección endoscópica parcial como tratamiento del QDD.