Sr. Director:
Presentamos un caso de perforación espontánea de esófago caracterizado por la atípica presentación e inicio de los síntomas.
Se trataba de un paciente varón de 44 años de edad, con antecedentes de dispepsia gástrica en los meses anteriores que, mientras dormía, fue despertado por un dolor brusco, localizado a punta de dedo en la región subxifoidea con irradiación hacia la espalda y a la base de hemitórax derecho. Posteriormente al dolor, el paciente tuvo un vómito bilioso.
Fue trasladado al servicio de urgencias 3 horas después del inicio del dolor, donde se realizó exploración física, analítica y radiológica básica y se avisó al servicio de cirugía a las 6 h del inicio del cuadro.
Encontramos a un paciente de aspecto grave, con una reacción neurovegetativa y dolor espontáneo que refería en la espalda y base de hemitórax derecho.
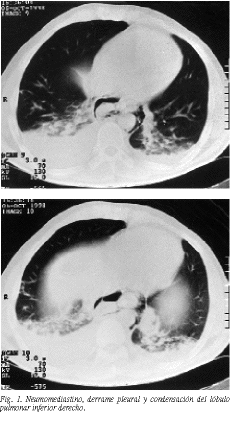
En la exploración física el abdomen era blando y depresible, ligeramente doloroso a la palpación profunda en epigastrio. Analíticamente se halló leucocitosis (25.000/ µ l) con desviación a la izquierda. El resto de los parámetros habituales fueron normales. Las radiografías de tórax y de abdomen eran normales, así como la ecografía abdominal. Dos horas después el paciente, con sueroterapia y analgesia, se encontraba mejor, sin dolor espontáneo y la leucocitosis había descendido hasta 15.000. Para tratar de clasificar el proceso solicitamos TAC toracoabdominal que informó de signos radiológicos de neumomediastino con derrame pleural y afectación parenquimatosa del lóbulo inferior del pulmón derecho (fig. 1).
Diagnosticamos perforación esofágica y propusimos intervención quirúrgica, de acuerdo con el cirujano torácico, que fue aceptada por el paciente, sin que consideráramos conveniente someterle a más pruebas diagnósticas.
Mediante toracotomía derecha por el sexto espacio intercostal se objetivó mediastinitis con afectación inflamatoria pulmonar y con una colección purulenta yuxtaesofágica desde la ácigos hasta la unión gastroesofágica, así como derrame pleural. En el tercio distal de esófago, próximo a cardias, se visualizaba perforación vertical de la cara anterior del mismo, de unos 2,5 cm de longitud, sin signos de necrosis esofágica.
Por vía torácica se limpió y drenó el mediastino y se dio un punto en el extremo superior de la perforación. Se practicó laparotomía media supraumbilical, observando discreta reacción inflamatoria en la unión esofagogástrica, así como estigmas de ulcus bulbar, siendo normal el resto de la cavidad abdominal.
Aislamos el esófago y completamos la sutura de la rotura mediante puntos simples, y protegimos dicha sutura con una plastia de fundus gástrico. Terminamos la intervención con gastrostomía aspirativa y yeyunostomía de alimentación.
El paciente fue trasladado inicialmente a la UCI y con posterioridad a la planta, con evolución favorable, reiniciando la alimentación oral en el undécimo día del postoperatorio, previa práctica de estudio radiológico digestivo con medio de contraste, que fue normal. Se propuso alta hospitalaria a los 15 días de la intervención, prescribiéndole tratamiento con omeprazol.
Se realizó revisión al mes del alta hospitalaria, y solicitamos un nuevo estudio radiológico digestivo, que fue normal. Posteriormente realizamos una esofagogastroduodenoscopia que también fue informada de normal.
La rotura espontánea de esófago o síndrome de Boerhaave es definida como una "dehiscencia de la pared esofágica en zona macroscópicamente sana, habitualmente a consecuencia de un aumento brusco de la presión esofágica1". La ausencia de vómitos previos y el hecho de presentarse durante el sueño hacen que este caso sea distinto de lo habitual.
En la etiopatogenia de la rotura se mencionan como factores predisponentes alteraciones gastroduodenales, como hernia de hiato y ulcus duodenal. En el caso que presentamos había engrosamiento de las paredes del bulbo duodenal con signos inflamatorios pospilóricos. En algunas series de síndrome de Boerhaave se reconoce un alto porcentaje de ulcus bulbar2. Con un elevado porcentaje de mortalidad, el tratamiento quirúrgico temprano favorece la supervivencia3.
La clínica es inespecífica; generalmente los vómitos preceden al dolor, aunque esta secuencia puede estar alterada4-8. El dolor es con frecuencia referido como retrosternal, pero también puede ser abdominal y se acompaña de síndrome neurovegetativo y shock. La aparición de enfisema subcutáneo es tardía e, inicialmente, la radiografía de tórax puede ser normal. La posibilidad de rotura espontánea de esófago debe ser considerada cuando coexistan síntomas respiratorios y gastrointestinales9 y el diagnóstico diferencial se debe establecer con pancreatitis aguda, neumonía por aspiración, gastritis alcohólica y perforación de ulcus duodenal o gástrico. Inculet et al10 describen un caso de síndrome de Boerhaave en un niño, confundido con apendicitis aguda. Aunque el diagnóstico de certeza se hace con la visualización extraluminal del contraste ingerido por vía oral, en ocasiones, como en nuestro caso, se puede hacer mediante TAC11.
Algunos autores12 preconizan el tratamiento médico, si bien la mayoría están de acuerdo que con el tratamiento quirúrgico precoz se obtienen mejores resultados, sin que la técnica empleada esté en relación directa con los resultados13.
Aunque se puede realizar toracoscopia14, la vía de abordaje habitual para lesiones de esta localización es la toracotomía izquierda. En este caso optamos por el abordaje derecho debido al importante derrame pleural de ese lado. La sutura con plastia, bien pleural o bien de músculo intercostal, cuando el proceso está en el inicio, o la esofaguectomía si la evolución es larga, son las técnicas de elección, aunque también se utiliza la sutura con tubo en T. La toracotomía asociada a laparotomía puede ser necesaria en perforaciones bajas15. En este caso, la plastia con fundus gástrico después de la sutura creemos que es lo adecuado. Si se hace laparotomía, la gastrostomía de descompresión aspirativa y la yeyunostomía de alimentación están indicadas.
En resumen, el síndrome de Boerhaave es un cuadro sumamente grave, aunque a partir de 1980 se han mejorado las cifras de mortalidad2, probablemente debido al diagnóstico precoz y a las UCI, que debemos sospechar en casos de pacientes graves con dolor retrosternal o abdominal, aunque no vaya precedido de vómitos, u otras acciones productoras de aumento de la presión intraesofágica.