Introducción
Las resecciones amplias de la pared abdominal por neoplasias primitivas o metastásicas plantean problemas técnicos quirúrgicos que suponen la reconstrucción del defecto aponeurótico con materiales sintéticos1,2. En esta situación, los tumores desmoides que se originan en las estructuras músculo-aponeuróticas de la pared abdominal precisan resección radical, debido a que tratamientos alternativos como quimioterapia, radioterapia, farmacoterapia y hormonoterapia no han demostrado ser eficazmente superiores a la cirugía. Estos tumores afectan principalmente a pacientes jóvenes y, debido a su potencial de invasión de estructuras vecinas, gran tendencia a recidivar localmente y condicionar en algunos casos la muerte del enfermo, han sido reclasificados como fibrosarcomas infiltrantes de bajo grado, del que se reconocen una forma de presentación esporádica y otra en relación con la poliposis colónica familiar3-5. Dejados a su libre evolución son capaces de adquirir enormes dimensiones ocasionando alteraciones estéticas, comprometiendo estructuras vitales por compresión y, excepcionalmente, originando metástasis6,7.
Caso clínico
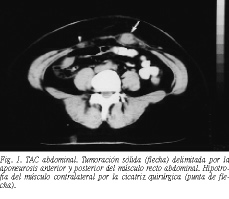
Mujer de 32 años con antecedente de colecistectomía por pancreatitis aguda biliar hacía 12 años. Acudió a consulta en mayo de 1996 por presentar dolor en el hipocondrio izquierdo, constante, progresivo e intenso de 2 meses de evolución. En esta región, inmediatamente por debajo de la cicatriz transversa, se palpaba una tumoración dura, redondeada, dolorosa y fija, de unos 4 cm. Los estudios analíticos sanguíneos no presentaban alteraciones. La ecografía objetivó una tumoración sólida, hipoecogénica, de 3,5 cm de diámetro, localizada en el tercio superior del músculo recto izquierdo. Tanto la TAC como la RMN pusieron de manifiesto una masa sólida, homogénea, limitada por las aponeurosis anterior y posterior de este músculo, sugiriendo un tumor desmoide como primera posibilidad diagnóstica (fig. 1).
Se procedió, por tanto, a la exéresis inmediata, encontrando en la intervención una tumoración de unos 4 cm de longitud, dura, de color blanquecino, adosada a la aponeurosis anterior y que abarcaba el espesor del músculo recto abdominal izquierdo en la zona de la cicatriz quirúrgica, donde además se identificó material de sutura antiguo. Fue preciso colocar una malla de polipropileno para cerrar el defecto aponeurótico de 8 cm de diámetro. El informe anatomopatológico fue de tumor desmoide de 3,5 cm, que alcanzaba uno de los bordes quirúrgicos. En el postoperatorio tardío se produjo una infección de la herida, aislándose Staphylococcus aureus, cuya persistencia motivó la reintervención a los 3 meses, procediendo a retirar la prótesis, ampliación de los bordes quirúrgicos y reparación del nuevo defecto mediante la implantación de una malla reabsorbible de ácido poliglicólico (Dexon) para evitar la evisceración. La anatomía patológica puso de manifiesto la presencia de un sinus abscesificado, con reacción de cuerpo extraño e intensa proliferación fibroblástica.
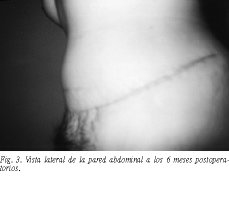
Eventualmente se produjo una importante debilidad del hemiabdomen superior izquierdo, por ausencia parcial y atrofia del músculo recto abdominal. Por ello, transcurridos 12 meses se programó para una abdominoplastia. Tras el levantamiento del colgajo abdominal y apreciar una eventración de 12 cm, se procedió a la disección, apertura del saco herniario y liberación de las adherencias intraperitoneales. La reparación consistió en colocar intraperitonealmente una malla de politetrafluoroetile no expandido (PTFE-e) (Gore-tex Dual-Mesh Plus) de 15 * 19 cm, de 2 mm de espesor, impregnada en nitrato de plata y clorhexidina, fijada con puntos en "U" a través de todo el espesor de la pared (fig. 2), aprovechamos el cierre del saco herniario, que cerramos a modo de solapa, para el aislamiento de la malla del tejido subcutáneo y así colocar una segunda malla de polipropileno de 20 * 30 supraaponeurótica que abarcaba el hemiabdomen izquierdo en su totalidad y parte del derecho. Se colocaron dos drenajes de Redón que se retiraron entre el sexto y noveno días, transcurriendo el postoperatorio sin complicaciones (fig. 3).
A los 18 meses de la última intervención, la pared mantenía una notable consistencia, y no se han demostrado recidivas en el seguimiento de 30 meses.
Discusión
Los tumores desmoides se originan en estructuras músculo-aponeuróticas de la pared abdominal, espalda, extremidades, cabeza y cuello, mesenterio y cicatrices quirúrgicas. Generalmente son únicos, pero en ocasiones pueden ser multicéntricos. Son neoplasias sólidas con apariencia macroscópica de estar delimitadas por una seudocápsula, aunque no en todos los casos. Microscópicamente presentan prolongaciones a modo de seudópodos en ocasiones distantes de la masa tumoral, pero en contigüidad con la misma. Por este motivo, márgenes de resección de 2 cm, considerados como adecuados, pueden ser insuficientes y condicionar recidivas locales3-5. Varios autores recomiendan el análisis intraoperatorio de los bordes quirúrgicos; sin embargo, la validez de esta prueba no está demostrada1,2.
Aproximadamente recidivan un 5% de los tumores desmoides que afectan a la pared abdominal anterior, apareciendo la gran mayoría (70-90%) durante los primeros 3 años. El tamaño tumoral y la afectación de los bordes quirúrgicos son considerados como los factores de riesgo más importantes. Cuando se produce la recidiva temprana, un hecho destacado por diferentes autores, es el rápido crecimiento del tumor, que alcanza en ocasiones un tamaño y peso similares e incluso superiores a la neoplasia predecesora4,5,8-10.
La cirugía es el tratamiento de elección y permite la confirmación histológica de la enfermedad, siendo la única modalidad de tratamiento que ha demostrado ser curativa. El principal objetivo es la ablación total del tumor con márgenes de resección adecuados y, por tanto, siempre debe ser inicialmente un procedimiento radical5,8,10. No obstante, los tumores voluminosos de pared abdominal que precisan exéresis amplias, las múltiples intervenciones por recidivas o las eventraciones secundarias a procesos sépticos de pared, como en nuestro caso, conllevan defectos aponeuróticos importantes con pérdida de masa y función muscular, precisando en la mayoría de los casos cirugía reconstructora de la pared abdominal con colgajos miocutáneos o con prótesis. En estos casos, la intervención y el tipo de incisión han de ser cuidadosamente planificadas.
Técnicas descritas en el pasado y aún vigentes para la reconstrucción de la pared abdominal se basan en la sutura primaria de los planos aponeuróticos o en la utilización de injertos pediculados. Los defectos en la pared abdominal pueden ser reparados con técnicas de afrontación de aponeurosis en dos planos (Gouilloud, 1892 y Quenu, 1896), a modo de solapa en dos planos (Judd, 1912), afrontación de aponeurosis con incisiones de relajación en las fascias (Gibson, 1920 y Clotteau-Prémont, 1972) e incisión transversa con incisión de relajación de la fascia suprapúbica y manteniendo al enfermo en posición de semiflexión en el postoperatorio (Die Goyanes, 1968). Las técnicas que emplean injertos pediculados de fascia del recto abdominal (autoplastia muscular de Welti-Eudel, 1941), injertos iliotibiales de fascia lata (Wangensteen, 1946) e injertos de músculo oblicuo mayor (Lesnick, 1953) se utilizan con poca frecuencia11,12.
Hoy día, gracias a la disponibilidad de buenos materiales protésicos, podemos extender los márgenes de resección y reparar los defectos músculo-aponeuróticos sin disecciones extensas y sin excesiva tensión en las líneas de afrontación de las aponeurosis13-15. En el caso que nos ocupa, la tumoración alcanzaba la proximidad de uno de los bordes quirúrgicos, de modo que se practicó una ampliación en la segunda exéresis. Sin embargo, la pieza demostraba un área de intensa proliferación fibroblástica que, debido a la presencia de la malla y la infección, fue muy difícil de precisar si se trataba de una recidiva en ausencia de tumor macroscópico. La sepsis y contaminación de la malla por Staphylococcus aureus supuso su retirada, y aunque la resistencia o tolerancia a la infección dependen del huésped y de las características biofísicas del material (porosidad, tipo de nudos y diámetro de las fibras), una vez que este germen coloniza un material protésico es muy difícil de erradicar16,17. En nuestra experiencia, con éste y otros casos más la implantación de una malla reabsorbible de ácido poliglicólico ha sido de gran utilidad, impidiendo inicialmente la evisceración, aunque la eventración fue evidente al cabo de unos meses. A este respecto, los estudios experimentales han demostrado que las mallas reabsorbibles producen un tejido fibroso fino con escasa capacidad de sostén, lo que se relaciona con una tasa de recidivas superior al 40%15. Su principal utilidad estriba en colocarlas en situaciones de sepsis o en casos donde es in evitable el contacto con estructuras viscerales. Algunos autores recomiendan, en casos de infección, colocar inicialmente una malla de material reabsorbible, para así, en unas semanas, proceder a colocar una segunda más consistente, o bien colocar a la vez una malla reabsorbible en contacto con las asas e inmediatamente por encima una segunda de polipropileno18. Consideramos que en casos de infección es preferible colocar únicamente una prótesis reabsorbible y esperar al menos un año antes de intentar una segunda reparación, dando la oportunidad de completar, en lo posible, los procesos de maduración y remodelación del tejido cicatrizal y evitar el riesgo de una segunda infección de la prótesis. En efecto, de este modo hemos actuado y obtenido un resultado muy satisfactorio.
También hemos combinado las ventajas que ofrece hoy día una malla de PTFE-e, con múltiples poros e impregnada en clorhexidina y nitrato de plata, con una malla fuerte como la de polipropileno, que es rápidamente incorporada en los tejidos. El PTFE-e es un material fuerte, resistente, pero a su vez elástico, bien tolerado y con una superficie inferior lisa poco adherente que permite su colocación intraperitoneal en contacto con las asas intestinales13-15. La implantación intraperitoneal posee la ventaja de producir una buena contención de la pared y escasas adherencias viscerales. Varios estudios experimentales han demostrado que la malla de PTFE-e, dentro de la cavidad abdominal en su cara visceral, es revestida por una capa de células mesoteliales formando un neoperitoneo bien definido al cabo de 7 días19. Las experiencias clínicas demuestran que las mallas intraperitoneales son bien toleradas y con una escasa morbilidad14. La impregnación con sales de plata y clorhexidina dis minuye la colonización bacteriana y ofrece la ventaja de su implantación en heridas infectadas previamente17, como en nuestro caso. El aislamiento de la malla de PTFE-e del tejido subcutáneo, cubriéndola con el saco herniario, el cual no resecamos, nos permitió la colocación de una segunda malla de polipropileno, que es rápida y completamente integrada por tejido cicatrizal y que mantiene una gran fuerza de tracción15,20. Esta técnica mixta ha sido exitosamente utilizada en la reparación de defectos producidos en la pared torácica tras resecciones de tumores, destacando la rigidez de la pared costal lograda con múltiples prótesis21.
Así, combinando conjuntamente las propiedades individuales de cada malla se logró una pared abdominal consistente y con una notable capacidad de contención.
Por último, queremos señalar que se desconoce el efecto que puede tener, en la evolución final de estos tumores, la implantación de materiales que precisan proliferación fibroblástica para su incorporación en los tejidos.