Introducción
El tumor sólido seudopapilar del páncreas (TSSP) es una neoplasia poco frecuente (el 1% de los tumores pan creáticos y el 12% de los tumores quísticos pancreá-ticos)1 . Es un tumor de baja agresividad biológica cuya línea celular de origen aún no ha sido bien aclarada2-5 .
Caso 1
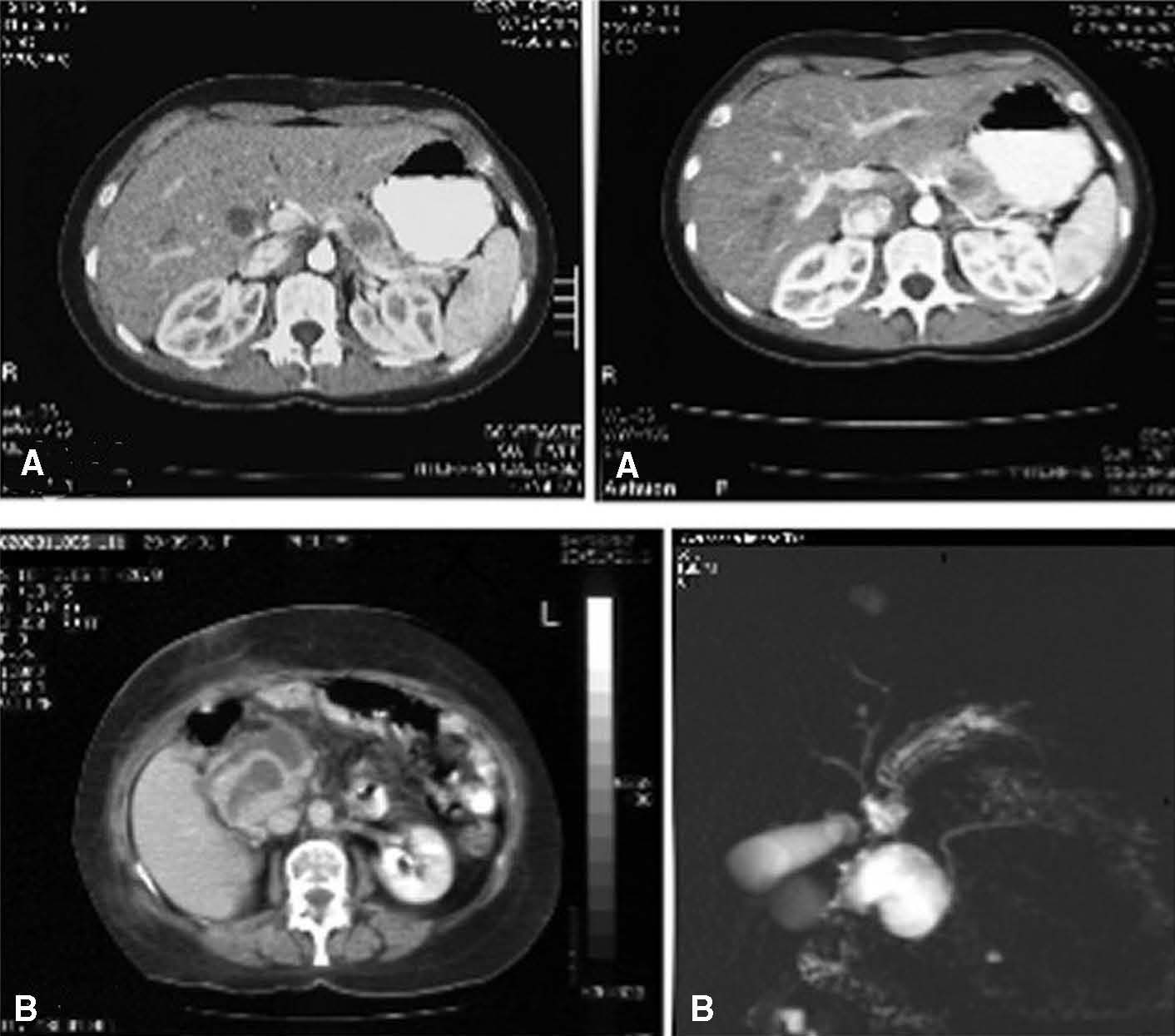
Mujer de 20 años, con antecedentes de 2 episodios de pancreatitis aguda de origen no determinado hacía 3 años. Las pruebas de imagen (tomografía computarizada [TC] y resonancia magnética [RM]) detectaron una lesión de aspecto nodular en el cuerpo-cola del páncreas (fig. 1A). En el seguimiento se objetivó crecimiento del nódulo, por lo que se decidió practicar una punción-aspiración con aguja fina (PAAF) que informó de la presencia de un tumor de célula pequeña regular. Con la sospecha de neoplasia epitelial sólida seudopapilar, se procedió a una pancreatectomía distal laparoscópica. El estudio anatomopatológico informó de una neoplasia epitelial sólida seudopapilar con márgenes libres. La evolución postoperatoria hasta la actualidad ha sido correcta.
Caso 2
Mujer de 62 años con antecedente de traumatismo abdominal hacía 6 meses y molestias abdominales inespecíficas. La analítica mostró un discreto aumento de la fosfatasa alcalina (FA) y GGT, con el resto de parámetros normales. La TC y la RM mostraron una lesión en cabeza pancreática, de contornos definidos e imagen quística trabeculada en su interior, con vías biliares de calibre normal y dilatación de la vía pancreática (fig. 1B). Orientada como lesión quística frente a seudoquiste postraumático de la cabeza del páncreas por el antecedente, se practicó una duodenopancreatectomía cefálica. La anatomía patológica de la pieza, de 4,5 cm de diámetro, demostró que se trataba de un TSSP de estructura quística, con área tumoral sólida de aspecto heterogéneo. La histología evidenció proliferación neoplásica de elementos de aspecto epitelial que formaban trabéculas con áreas sólidas. El seguimiento postoperatorio también ha sido satisfactorio.
DiscusiónEl TSSP fue descrito por primera vez por Frantz6 , en 1959. Desde entonces se han publicado más de 500 casos, y ha recibido diferentes denominaciones, como tumor sólido y epitelio-papilar, tumor papilar-quístico, y tumor sólido y quístico papilar del páncreas. A pesar de que se trata de una neoplasia pancreática con características propias, probablemente haya sido infradiagnosticada hasta la década de los noventa, al atribuirse a otros tipos histológicos7,8 .
Su presentación clínica depende del tiempo de evolución, desde indolente, detectado de forma casual en los de menor tamaño, a síntomas de compresión, dolor abdominal, sensación de plenitud con masa abdominal palpable en los de gran tamaño. No presenta asociación a otras neoplasias, enfermedades, síndromes paraneoplásicos de secreción hormonal ni marcadores séricos específicos. Se puede localizar en toda la glándula pancreática, aunque son algo más prevalentes en la cola.
Fig 1. A) Tomografía computarizada (TC) abdominal que muestra una tumoración de aspecto sólido de 2,5 cm de diámetro en el cuerpo-cola del páncreas. B) TC abdominal y resonancia magnética que evidencian una lesión en la cabeza pancreática, de 8 cm de diámetro, con contornos definidos e imagen quística trabeculada en su interior, con vías biliares de calibre normal y dilatación de la vía pancreática.
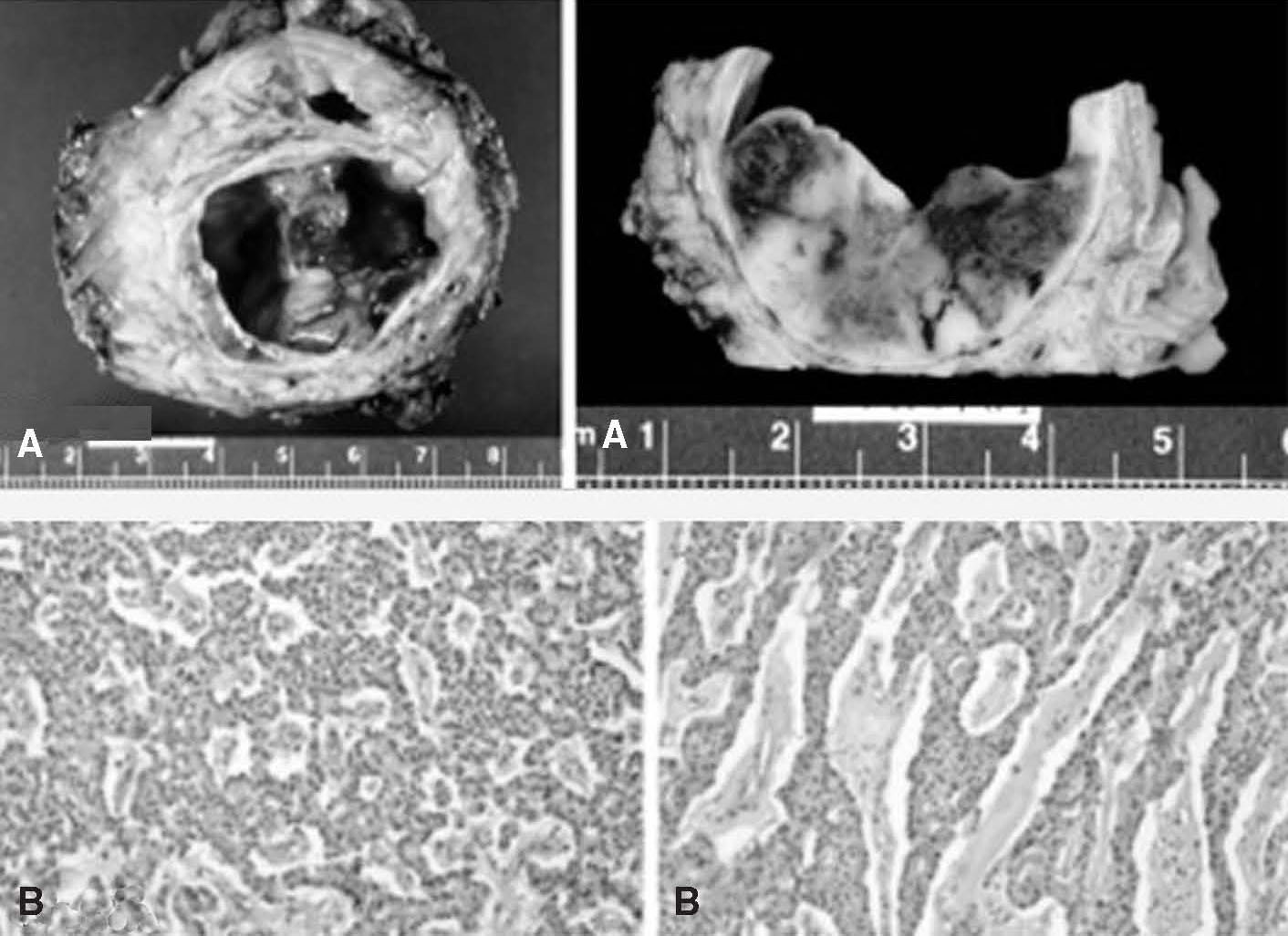
Fig. 2. A) Pieza macroscópica de estructura quística con lesión de aspecto tumoral y detalle de área tumoral sólida, de aspecto he terogéneo, alternando áreas hemorrágicas con otras de coloración pardusca. B) Histología de proliferación neoplásica de elementos de aspecto epitelial formando trabéculas con áreas sólidas.
El diagnóstico preoperatorio se realiza mediante pruebas de imagen (TC y RM). Existe controversia respecto al uso de la PAAF. En el caso de la PAAF percutánea guiada por TC, se cuestiona su uso para la biopsia de lesiones pancreáticas potencialmente resecables debido a las complicaciones que comporta, como hemorragia, lesión de órganos cercanos y la posibilidad de siembra de células malignas en el trayecto de la aguja. Aunque los datos actuales relacionan esta última posibilidad con el adenocarcinoma ductal y no con las neoplasias quísticas, es un riesgo que se debe tener en cuenta. Por otro lado, la emergencia del uso de la PAAF guiada por ecoendoscopia y sus prometedores resultados en la reducción del riesgo de siembra podrían ayudar a definir su uso en el tratamiento de lesiones quísticas sospechosas, ya que un diagnóstico preoperatorio certero mejora el abordaje terapéutico del paciente9 .
Como características morfológicas destacan un tamaño medio de 10,5 cm, el hecho de ser unicéntricos y una histología que varía en las diferentes regiones del tumor, según su tiempo de evolución: las áreas quísticas y seudopapilares son el resultado de cambios degenerativos graduales de tumores sólidos con una rica microvascularización como en el caso 2 (fig. 2B).
A pesar de tener el potencial de alcanzar gran tamaño, un crecimiento invasivo y metastatizar (el 10% en el diag-nóstico)1 , el TSSP es una neoplasia clasificada como carcinoma de bajo potencial de malignidad que no suele presentar metástasis metacrónicas.
Es importante el diagnóstico diferencial con otros procesos quísticos del páncreas. En primer lugar, con los seudoquistes pancreáticos, ya que suponen la lesión quística pancreática más frecuente. En las pruebas de imagen los seudoquistes son típicamente uniloculares y se asocian con frecuencia con cambios inflamatorios en la grasa peripancreática. La mejor forma de diferenciarlos es su seguimiento evolutivo, ya que el 60% de los seudoquistes se resuelven por sí solos, pero la gravedad de retrasar una intervención en una lesión potencialmente maligna hace que, en ausencia de antecedentes de pancreatitis aguda, como en el caso 2, de posible origen traumático, deban considerarse y tratarse como neoplasias quísticas. Otros diagnósticos diferenciales son los tumores endocrinos, el carcinoma de célula acinar, el pancreatoblastoma, el adenocarcnima ductal y los tumores quísticos del páncreas10 . La inmunohistoquímica puede ayudar a diferenciarlos, ya que el TSPP presenta una fuerte positividad focal a la α-1-antitripsina, como dato más característico, así como negatividad a marcadores endocrinos, como la cromogranina A y las enzimas pancreáticas.
El tratamiento de elección es la exéresis, que asegura prácticamente la curación, lo que resalta la importancia del diagnóstico temprano y certero de este tipo de lesiones.
Correspondencia: Dra. A. Hernández Puente. Pge. Maiol, 1, 1. o 3. a . 08013 Barcelona. España. Correo electrónico: angelahp@tiscali.es
Manuscrito recibido el 16-3-2004 y aceptado el 10-12-2004.