No existe ninguna herramienta validada para la estratificación de riesgo de los pacientes con enfermedad coronaria estable (ECE). Se ha visto que los niveles plasmáticos de la proteína quimioatractante de monocitos-1 (MCP-1), galectina-3 y pro-péptido natriurético tipo B aminoterminal (NT-proBNP) tienen valor pronóstico en esta población.
ObjetivoAnalizar la utilidad pronóstica de la escala clínica de riesgo del estudio Long-Term Intervention with Pravastatin in Ischemic Disease (LIPID) y la mejora de su capacidad predictiva al combinarla con los niveles plasmáticos de MCP-1, galectina-3 y NT-proBNP en pacientes con ECE.
Métodos y resultadosSe analizaron 706 pacientes con ECE y antecedentes de síndrome coronario agudo (SCA). Se realizó un seguimietno de 2,2±0,99años. El objetivo primario era la aparición de un evento isquémico (cualquier SCA, infarto cerebral o accidente isquémico transitorio), insuficiencia cardiaca o muerte.
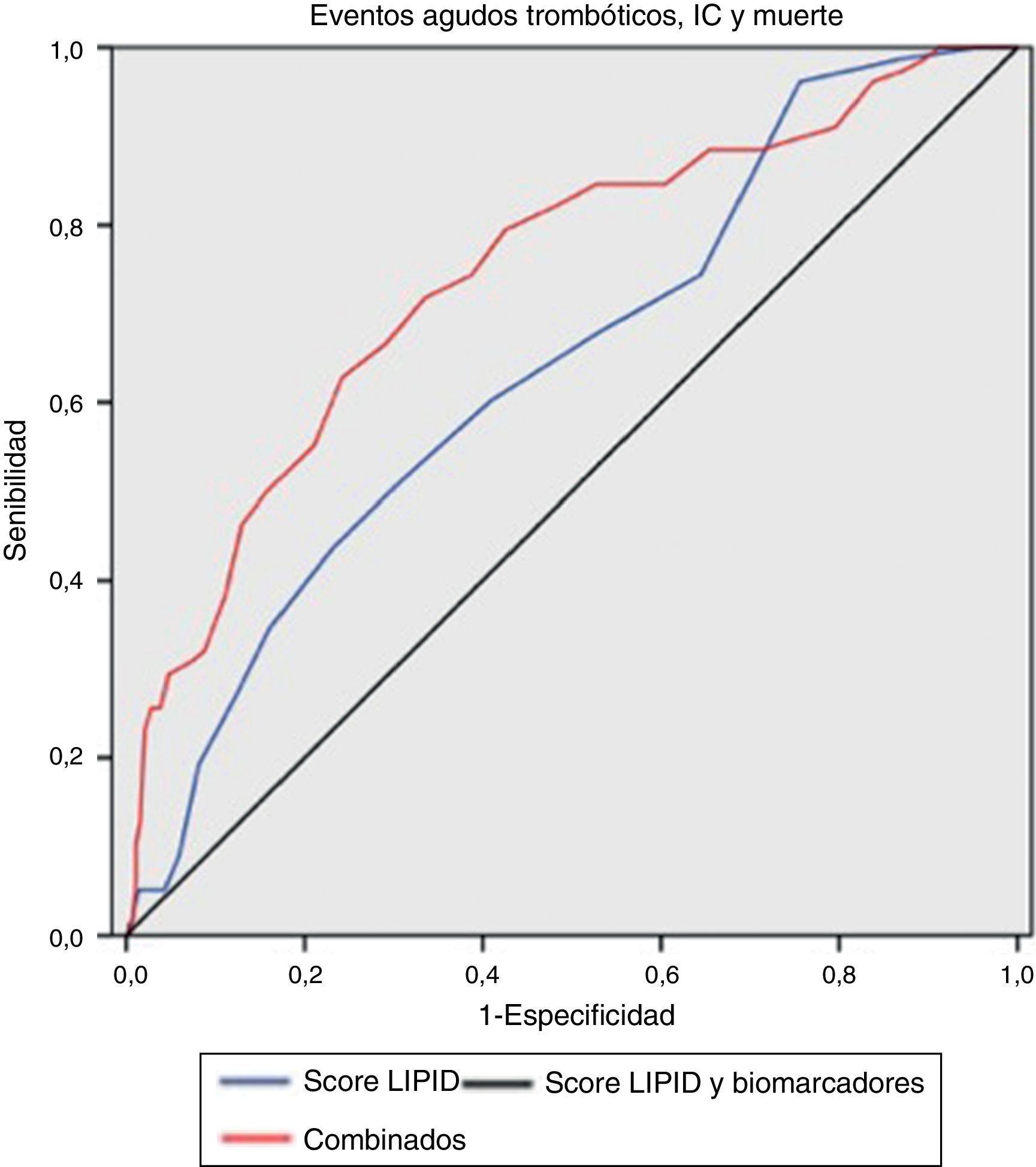
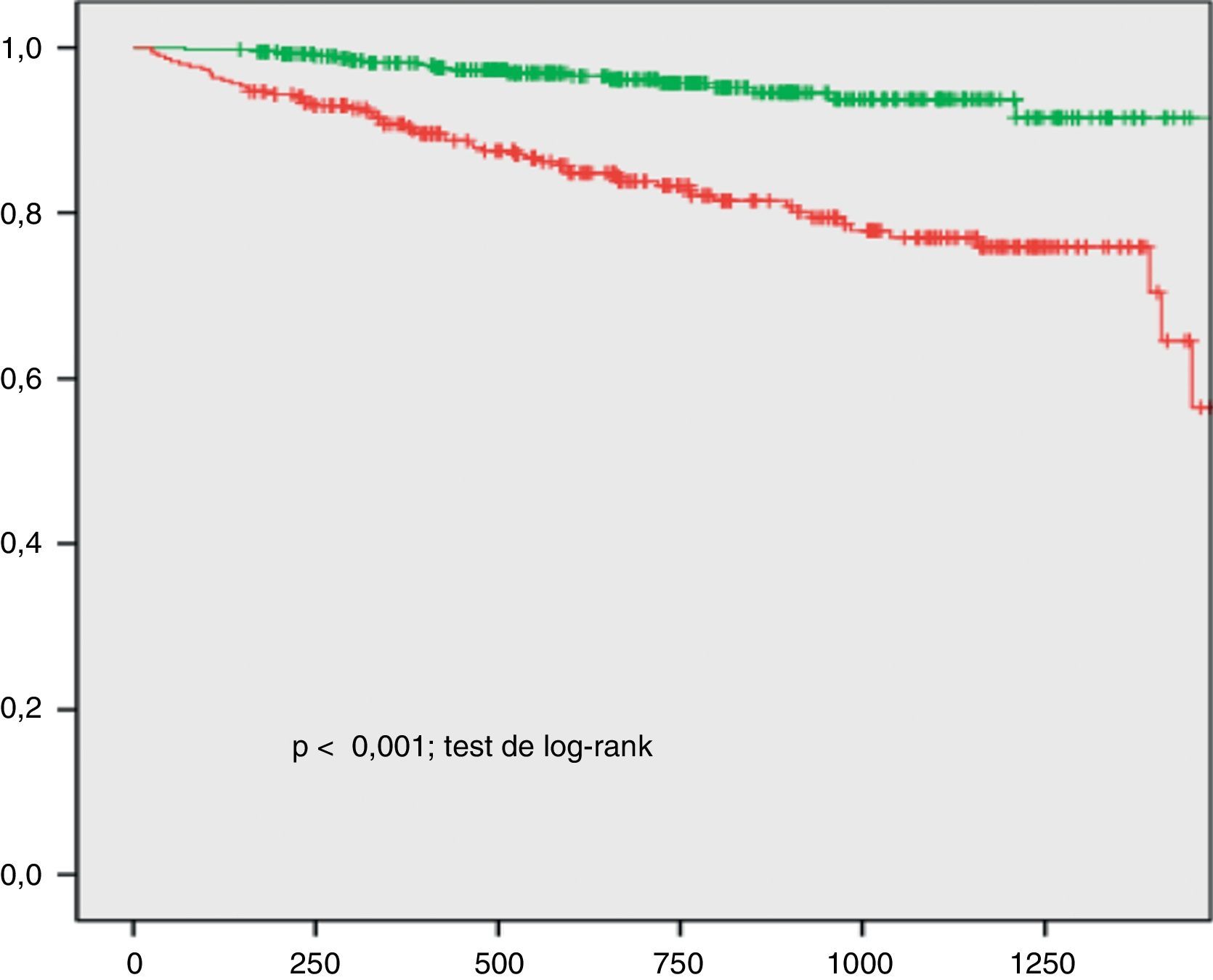
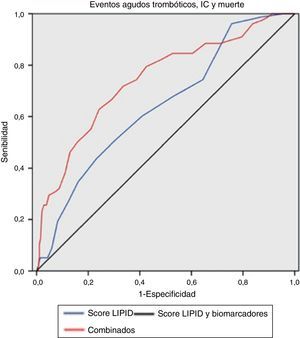
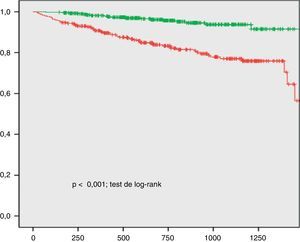
La escala clínica de riesgo predijo significativamente el desarrollo del objetivo primario, con un área bajo la curva receiver operating characteristic (ROC) de 0,642 (0,579-0,705); p<0,001. Desarrollamos una escala combinada sumando a las puntuaciones de la escala LIPID los deciles de los niveles plasmáticos de MCP-1, galectina-3 y NT-proBNP. El nivel predictivo mejoró con un área bajo la curva de 0,744 (0,684-0,805); p<0,001 (p=0,022 para la comparación). Una puntuación >21,5 mostró una sensibilidad del 74% y una especificidad del 61% para el desarrollo del objetivo primario (p<0,001; test de log-rank).
ConclusiónLos niveles plasmáticos de MCP-1, galectina-3 y NT-proBNP mejoran la capacidad de la escala clínica LIPID para predecir el pronóstico de los pacientes con ECE.
At present, there is no tool validated by scientific societies for risk stratification of patients with stable coronary artery disease (SCAD). It has been shown that plasma levels of monocyte chemoattractant protein-1 (MCP-1), galectin-3 and pro-B-type natriuretic peptide amino-terminal (NT-proBNP) have prognostic value in this population.
ObjetiveTo analyze the prognostic value of a clinical risk scale published in Long-term Intervention with Pravastatin in Ischemic Disease (LIPID) study and determining its predictive capacity when combined with plasma levels of MCP-1, galectin-3 and NT-proBNP in patients with SCAD.
Methods and resultsA total of 706 patients with SCAD and a history of acute coronary syndrome (ACS) were analyzed over a follow up period of 2.2±0.99 years. The primary endpoint was the occurrence of an ischemic event (any SCA, stroke or transient ischemic attack), heart failure, or death.
A clinical risk scale derived from the LIPID study significantly predicted the development of the primary endpoint, with an area under the ROC curve (Receiver Operating Characteristic) of 0.642 (0.579 to 0.705); P<0.001. A composite score was developed by adding the scores of the LIPID and scale decile levels of MCP -1, galectin -3 and NT-proBNP. The predictive value improved with an area under the curve of 0.744 (0.684 to 0.805); P<0.001 (P=0.022 for comparison). A score greater than 21.5 had a sensitivity of 74% and a specificity of 61% for the development of the primary endpoint (P<0.001, log -rank test).
ConclusionPlasma levels of MCP-1, galectin -3 and NT-proBNP improve the ability of the LIPID clinical scale to predict the prognosis of patients with SCAD.
Los pacientes que sufren un evento agudo isquémico, como un infarto de miocardio o un ictus, pueden fallecer antes de llegar al hospital y no beneficiarse de los avances de la medicina cardiovascular. Por esa razón es importante detectar qué pacientes tienen mayor riesgo de padecer un evento cardiovascular agudo. En este sentido, las nuevas guías europeas del manejo de la enfermedad coronaria estable ponen énfasis en la necesidad de estratificar el riesgo individual de cada paciente1.
La capacidad para predecir el riesgo en pacientes con enfermedad coronaria crónica a partir de los datos actuales disponibles en clínica es muy limitada. A diferencia de lo que ocurre en el síndrome coronario agudo (SCA), en la cardiopatía isquémica crónica no hay biomarcadores unánimemente aceptados en la práctica asistencial.
La búsqueda de biomarcadores sanguíneos es muy atractiva por 2 motivos. Primero, la sangre transporta moléculas que intercambia con la pared vascular aterosclerótica, por lo que puede darnos información de lo que ocurre en el interior de la misma. Segundo, los eventos isquémicos agudos se producen por formación de trombos, y estas estructuras están constituidas por elementos sanguíneos.
Varios biomarcadores han demostrado valor predictor de eventos cardiovasculares2-4. Sin embargo, se han observado resultados contradictorios en distintos estudios y añaden en general poco valor predictivo a la información clínica5-9. En el momento actual se emplean en clínica con este objetivo prácticamente 2 marcadores: los niveles de lípidos en plasma y, en pacientes con SCA, los niveles de troponina. Recientemente hemos demostrado que los niveles plasmáticos de la proteína quimiotáctica de monocitos 1 (MCP-1), galectina-3 (Gal-3) y pro-péptido natriurético tipo B aminoterminal (NT-ProBNP) predicen el desarrollo de eventos adversos en pacientes con cardiopatía isquémica (CI) estable10. Se trata de un conjunto de biomarcadores relacionados fundamentalmente con la inflamación11,12, la fibrosis, el remodelado miocárdico13 y la insuficiencia cardiaca14-16.
En este trabajo hemos investigado si la información proporcionada por este panel de biomarcadores mejora la capacidad predictiva de la escala de riesgo clínica basada en el estudio LIPID17.
MétodosPacientesSe incluyeron 711 pacientes con enfermedad coronaria crónica procedentes del estudio Biomarkers in Acute Coronary Syndrome & Biomarkers in Acute Myocardial Infarction (BACS & BAMI) realizado en 4 centros hospitalarios de Madrid: Fundación Jiménez Díaz, Hospital de Fuenlabrada, Fundación de Alcorcón y Hospital de Móstoles.
Todos los pacientes habían padecido entre 6 y 12meses antes del inicio del seguimiento al menos un SCA, con o sin elevación de ST (SCACEST y SCASEST, respectivamente). El SCASEST fue definido como dolor torácico de reposo de más de 20min en las 24h anteriores o aparición reciente de angina gradoiii-iv y descenso transitorio de ST o inversión de la onda T evaluado por un cardiólogo experimentado de dichos centros y/o elevación de troponina. El SCACEST fue definido como angina o síntomas agudos compatibles con el diagnóstico de más de 20min de duración con presencia de elevación del segmento ST en 2 derivaciones contiguas en el electrocardiograma y sin respuesta a la nitroglicerina y elevación de troponina.
Los criterios de exclusión fueron: edad mayor de 85años, coexistencia de otras cardiopatías excepto la hipertrofia ventricular izquierda secundaria a HTA, coexistencia de alguna enfermedad o hábito tóxico que limitara la supervivencia, enfermedad coronaria no susceptible de revascularización y sujetos cuyo seguimiento no fuera posible. Con el objetivo de evitar la variabilidad en los resultados debido a una excesiva heterogeneidad en los intervalos entre el evento agudo y la extracción de sangre, se incluyó como motivo de exclusión que el paciente no estuviera estable al sexto día desde el evento principal, ya que la extracción se realizaba entre el 2.° y el 6.° día.
Además de la sangre al alta, se extrajo una segunda muestra durante el seguimiento entre los 6-12meses desde el evento que motivó la inclusión del paciente. Este artículo es un subestudio de los estudios BACS & BAMI que reporta datos de los pacientes que acudían a esta consulta ambulatoria con el diagnóstico de enfermedad coronaria estable, siguiendo su evolución a partir de este momento.
Desde julio de 2006 hasta abril de 2010 se dieron de alta 1.898 pacientes desde los 4 hospitales que participaron en el estudio con un diagnóstico de SCASEST o SCACEST. De ellos, 838 pacientes fueron incluidos en el estudio. Los restantes no fueron seleccionados por alguno de los siguientes motivos: edad superior a 85años (17,3%), presencia de hábitos tóxicos u otras enfermedades que limitaban la supervivencia del paciente (29%), imposibilidad de realizar una revascularización completa (14,5%), coexistencia de otra enfermedad cardiaca (6,8%), imposibilidad de realizar un seguimiento (12%), inestabilidad clínica más allá del sexto día de ingreso (9,1%), negativa a participar en el estudio por parte del paciente (2%) e imposibilidad de los investigadores para incluirlos (9,3%). De los 838 pacientes incluidos, 7 murieron antes de la segunda visita y, de los restantes, 711 tenían una muestra de sangre en ese momento. Esta visita tuvo lugar entre enero de 2007 a febrero de 2011. La última visita de seguimiento fue en mayo de 2012.
Diseño del estudioTras firmar el consentimiento informado, se recogía una historia clínica completa que incluía numerosas variables clínicas entre las que destacaban la edad, el sexo, factores de riesgo coronario, la fracción de eyección del ventrículo izquierdo y el tratamiento habitual. Se añadió también una historia cardiovascular pormenorizada que comprendía el número de vasos enfermos, la gravedad de los mismos y la historia de revascularización, incluyendo el uso de stents en el evento isquémico previo a esa visita. Se recogían muestras de sangre venosa en recipientes con ácido etilendiaminotetraacético (EDTA) basalmente.
El objetivo primario era el desarrollo de eventos isquémicos agudos (SCASEST, SCACEST, infarto cerebral o accidente isquémico transitorio), insuficiencia cardiaca o muerte. El SCASEST y el SCACEST fueron definidos como explicamos con anterioridad. La presencia de una nueva cicatriz miocárdica fue definida como la aparición de nuevas ondas Q patológicas en el electrocardiograma junto con una nueva escara miocárdica concordante identificada por ecocardiograma o resonancia magnética cardiaca. El ictus isquémico fue definido como la rápida aparición de un déficit neurológico persistente atribuible a una lesión focal vascular de más de 24h de duración, o bien con resolución en menos de 24h pero acompañado de lesiones isquémicas en técnicas de imagen. El accidente isquémico transitorio fue definido como cuadro compatible con un ictus cuyos síntomas se resolvían antes de 24h desde su comienzo sin evidencia de lesiones isquémicas nuevas en las técnicas de imagen. Los eventos fueron adjudicados por al menos 2 investigadores del estudio, además de un especialista en Neurología para juzgar los eventos cerebrovasculares.
Estudios analíticos y biomarcadores empleadosLas muestras de sangre venosa fueron centrifugadas a 2.500g durante 10min. El plasma fue almacenado a –80°C. Todas las determinaciones fueron realizadas en los laboratorios de Patología Vascular y Bioquímica de la Fundación Jiménez Díaz, en Madrid. Los investigadores que realizaron los estudios en los laboratorios desconocían los datos clínicos de los participantes.
Se midieron por duplicado los niveles plasmáticos de MCP-1 y Gal-3 con kits de ELISA disponibles comercialmente (DCP00, R&D Systems; BMS279/2; Bender MedSystems, respectivamente) siguiendo las instrucciones de la casa comercial. Los coeficientes de variación intra e interensayo fueron del 4,6 y del 5,9% para MCP-1 y del 6,2 y del 8,3% para Gal-3.
El NT-proBNP se determinó por un test de inmunoanálisis (VITROS, Orthoclinical Diagnostics, EE.UU.). Los análisis de lípidos, glucosa y creatinina fueron realizados por los métodos estándar (ADVIA 2400 Chemisty System, Siemens, Alemania).
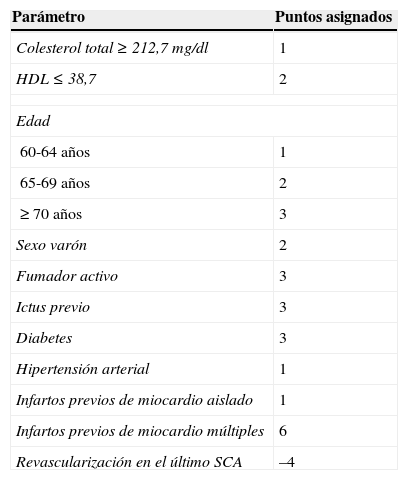
Escala clínica de riesgo y score combinadoElegimos la escala de riesgo clínico derivada del estudio LIPID para pacientes con enfermedad coronaria estable dado que incluye una completa relación de variables. Se tiene en cuenta el valor del colesterol total, del colesterol HDL, la edad, el sexo, el hábito tabáquico, antecedentes de ictus, diabetes (DM), hipertensión arterial (HTA), SCA previo o haber sido revascularizado. La tabla 1 muestra el sistema de puntuación en dicha escala. Para hallar la puntuación total, se van sumando los puntos proporcionados por cada variable.
Escala de riesgo clínico en pacientes con enfermedad coronaria crónica derivada del estudio LIPID
| Parámetro | Puntos asignados |
|---|---|
| Colesterol total ≥ 212,7 mg/dl | 1 |
| HDL ≤ 38,7 | 2 |
| Edad | |
| 60-64 años | 1 |
| 65-69 años | 2 |
| ≥ 70 años | 3 |
| Sexo varón | 2 |
| Fumador activo | 3 |
| Ictus previo | 3 |
| Diabetes | 3 |
| Hipertensión arterial | 1 |
| Infartos previos de miocardio aislado | 1 |
| Infartos previos de miocardio múltiples | 6 |
| Revascularización en el último SCA | –4 |
El rango de la escala va de un mínimo de –4 a un máximo de +24 puntos.
HDL: lipoproteína de alta densidad.
Los datos cuantitativos que siguieron una distribución normal se presentan como media±desviación estándar y se compararon mediante el test de la t de Student. Los que no siguieron una distribución normal se muestran como mediana (rango intercuartil) y se compararon con la prueba de Mann-Whitney. Las variables cualitativas se muestran como porcentajes y se compararon mediante Chi cuadrado o el test de Fisher, según correspondiera.
Se desarrollaron curvas receiver operating characteristic (ROC) para evaluar la capacidad predictiva de la escala de riesgo LIPID y del score combinado con los biomarcadores. Tras analizar la curva resultante se escogió un punto de corte de 21,5 en el score que proporcionaba una sensibilidad del 74% y una especificidad del 61%. Se realizaron las curvas de Kaplan-Meier utilizando este punto de corte y la prueba de log-rank para comparar el tiempo de supervivencia libre de eventos de acuerdo al score combinado. Los análisis estadísticos se realizaron mediante el programa informático SPSS 19.0 (SPSS Inc., Nueva York). Los tests estadísticos se consideraron significativos cuando el valor de p era <0,05 (2 colas).
ResultadosLa media de seguimiento fue de 2,2±0,99años. Se perdieron 5 pacientes durante el seguimiento, quedando 706 casos para el análisis. El tiempo desde el último evento coronario agudo hasta la extracción de plasma y el inicio de seguimiento fue de 7,5±3,0meses. Durante este evento, el 97,9% de los pacientes habían sido sometidos a angiografía coronaria.
Efecto de MCP-1, NT-proBNP y galectina-3 en el valor predictivo de la escala de riesgo clínicaLa escala clínica de riesgo del estudio LIPID obtuvo un valor predictivo significativo en las curvas ROC (área bajo la curva 0,642 [0,579-0,705]; p<0,0019) (fig. 1). Transformamos los niveles de MCP-1, Gal-3 y NT-proBNP en un valor del 1 al 10 según el decil de su concentración. A continuación desarrollamos una escala combinada sumando los deciles de los 3 marcadores a la puntuación de la escala clínica. Usando esta escala, el área bajo la curva aumentó a 0,744 (0,684-0,805; p<0,001). La comparación de las curvas ROC de la escala del estudio LIPID frente a la escala combinada (clínica más los biomarcadores) mostraba una diferencia significativa (p=0,022). Una puntuación de la escala combinada mayor de 21,5 se correspondía con una sensibilidad del 74% y una especificidad del 61% para el desarrollo del objetivo primario. La curva de Kaplan-Meier mostró que los pacientes que tenían una puntuación combinada <21,5 presentaban mejor pronóstico que los que tenían valores superiores (p<0,001; test de log-rank) (fig. 2).
Los pacientes que sufren un evento isquémico agudo pueden morir antes de recibir atención médica. Por lo tanto, identificar a las personas con riesgo de presentar eventos cardiovasculares en el futuro es muy importante para intensificar sobre ellas las medidas preventivas.
Hasta la fecha se ha examinado el papel pronóstico de múltiples biomarcadores plasmáticos. Junto a los niveles lipídicos, que pueden ser considerados biomarcadores, la creatincinasa tipo MB (CPK-MB) y, más tarde, las troponinas han mostrado ser efectivos como predictores pronósticos en el SCA, además de ser útiles en el diagnóstico18–20.
Los péptidos natriuréticos (BNP o NT-proBNP) se usan en el diagnóstico de la insuficiencia cardiaca (IC), e incluso han evidenciado valor pronóstico en esta patología14–16. También se ha asociado el nivel sérico tanto de BNP como de NT-proBNP con la incidencia de muerte y eventos cardiovasculares en sujetos asintomáticos sin IC. Kistorp et al.21 seleccionaron 537 personas sin antecedentes de enfermedad renal o cardiaca. Aquellos cuyos niveles de NT-proBNP se hallaban por encima del percentil 80 tuvieron un riesgo mayor de eventos cardiovasculares y muerte. E incluso en pacientes con SCA, tanto el BNP como el NT-proBNP han mostrado tener valor pronóstico22–23. Sin embargo, en la cardiopatía isquémica estable la literatura disponible sobre este biomarcador es menor. En un estudio de 1.085 pacientes con enfermedad coronaria crónica, sin IC y sin enfermedad inflamatoria crónica severa y con 2,5años de seguimiento, se comprobó que los pacientes con niveles basales de BNP en el cuartil superior (>100,3pg/ml) tenían un riesgo 6 veces superior de infarto de miocardio no fatal o muerte cardiovascular que los pacientes de BNP en el cuartil inferior (<11,8pg/ml)24.
MCP-1 es una molécula clave en la entrada de monocitos en la pared vascular, y su expresión es reducida por el tratamiento con estatinas o inhibidores de la enzima convertidora de angiotensina11,12,25,26. Estudios previos han mostrado que los niveles plasmáticos de esta molécula tienen valor predictor de eventos cardiovasculares en pacientes con enfermedad coronaria27,28. Por otra parte, Gal-3 está involucrada en fenómenos de fibrosis y cáncer13,29. Nuestro grupo ha publicado con anterioridad que, en pacientes con enfermedad coronaria estable, MCP-1 tiene valor pronóstico como predictor de eventos isquémicos agudos, mientras que NT-proBNP y Gal-3 predicen el desarrollo de IC y muerte10.
Aunque se han diseñado diversas escalas de riesgo clínico para la prevención primaria y el SCA, no hay ninguna aceptada en la práctica clínica para la enfermedad coronaria crónica30. Esto es una limitación adicional en el manejo del paciente coronario crónico, y es muy relevante para nuestra práctica clínica. Diariamente atendemos más pacientes con enfermedad coronaria crónica que casos de SCA, y estos pacientes son susceptibles de desarrollar un evento agudo en el futuro. Por tanto, debemos dirigir una parte importante de nuestros esfuerzos a tratar de identificar los casos de potencial alto riesgo.
Para la realización de este estudio elegimos la escala clínica que propone el estudio LIPID por considerarla la más completa, ya que tiene en cuenta varios factores clínicos y analíticos17.
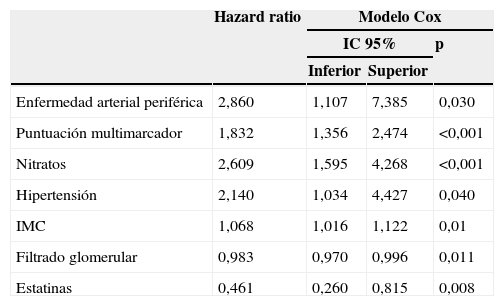
En nuestro trabajo, esta escala predijo significativamente la evolución de los pacientes, aunque la sensibilidad y la especificidad fueron modestas. Posiblemente esto está relacionado en parte con el hecho de que esta escala se generó en una población diferente a la española. Por otra parte, los pacientes fueron incluidos en este estudio entre 1990 y 1992, y los tratamientos usados han variado desde entonces. En todo caso, no existe ninguna escala clínica unánimemente aceptada para su uso en enfermedad coronaria estable. En el presente estudio hemos utilizado la escala LIPID como instrumento de medida para determinar si la adición de un panel de biomarcadores mejoraba nuestra capacidad pronóstica en una población con enfermedad coronaria estable. Añadiendo los deciles de NT-proBNP, Gal-3 y MCP-1, mejoraba significativamente la capacidad de esta escala para predecir eventos adversos. Así parece evidente que el papel del panel de biomarcadores que presentamos puede ser claramente beneficioso a la hora de estratificar el riesgo de los pacientes con enfermedad coronaria estable. Se precisan nuevos estudios con estos biomarcadores para confirmar que mejoran nuestra capacidad pronóstica en esta población. En caso de confirmarse, sería de interés analizar en el futuro si el empleo de tratamientos especialmente intensivos en pacientes con alteraciones en estos biomarcadores implica un mejor pronóstico (tabla 2).
Modelo de riesgo proporcionado de Cox para la incidencia del objetivo primario
| Hazard ratio | Modelo Cox | |||
|---|---|---|---|---|
| IC 95% | p | |||
| Inferior | Superior | |||
| Enfermedad arterial periférica | 2,860 | 1,107 | 7,385 | 0,030 |
| Puntuación multimarcador | 1,832 | 1,356 | 2,474 | <0,001 |
| Nitratos | 2,609 | 1,595 | 4,268 | <0,001 |
| Hipertensión | 2,140 | 1,034 | 4,427 | 0,040 |
| IMC | 1,068 | 1,016 | 1,122 | 0,01 |
| Filtrado glomerular | 0,983 | 0,970 | 0,996 | 0,011 |
| Estatinas | 0,461 | 0,260 | 0,815 | 0,008 |
Rango de la puntuación multimarcador que va de 0 a 3 y se refiere al número de biomarcadores que presentan un valor por encima de la mediana (MCP-1, galectina-3 y NT-proBNP). Modelo de Cox: se estimó el riesgo incluyendo factores como la edad, el sexo, DM, tabaquismo, HTA, IMC, niveles de lípidos, antecedentes de enfermedad arterial periférica, enfermedad cerebrovascular, fibrilación auricular, fracción de eyección <40%, tasa de filtración glomerular, PCR de alta sensibilidad, tratamiento con aspirina, clopidogrel, estatinas, acenocumarol, IECA, ARAII, betabloqueantes, nitroglicerina y el número de vasos enfermos y la existencia de una revascularización en el último evento, y por último los biomarcadores estudiados.
IC: intervalo de confianza; IMC: índice de masa corporal.
Excluimos del estudio los pacientes que no estaban estables al sexto día del evento principal, lo cual puede introducir un cierto sesgo, pues estos pacientes probablemente tienen peor pronóstico. Sin embargo, por este motivo solo se excluyó al 9% de la población, por lo que el posible impacto de este factor sobre el estudio es limitado.
FinanciaciónSociedad Española de Arteriosclerosis, FIS (PI: 05/451, 05/1497, 05/2475, 05/1043, 09/01405, 10/0234, Programa Estabilización a LBC), Sociedad Española de Cardiología, Fundación Española del Corazón, Ministerio de Ciencia e Innovación (SAF 2010/21852), Comunidad de Madrid (sGEN/0247/2006), Becas de Biobancos del Instituto CarlosIII FEDER, RD09/0076/00101 (Biobanco FJD).
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia
Conflicto de interesesNo hay conflictos de intereses.
Las siguientes personas participaron en este estudio (extracción de sangre, separación de plasma y organización del biobanco):
- •
IIS-Fundación Jiménez Díaz: Rosario de Nicolás-Miguel, Pilar Jiménez-Caballero, Marta Hernán-Bru, Esmeralda Serrano-Blázquez, Ana Encinas-Pastor, Arantxa Garciandia, Consuelo Ceballos, Belén Arribas-Moreno, Belén Picatoste y Elisa Ramírez-Bustillo.
- •
Hospital de Fuenlabrada: María Pacheco, Rosa Jiménez-Hernández, José M. Serrano-Antolín, Alejandro Curcio, Pedro Talavera y Catherine Graupner.
- •
Hospital de Móstoles: José M. Hernández-Riesco, María del Carmen García-García, Mercedes García-Rodrigo, Jose Luis Alonso-Guillén y Patricia Cuenca-Gómez.
- •
Hospital Fundación Alcorcón: Noelia Aragón-Díaz.