INTRODUCCIÓN
El cáncer asociado al embarazo es toda neoplasia maligna que se diagnostica durante la gestación o hasta un año después del parto. Algunos autores, no obstante, restringen la duración hasta 6 meses de puerperio (según la Organización Mundial de la Salud). La incidencia de cáncer se sitúa en torno al 0,07%1 y oscila levemente en distintas series, lo que supone el 0,8% de las mujeres con cáncer. El tipo más frecuente es el de cérvix, seguido del de mama (el más frecuente en pacientes mayores de 30 años), tiroides, melanoma, ovario, Hodgkin y leucemia2.
El diagnóstico de cáncer durante el embarazo plantea una situación compleja, cargada de sentimientos contradictorios. Si bien la gestación es un proceso de crecimiento ordenado con una promesa de vida, la neoplasia supone una amenaza a menudo real, incluso de muerte. El componente psicológico, por lo común importante ante la aceptación de un cáncer, se ve así complicado de un modo destacado.
Por tanto hay una serie de cuestiones particulares de la enfermedad sobre las que debemos aconsejar a la paciente:
¿Qué esquema diagnóstico y terapéutico debemos seguir?
¿El embarazo empeora el pronóstico materno ante un cáncer?
¿Se debe aconsejar interrumpir la gestación?
¿Cómo afecta el tumor al feto?
Trataremos de responder a cada una de estas preguntas, así como a todas las dudas que pudieran surgir entorno a éstas.
ESQUEMA TERAPÉUTICO
Nuestro objetivo último es la curación completa de la madre sin que afecte al feto; sin embargo, como este ideal no siempre se puede alcanzar, debemos optar en muchas ocasiones por el mal menor.
La filosofía básica es que debemos tratar el cáncer como si no existiera la gestación. Así, nuestro objetivo, igual que en cualquier proceso neoplásico, tras tener el diagnóstico de certeza sería:
1. Erradicar el cáncer
2. Paliarlo si no es posible curarlo
Este punto está matizado fundamentalmente por el momento de la gestación en que nos encontremos; obviamente no va a haber ningún dilema en el puerperio, y se aconseja terminar el embarazo si hay madurez fetal, antes de comenzar el tratamiento.
En los casos diagnosticados durante el primer trimestre y principios del segundo, debe primar el estado materno y no debe escatimarse tratamientos, aunque éstos puedan conllevar incluso la muerte fetal. No hay en ello ningún tipo de objeción moral por parte del mundo científico, incluso de la Iglesia.
La madre debe ser aconsejada cuidadosamente antes de la práctica de un aborto provocado previo al tratamiento, y debe valorar cada tipo de proceso en particular, sus tratamientos y sus posibles consecuencias. La evacuación uterina no siempre es garantía de una mejor evolución del cáncer.
Por último, hay un grupo de casos en los que se puede aconsejar demorar el tratamiento unas semanas, sin que ello conlleve un efecto nocivo para la evolución del cáncer, pero que permita mejorar la madurez fetal. Es conveniente resaltar la importancia de valorar el tipo de neoplasia, el estadio, el tratamiento que hay que aplicar y el estado de la gestación en cada caso para orientar a la paciente, y ofrecerle información detallada y clara para que en último término sea ella quien pueda adoptar la decisión que considere mejor, de acuerdo con sus creencias y valores.
PROCEDIMIENTO DIAGNÓSTICO
Una mención especial merece el procedimiento diagnóstico, donde nos podemos ver limitados ante determinadas estudios de extensión o la obtención de biopsias. No hay contraindicación a partir del segundo trimestre para la realización de una tomografía computarizada (TC) o una resonancia magnética (RM), pero puede incluso realizarse durante el primer trimestre ante la sospecha fundada o el diagnóstico de una neoplasia.
Los aspectos relativos al efecto deletéreo de la radiación ionizante se describen con mayor extensión en la parte dedicada al tratamiento radioterapéutico, pero baste adelantar que la dosis perniciosa comienza alrededor de 1 Gray (100 rads), cuando la energía absorbida en una radiografía simple de abdomen es menor de 1 cGy (1 rad).
EFECTO DEL EMBARAZO EN LA NEOPLASIA
Aunque aún hay opiniones divididas al respecto, cada vez la idea de que el embarazo no altera la historia natural de la enfermedad tiene más relevancia. El mecanismo mediante el cual el organismo materno permite el crecimiento de un cuerpo extraño puede inducir a pensar en cierta permisividad del sistema inmunitario, y por tanto mayor facilidad para el desarrollo tumoral. No obstante, parece que mientras sí tolera el crecimiento ordenado de la gestación, no parece existir esta facilidad con un crecimiento desordenado como la neoplasia.
Cuando analizamos la incidencia de neoplasias en gestantes y no gestantes, no encontramos diferencias para mujeres de la misma edad; por regla general se trata de mujeres jóvenes con su sistema inmunitario en plenitud, y por tanto con mayor capacidad de defensa. La aparición de la neoplasia estaría relacionada muy de cerca con el tiempo de exposición a los agentes carcinogénos. Se puede observar como con el retraso de la gestación ha aumentado la incidencia de los cánceres en el embarazo.
Por otro lado, al analizar las tasas de supervivencia a los 5 años, no hay diferencias significativas entre gestantes y no gestantes en el linfoma de Hodgkin y parece incluso disminuir en otros tumores como el cáncer de mama.
EFECTO DEL TUMOR EN EL EMBARAZO
No parece que el tumor tenga un efecto importante en el feto o la evolución del embarazo; la tasa de abortos y partos prematuros resulta similar en ambos casos, y sólo en algunos casos concretos, como leucemia, cáncer de cérvix, etc., aumentan las complicaciones propias como infecciones, hemorragias o dificultad para el parto vaginal.
Por otro lado, observamos que es rara la posibilidad de metástasis en la placenta; Querleu3 estableció ya en 1978 una diferencia entre las metástasis placentarias verdaderas con afectación de la vellosidad corial y alteración de la estructura arquitectural, muy poco probables, y la presencia de células neoplásicas a modo de émbolos en el espacio intervelloso, sin afectar a la vellosidad, algo más frecuentes.
La afectación fetal se produce en contadas ocasiones, y se produce casi únicamente en casos de melanomas.
BASES DEL TRATAMIENTO
El tratamiento se sustenta sobre cuatro pilares, los dos primeros se consideran tratamientos locoregionales, mientras que los segundos, tratamientos sistémicos.
Cirugía
Radioterapia
Quimioterapia
Agentes biológicos
Radioterapia. Es una forma física de tratamiento en la que se liberan ondas electromagnéticas a partir de la eyección de un electrón por parte de rayos X o gamma, y por tanto produce un efecto ionizante. Para administrar la energía hay tres modos principales: a) telemetría, con aplicación a distancia; b) braquiterapia, en el que se introduce cargas en vecindad de los tejidos afectados, y c) isótopos radiactivos, que se fijan a un destino concreto y liberan allí su carga radiante, como el yodo-131.
La radiación produce un efecto acumulado difícil de cuantificar, por lo que para describir un tratamiento debemos hablar de dosis total, dosis fraccionada y número de sesiones. Así, por ejemplo, el tratamiento tipo consistiría en una dosis total de aproximadamente 4.500 Gy en fracciones 150-200 cGy en sesiones de 5 días/semana.
La radioterapia está contraindicada durante el primer trimestre y se aplica directamente sobre la pelvis, aunque puede administrarse durante el segundo y tercer trimestres en el resto del organismo. Sus efectos deletéreos dependerán de la fase de desarrollo en que se encuentre el embarazo. Así, durante los días 18 al 38 de gestación se produce la organogénesis con máxima sensibilidad y posibilidad de anencefalia o microcefalia, alteraciones oculares, espina bífida, retraso mental, etc. También en etapas posteriores puede producir alteraciones del desarrollo fetal, retraso mental, alteraciones esqueléticas, retardo de crecimiento intrauterino, etc.
Quimioterapia. La quimioterapia debe evitarse durante el primer trimestre del embarazo, y debe evitarse los fármacos que alteran el metabolismo de los folatos, como el metrotexato y la aminoteptirina.
Se recomienda el tratamiento con un solo tipo de fármaco, como la vinblastina (agente antimitótico) o la doxorrubicina (antibiótico antineoplásico). Aunque recientemente los regímenes con cisplatino han demostrado ser útiles e inocuos en diversas publicaciones, así como algunas combinaciones con paclitaxel, han evidenciado ausencia de lesiones en la RM.
CÁNCER DE CÉRVIX Y EMBARAZO
La neoplasia maligna más frecuente en el embarazo es el cáncer de cérvix4. Se estima que la incidencia del cáncer de cérvix es de 1/2.500 embarazos, mientras que la incidencia de carcinoma in situ es muy superior, aproximadamente de 1/750 embarazos. Estos datos pueden experimentar un aumento debido a los programas de cribado que se practican en todas las mujeres de una forma cada vez más protocolizada5.
El tipo histológico más frecuente es el epidermoide, al igual que en la no gestante, por lo que al ser un tumor no hormonodependiente, no está influido por el hiperestrogenismo del embarazo6. No obstante, no se encuentran diferencias en la supervivencia de las mujeres respecto al momento del diagnóstico (1.er, 2.o o 3.er trimestre o posparto), y sí las hay dependiendo del estadio7.
Diagnóstico
Aunque ocasionalmente se presente como una hemorragia anormal, generalmente cursa de manera asintomática, por lo que, al igual que sucede en otros cánceres asociados al embarazo, el diagnóstico suele ser ocasional y tardío. El diagnóstico, al igual que en la paciente no gestante, se apoya en tres pilares fundamentales: a) citología y detección del virus del papiloma human; b) colposcopia, y c) biopsia.
Para el diagnóstico será fundamental el papel del cribado mediante citología cervicovaginal. Esto revela la importancia de la práctica sistemática de una citología a todas las gestantes en su primera visita de control. Siempre que la citología sea patológica o atípica, deberá seguirse de la búsqueda de lesiones macroscópicas mediante la observación directa o colposcopia, si bien hemos de tener presentes que hasta un 10% de las citologías pueden dar un resultado alterado por efecto del embarazo.
La colposcopia estará favorecida por la eversión fisiológica en el embarazo de la unión escamocolumnar del cérvix. La mayor vascularización cervical en la gestante no debe suponer un problema a la hora de practicar una biopsia, que se realizará siempre que se observe alguna imagen atípica y lo más pequeña posible5,8,9. Ante una lesión que no presente una biopsia positiva, procederemos a un control colposcópico trimestral, siempre y cuando no varíe.
Sin embargo, a la hora de practicar una conización nos encontramos con posibles complicaciones que pueden poner en peligro el embarazo, como son riesgo de aborto, hemorragia o posible infección.
Como ante CIN III (cervical intraepithelial neoplasia grade III) la conducta puede ser expectante, y si no hay cambios citológicos en los controles sucesivos que se realizarán cada 3 meses, el tratamiento se pospondrá hasta después del parto5,10. El CIN III no supone un impedimento para el parto por vía vaginal.
En los casos de lesiones microinvasivas, se puede seguir la misma pauta que en caso de un CIN III tras haber realizado una microrresección en los casos posibles6, o incluso proceder a una conización una vez aceptados sus riesgos, para reevaluar el caso tras finalizar el embarazo (tabla I).
Tratamiento
El tratamiento del cáncer cervical en la mujer gestante en principio debe plantearse como en la no gestante, de acuerdo con el estadio de la enfermedad (tabla II).
Manejo en la gestación
Deberá evitarse el parto vaginal (salvo E IA1) dada la posibilidad de hemorragias en tumores extensos o diseminación durante la dilatación.
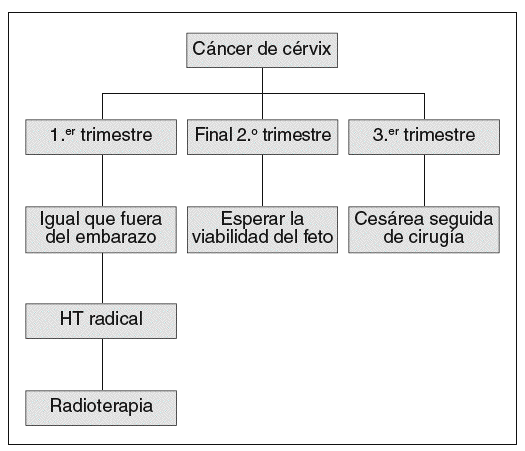
Si el diagnóstico se produce durante el tercer trimestre, se aconseja esperar hasta la madurez fetal (fig. 1).
Fig. 1. Resumen del tratamiento aconsejado para el cáncer de cérvix en una gestante. HT: histesectomía.
Tanto en los tratamientos más radicales como en los más conservadores, la paciente es la que debe decidir en última instancia cuál es el que quiere recibir una vez se le haya planteado toda la información disponible en nuestro medio. Es una decisión problemática ya que implica en muchas ocasiones el dilema de tener que elegir entre seguir adelante con la gestación o someterse a un tratamiento que asegure o mejore el pronóstico de la paciente, decisión que debe tomarse en poco tiempo y que crea un conflicto que suele afectar a la paciente, su entorno familiar y también al equipo médico. Una vez decidido su tratamiento individual debemos acercarnos lo más posible al tratamiento que hubiera recibido esa misma mujer en caso de no encontrarse en estado de gestación.
Así, ante el diagnóstico de un cáncer invasivo de cérvix en estadios iniciales y a una edad gestacional temprana, el tratamiento recomendado sería la cirugía radical con feto in situ en los estadios IB-IIA11. Otra alternativa para estadios iniciales es la radioterapia5. Se discute si puede ser beneficiosa la evacuación previa del feto, dado que la radioterapia a menudo provoca aborto al principio de la gestación y, por otro lado, hay autores que prefieren la evacuación del útero antes de administrarla. En los estadios IIB-IV se indicará radioterapia.
El mayor dilema a la hora de plantear un tratamiento es cuando éste se realiza en el segundo trimestre, principalmente cerca del período de viabilidad fetal, por los problemas éticos que plantea la instauración de un tratamiento potencialmente curativo y que implique cirugía radical.
Para edades gestacionales mayores de 20 semanas podría plantearse la posibilidad de diferir el tratamiento, si nos encontramos en estadios iniciales IA y IBI, pero siempre que la paciente sea consciente del riesgo que podría implicar este retraso en su salud12.
En el resto de estadios se valora seguir el mismo tratamiento que en la no gestante, salvo que la paciente asuma el riesgo de esperar a ser tratada tras alcanzar la madurez fetal, en cuyo caso se puede intentar diferir el tratamiento.
Durante el tercer trimestre hay acuerdo en que se debe demorar el tratamiento hasta después del parto, que será en cuanto se haya asegurado la madurez fetal, incluso en los estadios más avanzados en los que el pronóstico materno no mejora y, sin embargo, podemos obtener un recién nacido maduro8. Se recomienda practicar una cesárea con una histerectomía radical posterior.
A pesar de las recomendaciones establecidas, el tratamiento del cáncer de cérvix en una gestante debe plantearse de forma individual y atendiendo a aspectos propios del tumor, como su naturaleza y extensión, del embarazo, como la edad gestacional, así como de las características y los deseos de la paciente.
CÁNCER DE OVARIO
Una tumoración ovárica es toda formación dependiente del ovario que cause aumento de su volumen. Aunque vamos a encontrar una gran diferencia entre lo que pueda ser una neoplasia maligna y un simple cuerpo lúteo, su hallazgo va a provocar una situación compleja y de incertidumbre, tanto para el equipo médico como para la paciente, hasta conseguir un diagnóstico fiable6.
Por tanto, tiene interés agruparlos, sobre todo desde el punto de vista diagnóstico, para seguir luego una correcta línea de actuación, separar los procesos graves de los que no lo son, y finalmente reconocer los casos de cáncer para un tratamiento correcto.
Epidemiología
La incidencia de tumores ováricos en el embarazo se sitúa en torno a 1/1.000 nacimientos13. En su gran mayoría se trata de tumoraciones o masas anexiales funcionales; así en gestantes, los tumores malignos suponen sólo un 2-5% de las tumoraciones anexiales diagnosticadas, cifra que se aleja bastante del porcentaje de malignidad en no gestantes, que es aproximadamente del 18-20%5.
El cáncer de ovario supone alrededor del 5-6% de los tumores malignos en las mujeres y es la cuarta causa de muerte por cáncer en la mujer (después del cáncer de mama, intestino grueso y pulmón). Dentro de la ginecología oncológica ocupa el cuarto puesto en frecuencia (tras mama, endometrio y cérvix) y, no obstante, sigue siendo el que más casos de muerte provoca de entre los cánceres ginecológicos. En gran medida, esto se debe a la gran dificultad de un diagnóstico temprano, ya que el 65% de las pacientes se diagnostican en estadios avanzados, III y IV (según datos de la Sociedad Española de Ginecología y Obstetricia). Aparece aproximadamente en uno de cada 18.000 embarazos5, y en líneas generales presenta un comportamiento similar al de las mujeres no embarazadas.
Clasificación
Podemos diferenciar los tumores ováricos entre:
Funcionales. Son con diferencia los más frecuentes del embarazo, principalmente los quistes del cuerpo lúteo.
Neoplásicos. Los diferenciaremos entre benignos, malignos o borderline, y cada una de las categorías puede ser atendiendo a su estirpe celular, de células germinales, epiteliales o de los cordones sexuales. Añadir los tumores metastáticos.
De las tumoraciones no funcionales en gestantes, el tipo histológico más frecuente son los tumores epiteliales (cistadenomas mucinoso y seroso), que suponen más del 50% de los casos. Siguen en frecuencia los tumores de células germinales (teratomas quísticos) hasta en un 30% y de los cordones sexuales, y por último, en un 2% aproximadamente son de origen metastático14,15.
Clínica
En general, el cáncer ovárico suele evolucionar de forma asintomática; sin embargo, algunas mujeres presentan molestias abdominales inespecíficas, como hinchazón o sensación de distensión abdominal; incluso empiezan como abdomen agudo ocasionado por torsión tumoral o alguna otra complicación. Los signos y síntomas son similares a los de la no gestante, de modo que la mayoría de tumores ováricos cursa como asintomático y el dolor o distensión abdominal son síntomas fácilmente atribuibles al embarazo.
Diagnóstico
Las pruebas básicas que podemos utilizar para el cribado de cáncer de ovario son la exploración pélvica, la determinación de marcadores tumorales (CA-125) y la ecografía pélvica. Posteriormente, recurriremos a otras técnicas de imagen como TC, RM, etc., para completar el estudio. En general, son tres las pruebas de cribado que se pueden utilizar en el cáncer de ovario:
1. Tacto pélvico bimanual. Debe llevarse a cabo en la revisión de toda paciente no gestante, y al menos en la primera revisión de la embarazada. Ocasionalmente podemos encontrar una masa anexial en la exploración de la primera visita obstétrica sólo mediante palpación5.
2. Determinación de marcadotes tumorales. El CA-125 es el más significativo. Se encuentra elevado generalmente en neoplasias ováricas, sobre todo en estadios avanzados, aunque resulta bastante inespecífico, ya que se encuentra también aumentado en otros procesos benignos como la endometriosis. Otro marcador también utilizado, pero más específico de tumores mucinosos, es el CEA. En la gestante van a ser de poca utilidad, ya que se encuentran alterados de forma fisiológica8 y así fuera del embarazo se aceptan como normales los valores de CA-125 menores de 35 mU/ml, pero en la gestación el rango de normalidad varía desde 2,2 a 166,3, y se consideran como normales valores mucho más altos, principalmente en el primer trimestre16,17.
3. Ecografía transvaginal. Supone el pilar clave en el diagnóstico temprano de la neoplasia ovárica y, desde que forma parte de la exploración sistemática de la mayoría de gestantes, las posibilidades de diagnosticar un tumor ovárico en gestaciones incipientes e incluso más tarde han aumentado notablemente8. Mediante la ecografía podremos, además de diagnosticar una tumoración anexial, sospechar malignidad si la paciente presenta determinados signos, como tabiques, papilas o excrecencias, cápsula engrosada, ecogenicidad mixta, o se asocia a ascitis o a un Doppler alterado.
Manejo
El enfoque dependerá de la edad gestacional, de modo que en gestaciones iniciales éste se basará en la exploración pélvica y ecográfica inicial de la gestante13, que puede ser un momento idóneo para un posible diagnóstico, ya que los anexos permiten ser mejor valorados. Ante una tumoración dudosa, estaría plenamente justificado el uso de cualquier método de imagen que pudiera aclararnos el diagnóstico (TC o RM)8, aunque la RM es el método de elección preferiblemente a partir del segundo trimestre, cuando ya no se describen riesgos fetales.
El hallazgo durante el primer trimestre de una tumoración móvil, unilateral, encapsulada y de consistencia uniforme y sin signos de malignidad que mida hasta 8-10 cm18, podría mantenerse en observación con control ecográfico hasta el segundo trimestre. Así, si sospechamos de la existencia de un quiste simple o incluso ante la duda de un teratoma quístico, se recomendaría, por lo tanto, actitud expectante5. El tamaño tumoral no parece pues discriminante de malignidad hasta alcanzar los 8-10 cm, aunque otros autores disminuyen esta medida a 6 cm. Si esta masa persiste más allá de la semana 16, se aconseja la exploración quirúrgica8.
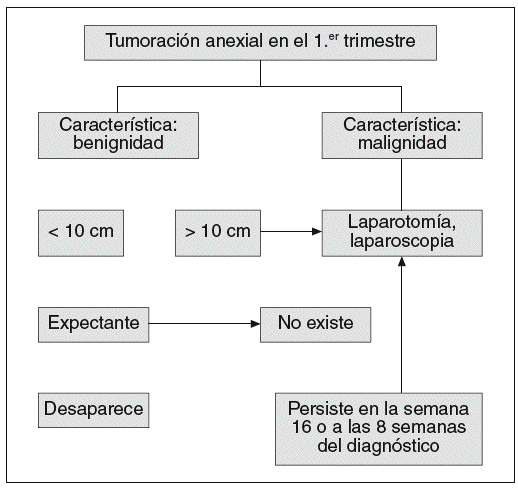
Sin embargo, ante la sospecha ecográfica de malignidad, o con algún signo de complicación (torsión, rotura, hemorragia), se indica la práctica de laparotomía o laparoscopia (según la experiencia del cirujano), independientemente del trimestre en que nos encontremos. En cualquier caso, en toda masa mayor de 8-10 cm debe practicarse biopsia y exéresis5,13,18 (fig. 2).
Fig. 2. Esquema de actuación ante una masa ovárica diagnosticada en el primer trimestre.
Estadios
La estadificación del cáncer de ovario se basa en la exploración clínica y quirúrgica, y se determinará definitivamente a partir de los hallazgos anatomopatológicos (tabla III).
Tratamiento
En la actualidad el tratamiento estándar del cáncer de ovario se apoya en dos pilares fundamentales: a) cirugía, y b) quimioterapia; la radioterapia y la hormonoterapia quedarían en un segundo nivel.
El enfoque dependerá de las características individuales de cada paciente, como la edad, el deseo genésico, así como las características propias del tumor. En una paciente gestante se debe dar un consejo individualizado, y además valorar las características del tumor, la viabilidad del feto y la edad gestacional, así como las características de la madre y asumir la decisión última de la paciente, ya que tanto ella como el personal médico tendrán que hacer frente a conflictos de tipo ético e incluso médico una vez disponga de toda la información que tenemos en nuestras manos, ya que hoy día ésta sigue siendo limitada.
Bases del tratamiento para el cáncer de ovario
Cirugía. El correcto tratamiento quirúrgico requiere la realización de: histerectomía total, anexectomía bilateral, apendicectomía, omentectomía y linfadenectomía pélvica y paraaórtica. Es necesario añadir un estudio anatomopatológico de muestras tomadas de cavidad peritoneal y ganglios retroperitoneales.
En estadios avanzados donde no se puede realizar una cirugía radical, la actitud recomendada es la cirugía citorreductora previa a la administración de quimioterapia.
Quimioterapia. Sólo los tumores en estadio IA G1-2 y IB G1-2, diploides, no precisan tratamiento adyuvante. Los tumores en estadio IA-B G3 y en estadio IC o aneuploides sí son subsidiarios del tratamiento adyuvante con quimioterapia (3 ciclos según el Grupo Ginecológico Oncológico Español).
Los tumores en estadios IIB y IIC deben ser tratados como los estadios III y IV, con esquemas de poliquimioterapia con derivados de platino y taxanos. En cuanto a la utilidad de la radioterapia ésta es muy limitada.
Tratamiento en la gestante
Ante la sospecha de una tumoración maligna debe actuarse en principio como si se tratara de una paciente no gestante: laparotomía con lavado peritoneal más exploración pélvica junto con biopsia intraoperatoria de la tumoración.
Sólo en caso de ser una tumoración en estadio IA y contando con el consentimiento de la paciente, debería realizarse cirugía conservadora, es decir una salpingoovariectomía unilateral, previa biopsia del ovario contralateral, biopsia de peritoneo, así como de los ganglios pélvicos y paraaórticos seguido en ambos casos de quimioterapia8.
La actitud clásica frente a un cáncer ovárico implicaba la necesidad de cirugía radical, asociada a quimioterapia (de 3 a 6 ciclos) y ocasionalmente radioterapia.
La cirugía radical se plantea independientemente del embarazo si el diagnóstico se realiza durante las primeras 24 semanas de gestación o previamente a la viabilidad fetal (salvo el estadio 1A1); de modo que sólo se planteaba la posibilidad de posponer la cirugía hasta alcanzar la madurez fetal si el diagnóstico se realizaba en los últimos 3 meses de embarazo.
Estas afirmaciones son ahora cuestionadas, ya que son varios los equipos de trabajo que defienden un tratamiento quirúrgico conservador en que se extirpe la tumoración y se respete el útero y anexo contralateral seguido de quimioterapia, para así lograr preservar el embarazo19. Tras la finalización de la gestación se completaría la cirugía.
Los resultados no han sido categóricos en ninguno de los dos sentidos, a falta de mayor experiencia, aunque el aborto o finalización temprana del embarazo no parece aumentar la supervivencia materna20; por tanto, la quimioterapia (generalmente basada en cisplatino) con preservación del feto debería considerarse y discutirse seriamente en caso de cáncer ovárico epitelial diagnosticado en el segundo trimestre del embarazo, que parece ser el momento de la gestación donde más controversia plantea el diagnóstico y las posibilidades terapéuticas de un cáncer de ovario21-24.
CÁNCER DE MAMA Y GESTACIÓN
El cáncer de mama es una patología poco frecuente en la mujer joven y su incidencia aumenta con la edad. La incidencia del cáncer de mama varícia a medida que las mujeres van retrasando la edad de su primera maternidad, tendencia cada día más acentuada principalmente en la población de los países desarrollados26.
El retraso de la maternidad hasta los 35 años o más triplica el riesgo de cáncer de mama comparado con las que tienen su primer hijo antes de los 20. El tipo histológico más frecuente en embarazadas, al igual que en la no gestante, es el carcinoma ductal infiltrante.
El cáncer de mama es claramente y en gran parte de los casos un tumor hormonodependiente y en el embarazo se alcanzan valores de estrógenos y progesterona entre 30 y 50 veces mayores6. Esto llevó a pensar que el estado hiperestrogénico que supone el embarazo provocaría una mayor radicalidad y, por tanto, un peor pronóstico ya que en los primeros estudios que se realizaron de mujeres afectadas de esta patología los resultados fueron desalentadores, y esto llevó a un tratamiento muy radical que implicaba incluso la interrupción del embarazo.
Sin embargo, se ha visto que el embarazo en sí no parece desempeñar un papel decisivo en la evolución e historia natural del cáncer, ya que ésta no difiere de la que presenta una mujer no gestante27, sino que son otros factores los que determinan que el pronóstico del cáncer de mama en la gestante sea ciertamente peor.
Se ha evidenciado que este empeoramiento del pronóstico no se debe a una mayor agresividad de estos tumores en la gestante, sino a factores como la juventud de las pacientes y, fundamentalmente, al retraso que habitualmente se produce en el diagnóstico, ya que los cambios anatómicos y fisiológicos de esta etapa enmascaran a menudo los posibles síntomas que pueda dar una tumoración incipiente28.
Clínica
La sintomatología es generalmente escasa, y suele limitarse al hallazgo casual de una tumoración, ocasionalmente dolorosa, y con menos frecuencia se presenta como supuración por el pezón o simulando una mastitis benigna. Estos y otros síntomas son fácilmente atribuibles al estado de gravidez de la paciente8.
Diagnóstico
Los medios que utilizaremos para el diagnóstico son los mismos que en la paciente no gestante, con algunas particularidades. El primer paso y fundamental para el diagnóstico temprano es la exploración mamaria, que el obstetra deberá realizar concienzudamente en la primera visita de control del embarazo a todas las pacientes8.
Aunque la mamografía es un método muy utilizado en la no gestante, en el embarazo encuentra varios problemas: la densidad mamaria se encuentra muy aumentada, por lo que pierde valor, y en gran medi da aumenta la tasa de falsos negativos29. Aunque no está contraindicada, en ocasiones los técnicos son muy reticentes a utilizarla en gestantes, así que en caso de utilizarla siempre se hará con protección abdominal.
La ecografía es un método frecuentemente utilizado en las pacientes jóvenes con tumores de mama y en la gestante puede ser de ayuda a la hora de valorar una tumoración.
Para valorar la extensión del tumor podemos emplear otras técnicas de imagen, como la RM, preferible a la TC antes de finalizar la gestación.
Ante toda lesión sospechosa, procederemos a un análisis histológico, y practicaremos una biopsia bajo anestesia local. En ocasiones puede recurrirse a la punción-aspiración con aguja fina (PAAF), aunque es preferible utilizar la biopsia tumoral.
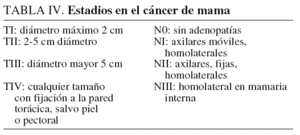
Estadificación (tabla IV)
Tratamiento
En general, a una paciente gestante con cáncer de mama se la debe tratar como a una no embarazada. El tratamiento va a implicar una visión global que implique el bienestar de la madre y el feto, de modo que podrá enfocarse a la protección del feto, pero esto va a depender de las características de la enfermedad y de la edad gestacional al diagnóstico27.
El tratamiento clásico es la mastectomía radical con exéresis de los ganglios axilares, aunque hoy día se tiende a disminuir la cirugía con cuadrantectomía o incluso tumorectomía, seguida de limpieza axilar guiada por ganglio centinela. El tratamiento local se completa con radioterapia de la zona afectada, y posteriormente se administra quimioterapia sistémica.
La interrupción del embarazo no ha demostrado tener beneficios en la evolución de la enfermedad8,30. Sólo en estadios muy avanzados del cáncer, y cuando nos encontramos en edades gestacionales tempranas, puede estar justificado proponer un aborto terapéutico para iniciar en el menor tiempo posible un tratamiento agresivo que no pueda ser demorado, dado que debe evitarse la radioterapia y la quimioterapia durante el primer trimestre.
Así, en el inicio de la gestación se aconseja posponer los tratamientos coadyuvantes de quimioterapia y radioterapia, y la cirugía conservadora no puede plantearse, ya que requiere dosis muy altas de radioterapia que serían letales para el feto, de modo que únicamente podría utilizarse en la segunda mitad del embarazo, cuando la radioterapia podrá administrarse a corto plazo4, y deberá recurrirse a una cirugía más agresiva.
Durante el segundo y tercer trimestres y en estadios iniciales de la enfermedad puede seguirse el esquema habitual de tratamiento con cirugía, radioterapia y quimioterapia, ya que los efectos en el feto son ya mínimos30.
En la quimioterapia mamaria se administran agentes oxidantes, como la ciclofosfamida, la doxorrubicina y la adriamicina, hay que evitar el metrotexato y tener la máxima precaución con el fluoracilo.
En cualquier caso se desaconsejará la lactancia materna.
MELANOMA Y GESTACIÓN
El melanoma es un tumor agresivo de comportamiento impredecible31. Su incidencia ha aumentado considerablemente en las últimas décadas y la edad media de aparición se ha visto reducida. Es uno de los tumores asociados más frecuentemente al embarazo, aproximadamente un 8%32.
Histopatología
El aumento de la secreción de hormona estimulante de los melanocitos, que se produce durante la gestación, principalmente en el segundo trimestre, así como la hiperpigmentación que presentan las gestantes debido a esta hormona, llevó a pensar que el melanoma en estas pacientes sería más agresivo5. Además, los melanocitos cuentan con receptores hormonales para estrógenos, progesterona y andrógenos, que explicaría un comportamiento hormonodependiente del melanoma33-35.
Estas teorías están actualmente en desuso, ya que además de los estudios histopatológicos que demuestran un contenido en receptores mucho menor que los tumores hormonodependientes36, en estudios recientes se ha comprobado que los melanomas en pacientes gestantes tienen una incidencia, agresividad y distribución por estadios similar al que se halla en las pacientes no gestantes37.
Pronóstico
En cuanto al pronóstico, dependerá, al igual que en las pacientes no gestantes, del estadio en que se diagnostique, y en sus fases iniciales vendrá determinado por la profundidad de éste en la piel (valores de invasión de Clark y Breslow)4.
No hay diferencias en cuanto a la supervivencia en gestantes respecto a las no gestantes38, por lo que el embarazo tampoco parece modificar la historia natural de la enfermedad4,39,40.
Tratamiento
En principio el tratamiento se planteará como en la paciente no gestante, de modo que cuando se localiza el melanoma, se realiza la escisión quirúrgica del tumor con los márgenes libres adecuados (1 cm si la profundidad es menor de 1 mm, o 2 cm cuando ésta mida entre 1,5 y 4,0 mm de espesor), así como la linfadenectomía completa del área afectada, siempre que haya ganglios positivos o la profundidad sea mayor de 1 mm.
En estadios metastáticos el tratamiento de elección será la quimioterapia a partir del segundo trimestre con un único fármaco o con tratamientos combinados4,41.
Metástasis placentarias
A pesar de que las metástasis en el feto vía placentaria son muy poco frecuentes, el melanoma maligno es la tumoración maligna que más frecuentemente metastatiza en la placenta y el feto, y representa más del 50% de los tumores que afectan a estructuras fetales. Cuando la placenta está afectada, el riesgo fetal de presentar metástasis es del 22%42-44, así que el recién nacido deberá tener un estrecho seguimiento por el alto riesgo que esto implica.
En definitiva, en cualquier cambio sospechoso en un nevo que se produzca durante el embarazo deberá realizarse una biopsia sin demora y, por supuesto, sin esperar hasta el final de la gestación, ya que de este tiempo puede depender la extensión y el pronóstico de éste.
LINFOMA DE HODGKIN Y EMBARAZO
El linfoma es la cuarta tumoración maligna más frecuente diagnosticada durante el embarazo45, con una incidencia de 1/1.000-6.000 partos. La enfermedad de Hodgkin es el tipo de linfoma más frecuentemente diagnosticado durante la gestación hasta en un 40% de todos los linfomas5.
Diagnóstico
Generalmente se presenta clínicamente como una adenopatía indolora4.
Para el diagnóstico será fundamental la biopsia y el estudio anatomopatológico de las adenopatías, que se considera además inocua durante todo el embarazo.
Para realizar la estadificación y el tratamiento de este tipo de tumores, se requiere utilizar procedimientos radiológicos, biopsia de médula ósea, exploración de las vísceras abdominales, etc., que se deben realizar sin que ello suponga un grave riesgo para el feto.
El pronóstico de la enfermedad no parece estar empeorado por la gestación, y al contrario de lo que se pensaba clásicamente, no produce exacerbaciones de la enfermedad, ni afecta a la tasa de supervivencia46, salvo que la gestación suponga un retraso en el diagnóstico o tratamiento.
Tratamiento
Aproximadamente se diagnostica a dos tercios de las pacientes en estadios I y II. El tratamiento terapéutico deberá plantearse, en principio, como en la paciente no gestante y, al igual que en ésta, estará condicionado por el estadio en el que se diagnostique la enfermedad, y generalmente se basará en una combinación de quimioterapia y radioterapia.
Hay autores que en el primer trimestre defienden sugerir el aborto terapéutico, ya que la quimioterapia y la radioterapia van a tener efectos muy nocivos en el feto, principalmente en pacientes con enfermedad muy avanzada en la que una demora en el tratamiento pueda suponer un grave empeoramiento del pronóstico47 (fig. 2).
La interrupción del embarazo también parece aconsejada en las pacientes con enfermedad infradiafragmática que requerirán irradiación pélvica.
En caso de que la paciente rechace este tratamiento, podría administrarse radiación supradiafragmática modificada o bien quimioterapia con un solo fármaco hasta el segundo trimestre48. Ésta parece ser la tendencia de las últimas investigaciones, que proponen como tratamiento campos limitados de radioterapia asociada a quimioterapia con asociaciones de fármacos, que parecen tener buenos resultados, tanto en la curación materna como en la escasa o mínima injuria fetal.
Para estos autores, el embarazo no debería ser un obstáculo para un correcto tratamiento del linfoma de Hodgkin, ya que en las series de RM estudiadas que se habían sometido a quimioterapia intrauterina no se encontró mayor proporción de malformaciones que en la población general49.
Respecto a la radioterapia, en trabajos recientes se afirma que los valores de radiación de 10 cGy, a nivel cervical y axilar, y con protección abdominal, podrían administrarse sin perjuicio de la gestación50.
Las pacientes diagnosticadas en el segundo o tercer trimestre deben tratarse con combinaciones de agentes quimioterápicos al igual que las pacientes no gestantes, y hay que deja para después del parto el tratamiento radioterapéutico.
CÁNCER DE TIROIDES Y GESTACIÓN
El cáncer de tiroides es una patología muy frecuente en mujeres en edad reproductiva, de tal modo que la incidencia de patología tiroidea es tres veces superior en mujeres que en varones durante esta época. Tras la diabetes mellitus, la patología tiroidea es la endocrinopatía más frecuente en la gestante51.
El embarazo es una situación favorable para la aparición de patología tiroidea, ya que se produce un balance negativo de yodo que propicia la formación de nódulos, así como un aumento considerable en la producción de hormonas con actividad estimulante del tiroides. Por todo ello, debería realizarse una exploración tiroidea de rutina en toda mujer gestante, principalmente en su primera visita obstétrica, y mejor si se realiza en una visita preconcepcional52.
El tipo histológico más frecuente es el papilar, y el cáncer folicular de tiroides se sitúa por detrás de él en frecuencia. Los dos juntos representan más de dos tercios de los cánceres de tiroides, ambos afortunadamente de buen pronóstico tanto en la paciente gestante como en la no gestante5.
Diagnóstico
Cuando en una exploración diagnosticamos una tumoración tiroidea, tanto el seguimiento ecográfico como la PAAF nos van a ser de gran ayuda para controlar su evolución y valorar el tratamiento48. La gammagrafía está contraindicada durante la gestación.
La PAAF ha demostrado ser segura durante todas las épocas del embarazo; podemos apoyarnos en la ecografía para realizar el seguimiento, controlar el crecimiento del tumor, la aparición de nódulos, microcalcificaciones sugerentes de malignidad, o la presencia de ganglios linfáticos regionales.
Si la citología resulta benigna o poco concluyente, será preciso seguir vigilando estas tumoraciones mediante sucesivas exploraciones manuales, ecografía y PAAF eventual.
Si comparamos la supervivencia entre mujeres gestantes y no gestantes no parece haber diferencia52.
Tratamiento
Todavía hay cierta controversia en el tratamiento que hay que adoptar, pero se recomienda adoptar uno conservador.
Si las muestras citológicas sugieren malignidad o proliferación folicular, debe practicarse tiroidectomía si se diagnostica al inicio del embarazo.
En caso de gestación avanzada o que la paciente decida posponer el tratamiento para después del parto, se puede realizar tratamiento hormonal supresor, si bien no está establecido el grado de supresión52.
Ante la evidencia de metástasis locales no debe aplazarse la realización de la cirugía; sólo en gestaciones que se encuentren alrededor de la semana 20 podría plantearse esta demora por el riesgo de parto prematuro, ya que parece que en estos casos este retraso en el tratamiento no modifica la historia natural del cáncer.
NEO COLON-RECTO
Se trata de una patología frecuente, aunque acontece muy rara vez asociada a la gestación, con pocos casos descritos en la literatura médica; aproximadamente podemos cifrarlo en 1/50.000 embarazos53.
La clínica puede quedar enmascarada entre los síntomas propios de la gestación, como náuseas, alteraciones del ritmo intestinal y sensación de distensión abdominal.
Ante la sospecha de tumoración debe recurrirse a una colonoscopia de preferencia a un enema opaco.
Durante el segundo y tercer trimestres se tiende a retrasar el tratamiento hasta la madurez fetal, con cesárea y posterior cirugía con radioterapia y quimioterapia54.
Se aconseja practicar cirugía radical en el primer trimestre y posponer la quimioterapia y la radioterapia si fuera posible.
SISTEMA NERVIOSO CENTRAL
Los tumores más frecuentes son los meningiomas, que por ser hormonas dependientes tienden a crecer durante la gestación. La clínica puede pasar desapercibida durante la gestación, y el tratamiento será como en la paciente no gestante, fundado básicamente en cirugía y radioterapia5.
FEOCROMOCITOMA
Es muy raro, aunque se asocia a una elevada mortalidad materna de hasta el 50%.
Si el diagnóstico se realiza en el segundo o tercer trimestre, se aconseja controlar la presión arterial con bloqueadores-* hasta la madurez fetal, realizar una CST y posteriormente proceder a una resección quirúrgica55.
Durante el primer trimestre se procederá a la cirugía en primera instancia, siempre con control exhaustivo con bloqueadores-*, para continuar posteriormente con la gestación.
LEUCEMIA
La incidencia se sitúa en torno a 1:75.000 embarazos, y principalmente se trata de leucemias agudas. No hay evidencias de que el embarazo empeore el pronóstico, y el tratamiento es igual que en la paciente no gestante56.
Durante el primer trimestre hay la posibilidad de teratogenia por la quimioterapia, con alto riesgo de aborto, por lo que muchos autores se plantean la evacuación uterina.
RESUMEN
El objeto de este trabajo es revisar la actuación en los cánceres asociados a la gestación, y tratar el manejo en cada uno de los posibles diagnóstico. Los más frecuentes son los cánceres de cérvix, mama, tiroides, melanoma y ovario.
La aparición de una neoplasia maligna durante la gestación (0,07%) supone una situación compleja y ambivalente que requiere grandes dosis de formación científica para su manejo, pero también un importante apoyo psicológico y una profunda preparación ética.
Entendemos como cáncer y embarazo toda neoplasia maligna que se produzca durante la gestación o hasta un año después del parto, y deberemos tratarla en principio como si la mujer no estuviera embarazada, sin olvidar por ello su estado y el momento de su gestación.
Es indispensable disponer de un diagnóstico certero, para lo cual nos basaremos en la clínica y las características concretas de cada tipo de cáncer. Podremos emplear en general los métodos de imagen convencionales (tomografía computarizada, resonancia magnética, etc.) para realizar un estudio de extensión, con mayores limitaciones durante el primer trimestre, donde el feto es más sensible.
Tampoco en el tratamiento suele haber limitaciones insalvables, teniendo en cuenta que la regla básica será posponer el tratamiento hasta finalizar la gestación cuando ésta esté avanzada y centrarnos sólo en la madre cuando sea muy incipiente. Siempre que fuere posible, será preferible el tratamiento quirúrgico, aunque a partir del segundo trimestre se pude asociar radioterapia y quimioterapia.