La endocarditis infecciosa es una patología poco prevalente en pediatría (0,5-1/1.000-1.300 pacientes pediátricos hospitalizados), con una morbimortalidad del 11-18%1, siendo cada vez más frecuente en pacientes sanos (10-20%)2,3. Los agentes habituales son el Staphylococcus aureus y el Staphylococcus tviridans2. El neumococo, a pesar de ser el principal agente causante de enfermedad bacteriana invasiva en pediatría, solo representa el 1% de los casos pediátricos de endocarditis infecciosa. Actualmente presenta un aumento de su incidencia (3-15%), por serotipos vacunales 14 y 18 y serotipos no vacunales resistentes a antibioterapia habitual4,5. La presencia de cardiopatía congénita es el único factor de riesgo claramente asociado6. Clínicamente se presenta como un soplo de nueva aparición o deterioro hemodinámico en el contexto de una bacteriemia por neumococo2. La endocarditis neumocócica es una infección rápidamente progresiva y destructiva de tejido valvular cardiaco o material protésico, con una mortalidad del 50-60% en casos sin cirugía1,2,6. Por tanto, el diagnóstico y tratamiento precoz, sobre todo en pacientes de riesgo, es clave para mejorar el pronóstico. Presentamos el caso de una lactante con neumonía, meningitis y endocarditis por neumococo, una rara asociación conocida como síndrome de Austrian7.
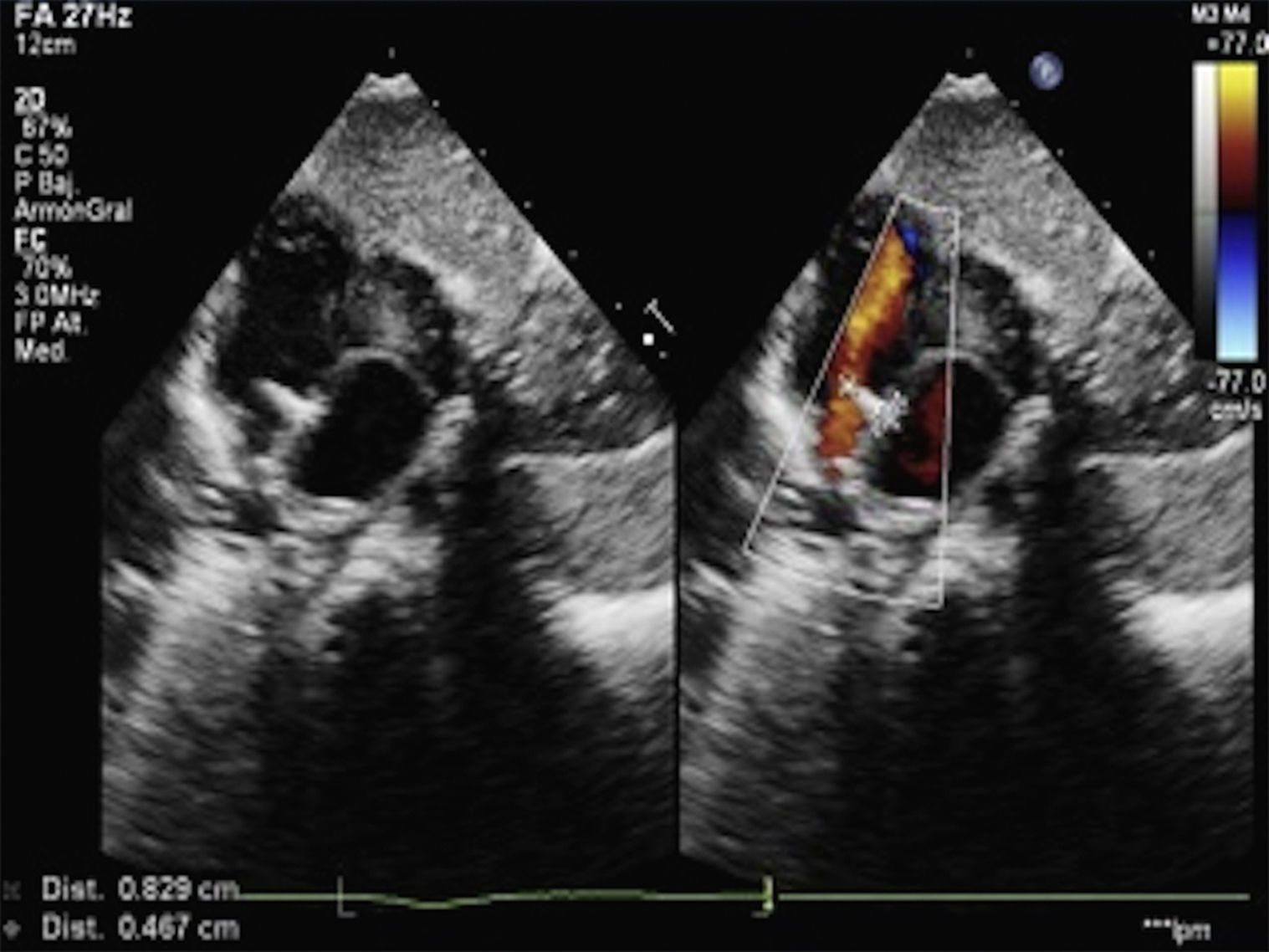
Lactante de 4 meses intervenida con 7 días de vida de interrupción de arco aórtico y CIA que ingresa en UCIP por shock séptico. No vacunada con la antineumocócica conjugada. Presentaba fontanela anterior abombada. Se realiza analítica con leucopenia, PCR elevada y coagulopatía, Rx tórax con condensación en lóbulo inferior izquierdo, TAC craneal normal y punción lumbar con LCR con 190 células (90% PMN), proteínas: 182,1mg/dl y glucosa: 5mg/dl. En ecocardiografías seriadas se objetivó verruga de 8×4mm en septo interauricular al tercer día de evolución (fig. 1), con estudios anteriores normales. En hemocultivo y cultivo de LCR creció Streptococcus pneumoniae resistente a penicilina y sensible a cefotaxima. Se envió a serotipar al Centro Nacional de Microbiologia, confirmando un serotipo 19-A. Con el diagnóstico de síndrome de Austrian se trató con cefotaxima y vancomicina. Se evitó cirugía cardiaca debido a coagulopatía e inestabilidad hemodinámica atribuidas a la sepsis. Evolucionó favorablemente con resolución completa de las alteraciones cardiacas, respiratorias y neurológicas, con hemocultivo y cultivo de LCR de control negativos. Se completó 4 semanas de antibioterapia intravenosa y 2 más con amoxicilina-clavulánico oral.
El síndrome de Austrian fue descrito por primera vez en 1862 por el patólogo austriaco Heschl. En 1956, el internista estadounidense R. Austrian describió la afectación preferente de la válvula aórtica en este cuadro7. Es rara su presentación de forma completa en niños, donde hasta 2004 se habían descrito 32 casos6,7, pero con una elevada morbimortalidad, siendo recomendable realizar screening ecocardiográfico seriado en todo paciente con meningitis neumocócica, más aún si asocia afectación pulmonar y compromiso hemodinámico, centrándose el estudio sobre todo en las válvulas mitral y aórtica6,8. En nuestro caso, la presencia de factores de riesgo como el antecedente de cirugía cardiovascular con material protésico obliga a descartar otras localizaciones menos frecuentes de endocarditis. El tratamiento de la endocarditis debe incluir un abordaje multidisciplinar, siendo la antibioterapia empírica precoz, combinada y prolongada el pilar terapéutico fundamental, teniendo en cuenta los diferentes microorganismos causantes y el aumento de resistencia a antibióticos. En el caso del Neumococo la combinación de una cefalosporina de 3.a generación más un glucopéptido parece una opción razonable hasta conocer el antibiograma6,9. Se debe completar 4-6 semanas de tratamiento intravenoso al tratarse de un tejido mal vascularizado y considerando la naturaleza invasiva del germen. La indicación de cirugía es controvertida6, debiéndose reservar para casos de disfunción valvular, fenómenos embólicos de repetición, inestabilidad hemodinámica refractaria, o persistencia de hemocultivos positivos a los 10 días de iniciar antibioterapia correcta10. Está por determinar el impacto de la vacuna conjugada en la prevención de la endocarditis neumocócica2,5,6.