Introducción: La radioterapia de intensidad modulada (IMRT) es una técnica de radioterapia conformal, que distribuye dosis muy alta y conformada en el volumen blanco y dosis reducidas en los órganos de riesgos (OAR).
El propósito de este artículo es presentar como opción de manejo a la IMRT en diversas neoplasias como tumores ginecológicos, tubo digestivo, retroperitoneo y vejiga.
Material y métodos: De septiembre de 2006 a diciembre de 2011, pacientes con diagnóstico de cáncer de diversos subsitios fueron tratados mediante la técnica de IMRT en la Unidad de Radioterapia del Servicio de Oncología del Hospital General de México. Se incluyeron 13 pacientes con tumores ginecológicos, 2 del tubo digestivo, 2 del retroperitoneo y uno de vejiga. Siendo un estudio de tipo observacional, retrospectivo longitudinal y descriptivo.
Todos los pacientes fueron tratados con IMRT en un Acelerador lineal Varian 211X, las dosis cambiaron de acuerdo a la patología, las variables incluidas fueron: sexo, edad, etapa clínica, reporte histopatológico del primario, dosis al volumen tumoral macroscópico (GTV), volumen tumoral clínico (CTV), volumen tumoral planeado (PTV) y dosis a los distintos órganos de riesgo (OAR), respuesta clínica y toxicidad. El análisis de la morbilidad aguda y crónica fue evaluado de acuerdos a los criterios de toxicidad de la RTOG.
Resultados: Un total de 13 neoplasias ginecológicas fueron tratados con IMRT: 11 con cáncer cervical (5 in situ, 3 EC IA y 3 EC IIB), un adenocarcinoma de endometrio EC IA y un caso de angiomixoma pélvico. Del grupo de tumores de tubo digestivo fueron 2: una paciente con sarcoma embrionario indiferenciado del hígado y otro con carcinoma del ámpula de váter. De los tumores retroperitoneales, 2 fueron sarcomas (liposarcomas) y finalmente, una paciente con cáncer de vejiga con recurrencia ganglionar en la ilíaca externa.
En todos los pacientes se realizó el análisis de los histogramas dosis volumen (DVH) en los distintos volúmenes de tratamiento GTV, CTV, PTV y OAR, en base a las recomendaciones establecidas en las guías internacionales de acuerdo al subsitio tumoral tratado.
Conclusiones: Independiente del subsitio, el control locorregional con IMRT es excelente en nuestra revisión. La IMRT proporciona una excelente cobertura del volumen blanco de tratamiento al depositar dosis muy altas en dicho blanco y dosis en los distintos órganos de riesgo muy por debajo de la dosis tolerancia de cada uno.
Introduction: Intensity modulated radiotherapy (IMRT) is a technique of conformal radiotherapy that distributes very high doses to target volume and low doses in the organs at risk (OAR).
The proposal of this article is show-up as an option of management with intensity modulated radiotherapy of diverse neoplasia such as gynecological, digestive tube, retroperitoneum and bladder tumors.
Material and methods: From September 2006 to December 2011 patients with diagnosis of different subsite were treated with technique of IMRT in the department of Radiotherapy at Service of Oncology from General Hospital of Mexico. Were included 13 patients with gynecological tumors, 2 digestive tube, 2 of retroperitoneum, and one of bladder. Observational, retrospective, longitudinal and descriptive study.
All patients were treated with IMRT in Linear Accelerator (Varian 21eX), the variations of doses was related to the pathology. The variables included were: sex, age, clinical stage, histopathology of primary, doses at gross target volume (GTV), clinical target volume (CTV), planning target volume (PTV) and doses in different OAR, clinical response and toxicity. The analysis of toxicity acute and late was evaluated according criterions to toxicity of the RTOG.
Results: A total 13 patients with gynecological neoplasia were treated with IMRT, 11 with cervical cancer (5 in situ, 3 clinical stage IA and 3 clinical stage IIB), 1 endometrial adenocarcinoma clinical stage IA and 1 case of pelvic angiomyxoma. There were 2 tumors of the digestive tube: one case of undifferentiated embryonary sarcoma of liver and 1 ampulla of Vater carcinoma. At retroperitoneum, there were 2 tumors, 2 were sarcomas (liposarcoma) and finally one patient with bladder cancer with recurrence in external iliac nodes.
In all patients was realized the analysis of doses volume histogram (HVD) in the different volumes of treatment (GTV, CTV, PTV and OAR) in base to the recommendations established for international guides accord sub-site tumoral treated.
Conclusions: Regardless of sub-site, the locoregional control with IMRT is excellent in our review. The IMRT provide excellent target volume coverage, deposit higher doses in this target and doses in the different organs at risk very low of the tolerance each one.
Introducción
En la radioterapia de intensidad modulada (IMRT) se busca distribuciones de dosis homogéneas y/o heterogéneas con gradientes acelerados, empleando haces de radiación de intensidad no uniforme, en los que se modula o controla la intensidad del haz de radiación para lograr altas dosis en el tumor y al mismo tiempo minimizar la dosis en los tejidos sanos adyacentes1-8.
El empleo de la IMRT ha llegado a ser especialmente importante en el manejo de los tumores del área de cabeza y cuello seguido por la próstata. La comparación de planes entre la radioterapia convencional con la RT-3D y más recientemente con la IMRT en otros sitios como son las lesiones del sistema nervioso central9,10, sarcomas de partes blandas y del retroperitoneo11-13 y en los tumores ginecológicos14,15 ha demostrado un claro beneficio en los aspectos dosimétricos con una mejor conformidad y una mayor cantidad de tejido normal o crítico, que puede ser fácilmente mantenido por debajo de la dosis de máxima tolerancia.
En nuestro país, la primera Institución en iniciar procedimientos de IMRT, fue la Unidad de Radioterapia del Servicio de Oncología del Hospital General de México, en este artículo se presenta la experiencia obtenida en el manejo de estos primeros pacientes y específicamente en los tumores ginecológicos, tubo digestivo, retroperitoneo y cáncer vesical, haciendo énfasis en los detalles y consideraciones técnicas del procedimiento y su correlación clínica.
Material y métodos
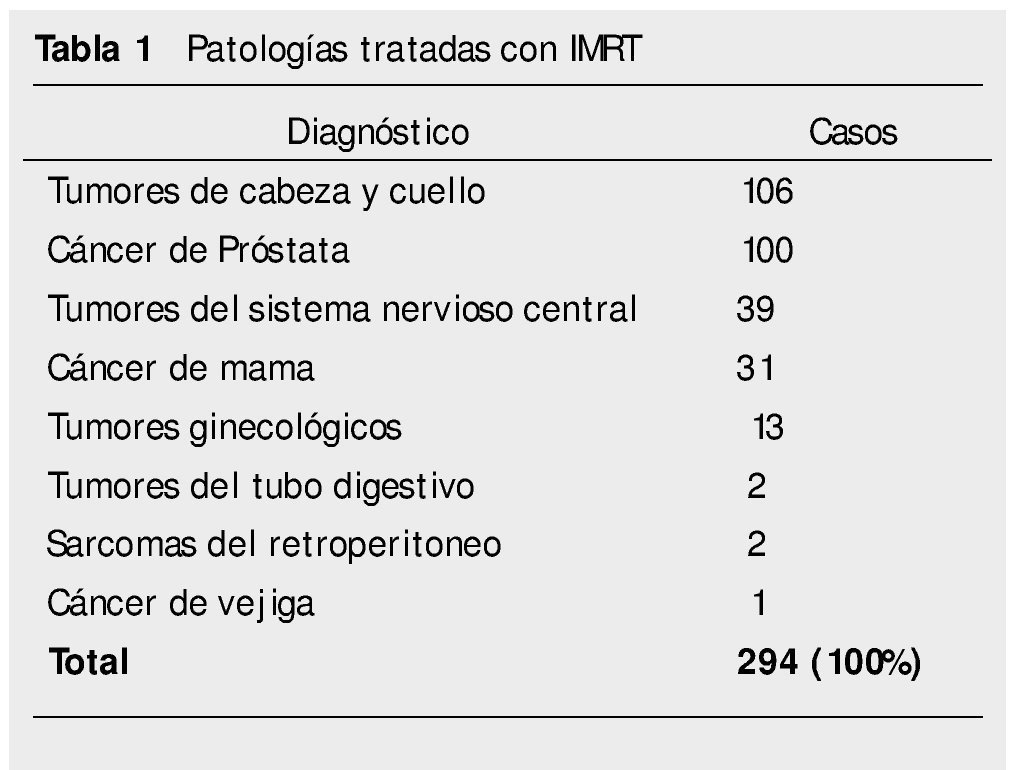
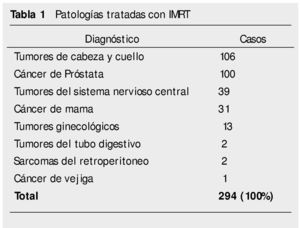
De septiembre de 2006 a diciembre de 2011, un total de 294 pacientes fueron tratados mediante técnica de IMRT por diversas patologías oncológicas en nuestra Institución que se resumen en la tabla 1.
Para efectos del presente estudio y siendo el objetivo del mismo, se analizaron a los pacientes que corresponden a tumores ginecológicos, tubo digestivo, retroperitoneo y vejiga, dando un total de 18 pacientes.
Todos los pacientes fueron tratados con IMRT con un Acelerador Lineal Varian® 21 EX, las dosis variaron de acuerdo a la entidad tratada y se especificarán en los párrafos subsecuentes.
Los equipos para el procedimiento de la IMRT consta de:
1. Tomógrafo GE multicorte.
2. Sistemas de fijación de acuerdo al subsitio de tratamiento.
3. Sistema de planeación Eclipse® v.7.25, con sistema Somavisión® v.7.25.
4. Acelerador Lineal dual marca Varian® 21 EX.
Para la planeación del tratamiento de la IMRT se realizaron fusiones de imágenes de resonancia magnética (IRM) y/o PET-CT con imágenes tomográficas simples y/o contrastadas del caso o sitio a tratar.
Las variables estudias fueron:
a. Sexo.
b. Edad.
c. Etapa clínica.
d. Reporte histopatológico de acuerdo al sitio del primario.
e. Dosis al volumen grueso tumoral (GTV).
f. Dosis al volumen tumoral clínico (CTV).
g. Dosis al volumen tumoral planeado (PTV).
h. Dosis a los distintos órganos de riesgos (OAR).
i. Tiempo total de tratamiento.
j. Respuesta clínica.
k. Respuesta radiológica posradioterapia.
l. Toxicidad aguda.
Siendo esta revisión un estudio de tipo observacional, retrospectivo longitudinal, descriptivo (promedio, media, rango), para determinar la asociación entre 2 variables se realizó la prueba de ji cuadrada para independencia. Para el análisis de control local, falla local, locorregional, metástasis a distancia y muerte fueron estimados por el método de Kaplan-Meier.
Todos los pacientes fueron evaluados semanalmente durante el tratamiento de IMRT y al término del mismo, al mes y posteriormente cada 2 meses el primer año. Cada 2 a 3 meses el segundo año y cada 4 meses a partir del tercer año. Durante el seguimiento se realizó exploración clínica, estudios de imágenes dependiendo del sitio (tomografía computarizada TC, IRM) y pruebas de laboratorio incluyendo marcadores tumorales En caso de surgir alguna duda que no se aclarara con los estudios ya señalados, se solicitó el PECCT corporal. La morbilidad aguda y crónica fue evaluada de acuerdos a los criterios de toxicidad de la RTOG16.
Resultados
Se trataron un total de 18 pacientes, de los cuales 13 corresponden a tumores ginecológicos, 2 del tubo digestivo, 2 retroperitoneales y uno de cáncer vesical (tabla 1).
Los resultados de acuerdo a cada subsitio tratado con IMRT y en función de las variables definidas para su análisis se describen a continuación.
Tumores ginecológicos
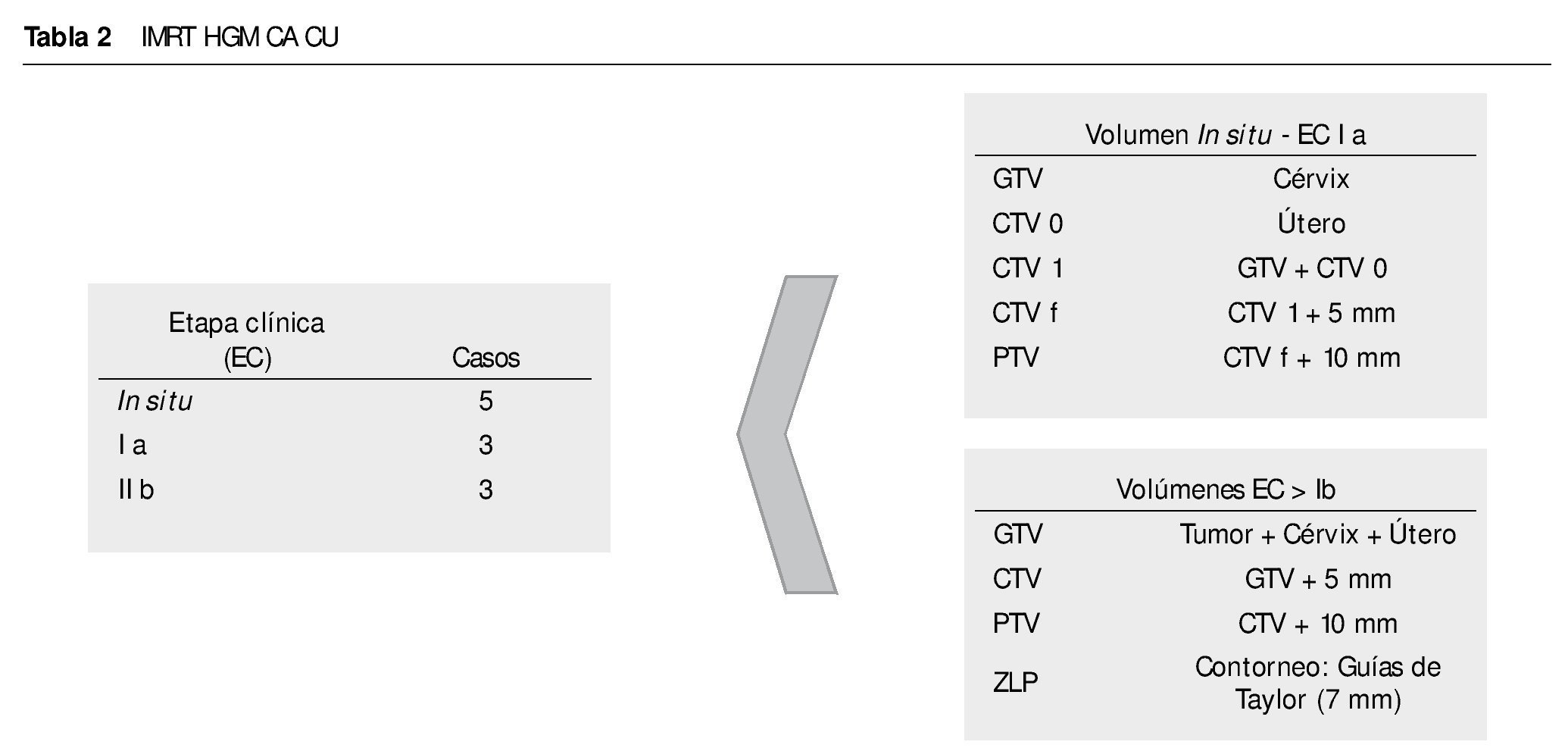
Un total de 13 neoplasias ginecológicas han sido tratada con la modalidad de IMRT, 11 son patología cervical (5 cáncer cervicouterino in situ, 3 EC IA y 3 EC IIB), un caso de adeno-carcinoma de endometrio EC IA y otro caso de angiomixoma pélvico, siendo el promedio de edad de 52.6 años y el rango de 19 a 69 años.
De los 11 casos del cérvix, 5 son cáncer cervicouterino in situ, que no fueron candidatos a cirugía por tener alguna patología concomitante con riesgo quirúrgico o anestésico alto. Entre el grupo de enfermedades concomitantes se observaron: diabetes mellitus tipo 2 más cirrosis hepática en una de las pacientes o cardiopatía por fibrilación auricular o cardiopatía hipertensiva más hipertrofia ventricular concéntrica izquierda o diabetes mellitus insulinodependiente de difícil control o cardiopatía reumática con estenosis mitral más valvulopatía y anticoagulación oral u obesidad importante mayor de 100 Kg.
La dosis prescrita en el cáncer in situ fue en 4 con 6,000 cGy en 30 fracciones y uno de 6,560 cGy en 32 fracciones e igual dosis en los 3 casos de EC IA, realizándose la definición de volúmenes para GTV (tumor cervical), CTV0 (útero), CTV1 (GTV + CTV0), CTV final o CTVf (CTV1 más margen de 5 a 10 mm), PTV (tabla 2), puntos A y B de Manchester y órganos de riesgos (vejiga, recto, cabezas femorales).
La dosis promedio en el GTV (cérvix) en la curva del 95% fue de 61.20 Gy y en el 100% es de 60.40 Gy. En el CTV0 (útero) las dosis del 95% y del 100% son 60.80 Gy y 59.80 Gy, respectivamente, correspondiendo al CTV1 (GTV más CTV0) las dosis del 95% y 100% de 60.90 Gy y 59.80 Gy. Respecto al PTV las dosis del 95% y del 100% son 60.20 Gy y 59.60 Gy, respectivamente. En cuanto a las dosis en los órganos de riesgo se siguieron los mismos parámetros de tolerancia que se tienen para el cáncer de próstata (RTOG 0126) en recto, vejiga, además de la guía de nuestra Unidad y más recientemente la guía del protocolo TMH al administrar dosis de 5000 cGy con IMRT a la pelvis17,18, obteniéndose dosis en el 15% del volumen rectal de 59.20 Gy, en el 25% de 57.90 Gy, en el 35% de 56.20 Gy y en el 50% de 53.80 Gy. Las dosis en la vejiga fueron en el 15% del volumen vesical de 60.80 Gy, en el 25% de 60.50 Gy, en el 35% de 59.80 Gy y en el 50% de 53.80 Gy, respectivamente. Las dosis en las cabezas femorales fueron en el rango de 23.90 a 25.80 Gy en el 15% del volumen y de 20.00 a 25.80 Gy en el 35% del volumen. Estas 8 pacientes se encuentran sin evidencia de actividad tumoral con un seguimiento promedio de 20 meses y un rango de 14 a 43 meses.
De los 3 casos restantes, uno corresponde a cáncer cervicouterino EC IIb con riñón ectópico en la pelvis y con obesidad grado II. Administrándose el tratamiento de IMRT en 2 fases, la primera con una dosis de 5,000 cGy en 25 fracciones a la pelvis y posteriormente un incremento (puntos A de Manchester) de 2,500 cGy en 12 fracciones. Definiéndose los volúmenes clínicos respectivos y órganos de riesgos (vejiga, recto y en especial el riñón ectópico) (tabla 2). En los órganos de riesgo se siguieron los parámetros de tolerancia que se tienen para el cáncer de próstata (RTOG 0126) y de las guías de nuestra Unidad, obteniéndose dosis en el 15% del volumen rectal de 60.20 Gy, en el 25% de 59.90 Gy, en el 35% de 57.20 Gy y en el 50% de 55.80 Gy. Las dosis en la vejiga fueron en el 15% del volumen vesical de 63.80 Gy, en el 25% de 62.50 Gy, en el 35% de 61.80 Gy y en el 50% de 55.80 Gy, respectivamente. Las dosis en las cabezas femorales fueron en el rango de 23.90 a 25.80 Gy en el 15% del volumen y de 20.00 a 25.80 Gy en el 35% del volumen. La dosis en el riñón ectópico se mantuvieron por debajo de una dosis promedio de 18 Gy. La paciente tiene un seguimiento de 24 meses, se encuentra sin evidencia de actividad tumoral y con función renal normal.
Los otros dos casos son EC IIb que recibe tratamiento de IMRT en 2 fases, la primera a la pelvis dosis de 5,000 cGy en 25 fracciones seguido de incremento prescrito a los puntos A de Manchester dosis de 3000 cGy en 15 fracciones. Definiéndose los volúmenes clínicos respectivos y la de los órganos de riesgos (vejiga, recto). Para la definición de los volúmenes blancos en las zonas linfoportadoras (ZLP) se siguieron las recomendaciones de las guías de Taylor19 y para el CTV del cérvix las del consenso para el contorneo del primario20,21 (tabla 2). Estas 2 pacientes se encuentran sin evidencia de actividad tumoral a 13 y 20 meses de seguimiento respectivamente.
Respecto, al adenocarcinoma de endometrio se trata de una EC IA con patología concomitante de obesidad grado III más diabetes mellitus tipo 2 con hipertensión arterial e insuficiencia renal crónica en programa de diálisis peritoneal continua ambulatoria. Se administró el tratamiento en 2 fases, la primera a la pelvis con técnica de RT-3D dosis de 4500 cGy en 25 fracciones, seguido de un incremento con IMRT al CTV y PTV de 3040 cGy en 17 fracciones. Las dosis en los volúmenes planeados de CTV, PTV y órganos de riesgos (vejiga, recto) se lograron sin problema. Esta paciente tiene 13 meses de seguimiento, se encuentra sin datos de AT y sin morbilidad.
El último caso de los tumores ginecológicos, se trata de una femenina de 19 años con diagnóstico de un angiomixoma pélvico derecho, siendo un tumor de localización retro cecal de 11 cm y con resección marginal. Ante la edad e imposibilidad de lograr márgenes adecuados se le programa IMRT a la pelvis derecha dosis de 6,000 cGy en 30 fracciones. En este tratamiento se contempló como órganos de riesgo además de la vejiga, recto y el ovario contra lateral. Siendo el seguimiento de esta paciente de 18 meses, sin evidencia de recurrencia y con función hormonal normal.
Tumores del tubo digestivo
Dos pacientes con tumores malignos de esta área se han tratado con IMRT, el primero se trata de un sarcoma embrionario indiferenciado hepático recurrente a nivel local, inicialmente tratado con cirugía (lobectomía derecha) que recurrió a los 6 meses, se le realiza una nueva cirugía con resección de la recurrencia con margen, sin embargo al solicitar PET-CT se documenta datos de persistencia tumoral en lecho y marginal. Ante lo anterior se le programa manejo de IMRT más RPM, siendo la dosis de IMRT de 6,120 cGy en 34 fracciones. Los volúmenes que se definieron fueron un CTV, PTV, órganos de riesgos como hígado, pulmones, corazón, riñones, estómago, intestino delgado y médula espinal, no sobrepasándose en ninguno de estos órganos de riesgo las dosis de tolerancia, siguiéndose la guía de tumores de tubo digestivo de la unidad. Esta paciente después de un intervalo libre de enfermedad de 18 meses sin evidencia de actividad tumoral clínica y por estudios de PET-CT evoluciona con múltiples metástasis pulmonares falleciendo.
El otro caso se trata de un cáncer de ámpula de Váter, postoperado y con márgenes quirúrgicos positivos. Administrándose también IMRT más RPM, siendo la dosis de 5,400 cGy en 30 fracciones. Se delinearon un CTV, PTV y órganos de riesgos. Con un seguimiento de 12 meses se encuentra sin evidencia de actividad tumoral tanto clínica como en el PET-CT.
Tumores del retroperitoneo
Dos sarcomas retroperitoneales han sido abordado con esta técnica, el primero se trata de un liposarcoma retroperitoneal izquierdo, lesión de 13 x 15 x 10 cm, resecada sin embargo en el reporte patológico definitivo describen borde profundo con positividad. Se administra IMRT al lecho quirúrgico, orientado por las grapas metálicas dejada por el cirujano, dosis de 5,000 cGy en 25 fracciones, definiéndose un CTV, PTV y órganos de riesgo (intestino delgado, colon, riñones y médula espinal).
El segundo caso es de un liposarcoma retroperitoneal desdiferenciado derecho, lesión de 15 x 14 x 18 cm, resecado pero con residual macroscópico paravertebral de 3 x 3 cm. Se administra IMRT en 2 fases, PTV1 dosis de 5,000 cGy en 25 fracciones y un incremento al PTV2 de 1,600 cGy en 8 fracciones.
Ambos casos se encuentra sin evidencia de actividad tumoral tanto clínica como en TC a 30 y 20 meses, respectivamente.
Cáncer de vejiga
Después de 2 años de seguimiento de un cáncer vesical T2b-NoMo que recibió inicialmente manejo de conservación del órgano vesical con quimioterapia más radioterapia conformada 3D, dosis de 6,740 cGy en 37 sesiones, se documenta en estudios de imágenes de control recurrencia ganglionar pélvica (ilíaca externa izquierda) como único sitio de actividad tumoral. Se le propone cistectomía radical de rescate, sin embargo la paciente no acepta la cirugía, ante lo anterior se le plantea tratamiento de reirradiación con IMRT al sitio de la recurrencia ganglionar. Se administra una dosis de 4,500 cGy en 25 fracciones, definiéndose CTV ganglionar y un PTV más los órganos de riesgos en vejiga, recto, cabezas femorales. La paciente tiene un seguimiento de 31 meses después de la IMRT, encontrándose clínicamente y por estudios de endoscopía vesical y de TC abdominopélvico sin evidencia de actividad tumoral.
Discusión
Nuestro estudio confirma las observaciones de otras instituciones respecto a las patologías que pueden ser abordadas por medio de la IMRT7,22,23. Los tumores del área de cabeza y cuello son el grupo más frecuentemente tratados con esta modalidad y que en nuestra serie correspondieron a 106 pacientes (36.0%), seguido por el cáncer de próstata con 100 casos (34.0%), en tercer lugar por las lesiones del sistema nervioso central con 39 pacientes (13.3%) seguidos por el cáncer de mama con 31 (10.6%), tumores ginecológicos 13 pacientes (4.4%), tumores del tubo digestivo y sarcomas retroperitoneales con 2 pacientes (0.7%) respectivamente, y una paciente (0.3%) con cáncer de vejiga.
Tumores ginecológicos
El tratamiento del cáncer cervical ha sido y es aún del dominio de la radioterapia. En las últimas décadas ha habido un esfuerzo por combinar la radioterapia con otras modalidades mayormente quimioterapia, que resulta en un mejor control locorregional y mejoría en la supervivencia, aún se continúan los esfuerzos para una adecuada optimización de la RTE. En el caso de la RTE con técnica de 4 campos generados de acuerdo a la anatomía corporal acompaña adecuadamente el volumen blanco en los pacientes. Los estudios de TC, IRM y el PET identifican el cérvix, ganglios y órganos de riesgo. La IRM es superior a la TC en demostrar el tumor cervical, la invasión parametrial, infiltración del útero, invasión de la vejiga o del recto24. La RT3D y la IMRT mejoran claramente la conformidad de la dosis comparada con la RTE convencional.
Las primeras publicaciones del uso de la IMRT, en los tumores ginecológicos destacan la reducción de la dosis en el intestino delgado al comparar las planeaciones de La IMRT con la RTE convencional25-27.
La definición de volúmenes y su contorneo para el cáncer cervicouterino invasor, ya han sido establecidas, los volúmenes ganglionares pélvicos pueden definirse en base a los límites anatómicos o en su relación con los vasos arteriales28,29, en cambio para los volúmenes ganglionares perivesicales, para-úterovaginales y para-rectales se definen mejor describiendo sus límites anatómicos28,29. Los volúmenes ganglionares alrededor de los vasos se definen con mayor precisión realizando expansiones isotrópicas de 5-15 mm, siendo 7 mm la recomendación y en algunas ocasiones en un sentido con expansiones anisotrópicas19.
La definición del GTV, CTV y PTV para el tratamiento radical con IMRT en cérvix intacto, han sido recientemente publicadas20,21. El GTV en el cáncer de cérvix es definido como el cérvix, útero, tumor y/o la extensión tumoral en las pacientes con útero intacto y en los casos post histerectomía los cambios posquirúrgicos y la cúpula vaginal. El CTV generalmente incluye todas las áreas del volumen tumoral microscópico o visible más la mitad superior de la vagina, parametrios y los ganglios linfáticos pélvicos (CTV ganglionar), respectos a estos últimos en los cortes de TC contrastada se delinearon los vasos pélvicos más un margen (5 a 15 mm) para definir los ganglios linfáticos de la ilíaca externa, interna y de la común hasta el nivel del espacio entre L4-L5. Los ganglios de la región sacra también son dibujados hasta el borde superior de S3 para de esta forma cubrir la zona ganglionar presacra y el ligamento úterosacro. Finalmente el CTV es expandido en forma simétrica 1 cm en todas las direcciones para formar el PTV19,28-32.
Salama J et al.33 también define los parámetros para los distintos volúmenes en caso de radioterapia con campos extendidos abordados con IMRT y más recientemente, Small W et al.34 define los volúmenes del CTV para IMRT en pacientes posquirúrgicas con cáncer endometrial y cervical.
La IMRT en cáncer cervical además de ser usada como tratamiento radical20,21,24,26,30-32,35,36, también puede emplearse como un tratamiento definitivo para la enfermedad metastásica en ganglios para-aórticos33,37 y como incremento a la pelvis específicamente al sitio del primario (cérvix) en caso de haber alguna contraindicación médica para la aplicación de la braquiterapia37.
En nuestra serie, un total de 13 casos de neoplasias ginecológicas fueron abordados con esta tecnología, de los cuales 11 son del cérvix, un adenocarcinoma de endometrio y un angiomixoma pélvico. De los 11 casos del cérvix, 5 son in situ y 3 cáncer cervicouterino iA que no fueron candidatos inicial a cirugía por tener patología concomitante de riesgo quirúrgico o anestésico alto y también de riesgo alto sobre todo anestésico para la aplicación de la braquiterapia. Se dibujaron los volúmenes de tratamiento para estos casos, definiéndose como GTV al tumor cervical, CTV0 al resto del útero, se crea un CTV1 que es la suma del GTV con el CTV0, se expande el CTV1 con un margen a todos los lados entre 5 a 10 mm para formar el CTV final (CTVf) y por ultimo un crecimiento a este CTVf con un margen isotrópico de 1 cm para formar el PTV. Igualmente se dibujan los distintos órganos de riesgo en la pelvis (recto, vejiga, cabezas femorales) y se localizan en la TC los puntos A y B de Manchester para los aspectos dosimétricos de la prescripción de la dosis en estos casos.
Sobre estos volúmenes que se definieron para el cáncer del cérvix in situ, no hay nada escrito en la literatura respecto al manejo con IMRT para este grupo de patología, por lo que se revisaron los volúmenes descritos para las etapas clínicas invasoras y se realizaron las definiciones para los distintos volúmenes del cáncer cervical in situ.
La dosis administrada fue de 6,000 cGy en 30 fracciones en 4 casos y de 6,550 cGy en 32 fracciones en un caso, siendo la prescripción de la dosis al punto A de Manchester. La dosis promedio en el GTV (cérvix) en la curva del 95% fue de 61.20 Gy y en el 100% es de 60.40 Gy, para el CTV0 (útero) las dosis del 95% y del 100% son 60.80 Gy y 59.80 Gy, respectivamente, correspondiendo al CTV1 (GTV más CTV0) las dosis del 95% y 100% de 60.90 Gy y de 59.80 Gy y siendo las dosis del 95% y del 100% de 60.20 Gy y de 59.60 Gy, respectivamente en el PTV.
Con el uso de la IMRT, Roeske et al. encontró que el volumen del intestino delgado que recibe la dosis prescrita fue reducida por un factor de 2 al compararse con el tradicional plan de 4 campos a la pelvis, además el volumen del recto y de la vejiga que reciben la dosis prescrita fue reducida en un 23%30. Mudnt A et al. Reporta en sus resultados que un 75% de las pacientes tratadas no requirieron medicamentos antidiarreicos durante el tratamiento de IMRT a la pelvis31.
En nuestro grupo de pacientes, las dosis en los OAR (recto, vejiga) permitió que el tratamiento fuese bien tolerado y con pocos efectos secundarios agudos tanto gastrointestinal como genitourinario.
El sexto caso del cérvix, corresponde a una etapa invasora IIb con presencia de un riñón ectópico pélvico, en quien se le programa IMRT en 2 fases, pelvis y luego un incremento al cérvix con prescripción de la dosis en la segunda fase a los puntos A de Manchester. En este caso lo importante como órgano de riesgo es la presencia del riñón ectópico en la pelvis y en quien se logró tener una distribución de la dosis promedio en dicho órgano menor de 18 Gy, con excelente evolución clínica, sin evidencia de actividad tumoral y con función renal excelente.
En cuanto a la tolerancia renal, en reciente publicación38 analizan nuevas restricciones dosis volumen para estimar un riesgo de complicación menor del 5% y bajo estas recomendaciones se sugiere que los riñones dosis volumen no debe de sobrepasar los siguientes parámetros: V28 Gy < 20%, V23 Gy < 30%, V20 Gy < 32%, V12 Gy < 55%. respecto al adenocarcinoma de endometrio EC iA, se delinearon los volúmenes de tratamiento de acuerdo a las guías ya establecidas y comentadas previamente en el cáncer del cérvix y que también aplican para el cáncer de endometrio30-32.
Los datos del uso de la IMRT en los tumores ginecológicos van en aumento y no sólo exploran en papel en el postoperatorio, sino como un tratamiento primario e identificar en cuál de estas neoplasias, la IMRT es el tratamiento de elección.
Uso de IMRT en otros sitios
Diversos estudios han sido publicados aunque en menor número, respecto al uso de la IMRT en otras neoplasias y entre estos están: cáncer de tiroides39,40, cáncer de esófago41,42, cáncer de vejiga43,44, cáncer de mama45-47, cáncer de pulmón (48), sarcomas de partes blandas y del retroperitoneo11-13,49, y en todos ellos la IMRT proporciona una mejor planificación con dosis más altas en el CTV, PTV pero con una menor dosis en los distintos órganos críticos al compararse con las planeaciones convencionales.
Conclusiones
La IMRT en comparación con otras técnicas de planeación ofrece la mejor posibilidad de separar las estructuras críticas cercanas al volumen tumoral. Los resultados de estudios preliminares y que analizan las curvas de distribución de dosis en las planeaciones e independientes del subsitio tratado, está asociado con una sustancial reducción en la toxicidad asociada al tratamiento. La IMRT puede reducir los puntos calientes en forma significativa en el tejido sano circunvecino y en la piel. En los tumores ginecológicos el uso de la IMRT se ha incrementado en forma significativa en los últimos años y los resultados obtenidos es que hay una reducción en la toxicidad gastrointestinal, tanto aguda como la crónica al compararse con la técnica estándar de 4 campos a la pelvis. En los sarcomas de partes blandas y del retroperitoneo la técnica de IMRT también ha demostrado su utilidad en la reducción de dosis a los tejidos y órganos sanos, y en la reducción de dosis en las estructuras óseas y en los órganos de riesgo del retroperitoneo.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Financiamiento
Los autores no recibieron patrocinio para llevar a cabo este artículo.
* Autor para correspondencia:
Dr. ATL N° 6 Manzana 3, Unidad Belisario Domínguez, Tlalpan, C.P. 14310, México D.F., México.
Teléfono: (55) 5678 5918. Celular: (55) 5452 3006.
Correo electrónico: pjlujanc@yahoo.com.mx (Pomponio J. Luján-Castilla).