La mesalazina es un derivado del ácido 5-aminosalicílico (5-ASA) muy utilizado para el tratamiento de la enfermedad inflamatoria intestinal. La sulfasalazina es el salicilato más antiguo y está constituido por 2 moléculas: la sulfapiridina y el 5-ASA. A la sulfapiridina se le ha atribuido la mayoría de los efectos secundarios descritos como reacciones de hipersensibilidad, neutropenia, fiebre, urticaria, hepatitis, etc.1. Este es el motivo por el que las nuevas moléculas prescinden de ella. A pesar de ello siguen describiéndose casos de urticaria, angioedema, neumonitis, hepatitis e incluso pancreatitis debidos a la mesalazina2.
Presentamos el caso de un paciente que desarrolló una hepatitis aguda secundaria al consumo de mesalazina.
Varón de 53 años diagnosticado de proctitis ulcerosa moderada en noviembre de 2013, y en tratamiento con 3 comprimidos de mesalazina (Mezavant®) de 1.200mg y un supositorio de mesalazina de 1.000mg/día. Sin otros antecedentes de interés ni toma de otros fármacos. No hábitos tóxicos ni ingesta de alcohol. En un control realizado en enero de 2014 el paciente está asintomático, sin datos de actividad, pero en la analítica de rutina se aprecia elevación de las cifras de ALT en rango de hepatitis (tabla 1) junto con leucopenia, sin eosinofilia. La exclusión de causas alternativas se realiza mediante la valoración de la ausencia de infecciones virales recientes tanto por virus hepatotropos (virus de la hepatitis A, B y C), como por otros virus como el de Epstein-Barr, el citomegalovirus y el herpes virus, marcadores de autoinmunidad (ANA, AMA, anti-LKM1, AML), marcadores metabólicos (ceruloplasmina, índice de saturación de transferrina, alfa 1-antitripsina) y la realización de pruebas de imagen para descartar lesiones neoplásicas, vasculares y enfermedad de la vía biliar (ecografía, TAC y colangio-resonancia). Se suspende la administración de mesalazina por vía oral, manteniendo tan solo el uso de supositorios de 500mg/72h. El enfermo presenta mejoría paulatina de los niveles de transaminasas normalizándolas transcurridos 55 días desde su supresión (tabla 1).
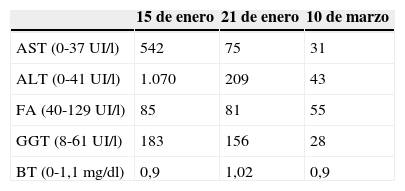
Evolución de parámetros analíticos
| 15 de enero | 21 de enero | 10 de marzo | |
|---|---|---|---|
| AST (0-37UI/l) | 542 | 75 | 31 |
| ALT (0-41UI/l) | 1.070 | 209 | 43 |
| FA (40-129UI/l) | 85 | 81 | 55 |
| GGT (8-61UI/l) | 183 | 156 | 28 |
| BT (0-1,1mg/dl) | 0,9 | 1,02 | 0,9 |
ALT: alanina aminotransferasa; AST: aspartato aminotransferasa; BT: bilirrubina total; FA: fosfatasa alcalina; GGT: gamma glutamil transpeptidasa.
Es bien conocido el potencial hepatotóxico de la sulfasalazina en los pacientes con enfermedad inflamatoria intestinal, sin embargo, el daño hepático secundario a la mesalazina se ha descrito en muy pocos casos3,4. Se estima que la incidencia de hepatitis tóxica es de 3,2 casos por millón de prescripciones de mesalazina2.
Nuestro caso siguió un patrón de daño hepatocelular al igual que el publicado por Coumaros et al.5, aunque también se han comunicado casos con patrón colestásico o mixto3,4. Cuando aplicamos la escala de Council for International Organizations of Medical Sciences (CIOMS)6 obtenemos una puntuación de 9 (altamente probable o definitiva).
El mecanismo por el que la mesalazina provoca daño hepático no está aclarado, postulándose mecanismos de idiosincrasia, pudiendo o no acompañarse de fenómenos de hipersensibilidad7. Se teoriza que por similitud estructural con los salicilatos, podría compartir el mismo mecanismo patogénico, mediante la generación de tóxicos intermediarios resultantes de la producción de ácido salicílico y glucurónido salicil-fenólico, y la afectación de la síntesis de ATP mitocondrial, por el desacoplamiento de la fosforilación oxidativa3,8–10. En nuestro caso se mantuvo la mesalazina tópica a dosis bajas y, aunque, la absorción sistémica del fármaco por esta vía es menor, hasta un 10-20% de la dosis es absorbida11. Es probable que la continuación del fármaco por vía tópica no influyera en la persistencia del cuadro debido a la adaptación y tolerancia que desarrolla el tejido hepático12.
Concluimos que la mesalazina es un fármaco seguro y muy utilizado en la práctica clínica diaria, con bajo riesgo de hepatotoxicidad, sin embargo se debe pensar en él como causa de alteraciones hepáticas en la que se hayan descartado otras etiologías.