Sr. Director:
La metformina (dimetilbiguanida) es un hipoglucemiante oral, del grupo de las biguanidas, que se utiliza en el tratamiento de los pacientes con diabetes tipo 2 desde hace más de 50 años. Actúa como un agente sensibilizador de la insulina; disminuye las concentraciones plasmáticas de ésta, induce una mayor utilización periférica de la glucosa y disminuye la producción de glucosa hepática1 . Es en la actualidad uno de los hipoglucemiantes orales más utilizados en todo el mundo, ya que tiene una potencia hipoglucemiante similar a las sulfonilureas pero con menor riesgo de hipoglucemias y menor ganancia de peso que éstas. Se considera un fármaco seguro, y sus efectos secundarios más frecuentes son las alteraciones digestivas menores, del tipo diarrea, náuseas y vómitos. En este mismo orden, cabe decir que la acidosis láctica, que es su efecto secundario más conocido, debe considerarse un efecto adverso inusual (incidencia estimada de 0,03 por 1.000 pacientes/año), especialmente si se respetan sus contraindicaciones, en particular la insuficiencia renal1 . La toxicidad hepática por metformina es extraordinariamente rara y la base de datos MEDLINE únicamente recoge 4 casos descritos2-5 . (Descriptores: Metformin/adverse effects AND Hepatitis or Cholestasis. MEDLINE: 1966-2004.) Presentamos el caso de una paciente en tratamiento con metformina que desarrolló un cuadro de hepatitis colestásica.
Mujer de 80 años de edad, con historia de diabetes mellitus tipo 2, de reciente diagnóstico y sin complicaciones macro o microvasculares conocidas, hipertensión arterial y poliartrosis, que ingresó en enero de 2004 por ictericia. Seguía tratamiento con bisoprolol (5 mg/día), torasemida (5 mg/día) y lercanidipino (10 mg/día) desde hacía 2 años, y con glucosamina (1,5 g/día) desde hacía uno. En la última modificación del tratamiento, que se había producido hacía 3 meses, se incluyó metformina a dosis de 1.700 mg/día. Carecía de antecedentes de enfermedad hepática, transfusiones sanguíneas o ingesta de alcohol. No había historia familiar de hepatopatía. La paciente ingresó refiriendo molestias digestivas con dolorimiento abdominal y pesadez posprandial de 2-3 semanas de evolución, a los que en la última semana se habían añadido astenia intensa y pérdida del apetito. Asimismo, en los últimos días había notado coloración ictérica, orinas colúricas y prurito cutáneo generalizado. Negó la existencia de náuseas, vómitos o hipocolia. La exploración física fue normal salvo por una intensa ictericia cutaneomucosa. No se palpaban organomegalias y la exploración del hipocondrio derecho era indolora. Las exploraciones complementarias realizadas fueron: hemograma (hemoglobina de 1,73 mmol/l, hematocrito de 0,33l/l, volumen corpuscular medio de 94 fl, hemoglobina corpuscular media de 0,50 fmol/células, 5,8 ×106 /l de leucocitos con fórmula normal y 205 × 109 /l de plaquetas), estudio de coagulación, que fue normal, bioquímica (glucosa de 12,5 mmol/l, urea de 15 mmol/l, creatinina de 079 µmol/l, bilirrubina total de 90,6 µmol/l, bilirrubina directa de 58 µmol/l, lactatodeshidrogenasa de 473 U/l, aspartatoaminotransferasa de 212 U/l, alaninaaminotransferasa de 174 U/l, fosfatasa alcalina de 199 U/l y gammaglutamiltranspeptidasa de 442 U/l, con amilasa, sodio, potasio y calcio normales). La velocidad de sedimentación globular era de 30 mm/h y la cifra de hemoglobina glucosilada de 0,065 l/l. Las determinaciones séricas de títulos de anticuerpos frente a los virus de la hepatitis A, B y C, citomegalovirus, virus de Epstein-Barr, anticuerpos antinucleares, antimitocondriales, antimicrosómicos hepáticos de tipo 1, antimúsculo liso y antirreticulina fueron negativas, al igual que alfafetoproteína, antígeno carcinoembrionario y CA-19.9. Se realizaron radiografía de tórax y simple de abdomen, colonoscopia, ecografía, tomografía computarizada de abdomen y colangiorresonancia magnética, que fueron normales. Los resultados de las pruebas de función hepática continuaron empeorando, hasta llegar a un pico de bilirrubina total 256 µmol/l y de bilirrubina directa de 210 µmol/l, con aspartatoaminotransferasa de 1.198 U/l, alaninaaminotransferasa de 596 U/l, fosfatasa alcalina de 164 U/l y gammaglutamiltranspeptidasa de 260 U/l. No se realizó ningún tratamiento específico para la ictericia colestásica. Se había retirado la metformina en el momento del ingreso y para el control de la diabetes se utilizó insulina. Después de 2 meses la paciente se encontraba asintomática y las alteraciones analíticas habían mejorado; a los 3 meses eran normales. La paciente no ha presentado ningún síntoma atribuible a enfermedad hepática y las determinaciones analíticas son normales tras 9 meses de seguimiento.
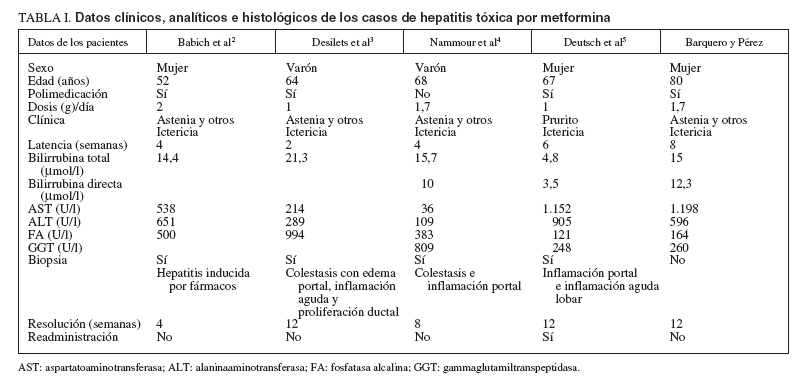
TABLA I. Datos clínicos, analíticos e histológicos de los casos de hepatitis tóxica por metformina
Se estableció el diagnóstico de hepatitis colestásica por fármacos al descartarse de forma razonable otras posibles etiologías. De todos los fármacos que recibía la paciente, la metformina parece el más probablemente responsable, siguiendo el protocolo propuesto por Nierenberg6 : a) existen otros casos publicados de hepatotoxicidad asociada a metformi-2-5 ; b) la latencia entre el inicio de la exposición hasta la aparición de los síntomas fue de pocas semanas3,4 , como en los otros casos publicados; c) el cuadro mejoró hasta su resolución tras la retirada del fármaco, y d) se excluyeron otras causas de hepatitis. En nuestro caso, no se procedió a la reintroducción del fármaco, ya que no habría estado justificada al existir otras opciones terapéuticas para el tratamiento de la diabetes. En los casos recogidos en la bibliografía se realizó estudio histológico hepático (tabla I), pero no se efectuó en el que aquí presentamos, ya que la paciente no prestó su consentimiento. La biopsia hepática no forma parte del protocolo de Nierenberg6 ni de otras escalas de diagnóstico de hepatitis por fármacos, y se realiza sólo para excluir otras causas de hepatopatía o con finalidad pronóstica, ya que usualmente carece de utilidad para el diagnóstico hepatotoxicidad7 . Se desconoce el mecanismo fisiopatológico de la hepatotoxicidad por metformina2 , ya que, aunque se concentra en el hígado, no presenta metabolismo hepático y se excreta inalterada por orina3 . Además, no existen datos de hepatotoxicidad dependiente de la dosis (pacientes que tomaron grandes dosis, generalmente con fines suicidas, no mostraron alteraciones en la bioquímica hepática), lo cual, junto con el período de latencia de varias semanas entre la introducción del fármaco y la aparición de la clínica, hace pensar en una reacción de tipo idiosincrásico2 . Aunque la incidencia sea muy baja, la hepatoxicidad por metformina debe tenerse en cuenta en los pacientes diabéticos que reciben metformina y desarrollan alteraciones hepáticas.