Con la incorporación de los inhibidores de proteasa (telaprevir y boceprevir) en el tratamiento de la hepatitis crónica por el virus C (VHC), asociado a interferón pegilado (peg-IFN) y ribavirina (RBV), se han incrementado las posibilidades de curación, elevándose significativamente las tasas de respuesta virológica sostenida (RVS), pero también han aumentado notablemente los efectos adversos1. Se han descrito entre un 3 y un 7% de reacciones adversas cutáneas graves (RACG) asociadas al telaprevir, como el síndrome de Stevens-Johnson (SSJ) y el síndrome de reacción cutánea con eosinofilia y síntomas sistémicos (DRESS)2, que son potencialmente mortales, por lo que se requiere la suspensión de la triple terapia antiviral. El DRESS se debe a una respuesta inmune específica a fármacos y está asociado a la reactivación del virus herpes. La mayoría de los pacientes se recuperan tras la suspensión del tratamiento en un periodo de semanas a meses. Presentamos el caso excepcional en la literatura de un paciente diagnosticado de DRESS secundario a triple terapia antiviral con telaprevir.
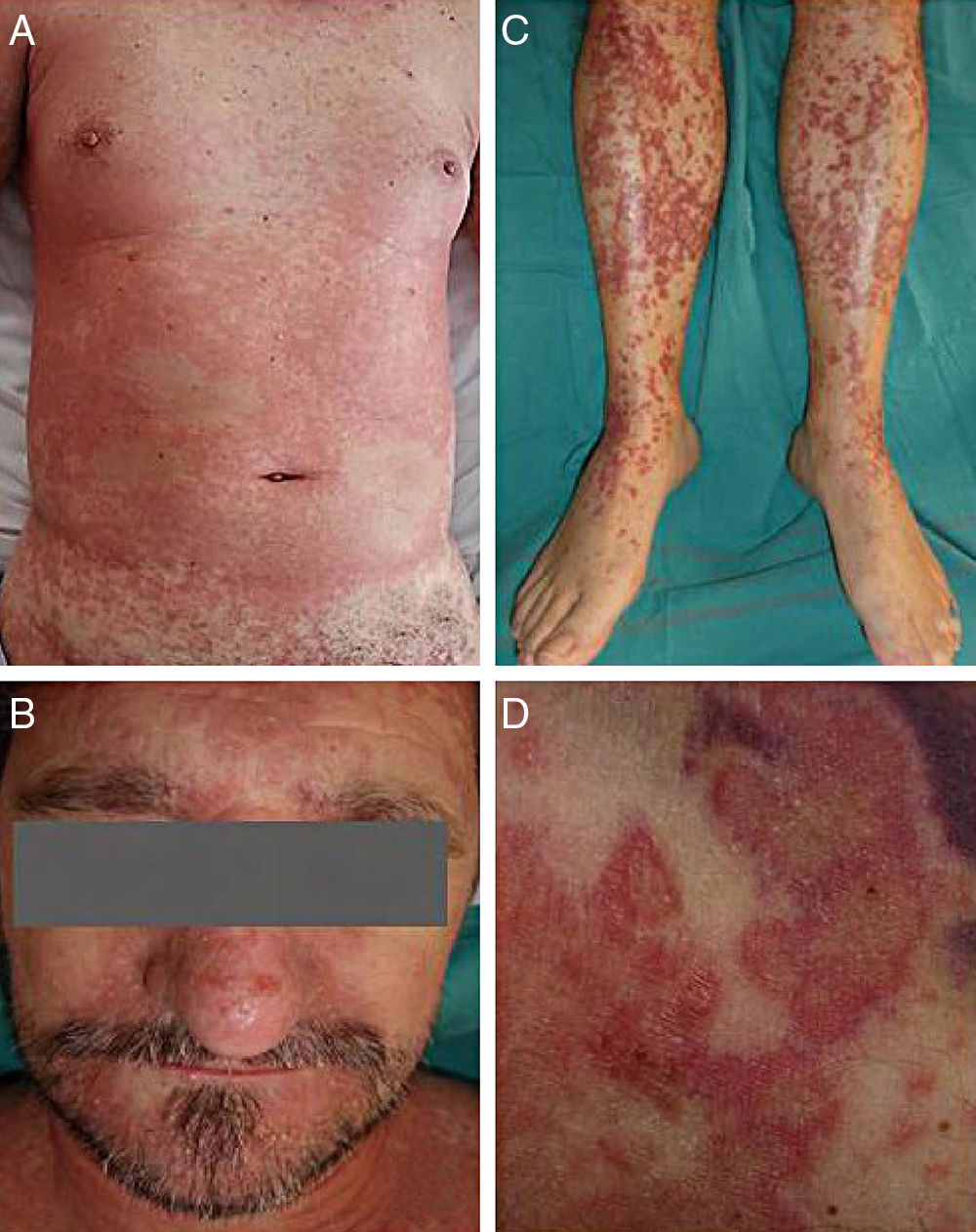
Se trata de un varón de 53 años, diagnosticado de hepatitis crónica C desde 1992, que no había recibido tratamiento antiviral previamente (naïve), genotipo 1b y polimorfismo de la IL-28B (rs 12979860) CT, con esteatosis hepática, fibrosis significativa F3 por fibroscan y RNA del VHC 7×106UI/ml. Inició la triple terapia antiviral con peg-IFN, RBV y telaprevir. En la semana 4 del tratamiento obtuvo respuesta viral rápida (RVR) con carga viral indetectable y presentó anemia que precisó descenso de dosis de RBV a 800mg/día. En la semana 8 de tratamiento acudió a urgencias por la aparición de lesiones maculopapulares eritematosas, levemente pruriginosas, de inicio en la región cervical con diseminación a tronco y extremidades superiores, además de febrícula (37,3°C), por lo que se pautó tratamiento con corticoides tópicos y antihistamínicos orales. Dos días después consultó nuevamente por fiebre de 39°C y extensión de las lesiones cutáneas alcanzando más del 70% de la superficie corporal, haciéndose confluentes, afectando los miembros inferiores y cara con pústulas en dorso nasal. En algunas zonas las placas adoptaron una morfología anular o en diana de borde eritematoso y centro más claro (en «escarapela») (fig. 1). Aparecieron adenopatías cervicales, axilares e inguinales no dolorosas. La analítica mostró los siguientes hallazgos: hemoglobina 10,9g/dl, leucocitos 7.500×103U/l, linfocitos 10,3%, eosinófilos 1.087×103U/l (14,5%), GGT145U/l, LDH 423U/l; las transaminasas, plaquetas y coagulación fueron normales.
Se ingresó al paciente a cargo del servicio de aparato digestivo y se suspendió la triple terapia antiviral. Durante el ingreso se descartó enfermedad infecciosa (hemocultivos y urocultivo negativos) y las serologías para los virus fueron: Epstein-Barr IgG (+), Paul-Bunnel (−), microarrays virus herpes 7 (−). La biopsia cutánea mostró espongiosis superficial dérmica con infiltrado linfocitario perivascular y exocitosis irregular de linfocitos (hematoxilina-eosina), compatible con reacción medicamentosa (fig. 2). Se inició tratamiento con metilprednisolona intravenosa a dosis de 1mg/kg/día. La eosinofilia alcanzó un pico de 37% en los primeros días del ingreso, la fiebre desapareció y las lesiones cutáneas fueron aclarándose. El paciente fue dado de alta con metilprednisolona oral en pauta descendente durante 3 semanas y corticoides tópicos, con resolución completa del cuadro al mes, y tanto el hemograma como el perfil hepático se normalizaron. No se observaron secuelas durante el seguimiento, sin embargo, el RNA del VHC fue detectable a los 6 meses tras la interrupción de la triple terapia antiviral.
La dermatitis relacionada con telaprevir se presenta entre el 36-60% de los pacientes tratados3; las reacciones cutáneas leves o moderadas no precisan la suspensión de la triple terapia y pueden ser tratadas utilizando principalmente emolientes/humectantes y corticoides tópicos, así como antihistamínicos tópicos o sistémicos. Según las guías clínicas, las erupciones cutáneas graves requieren la interrupción inmediata del telaprevir y si no hay mejoría o se agrava antes de 7 días, se debe interrumpir además la RBV y el peg-IFN. Algunos casos de afectación de más del 50% de la superficie corporal, sin signos RACG pueden ser manejados con corticoides tópicos sin interrupción de la triple terapia; sin embargo, se requiere la hospitalización del paciente y el seguimiento dermatológico estrecho para detectar precozmente los signos de progresión2,4. En nuestra experiencia, la rápida extensión del exantema, la presencia de fiebre y la sospecha de RACG, obligó a la suspensión del telaprevir y, posteriormente, del peg-IFN y la RBV en un plazo de 24h.
No existe un consenso mundial sobre la definición de RACG, sin embargo, son conocidas como condiciones dermatológicas de peligro mortal, atribuidas con frecuencia al uso de medicamentos. Las RACG asociadas a la terapia con telaprevir incluyen el SSJ, la necrólisis epidérmica tóxica, la pustulosis exantemática generalizada aguda y el DRESS, también conocido como hipersensibilidad inducida por drogas o hipersensibilidad multiorgánica retardada inducida por fármacos2,3. Los hallazgos histopatológicos de las biopsias de piel de un síndrome DRESS revelan espongiosis leve, un infiltrado linfocitario en la dermis superficial, predominantemente perivascular, con presencia variable de eosinófilos y edema dérmico5.
Existen 3 sistemas de diagnóstico y clasificación para el DRESS: 1) la clasificación de Bocquet et al.6, 2) la clasificación del grupo japonés para el diagnóstico del síndrome de hipersensibilidad inducido por drogas (SCAR-J)7, y 3) el Registro Europeo de Reacciones Adversas Cutáneas Graves (European Registry of Severe Cutaneous Adverse Reaction [RegiSCAR]). Esta última es la mayormente empleada en Europa y requiere del cumplimiento de los siguientes criterios: erupción cutánea, fiebre (>38°C), adenopatías en al menos 2 territorios ganglionares, afectación de órganos internos (hepática, renal o pulmonar) y alteraciones hematológicas; si se cumple con 6 o más criterios diagnósticos se clasifica como DRESS definitivo, y DRESS probable si cumple con menos de 6 criterios8. El paciente que presentamos cumplía 6 de 7 criterios de RegiSCAR, por lo que el diagnóstico fue DRESS definitivo. Desde los estudios de registro del telaprevir (fase III y IV) así como en el programa de acceso expandido internacional, se han descrito en la literatura mundial menos de 20 casos de DRESS, siendo el paciente presentado el primer caso descrito en España4,9,10.
El manejo inicial del DRESS relacionado con telaprevir se basa en una alta sospecha clínica ante una erupción cutánea que puede aparecer en cualquier momento una vez iniciado el tratamiento, aunque en la mayoría de los casos aparece entre 6 y 10 semanas después del inicio del tratamiento y progresa rápidamente11. Si se encuentra algún criterio confirmatorio, se debe valorar la interrupción del tratamiento completo (peg-IFN, RBV y telaprevir) y el paciente debe ser evaluado por un servicio de dermatología especializado. La mayoría de los pacientes se recuperan por completo en semanas o meses después de la retirada del fármaco2, sin embargo, la prevalencia de secuelas es desconocida, ya que no hay estudios de seguimiento a largo plazo de casos de DRESS secundario a telaprevir.