Presentamos el caso de un paciente de 77 años de edad, con antecedentes personales de hipertensión arterial controlada con medidas higiénico-dietéticas y un GIST yeyunal (c-kit positivo difuso, CD34 positivo focal, S100 negativo), diagnosticado a partir del estudio de una hemorragia digestiva baja en 2012. El paciente fue intervenido quirúrgicamente con éxito ese mismo año y se inició tratamiento con imatinib 400mg/día, pero presentó una recidiva en forma de metástasis hepática única, por lo que se aumentó la dosis a 800 mg/día en 2014. En agosto de 2019 se cambió el tratamiento a sunitinib por mala tolerancia gastrointestinal, presentando en ese momento enfermedad estable de acuerdo a los criterios RECIST.
El paciente acudió siete meses después de iniciar sunitinib a urgencias, derivado por su médico de atención primaria, por presentar un cuadro de astenia, malestar general e ictericia mucocutánea, sin ninguna otra clínica asociada (incluyendo encefalopatía), incluyendo fiebre, tiritona, dolor abdominal o alteración del ritmo gastrointestinal. Los valores analíticos previos a la aparición de la clínica, a su llegada a urgencias y durante el ingreso, pueden verse en la tabla 1. En estos datos analíticos podemos ver la predominancia del daño citolítico sobre el colestásico, con un índice R que está claramente por encima de cinco, umbral de definición de patrón citolítico.
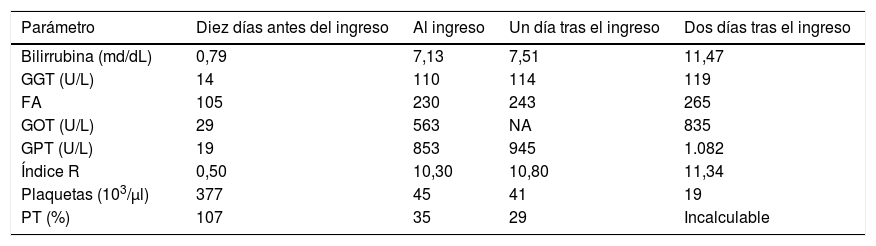
Valores analíticos antes y durante el ingreso. Puede verse un predominio claro de la citólisis (índice R > 5), congruente en las alteraciones descritas en el tratamiento con sunitinib
| Parámetro | Diez días antes del ingreso | Al ingreso | Un día tras el ingreso | Dos días tras el ingreso |
|---|---|---|---|---|
| Bilirrubina (md/dL) | 0,79 | 7,13 | 7,51 | 11,47 |
| GGT (U/L) | 14 | 110 | 114 | 119 |
| FA | 105 | 230 | 243 | 265 |
| GOT (U/L) | 29 | 563 | NA | 835 |
| GPT (U/L) | 19 | 853 | 945 | 1.082 |
| Índice R | 0,50 | 10,30 | 10,80 | 11,34 |
| Plaquetas (103/μl) | 377 | 45 | 41 | 19 |
| PT (%) | 107 | 35 | 29 | Incalculable |
El paciente negó en todo momento consumo alguno de alcohol u otros fármacos, incluyendo AINEs, paracetamol y antibióticos, así como productos de herboristería o cualquier otra sustancia. Las serologías de virus hepatótropos, incluyendo VHC, VHB, VHA, VHE, CMV, VEB, VES y VVZ resultaron todas negativas. Se realizó también una ecografía con Doppler vascular que descartó patología trombótica portal o suprahepática, así como progresión de la enfermedad neoplásica. El estudio de autoinmunidad realizado durante el ingreso y cuyos resultados se obtuvieron posteriormente fue negativo.
Se inició de manera empírica tratamiento con corticoides y perfusión de N-acetilcisteína ante la posibilidad de una etiología diferente a la toxicidad farmacológica. A pesar de ello, el paciente presentó un empeoramiento clínico y analítico progresivo, apareciendo encefalopatía hepática grado III-IV, fracaso renal AKI-III e insuficiencia respiratoria, falleciendo tres días después de llegar a urgencias. Dado el rápido empeoramiento del paciente, la edad avanzada y la patología oncológica activa, se decidió en sesión, de acuerdo con oncología médica, que el paciente no era candidato a trasplante ni a recambios plasmáticos en contexto de ensayo clínico.
El fallo hepático fulminante es una complicación rara, pero especialmente peligrosa en pacientes con enfermedad oncológica, dado que esto supone una contraindicación para el trasplante hepático, única opción terapéutica en muchos casos. Sunitinib es un inhibidor de tirosina-quinasa, que se usa en el tratamiento del carcinoma de células renales, tumores pancreáticos neuroendocrinos y tumores del estroma gastrointestinal. Un metaanálisis1 de 2013 reportó un 40% de pacientes con elevación de enzimas hepáticas (con patrón de citólisis predominantemente) durante el tratamiento con sunitinib, siendo de grado III/IV en un 3% de los pacientes.
No obstante, se han descrito ya hasta cinco casos de fallo hepático asociado al tratamiento con sunitinib, tres en pacientes con cáncer de células renales, uno en paciente con tumores estromales2 y otro en una paciente con cáncer de ovario3, siendo en estos dos últimos letal.De acuerdo con las escalas de Naranjo4 y CIOMS/RUCAM de probabilidad de efectos adversos y de hepatotoxicidad relacionada con fármacos, respectivamente, la reacción adversa se clasifica como «probable» en ambas, teniendo en cuenta que la rapidez y la gravedad de la misma no permitió evaluar la respuesta a la suspensión del fármaco, el uso de placebo ni la reintroducción del fármaco.
El fallo hepático por sunitinib es un efecto adverso raro, poco probable y que podría encuadrarse en las reacciones adversas de tipo B, esto es, idiosincrático, impredecible, dosis independiente y no relacionado con la farmacología del medicamento. Se ha propuesto un mecanismo de daño isquémico como causa del fallo hepático, más que un daño hepático directo como responsable del fallo hepático5.