La insuficiencia cardíaca (IC) es un problema de salud pública que genera una gran carga asistencial tanto hospitalaria como en atención primaria (AP).
La publicación de numerosos estudios sobre IC durante los últimos años ha supuesto un cambio de paradigma en el abordaje de este síndrome, en el que la labor de los equipos de AP va adquiriendo un protagonismo mayor. Las recientes guías publicadas por la Sociedad Europea de Cardiología han introducido cambios fundamentalmente en el manejo del paciente con IC. La nueva estrategia propuesta, con fármacos que reducen las hospitalizaciones y frenen la progresión de la enfermedad, debe ser ya una prioridad para todos los profesionales implicados. En este documento de posicionamiento se analiza una propuesta de abordaje basada en equipos multidisciplinares con el liderazgo de los médicos de familia, clave para proporcionar una atención de calidad a lo largo de todo el proceso de la enfermedad, desde su prevención hasta el final de la vida.
Heart failure (HF) is a public health problem that generates a large healthcare burden both in hospitals and in Primary Care (PC).
The publication of numerous studies about HF in recent years has led to a paradigm shift in the approach to this syndrome, in which the work of PC teams is gaining greater prominence. The recent guidelines published by the European Society of Cardiology have fundamentally introduced changes in the management of patients with HF. The new proposed strategy, with drugs that reduce hospitalizations and slow the progression of the disease, should now be a priority for all professionals involved. This position document analyzes a proposal for an approach based on multidisciplinary teams with the leadership of family doctors, key to providing quality care throughout the entire process of the disease, from its prevention to the end of the life.
La enfermedad cardiovascular ocupa más del 50% de las consultas diarias de atención primaria (AP)1. La insuficiencia cardíaca (IC) es un problema de salud pública, que aumenta año a año en todo el mundo y genera una gran carga asistencial, no solo en el ámbito hospitalario sino también en la AP. Su prevalencia aumenta de forma exponencial con la edad, pero también con la comorbilidad asociada2. En España la prevalencia de la IC en el año 2019 era del 1,89% de la población de 18 o más años, con una incidencia de 2,78/1.000 sujetos/año. Además, la IC es un problema de salud asociado con el envejecimiento y alcanza una prevalencia del 9% de los octogenarios3.
La IC es un síndrome multifactorial, con signos y síntomas específicos. La identificación de marcadores funcionales como la fracción de eyección favorece su adecuado diagnóstico y la mejor estrategia de tratamiento2. En la actualidad se dispone de herramientas de diagnóstico y tratamiento que han cambiado la historia del manejo del paciente con IC, y que son de especial utilidad en AP, la cual puede y debe tomar el protagonismo que le corresponde en el diagnóstico y tratamiento, pese a la heterogeneidad del propio síndrome2,4.
Las guías de práctica clínica (GPC) constituyen un elemento clave de la medicina asistencial, que facilita a los médicos y otros profesionales de la salud aquellas recomendaciones basadas en la evidencia científica más actualizada, favoreciendo mejorar la práctica clínica asistencial y disminuir la incertidumbre. Durante los últimos años se ha vivido una auténtica revolución en el ámbito de la IC, con la publicación de GPC, numerosos ensayos clínicos aleatorizados, así como metaanálisis y revisiones sistemáticas. Cuando se genera tal cuerpo de evidencia en tan poco tiempo es difícil asimilar todos los cambios, sobre todo en el ámbito de la AP, donde la cantidad de enfermedades que se atiende es muy variada. Además, las GPC en general, y en especial las publicadas por la Sociedad Europea de cardiología (ESC) en 20215, en muchas ocasiones generan dudas respecto a su aplicación clínica en el mundo real, por lo que se hace imprescindible realizar una lectura práctica y un análisis crítico de las recomendaciones que plantean.
Por otra parte, el exceso de información, la rapidez en la implementación de nuevas estrategias de tratamiento, junto a las consecuencias sociosanitarias que se padecen desde marzo de 2020 como consecuencia de la pandemia por la COVID-19, genera gran incertidumbre e incluso puede que desconfianza para implementar las directrices que se marcan y su cumplimiento en la práctica diaria. Todo ello hace necesario establecer una estrategia encaminada a clarificar y simplificar los cambios de las GPC, sintetizando la información de estas y, de esta forma, facilitar su implementación en el ámbito de la AP.
Se hace necesario que las sociedades científicas de AP, ámbito en el cual la prevalencia de IC es muy relevante, evalúen las directrices internacionales de la IC, sobre todo en momentos en los que se modifica sustancialmente el manejo de esta enfermedad. El presente documento tiene como objetivo analizar los cambios y novedades propuestos en las recién publicadas guías europeas para el diagnóstico y tratamiento de la insuficiencia cardíaca aguda y crónica (2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure)5, en consonancia con la estrategia puesta en marcha por la Junta Directiva Nacional de la Sociedad Española de Médicos de Atención Primaria (SEMERGEN). Este consenso sobre el abordaje diagnóstico y el manejo terapéutico del paciente con IC en AP surge sobre la base de la última evidencia, y está dirigido a todos los médicos de familia, dado que la IC supone uno de los motivos más frecuentes de consulta, con un elevado coste en recursos materiales y humanos.
MetodologíaEl presente documento de consenso ha sido elaborado por un comité de redacción, constituido por miembros del Grupo de Trabajo de Hipertensión Arterial y Enfermedad Cardiovascular de SEMERGEN, todos ellos expertos en el manejo clínico del paciente con IC en el contexto de AP y Cardiología. Para ello, los autores han revisado las últimas guías europeas de insuficiencia cardíaca5 y alguna otra evidencia científica relevante, algunos temas relacionados con el manejo diagnóstico y terapéutico en AP y cardiología.
Los autores, miembros del Grupo de Trabajo de Hipertensión Arterial y Enfermedad Cardiovascular de la SEMERGEN, manifiestan que esta es la opinión de este grupo de trabajo, estimando que las reflexiones y recomendaciones que se plantean están adaptadas a las necesidades del médico de familia que diagnostica y trata a estos pacientes diariamente en su consulta. Las limitaciones son las propias de un documento de opinión de expertos, que han analizado la evidencia más reciente, intentando exponer en una lectura breve el posicionamiento de una sociedad científica conocedora de la AP en España.
Magnitud del problema de la insuficiencia cardíaca en EspañaLa IC constituye un importante problema de salud pública en todo el mundo, estimándose que afecta a más de 37,7millones de personas6. Presenta una alta morbimortalidad, confiriendo un aumento en la carga de enfermedad de los pacientes. En España esta enfermedad consume numerosos recursos sanitarios. Se estima que el coste total medio por paciente con IC en el año 2010 osciló entre 12.995 y 18.220euros, dependiendo del escenario elegido. La partida de mayor peso fue la de cuidados no profesionales (59,1-69,8% del coste total), seguido del gasto sanitario (26,7-37,4%) y los cuidados profesionales (3,5%). De los costes sanitarios los originados a nivel hospitalario acaparan su mayor partida seguida por los debidos a la medicación. Asimismo, se identificaron diferencias significativas de costes entre los pacientes en clase ii de la NYHA y los de clase iii-iv7. Asimismo, se identificaron diferencias significativas de costes entre los pacientes en clase iide la NYHA y los de clase iii-iv7.
La incidencia de IC en los países europeos varía entre 3 y 5 casos por 1.000 personas-año, dependiendo en gran medida de la población estudiada y de los criterios diagnósticos empleados4,8. Aunque parece estar disminuyendo en países desarrollados (por un mejor manejo de la ECV), todavía existe un importante porcentaje de población no diagnosticada4. En España, pese a no tener una incidencia tan elevada, sí presenta tasas de hospitalización muy altas9. Por ello, mejorar el tratamiento con el empleo de fármacos que reduzcan la hospitalización y mejoren el pronóstico, así como un abordaje multidisciplinar y con continuidad asistencial estructurada (atención primaria-hospitalaria) pueden resultar fundamentales para reducir la carga de la IC.
Concepto y clasificación de la insuficiencia cardíacaEn las últimas guías de la ESC4 se define la IC como un síndrome clínico que se caracteriza por síntomas cardinales (por ejemplo disnea, edema en los tobillos y fatiga) que puede estar acompañado de signos (por ejemplo elevación de presión venosa yugular, crepitantes pulmonares y edema periférico) causados por una anomalía estructural y/o funcional del corazón que provoca una reducción en el gasto cardíaco y/o elevación de las presiones intracardíacas en reposo o durante el ejercicio.
Se emplean numerosos criterios para clasificar correctamente al paciente con IC, tal y como se detalla en la tabla 1.
Criterios para clasificar correctamente al paciente con insuficiencia cardíaca
| Criterio de clasificación | |
|---|---|
| Según el ventrículo afectado | Izquierdo, derecho o biventricular |
| Fracción de eyección del ventrículo izquierdo (FEVI) | FEVI reducida:≤40%.FEVI levemente reducida: 41-49%FEVI preservada:>50%. |
| Clase funcional según la New York Heart Association (NYHA) | I, II, III, IV |
| Estado evolutivo | A, B, C y D |
| Etiología | Isquémica, miocardiopatía dilatada, hipertensión arterial, valvular, congénita, miocardiopatía hipertrófica, miocardiopatía restrictiva, miocardiopatía |
Adaptado y modificado de Seferovic et al.10.
Tradicionalmente, la IC se ha dividido en distintos fenotipos basados en la medición de la fracción de eyección del ventrículo izquierdo (FEVI). Sin embargo, dado que la medición de la FE por ecocardiografía está sujeta a variabilidad, la ESC ha propuesto la siguiente clasificación4 (tabla 2).
Clasificación de la insuficiencia cardíaca según la fracción de eyección del ventrículo izquierdo
| Tipos de IC | IC FEr | IC FElr | IC FEp |
|---|---|---|---|
| Criterios | Síntomas±signos | Síntomas±signos | Síntomas±signos |
| FEVI≤40% | FEVI 41-49% | FEVI≥50% | |
| - | - | Evidencia objetiva de anormalidades cardíacas estructurales y/o funcionales consistentes con la presencia de disfunción diastólica del VI/presiones de llenado del VI elevadas y/o péptidos natriuréticos |
FEVI: fracción de eyección del ventrículo izquierdo; IC: Insuficiencia cardíaca; IC FElr: insuficiencia cardíaca con fracción de eyección del ventrículo izquierdo levemente reducida; IC FEp: insuficiencia cardíaca con fracción de eyección del ventrículo izquierdo preservada; IC FEr: insuficiencia cardíaca con fracción de eyección del ventrículo izquierdo reducida; VI: ventrículo izquierdo.
Modificada de Wagner y Dimmeler4.
Para cuantificar la severidad de la alteración funcional en la IC, la clasificación más utilizada es la de la NYHA (New York Heart Association), que identifica 4 clases funcionales (i, ii, iii y iv) dependiendo de los síntomas atribuibles a la IC y de la limitación a la actividad física4 (tabla 3).
Clasificación de la insuficiencia cardíaca según la New York Heart Association
| Clase I | Sin limitación de la actividad física. El ejercicio físico normal no causa fatiga, palpitaciones o disnea |
| Clase II | Ligera limitación de la actividad física, sin síntomas en reposo. La actividad física normal causa fatiga, palpitaciones o disnea |
| Clase III | Ligera limitación de la actividad física, sin síntomas en reposo. La actividad física normal causa fatiga, palpitaciones o disnea |
| Clase IV | Incapacidad de realizar actividad física sin molestias. Los síntomas están presentes hasta en reposo. Si se realiza alguna actividad física, aumentan los síntomas |
Modificada de Wagner y Dimmeler4.
Diversas sociedades han elaborado un informe sobre la clasificación universal de la IC, estableciendo una nueva clasificación de la IC en 4 estadios evolutivos (A, B, C y D), evidenciando el carácter progresivo y prevenible de la enfermedad10 (tabla 4). De estos los estadios A y B no son propiamente IC, sino estadios preclínicos, aunque su consideración es fundamental para ayudar a la identificación y al tratamiento correcto de estos pacientes con alto riesgo de IC futura. Si bien el papel de la AP es importante en todas las fases de la IC, en las fases subclínicas (A y B) su labor es crucial.
Estadios evolutivos de la insuficiencia cardíaca
| Criterio de clasificación | |
|---|---|
| A (con riesgo de IC) | Pacientes con alto riesgo de desarrollar IC por la presencia de comorbilidades fuertemente asociadas al desarrollo de IC (hipertensión arterial, diabetes mellitus, enfermedad cardiovascular, historial de tratamiento cardiotóxico, historial de cardiomiopatía), pero sin síntomas, signos, ni marcadores estructurales o genéticos de enfermedad cardíaca |
| B (pre-IC) | Pacientes sin síntomas y/o signos de IC, pero con evidencia de uno de los siguientes criterios:Enfermedad cardíaca estructuralFunción cardíaca anormalElevación de péptidos natriuréticos o elevación de niveles de troponinas |
| C (IC) | Pacientes con síntomas y/o signos de IC causados por anormalidades cardíacas funcionales y/o estructurales:IC en remisiónIC permanente |
| D (IC avanzada) | Síntomas y/o signos severos de IC, hospitalizaciones recurrentes a pesar de tratamiento optimizado, refractariedad o intolerancia al tratamiento. Dichos pacientes precisan de terapias avanzadas, como trasplante, soporte circulatorio mecánico o cuidados paliativos |
IC: insuficiencia cardíaca.
Adaptada y modificada de Seferovic et al.10.
La IC es un síndrome clínico que consta de signos y síntomas causados por una anomalía estructural y/o funcional del corazón, que da como resultado presiones intracardíacas elevadas y/o un gasto cardíaco inadecuado en reposo y/o durante el ejercicio4,11.
El diagnóstico de la IC debe hacerse de manera secuencial, comenzando con la valoración de la historia clínica que incluya los antecedentes sanitarios, anamnesis y adherencia terapéutica. La consideración de los antecedentes y enfermedades concomitantes del paciente facilita el manejo diagnóstico de la IC. Entre los antecedentes más relevantes destacan la cardiopatía isquémica, la hipertensión arterial (HTA), la diabetes mellitus (DM), la enfermedad renal crónica (ERC), el abuso de alcohol, la quimioterapia o los antecedentes de miocardiopatía, entre otros. La presencia de uno o varios de ellos aumenta la posibilidad de que, ante una clínica típica, el paciente presente IC4.
La etapa fundamental en el diagnóstico de la IC es la detección de la presencia de síntomas y/o signos más o menos típicos y/o específicos (tabla 5)4,10,11. El proceso diagnóstico puede resultar complejo debido a que estas manifestaciones también pueden estar presentes en otras situaciones clínicas. La disnea de esfuerzo es el único síntoma que tiene una alta sensibilidad (89%) pero moderada especificidad (51%) para el diagnóstico de la IC12. La disnea puede ser sutil en pacientes con IC y FEVI preservada (IC-FEp), en ocasiones solo provocada por el esfuerzo, o puede atribuirse erróneamente a otras morbilidades pulmonares o sistémicas. La ortopnea es bastante específica pero poco sensible. Por otra parte, los signos de la IC pueden estar enmascarados por la adiposidad, y el aumento del volumen central también puede ser debido a hipertensión pulmonar12.
Síntomas y signos de insuficiencia cardíaca
| Síntomas | Signos |
|---|---|
| Típicos | Más específicos |
| Disnea. Ortopnea | Presión venosa yugular aumentada |
| Disnea paroxística nocturna | Reflujo hepatoyugular |
| Tolerancia al ejercicio disminuida | Tercer tono cardíaco (ritmo de galope) |
| Fatiga, astenia, mayor tiempo de recuperación tras el ejercicio | Desplazamiento lateral del impulso apical |
| Hinchazón de tobillo u otras zonas | Respiración de Cheyne-Stokes |
| Menos típicos | Menos específicos |
| Tos nocturna | Aumento de peso (>2 kg/semana) |
| Sibilancias | Pérdida de peso (insuficiencia cardíaca avanzada). Caquexia |
| Sensación de hinchazón | Edemas periféricos (maleolar, sacro, escroto) |
| Pérdida de apetito | Soplo cardíaco. Taquicardia. Pulso irregular |
| Confusión (especialmente en ancianos) | Presión de pulso estrecha |
| Decaimiento. Depresión | Crepitantes pulmonares |
| Palpitaciones | Derrame pleural (matidez a la percusión en bases) |
| Mareo. Síncope | Taquipnea (>16rpm) |
| Bendopnea | Hepatomegalia. Ascitis |
| Extremidades frías. Oliguria |
Modificada de Wagner y Dimmeler4.
La semiología clínica también ayuda a sospechar el diagnóstico de IC y clasificar a los pacientes con IC según la clase funcional, atendiendo a la severidad de los síntomas y su tolerancia al ejercicio (criterios NYHA)4,13 (tabla 3).
La demostración de las lesiones cardíacas estructurales o funcionales sirve para precisar el diagnóstico y ayuda a valorar la progresión y gravedad de la IC. La clasificación de la American College of Cardiology/American Heart Association (ACC/AHA) categoriza en 4 etapas la IC según el desarrollo de los síntomas y los cambios estructurales10,11 (tabla 4).
La reciente definición universal de la IC precisa que, además de la presencia de los signos y/o síntomas, el diagnóstico de la IC se corrobore con concentraciones elevadas de péptidos natriuréticos (PN) y/o la evidencia objetiva de congestión pulmonar cardiogénica o sistémica mediante modalidades de diagnóstico de imágenes o medición hemodinámica en reposo o con provocación10.
En consecuencia, se necesitan pruebas complementarias adicionales para llegar al diagnóstico de IC, y esto en ocasiones dificulta el diagnóstico4,11,12,14,15. En un estudio realizado en España, en el que se incluyeron mujeres ≥65años con HTA con 6 o más meses de evolución, mientras que el 19% presentaba IC confirmada el 21% presentaba IC no reconocida por los clínicos16.
Siempre hay que realizar un electrocardiograma (ECG) de 12 derivaciones, ya que aporta información muy relevante y tiene un elevado valor predictivo negativo (VPN). Un ECG completamente normal puede predecir que el diagnóstico de IC sea poco o nada probable4. El ECG puede revelar una comorbilidad frecuente de la IC como es la fibrilación auricular (FA), identificar una IC de novo o un empeoramiento clínico de la IC. La presencia de ondas Q puede orientar hacia un IM previo. La hipertrofia ventricular izquierda puede indicar una HTA mal controlada o miocardiopatía hipertrófica, y un bloqueo completo de rama izquierda obliga a descartar la presencia de cardiopatía estructural. Además, su presencia se asocia con un peor pronóstico en los pacientes con IC4,17,18.
Si tras la valoración de la historia clínica, exploración física y ECG, existe sospecha de IC, se deben evaluar las concentraciones plasmáticas de PN si están disponibles4, debido a que están elevadas en pacientes con IC, y son los biomarcadores más importantes de apoyo para la detección, diagnóstico y evaluación del pronóstico de la IC4,11. La elevación de los PN se asocia con un aumento en el riesgo de muerte y hospitalización en pacientes con IC19.
Los VPN de los niveles umbrales de los PN (PN tipo B [BNP]<35 pg/ml; fragmento aminoterminal del BNP [NT-proBNP]<125pg/ml) son altos y muy similares, tanto en el entorno agudo como en el no agudo, pero los valores predictivos positivos (VPP) son más bajos en el contexto agudo y en el crónico. Esto significa que, en pacientes con síntomas sugestivos de IC, es muy recomendable la determinación de los PN como prueba diagnóstica inicial, debido a que valores inferiores a los de corte descartan, con una alta probabilidad, el diagnóstico de IC y FEVI reducida (IC-FEr), aunque no excluyen el diagnóstico de IC-FEp. En el ámbito ambulatorio esto adquiere especial relevancia cuando se desconoce la etiología de la disnea de nueva aparición, disminuyendo el riesgo de falsos diagnósticos de IC y, por lo tanto, la no indicación de ecocardiografía4,20.
Los valores elevados de PN (BNP≥35 pg/ml; NT-proBNP≥125pg/ml) facilitan el diagnóstico de IC, sobre todo en pacientes con clínica no aguda o cuando el ecocardiograma no está disponible a corto plazo. La determinación de NT-proBNP es mejor para detectar IC-FEr que IC-FEp, y en personas con 70 o más años el umbral de 125pg/ml es más preciso para detectar o excluir la IC14.
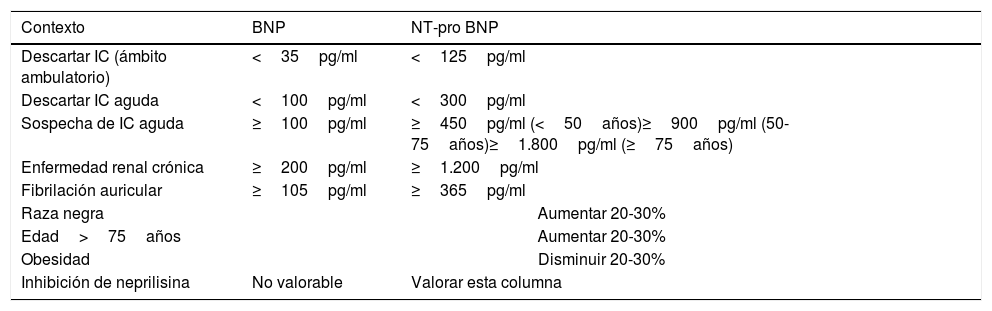
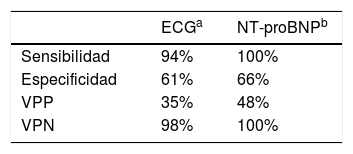
Estos umbrales pueden tener menor especificidad en pacientes mayores, con FA o con ERC, por lo que se suele recomendar unos umbrales un 25% más altos para diagnosticar la IC21 (tabla 6). En la tabla 7 se describen la sensibilidad, especificidad y valores predictivos, tanto del ECG como del NT-proBNP22,23.
Umbrales de los péptidos natriuréticos tipo B
| Contexto | BNP | NT-pro BNP |
|---|---|---|
| Descartar IC (ámbito ambulatorio) | <35pg/ml | <125pg/ml |
| Descartar IC aguda | <100pg/ml | <300pg/ml |
| Sospecha de IC aguda | ≥100pg/ml | ≥450pg/ml (<50años)≥900pg/ml (50-75años)≥1.800pg/ml (≥75años) |
| Enfermedad renal crónica | ≥200pg/ml | ≥1.200pg/ml |
| Fibrilación auricular | ≥105pg/ml | ≥365pg/ml |
| Raza negra | Aumentar 20-30% | |
| Edad>75años | Aumentar 20-30% | |
| Obesidad | Disminuir 20-30% | |
| Inhibición de neprilisina | No valorable | Valorar esta columna |
BNP: péptido natriurético tipo B; IC: insuficiencia cardíaca; NT-proBNP: fragmento N-terminal del propéptido natriurético tipo B.
Modificada de Kelder et al.21.
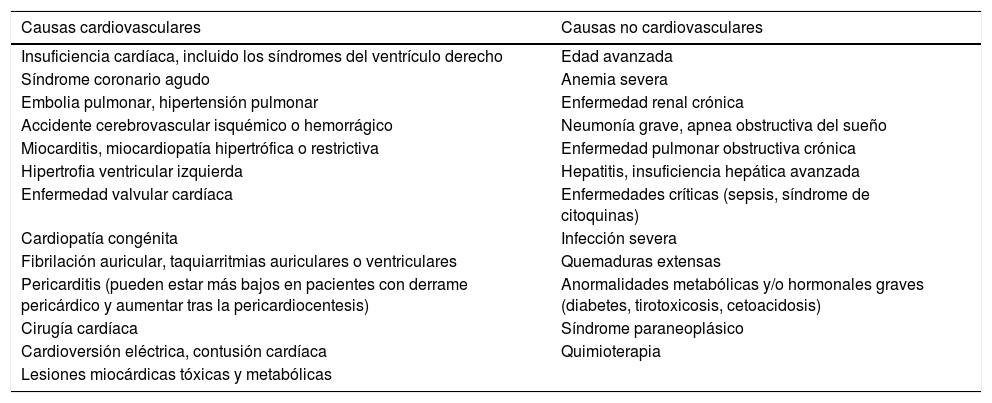
Por otra parte, se debe tener presente que las concentraciones plasmáticas elevadas de los PN se han asociado con una amplia variedad de enfermedades cardíacas y no cardíacas que se deben tener en cuenta al realizar el diagnóstico diferencial24 (tabla 8).
Causas que aumentan los péptidos natriuréticos tipo B
| Causas cardiovasculares | Causas no cardiovasculares |
|---|---|
| Insuficiencia cardíaca, incluido los síndromes del ventrículo derecho | Edad avanzada |
| Síndrome coronario agudo | Anemia severa |
| Embolia pulmonar, hipertensión pulmonar | Enfermedad renal crónica |
| Accidente cerebrovascular isquémico o hemorrágico | Neumonía grave, apnea obstructiva del sueño |
| Miocarditis, miocardiopatía hipertrófica o restrictiva | Enfermedad pulmonar obstructiva crónica |
| Hipertrofia ventricular izquierda | Hepatitis, insuficiencia hepática avanzada |
| Enfermedad valvular cardíaca | Enfermedades críticas (sepsis, síndrome de citoquinas) |
| Cardiopatía congénita | Infección severa |
| Fibrilación auricular, taquiarritmias auriculares o ventriculares | Quemaduras extensas |
| Pericarditis (pueden estar más bajos en pacientes con derrame pericárdico y aumentar tras la pericardiocentesis) | Anormalidades metabólicas y/o hormonales graves (diabetes, tirotoxicosis, cetoacidosis) |
| Cirugía cardíaca | Síndrome paraneoplásico |
| Cardioversión eléctrica, contusión cardíaca | Quimioterapia |
| Lesiones miocárdicas tóxicas y metabólicas |
Modificada de Davies et al.22.
El ecocardiograma transtorácico es una prueba clave en el diagnóstico de la IC. Además de la medición de la FEVI, la ecocardiografía también proporciona información del tamaño de la cámara, la presencia de hipertrofia de ventrículo izquierdo excéntrica o concéntrica, anomalías segmentarias del movimiento de la pared, función sistólica del ventrículo derecho, hipertensión pulmonar, valvulopatías, función diastólica o derrame pericárdico. La FEVI debe medirse, no estimarse, para clasificar y valorar la gravedad de la IC y facilitar el tratamiento farmacológico más adecuado según esté reducida o preservada4,25 (tabla 2).
Tras el diagnóstico de IC se considerará la realización de pruebas diagnósticas adicionales para identificar las posibles causas de la IC o de su eventual empeoramiento clínico, para valorar comorbilidades y para iniciar o titular la medicación.
Es importante realizar una analítica sanguínea para detectar alteraciones y/o comorbilidades de la IC que incluya hemograma, ferritina, saturación de transferrina, creatinina, tasa de filtración glomerular estimada, electrolitos, HbA1c, función hepática y tiroidea5. Igualmente, es recomendable la realización de una radiografía de tórax para descartar otras causas de disnea, y/o para observar cardiomegalia u otros signos radiológicos de IC5.
El médico de AP debe plantear una estrategia de manejo de la IC con las herramientas diagnósticas que tenga disponibles. Desafortunadamente, los PN no están accesibles en muchos departamentos/áreas de salud, y la ecocardioscopia es todavía poco o nada utilizada en AP. Por ello, el médico de AP debe actuar según las condiciones de cada centro y consensuar protocolos locales con los servicios de cardiología y/o medicina interna que sean claros y realistas, con el fin de precisar el diagnóstico de IC de la forma más eficiente y rápida posible.
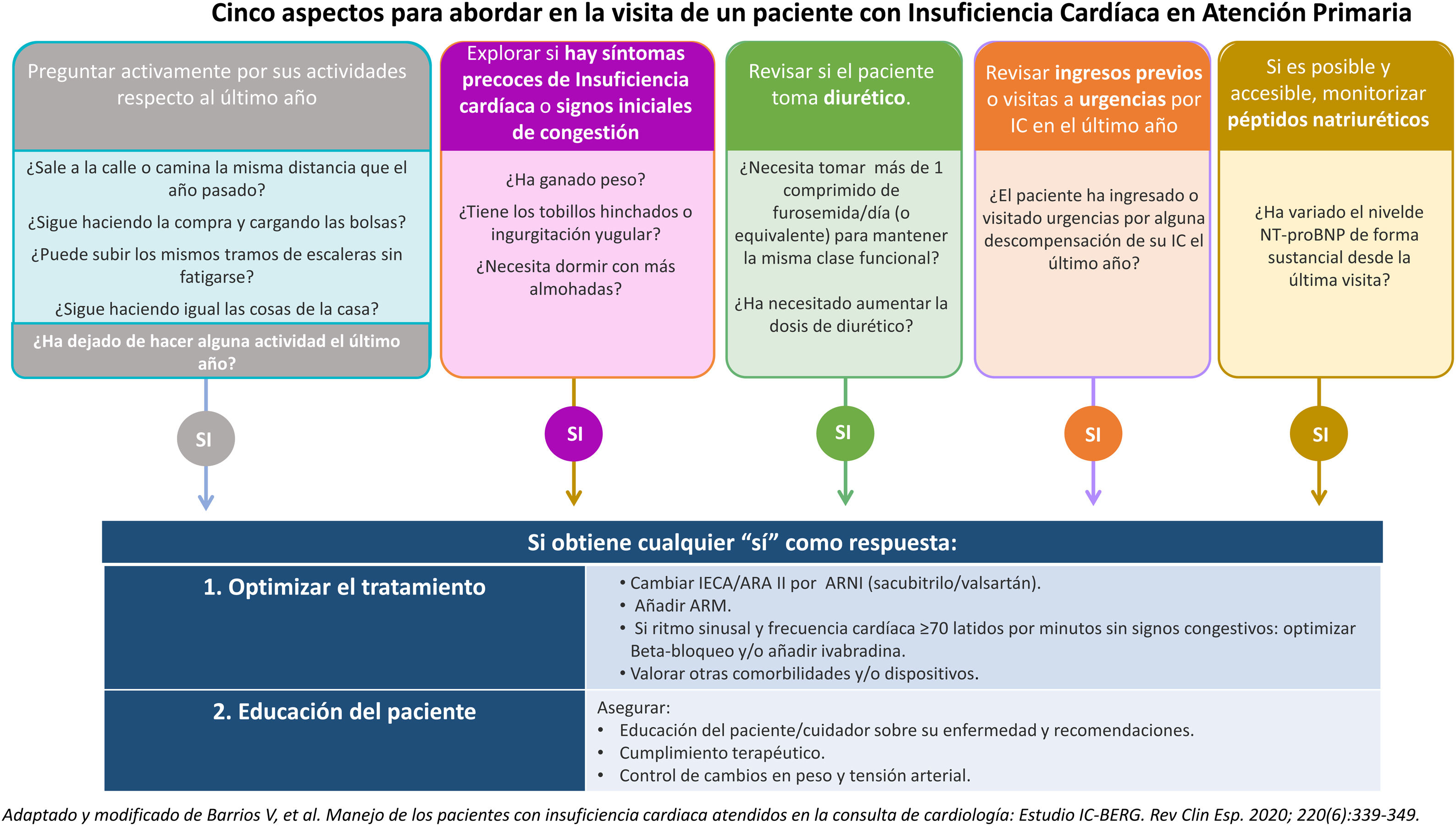
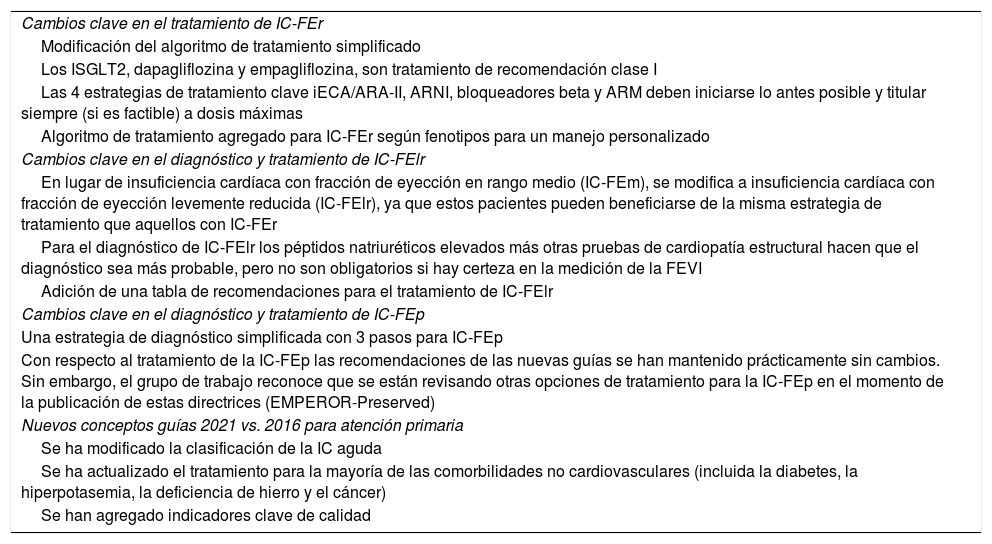
Detección de pacientes falsamente estables en atención primariaLa IC es una enfermedad que evoluciona de manera progresiva. Sin embargo, la optimización de su manejo diagnóstico y terapéutico puede enlentecer la velocidad de deterioro de la función cardíaca. La supuesta idea de la estabilidad de la IC puede inducir al médico de familia a mantener una inercia terapéutica que conviene corregir. Por lo tanto, la detección desde AP de estos pacientes «falsamente estables» es fundamental para reducir futuras hospitalizaciones.
Para ello, es de utilidad incluir el esquema de 5 preguntas básicas propuesto en el proyecto ICEBERG26 (fig. 1). Aunque este estudio fue desarrollado en el ámbito de consultas de cardiología, su fácil aplicación y la gran información que aporta lo convierten en una herramienta de gran utilidad igualmente para el médico de familia.
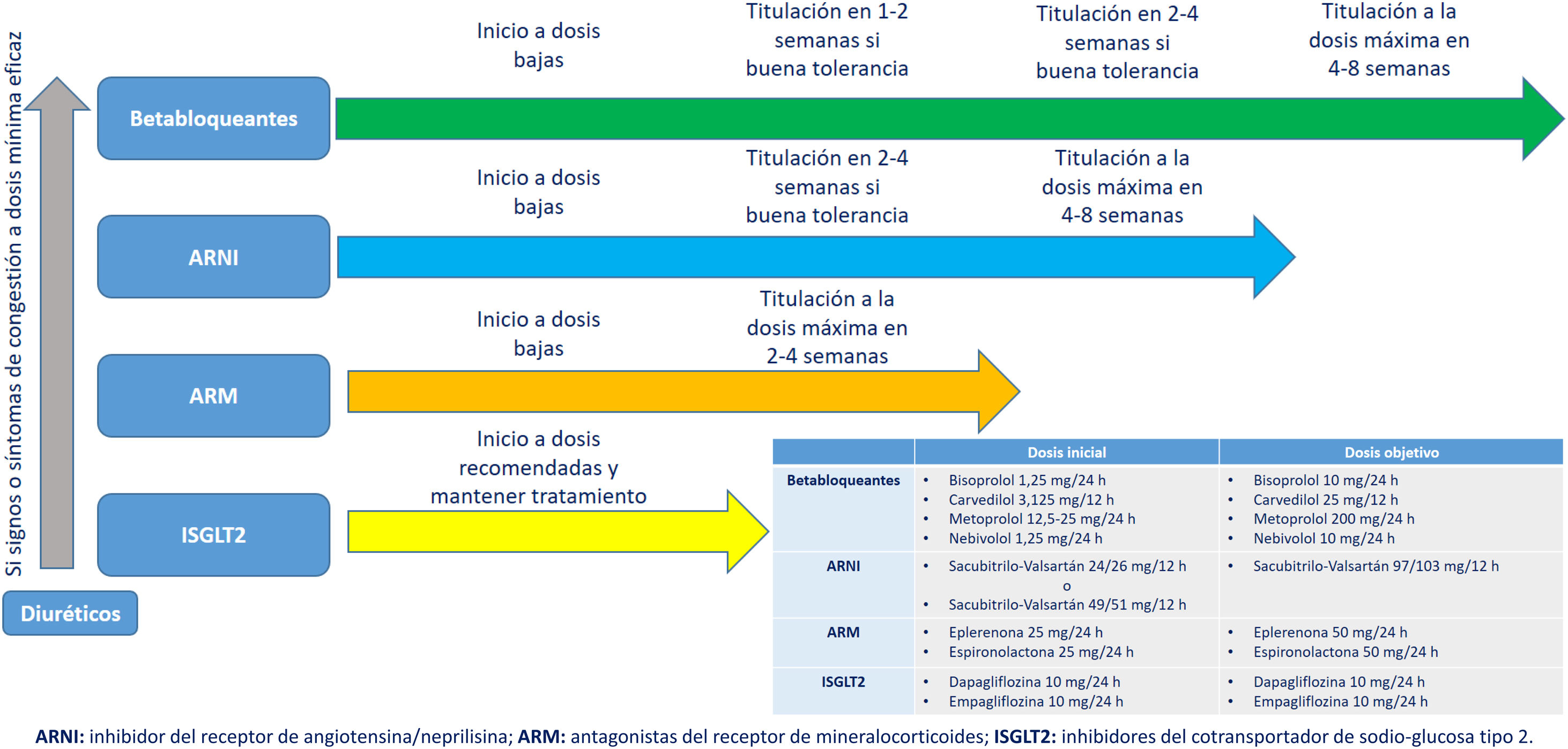
Tratamiento farmacológico de la insuficiencia cardíaca con fracción de eyección del ventrículo izquierdo reducidaFármacos de primera línea en insuficiencia cardíaca-fracción de eyección reducidaEn la actualidad la estrategia del manejo farmacológico que ha demostrado mayores beneficios clínicos en pacientes con IC-FEr (FEVI<40%) incluye 4 grupos terapéuticos: el inhibidor dual de neprilisina y angiotensina sacubitrilo/valsartán o inhibidores de la enzima convertidora de angiotensina (IECA) o antagonistas del receptor de angiotensina ii(ARA-II), bloqueadores beta, antagonistas de los receptores mineralcorticoides (ARM) (espironolactona/epleronona) e inhibidores del cotransportador sodio-glucosa tipo 2 (ISGLT-2) (dapagliflozina/empagliflozina)5.
Existe un amplio consenso en la necesidad de iniciar los 4 grupos de fármacos lo más precozmente posible, aunque no sobre cuál debe ser el orden de inicio de cada fármaco, dejando esta decisión a criterio del clínico en función de las características individuales de cada paciente27–29. El médico de familia se encuentra en una situación privilegiada para detectar pacientes tanto con IC de novo como aquellos ya diagnosticados y que precisen optimizar el tratamiento.
Numerosos estudios han constatado la superioridad de sacubitrilo/valsartán frente a enalapril en cuanto a reducción de tiempo hasta el primer ingreso y mortalidad cardiovascular en pacientes ambulatorios30,31, reducción de niveles de NT-proBNP, rehospitalizaciones y efecto beneficioso precoz sobre el remodelado cardíaco frenando la progresión de la enfermedad32.
Otros beneficios de sacubitrilo/valsartán son la mejoría en la calidad de vida32, la reducción en la caída del filtrado glomerular33 y la reducción de la necesidad de uso de diuréticos de asa34.
En función del volumen de evidencia publicada y de la experiencia acumulada en la práctica clínica, el sacubitrilo/valsartán debe considerarse como fármaco de primera línea en el tratamiento de pacientes con IC-FEr, estuvieran o no tratados previamente con bloqueadores del sistema renina angiotensina (IECA o ARA-II).
Los IECA han sido considerados clásicamente el primer escalón en el tratamiento de la IC-FEr, por ser el primer grupo terapéutico que demostró reducción de la morbimortalidad y de la sintomatología35–37. En la actualidad deberían quedar limitados como opción alternativa en caso de intolerancia o contraindicación para el uso del sacubitrilo/valsartán.
Los bloqueadores beta38–43, ARM (espironolactona/eplerenona)44,45, IECA y el sacubitrilo/valsartán30–37 han demostrado reducción de morbimortalidad y mejoría clínica. En todos estos grupos terapéuticos la titulación hasta alcanzar la dosis objetivo o la dosis máxima tolerada debe realizarse de forma activa por parte del médico de familia, en consenso con el cardiólogo o internista de referencia en su área o departamento de salud.
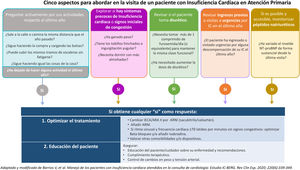
El último grupo en incorporarse a la terapia base de los pacientes con IC-FEr han sido los ISGLT-2. Los mecanismos implicados en su beneficio en la IC son complejos y continúan actualmente siendo objeto de múltiples estudios.
Un metaanálisis de los 3 estudios pivotales de empagliflozina, canagliflozina y dapagliflozina (EMPA-REG46, CANVAS47 y DECLARE-TIMI48 respectivamente) indicó que los iSGLT2 reducen en un 32% el riesgo de hospitalización por IC en pacientes diabéticos. Esta reducción es independiente de la presencia de historia conocida de IC y es mayor cuanto peor es la función renal basal49.
DAPA-HF fue el primer estudio en evaluar la eficacia de un iSGTL2 en pacientes con IC y FEVI reducida en pacientes diabéticos y no diabéticos50. Se demostró, a favor de la dapagliflozina, una reducción del 26% del combinado de mortalidad cardiovascular y hospitalización por IC en pacientes con tratamiento médico optimizado, siendo estos resultados observados de forma precoz tras el inicio del tratamiento e independientes de la presencia o no de DM. Igualmente se demostró una reducción en la mortalidad por todas las causas, mejoría en la capacidad funcional, sintomatología y calidad de vida. Este estudio supuso una nueva era en el tratamiento de la IC con FEVI reducida sin DM. Posteriormente, el EMPEROR-Reduced51, que analizó el efecto de la empagliflozina en pacientes con ICy FEVI reducida sobre la mortalidad cardiovascular y hospitalizaciones por IC, en pacientes con y sin DM, demostró una reducción del 25% del objetivo primario combinado. Aunque inicialmente los resultados para la variable de mortalidad cardiovascular no fueron significativos, un metaanálisis posterior de DAPA-HF y EMPEROR-Reduced demostró la no existencia de diferencias significativas a este respecto52.
La indicación y titulación de estos fármacos, hasta la fecha empleados como antidiabéticos por su efecto glucosúrico, debe ser conocida y manejada de forma adecuada por el médico de AP (fig. 2).
Otros fármacos en el tratamiento de pacientes con insuficiencia cardíaca-fracción de eyección reducidaActualmente los diuréticos no han demostrado reducir ni la mortalidad ni la progresión de la IC. Su uso se recomienda para mejorar la clínica en pacientes con IC que muestran signos o síntomas de congestión. El objetivo es conseguir una situación de euvolemia a la dosis mínima posible. Es fundamental, por parte tanto de médicos como de enfermeras de AP, la educación del paciente para la detección precoz de estados congestivos y el manejo correcto de los diuréticos5.
Otros grupos terapéuticos como ARA-II, ivabradina, digoxina, o la combinación de dinitrato de isosorbida e hidralacina pueden tener indicación en situaciones clínicas concretas en pacientes con IC-FEVI reducida, añadidos a los fármacos de primera línea o en caso de intolerancia a alguno de ellos5.
Tratamiento farmacológico de la insuficiencia cardíaca con fracción de eyección del ventrículo izquierdo levemente reducidaAunque las características clínicas, factores de riesgo y patrones de remodelado cardíaco pueden solaparse entre las distintas categorías de IC en función de la FEVI, parece haber una mayor similitud fenotípica entre los pacientes con fracción de eyección levemente reducida (IC-FElr) (40-49%) y los que presentan una IC-FEr (<40%), que con pacientes con IC-FEp (≥50%)5. Este hecho debe ser considerado por el médico de AP a la hora de optimizar el tratamiento farmacológico de estos pacientes.
Hasta la fecha no existen ensayos con algún fármaco específicamente diseñados para pacientes con IC-FElr, aunque diferentes estudios han arrojado resultados beneficiosos para pacientes en este rango de FEVI. Tanto el candesartán53 como la espironolactona54 han demostrado reducción de hospitalizaciones en pacientes con FEVI<55%, aunque no de la mortalidad cardiovascular ni global. En este grupo de pacientes se pueden emplear IECA/ARA-II, bloqueadores beta y ARM para reducir su sintomatología y las hospitalizaciones.
En un análisis de subgrupos del estudio PARAGON-HF55, que incluyó pacientes con FEVI>45%, se observó un beneficio de sacubitrilo/valsartán frente a valsartán en aquellos con FEVI más baja (hasta 57%), si bien este estudio no demostró una reducción estadísticamente significativa del objetivo primario combinado (muerte cardiovascular e ingreso por IC). Este resultado se alcanzó sobre todo a expensas de la disminución de las hospitalizaciones por IC. También se detectaron diferencias a favor de sacubitrilo/valsartán en cuanto a reducción de síntomas, mejoría de calidad de vida y de la función renal. Por lo tanto, el uso de sacubitrilo/valsartán puede ser beneficioso en pacientes con IC-FElr, aunque en la actualidad esta indicación no está recogida en la ficha técnica del fármaco.
En el momento actual no se dispone de datos sobre el uso de iSLGT2 en este subgrupo de pacientes con IC-FElr.
Tratamiento farmacológico de la insuficiencia cardíaca con fracción de eyección preservada en atención primaria. Estudio EMPEROR-PreservedSi la comprensión del síndrome de la IC es compleja, mucho más lo es la IC-FEp, al tratarse de una entidad no adecuadamente definida, con enorme variedad de etiologías y fenotipos, que en las últimas décadas ha generado una enorme preocupación dada su especial naturaleza, su elevada incidencia y un diagnóstico desafiante, a lo que hay que sumar la falta de terapias específicas que mejoren su pronóstico5,56–58.
Actualmente, la prevalencia de la IC-FEp es mayor que la IC-FEr y es característica de los pacientes con DM, HTA, de edad avanzada, del sexo femenino, o con otras comorbilidades, por lo que la proporción de pacientes con IC-FEp sobre el total de enfermos con IC es mayor en las consultas de AP que en las de especialidades hospitalarias.
La Sociedad Europea de Cardiología define la IC-FEp como un síndrome clínico que puede diagnosticarse en presencia de signos y/o síntomas de IC, FEVI≥50%, concentraciones elevadas de PN y al menos un criterio adicional como cardiopatía estructural o disfunción diastólica del ventrículo izquierdo5.
Hasta hace poco ningún tratamiento había demostrado beneficios en la IC-FEp. De hecho, las recomendaciones de las últimas guías de práctica clínica acerca del manejo del paciente con IC-FEp son escasas5, limitándose al empleo de diuréticos para disminuir los síntomas congestivos y a la búsqueda, control y tratamiento de las comorbilidades cardíacas y no cardíacas en estos pacientes5. No obstante, algún tratamiento específico sí había mostrado una tendencia positiva, al menos en la disminución del riesgo de hospitalización por IC29,55,59–63.
Sin embargo, recientemente se han publicado los resultados del estudio EMPEROR-Preserved, que incluyó pacientes sintomáticos con IC en clase funcional II-IV (NYHA), FEVI>40% y elevación de PN (NT-proBNP>300pg/ml en ritmo sinusal y>900pg/ml en FA). El estudio demostró que el empleo de empagliflozina (10mg/24h) en comparación con placebo, tras 26,2 meses de seguimiento, reducía de forma significativa (21%) la variable combinada de muerte cardiovascular u hospitalización por IC, especialmente por un descenso de las hospitalizaciones por IC (27%), siendo este efecto independiente de la presencia de DM64. Tras muchos años se dispone de un ensayo clínico con resultados positivos en el objetivo primario en pacientes con IC-FEp, aunque persiste la duda de los resultados que se obtengan del análisis por subgrupos, sobre todo en aquellos pacientes con FEVI>60%, donde el beneficio de esta estrategia se ve reducido, al ser pacientes de mayor edad, mayor IMC, predominar las mujeres y las concentraciones de NT-proBNP son más bajas que en el resto de subgrupos.
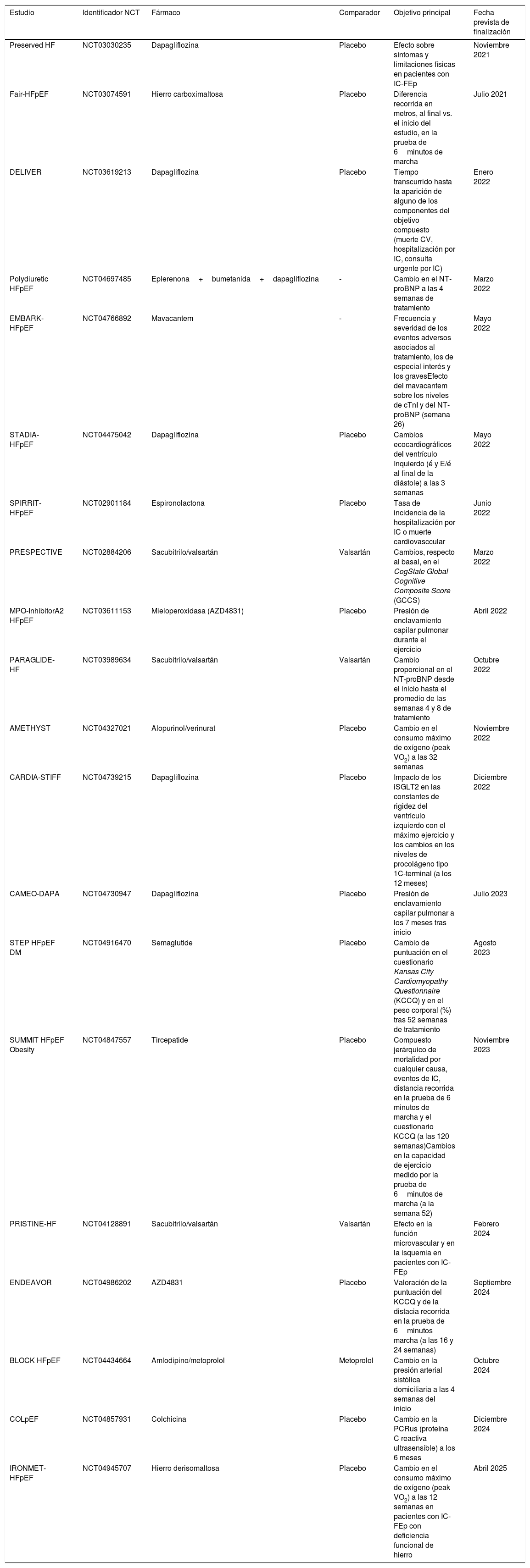
Estos resultados son muy esperanzadores y posibilitan combinar adecuadamente los resultados de EMPEROR-Preserved con el buen control de las comorbilidades asociadas (obesidad, HTA, dislipidemia, DM, etc.) y el estilo de vida de los pacientes con IC5–65. Numerosos ensayos clínicos en marcha tratarán de resolver muchas dudas que plantea este complejo síndrome, esperando disponer de sus resultados a lo largo de los próximos 3 años (tabla 9)66.
Ensayos clínicos activos para insuficiecnia cardíaca con fracción de eyección preservada (IC-FEp)
| Estudio | Identificador NCT | Fármaco | Comparador | Objetivo principal | Fecha prevista de finalización |
|---|---|---|---|---|---|
| Preserved HF | NCT03030235 | Dapagliflozina | Placebo | Efecto sobre síntomas y limitaciones físicas en pacientes con IC-FEp | Noviembre 2021 |
| Fair-HFpEF | NCT03074591 | Hierro carboximaltosa | Placebo | Diferencia recorrida en metros, al final vs. el inicio del estudio, en la prueba de 6minutos de marcha | Julio 2021 |
| DELIVER | NCT03619213 | Dapagliflozina | Placebo | Tiempo transcurrido hasta la aparición de alguno de los componentes del objetivo compuesto (muerte CV, hospitalización por IC, consulta urgente por IC) | Enero 2022 |
| Polydiuretic HFpEF | NCT04697485 | Eplerenona+bumetanida+dapagliflozina | - | Cambio en el NT-proBNP a las 4 semanas de tratamiento | Marzo 2022 |
| EMBARK-HFpEF | NCT04766892 | Mavacantem | - | Frecuencia y severidad de los eventos adversos asociados al tratamiento, los de especial interés y los gravesEfecto del mavacantem sobre los niveles de cTnI y del NT-proBNP (semana 26) | Mayo 2022 |
| STADIA-HFpEF | NCT04475042 | Dapagliflozina | Placebo | Cambios ecocardiográficos del ventrículo Inquierdo (é y E/é al final de la diástole) a las 3 semanas | Mayo 2022 |
| SPIRRIT-HFpEF | NCT02901184 | Espironolactona | Placebo | Tasa de incidencia de la hospitalización por IC o muerte cardiovasccular | Junio 2022 |
| PRESPECTIVE | NCT02884206 | Sacubitrilo/valsartán | Valsartán | Cambios, respecto al basal, en el CogState Global Cognitive Composite Score (GCCS) | Marzo 2022 |
| MPO-InhibitorA2 HFpEF | NCT03611153 | Mieloperoxidasa (AZD4831) | Placebo | Presión de enclavamiento capilar pulmonar durante el ejercicio | Abril 2022 |
| PARAGLIDE-HF | NCT03989634 | Sacubitrilo/valsartán | Valsartán | Cambio proporcional en el NT-proBNP desde el inicio hasta el promedio de las semanas 4 y 8 de tratamiento | Octubre 2022 |
| AMETHYST | NCT04327021 | Alopurinol/verinurat | Placebo | Cambio en el consumo máximo de oxígeno (peak VO2) a las 32 semanas | Noviembre 2022 |
| CARDIA-STIFF | NCT04739215 | Dapagliflozina | Placebo | Impacto de los iSGLT2 en las constantes de rigidez del ventrículo izquierdo con el máximo ejercicio y los cambios en los niveles de procolágeno tipo 1C-terminal (a los 12 meses) | Diciembre 2022 |
| CAMEO-DAPA | NCT04730947 | Dapagliflozina | Placebo | Presión de enclavamiento capilar pulmonar a los 7 meses tras inicio | Julio 2023 |
| STEP HFpEF DM | NCT04916470 | Semaglutide | Placebo | Cambio de puntuación en el cuestionario Kansas City Cardiomyopathy Questionnaire (KCCQ) y en el peso corporal (%) tras 52 semanas de tratamiento | Agosto 2023 |
| SUMMIT HFpEF Obesity | NCT04847557 | Tircepatide | Placebo | Compuesto jerárquico de mortalidad por cualquier causa, eventos de IC, distancia recorrida en la prueba de 6 minutos de marcha y el cuestionario KCCQ (a las 120 semanas)Cambios en la capacidad de ejercicio medido por la prueba de 6minutos de marcha (a la semana 52) | Noviembre 2023 |
| PRISTINE-HF | NCT04128891 | Sacubitrilo/valsartán | Valsartán | Efecto en la función microvascular y en la isquemia en pacientes con IC-FEp | Febrero 2024 |
| ENDEAVOR | NCT04986202 | AZD4831 | Placebo | Valoración de la puntuación del KCCQ y de la distacia recorrida en la prueba de 6minutos marcha (a las 16 y 24 semanas) | Septiembre 2024 |
| BLOCK HFpEF | NCT04434664 | Amlodipino/metoprolol | Metoprolol | Cambio en la presión arterial sistólica domiciliaria a las 4 semanas del inicio | Octubre 2024 |
| COLpEF | NCT04857931 | Colchicina | Placebo | Cambio en la PCRus (proteína C reactiva ultrasensible) a los 6 meses | Diciembre 2024 |
| IRONMET-HFpEF | NCT04945707 | Hierro derisomaltosa | Placebo | Cambio en el consumo máximo de oxígeno (peak VO2) a las 12 semanas en pacientes con IC-FEp con deficiencia funcional de hierro | Abril 2025 |
Elaboración propia a partir de datos extraídos de la página web de: clinicaltrials.gov66.
Es fundamental la detección precoz y el manejo correcto por el médico de familia de las comorbilidades, tanto cardiovasculares como no cardiovasculares que se presentan en el paciente con IC, y sin duda la consulta de AP es el escenario más adecuado para ello.
El control de la HTA, la detección de la FA y el inicio y control de una adecuada anticoagulación para la prevención de eventos tromboembólicos, la detección de la isquemia miocárdica y de la enfermedad arterial periférica de miembros inferiores deben ser una prioridad para el médico de AP. Igualmente debe serlo el manejo adecuado de los fármacos antidiabéticos, priorizando el uso de los ISGLT2 por su efecto demostrado para reducir hospitalizaciones y morbimortalidad en el paciente con IC5.
La detección del déficit de hierro debe incluirse de rutina en el seguimiento del paciente con IC en AP y estructurar junto a los servicios de cardiología y medicina interna vías para el acceso de los pacientes que lo presenten al tratamiento con hierro carboximaltosa intravenoso, por su efecto beneficioso en la mejoría de la sintomatología y reducción de la morbimortalidad5.
Otras comorbilidades con impacto sobre la calidad de vida y el pronóstico del paciente con IC como la depresión, la enfermedad pulmonar obstructiva crónica o la enfermedad renal crónica deben ser buscadas y tratadas de forma activa por el médico de AP, siendo el principal responsable del desarrollo de una estrategia de tratamiento global adecuada e individualizada para cada paciente y de la conciliación de la medicación después de cada intervención o modificación.
El tratamiento de las principales comorbilidades se resume en la tabla 10.
Manejo de las principales comorbilidades en insuficiencia cardíaca en atenciaón primaria
| Diabetes | Beneficiosos | ISGLT2 |
|---|---|---|
| Neutros | Metformina, IDPP4 (salvo saxagliptina) | |
| Contraindicados | Glitazonas | |
| Hipertensión arterial | IECA, ARA II, ARM o ARNI | |
| Enfermedad renal crónica | IECA, ARA II o ISGLT2 | |
| Anemia/déficit de hierro | Carboximaltosa de hierro intravenosa: en pacientes sintomáticos con FEVI<50% y déficit de hierro | |
| Depresión | Inhibidores de la recaptación de serotonina (ISRS). Inicio a dosis bajas | |
| Apnea del sueño | Presión positiva continua en vía aérea (CPAP) | |
AP: atención primaria; ARA II: antagonistas de los receptores de la angiotensina II; ARM: antagonistas de los receptores mineralocorticoides; ARNI: inhibidor del receptor de angiotensina/neprilisina; FEVI: fracción de eyección del ventrículo izquierdo; IDPP4: inhibidores de la dipeptidil peptidasa 4; IECA: inhibidores de la enzima convertidora de angiotensina; ISGLT2: inhibidores del cotransportador sodio-glucosa tipo 2;
Modificada de Wagner y Dimmeler4.
Aunque difícil de definir, pudiéramos circunscribir esta etapa al último año de vida del paciente al estar limitadas ciertas medidas (desfibrilador-cardioversión/resincronización) en aquellos con esperanza de vida<1 año5, aunque otros autores lo reducen a 6 meses por ser la esperanza de vida de aquellos con persistencia de síntomas refractarios y frecuentes hospitalizaciones, a pesar del tratamiento adecuado67. La eficacia de los nuevos tratamientos30,46,57,68,69, incluso en pacientes de edad avanzada70, hace que los modelos pronósticos de supervivencia71,72 hayan quedado desfasados, por lo que la situación clínica y la calidad de vida del paciente fundamentan la toma de decisiones.
Llegada esta situación el papel del equipo de AP cobra aún más protagonismo si cabe, al ser imprescindible su actuación si el paciente decide permanecer en el domicilio hasta el final de su vida (tabla 11).
Estrategia de abordaje de la insuficiencia cardíaca al final de la vida
| Objetivo |
| Mantenimiento de la calidad de vida |
| Evitar el ensañamiento terapéutico |
| Mantener un entorno poco hostil (minimizar hospitalizaciones/no duplicar pruebas) |
| Organización/planificación |
| Atención primaria como eje coordinador del equipo multidisciplinar |
| Indagar en expectativas, preferencias y creencias del paciente |
| Disponer de colaboración en el entorno familiar |
| Informar de la situación clínica/pronóstico del paciente |
| Planificar actuaciones anticipándose a las complicaciones |
| Dejar por escrito pautas de actuación (tratamiento, necesidad o no resucitación cardiopulmonar, desactivación de DAI…) |
DAI: desfibrilador automático implantable.
Elaboración propia.
En situación de últimos días, entre otras medidas, se debe valorar la pertinencia del uso de vía subcutánea en caso de pérdida de la vía oral para facilitar la permanencia del paciente en el domicilio. Esta vía puede ser instaurada y controlada por el equipo de AP, así como la titulación de los fármacos necesarios para el control de síntomas.
El control de los principales síntomas del paciente con IC al final de la vida se resume en la tabla 12.
Control de síntomas más frecuentes en el paciente con insuficiencia cardíaca al final de la vida
| Síntomas | Manejo en función de sintomatología del paciente |
|---|---|
| Edemas | Diuréticos de asa, a menudo vía intravenosa, solos o en combinación con diuréticos tiacídicosValorar la posibilidad de diuréticos en infusión subcutánea según la disponibilidad en cada zona |
| Disnea | Intensificar diuresis manteniendo normovolemia; digoxina en IC FEr con ritmo sinusal/considerarla en IC FEr con FA en tratamiento con bloqueadores beta y frecuencia cardíaca>110latidos/minValorar necesidad de oxigenoterapia domiciliaria |
| Dolor | Paracetamol/opiáceos/fentanilo. Evitar AINEValorar tratamiento con opiáceos y titulación |
| Fatiga/debilidad | Descartar/tratar otras etiologías (anemia/alteraciones tiroideas/apnea de sueño/depresión) |
| Náuseas | Antieméticos/ondasetrón |
| Estreñimiento | Dieta rica en fibraLaxantes/enemas/desimpactación manual |
| Confusión/delirio | Indagar causas reversiblesReducir dosis de antihipertensivos si PAS<100mmHgReorganizar periodos sueño/vigilia. Haloperidol a dosis bajas |
| Tos | Indagar etiología. Codeína/dextrometorfano cuando fuera preciso |
AINE: antiinflamatorios no esteroideos; IC Fer: insuficiencia cardíaca con fracción de eyección reducida; PAS: presión arterial sistólica.
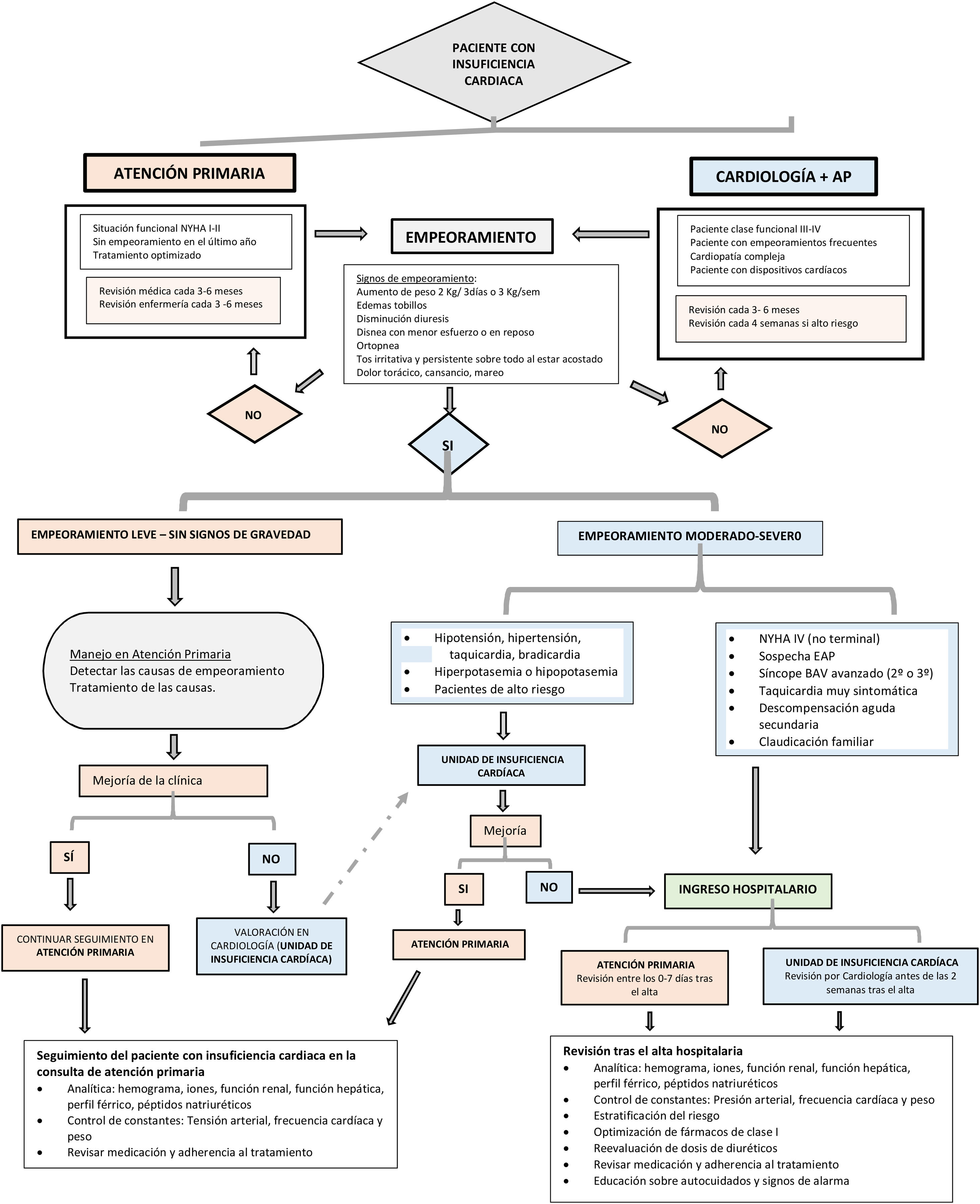
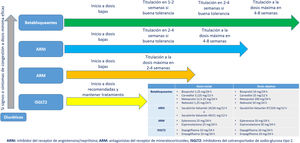
El paciente con IC es un paciente complejo, en el que la optimización del tratamiento, que incluye cambios en el estilo de vida, tratamiento farmacológico adecuado tanto para la IC como para el resto de comorbilidades, y el empleo de dispositivos, en su caso, es fundamental para disminuir la mortalidad, mejorar la calidad de vida de los pacientes y retrasar la progresión de la enfermedad5. Para ello es necesario el desarrollo de programas multidisciplinares para el adecuado abordaje de la IC, que permita atender todos los aspectos de la enfermedad, incluyendo el tratamiento farmacológico y no farmacológico, y que abarque todo el espectro de la enfermedad, desde sus estadios más iniciales, incluyendo la prevención del desarrollo de IC mediante el control adecuado de los factores de riesgo, hasta las fases terminales de la IC (cuidados paliativos), englobando no solo los periodos de empeoramiento, sino también los de aparente estabilidad clínica73. De hecho, las recientes guías europeas de práctica clínica de IC establecen como recomendación IA la inclusión de los pacientes con IC en programas multidisciplinarios de abordaje de la IC, con el doble objetivo de reducir el riesgo de hospitalizaciones por IC y la mortalidad5. El desarrollo de estos programas se deberá adaptar a las posibilidades reales de cada área sanitaria (infraestructuras, personal, posibilidades del paciente, etc.), y podrá incluir programas domiciliarios, telemedicina, visitas presenciales, hospital de día, etc. En estos programas multidisciplinares deberían participar distintas especialidades médicas (AP, cardiología, medicina interna, etc.), enfermería y otros profesionales sanitarios, según las necesidades individuales de cada sujeto, y siempre poniendo en el centro al paciente con IC5,74. No solo se trata de atender a la IC, sino también a todas las comorbilidades que pueda presentar el paciente, como arritmias, HTA, DM, ERC, depresión, etc., siempre considerando un enfoque global de la enfermedad5.
La estrategia de abordaje conjunto entre AP y cardiología se recoge en la figura 3
Telemedicina en el abordaje de la insuficiencia cardíaca en atención primariaLa situación de pandemia por la COVID-19ha supuesto un cambio en el modelo de atención a los pacientes crónicos, implementándose la consulta telefónica como vía de comunicación principal entre ellos y el equipo de AP75.
La teleconsulta, que lleva años llevándose a cabo con éxito en muchos servicios de cardiología, también aporta una nueva herramienta útil para el seguimiento de pacientes con IC en AP, permitiendo desarrollar programas mixtos presenciales y telefónicos que mejoren el seguimiento de los pacientes76.
Los programas de teleconsulta permiten la comunicación entre los componentes del equipo multidisciplinar mencionado anteriormente. Estos programas pueden realizarse de forma conjunta por médicos y enfermeras, utilizando preguntas estructuradas que permitan detectar la necesidad de una visita presencial o de realizar modificaciones en el tratamiento y potenciar la implicación del paciente y/o el cuidador en la enfermedad.
Los programas de seguimiento mixtos deben iniciarse precozmente en AP tras el diagnóstico de IC o tras el alta hospitalaria, al ser esos momentos claves para iniciar o continuar la titulación de fármacos, reforzar las medidas no farmacológicas y evitar la rehospitalización del paciente.
Los cambios clave de las guias de insuficiencia cardíaca 2021La AP lidera la prevención de la enfermedad, con especial relevancia en el ámbito cardiovascular, dada su alta prevalencia en las consultas de AP1. Las guías europeas de insuficiencia cardíaca 2021 de la ESC5 se centran en la importancia del diagnóstico, y sobre todo en el tratamiento, y menos en la prevención de la IC, pese a la inclusión de 2 representantes de pacientes (Richard Mindham y Anne Kathrine Skibelund) en el grupo de trabajo de estas. Los cambios clave en el tratamiento tanto de la IC-FEr y la IC-FEp, así como los nuevos conceptos no descritos en las guías anteriores están detallados en la tabla 13.
Cambios clave y nuevos conceptos para atención primaria de las guías 2021 de insuficiencia cardíaca de la Sociedad Europea de Cardiología
| Cambios clave en el tratamiento de IC-FEr |
| Modificación del algoritmo de tratamiento simplificado |
| Los ISGLT2, dapagliflozina y empagliflozina, son tratamiento de recomendación clase I |
| Las 4 estrategias de tratamiento clave iECA/ARA-II, ARNI, bloqueadores beta y ARM deben iniciarse lo antes posible y titular siempre (si es factible) a dosis máximas |
| Algoritmo de tratamiento agregado para IC-FEr según fenotipos para un manejo personalizado |
| Cambios clave en el diagnóstico y tratamiento de IC-FElr |
| En lugar de insuficiencia cardíaca con fracción de eyección en rango medio (IC-FEm), se modifica a insuficiencia cardíaca con fracción de eyección levemente reducida (IC-FElr), ya que estos pacientes pueden beneficiarse de la misma estrategia de tratamiento que aquellos con IC-FEr |
| Para el diagnóstico de IC-FElr los péptidos natriuréticos elevados más otras pruebas de cardiopatía estructural hacen que el diagnóstico sea más probable, pero no son obligatorios si hay certeza en la medición de la FEVI |
| Adición de una tabla de recomendaciones para el tratamiento de IC-FElr |
| Cambios clave en el diagnóstico y tratamiento de IC-FEp |
| Una estrategia de diagnóstico simplificada con 3 pasos para IC-FEp |
| Con respecto al tratamiento de la IC-FEp las recomendaciones de las nuevas guías se han mantenido prácticamente sin cambios. Sin embargo, el grupo de trabajo reconoce que se están revisando otras opciones de tratamiento para la IC-FEp en el momento de la publicación de estas directrices (EMPEROR-Preserved) |
| Nuevos conceptos guías 2021 vs. 2016 para atención primaria |
| Se ha modificado la clasificación de la IC aguda |
| Se ha actualizado el tratamiento para la mayoría de las comorbilidades no cardiovasculares (incluida la diabetes, la hiperpotasemia, la deficiencia de hierro y el cáncer) |
| Se han agregado indicadores clave de calidad |
ARA-II: antagonistas del receptor de angiotensina II; ARNI: inhibidores duales de la neprilisina y la angiotensina; ARM: antagonistas de receptor mineralcorticoide; IC: insuficiencia cardíaca; IECA: inhibidores de la enzima convertidora de angiotensina; IC-FElr: insuficiencia cardíaca con Fracción de eyección levemente reducida; IC-FEr: insuficiencia cardíaca con fracción de eyección reducida; IC-FEp: insuficiencia cardíaca con fracción de eyección preservada; ISGLT 2: inhibidores del cotransportador sodio-glucosa tipo 2.
Existe cada vez más evidencia de la necesidad de trabajar de forma conjunta entre AP y cardiología, y así lo reflejan las GPC4 y la propia experiencia de la práctica asistencial en AP. Diferentes grupos de expertos ya han destacado el papel fundamental del médico de familia en todo el proceso del paciente con IC76. Sin embargo, el volumen de evidencia publicado durante los últimos años en cuanto al diagnóstico, y sobre todo al tratamiento farmacológico de la IC, ha generado mucha incertidumbre en el médico de familia a la hora de ejercer un papel más activo en esta enfermedad.
Las dificultades a la hora de acceder a pruebas diagnósticas básicas, de gestionar interconsultas o de lograr un tiempo razonable para la atención a estos pacientes en las consultas de AP, han hecho también que la participación del médico de familia se haya visto frenada en múltiples ocasiones. A pesar de todo, la implicación de AP en la IC ha ido creciendo en los últimos años, aunque aún queda un largo camino por recorrer.
La accesibilidad y la longitudinalidad, características propias de la AP, posicionan al médico de familia en una situación de máximo protagonismo en el manejo y control del paciente con IC, siendo su papel básico en todo el continuo de esta enfermedad, desde la prevención, diagnóstico, detección precoz de las descompensaciones, inicio y optimización del tratamiento farmacológico y no farmacológico, manejo de las comorbilidades, seguimiento al alta hospitalaria y acompañamiento del paciente y la familia hasta el final de la vida.
Los nuevos esquemas de manejo terapéutico de los pacientes con IC-FEr, los cuales han demostrado reducir la progresión de la enfermedad y la mortalidad, precisan un seguimiento individualizado en cada paciente, que puede coordinarse entre el médico de familia y el cardiólogo o internista.
La llegada de la telemedicina al ámbito de la AP debe aportar un valor añadido para médicos y enfermeras en el seguimiento de la IC, si bien esta herramienta debe ser desarrollada e implantada más allá de la mera llamada telefónica para que aporte mucho más valor.
Por lo tanto, el papel del médico de familia debe consistir en ejercer como eje vertebrador de todo el proceso de la IC centrado en el paciente, e integrase en un equipo multidisciplinar que incluya cardiólogos, internistas, enfermería, trabajadores sociales y fisioterapeutas entre otros profesionales de la salud.
El punto de partida debe ser el trabajo conjunto entre AP y cardiología o medicina interna localmente en cada área/departamento de salud a través de la creación de unidades específicas, sustentadas en la comunicación entre los profesionales implicados y en protocolos de actuación consensuados y adaptados a la realidad de cada área.
Las dificultades que pueden aparecer no deberían obstaculizar el ofrecer una atención de calidad, sino más bien argumentos que justifiquen la solicitud de dotación de los recursos materiales y humanos necesarios para conseguir, de la atención multidisciplinar al paciente con IC, una realidad independientemente del lugar en el que viva.
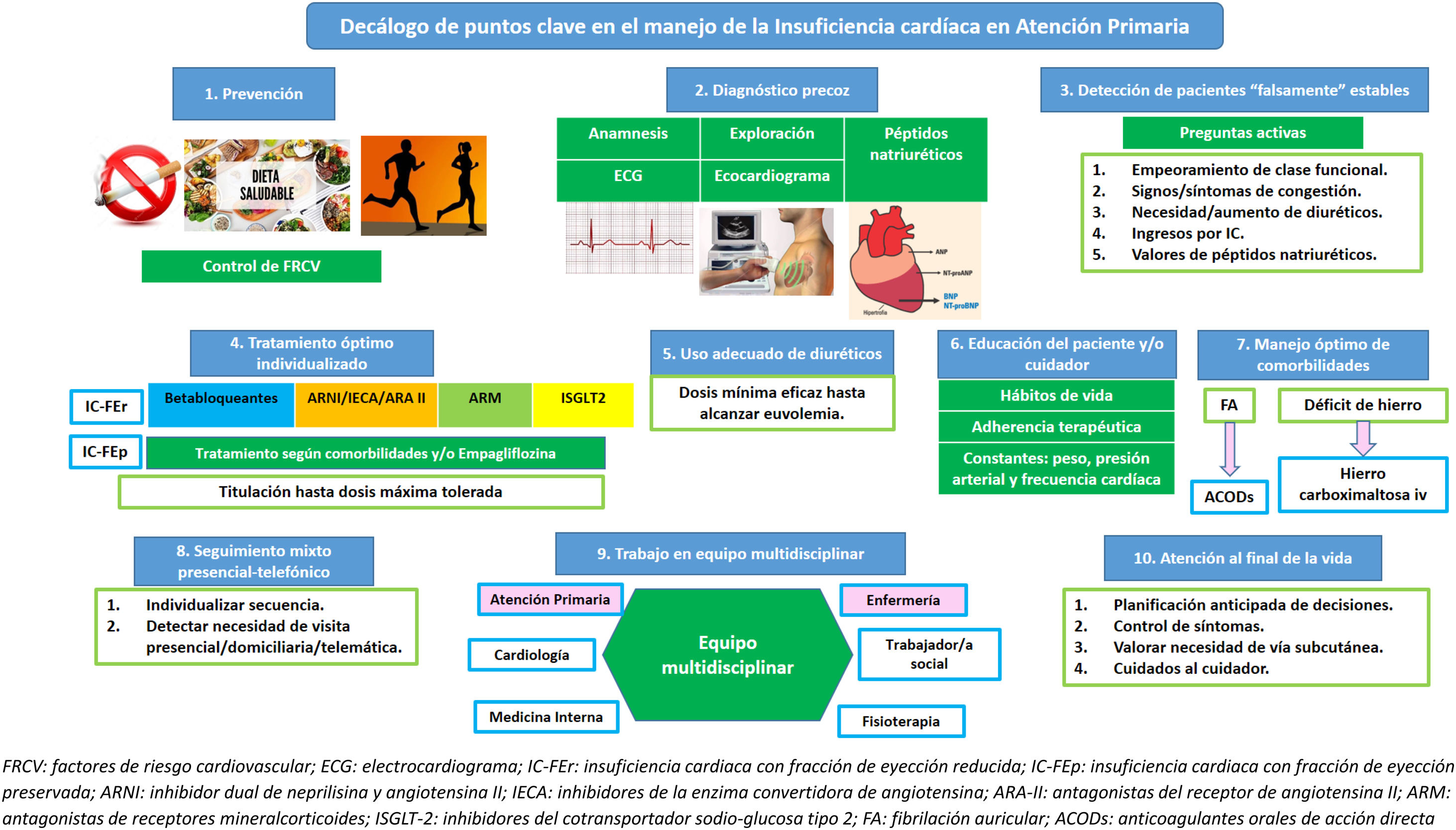
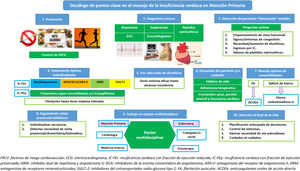
Los puntos clave en el manejo del paciente con IC en AP se resumen en la figura 4.
AutoríaM.J. Castillo Moraga, M. Turégano Yedro: redacción, análisis, búsqueda bibliográfica, elaboración gráfica, revisión y validación final.
V. Pallarés Carratalá, V. Barrios: idea, redacción, análisis, búsqueda bibliográfica, revisión y validación final.
M.C. Seonae Vicente: redacción, elaboración gráfica, revisión y validación final.
A. Serrano Cumplido, A. Ruiz García, E. Martín Rioobó, C. Escobar Cervantes, J. Polo García: redacción, revisión y validación final.
Todos los autores han leído y aprobado la versión final del artículo de posicionamiento.
FinanciaciónNo existe ningún tipo financiación para la realización de este posicionamiento ni los autores han recibido honorario alguno por ello.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.
M. Ajenjo González, F.J. Alonso Moreno, L. Araujo Márquez, C. Arina Cordeu, L.M. Artigao Rodenas, A. Barquilla García, V. Barrios Alonso, P. Beato Fernández, V. Caballero Pajares, F. Cabezudo Moreno, A. Calderón Montero, E. Carrasco Carrasco, J.L. Carrasco Martín, J. Carrizo Sánchez, M.J. Castillo Moraga, S. Cinza Sanjurjo, R. Crespo Sibaris, M.P. de las Cuevas Miguel, J.A. Divisón Garrote, H. Eguía, C. Escobar Cervantes, M.B. Esteban Rojas, J.M. Fernández Toro, M. Frías Vargas, D. Fuentes Martínez, E. García Criado, A. García Lerín, L. García Matarín, O. García Vallejo, R. Genique Martínez, I. Gil Gil, I. González Casado, I. González Lillo, J.L. Górriz Teruel, E. Jiménez Baena, J. Juan Gaceo, J.C. Martí Canales, E. Martín Rioboó, J.J. Mediavilla Bravo, F. Molina Escribano, S. Morales Quintero, A. Moyá Amengual (secretaria), G. Nieto Barco, A. Ochoa Linares, V. Pallarés Carratalá (coordinador), E. Pérez Vázquez, A. Piera Carbonell, J. Polo García, M.A. Prieto Díaz, T. Rama Martínez, M. Redondo Prieto, D. Rey Aldana, B.E. Riesgo Escudero, G.C. Rodríguez Roca, G.A. Rojas Martelo, A. Romero Sencin, J.C. Romero Vigara, A. Ruiz García, R. Sánchez Rodríguez, T. Sánchez Ruíz, C. Santos Altozano, F.J. Sanz García, M.C. Seoane Vicente, A. Serrano Cumplido, M. Turégano Yedro, F. Valls Roca, S.M. Velilla Zancada y A. Vicente Molinero.