La implantación de acciones clínicas preventivas en Atención Primaria permitiría actuar sobre la alta incidencia de urolitiasis y sus factores de riesgo corregibles. Este estudio piloto comparó un seguimiento sistemático (SS) frente al seguimiento habitual (SH) en términos de viabilidad, seguridad y eficacia clínica.
Materiales y métodosRealizamos un estudio piloto multicéntrico y controlado en 30 pacientes, comparando el SS y el SH. Los pacientes fueron aleatorizados según una lista generada por ordenador. Se definió el «éxito del estudio» como la consecución de los objetivos de viabilidad: tasa de reclutamiento, adherencia, finalización del seguimiento y recursos humanos necesarios. Se recogieron variables clínicas (dolor y fiebre), analíticas (sangre y orina) y de imagen (ecografía y radiografía) a los 10, 45 y 90 días en el grupo de SS y a los 3 meses en el de SH. En el grupo de SS se entregaron recomendaciones dietéticas y analgésicas. Se hizo una comparación clínica preliminar y se registraron las complicaciones en cada grupo.
ResultadosLos objetivos de viabilidad se consiguieron como sigue: 94,1% de tasa de reclutamiento, 5,9% de rechazo a la aleatorización, 10 pacientes reclutados al mes, adherencia del 93,1% y 90% de asistencia a la revisión final. Los resultados clínicos no favorecieron significativamente a ninguno de los dos grupos. En el grupo de SH hubo una recidiva.
ConclusionesSe cumplieron los objetivos de viabilidad estudiados excepto los relacionados con los recursos humanos. Los resultados clínicos no favorecieron a ningún grupo ni contraindicaron el desarrollo de un futuro ensayo clínico.
The implementation of preventive clinical actions in Primary Care would allow to act on the high incidence of urolithiasis and the correctable risk factors. This pilot study compared a systematic follow-up (SFU) versus a regular follow-up (RFU) in terms of feasibility, safety and clinical outcomes.
Materials and methodsWe conducted a multicentric and controlled pilot study in 30 patients comparing SFU versus RFU. Patients followed allocation concealment by an independent blocked computer-generated list. We defined “success” if feasibility objectives were matched including recruitment rate, follow-up compliance, completion and staff resources. Clinic variables (pain and fever), analytics (blood and urine) and image techniques (echography and radiography) were recorded at 10, 45 and 90 days in SFU and at 3 months in RFU. The SFU group received nutritional and analgesic recommendations. Preliminary clinical outcomes were compared and complications were recorded in each group.
ResultsThe feasibility objectives were matched as follows: 94.1% of recruitment rate, 5.9% refused to participate, 10 patients/month were recruited, 93.1% of follow-up compliance and 90% of completion. No clinical differences were found between groups. There was a recurrence in the RFU group.
ConclusionsThe feasibility objectives were matched except those related to human resources. Clinical outcomes did not favour any group or contraindicate the development of a future clinical trial.
La urolitiasis (UL) afecta aproximadamente a una de cada 11 personas en Estados Unidos, suponiendo un importante gasto sanitario1 con una tendencia creciente en los países desarrollados2,3. En la población española de entre 40 y 65 años se ha observado una prevalencia del 14,6% y una incidencia anual del 2,9%, sin distinción entre sexos, con una tasa de recidiva del 52,8%4. A pesar de tratarse de una patología benigna, la UL se ha asociado a complicaciones mayores como: sepsis, pérdida de la función renal, ingresos hospitalarios o efectos adversos medicamentosos5,6.
El aumento en la incidencia de los últimos años7,8 se ha puesto en relación con los actuales hábitos higiénico-dietéticos como la baja ingesta hídrica9, el aumento en el consumo de sal10 o de bebidas azucaradas11. Otros factores de riesgo identificados son: presencia de antecedentes familiares de UL12, gota13 u obesidad14. Diversos autores defienden la implantación de protocolos de seguimiento15–17 y la utilización de la ecografía a pie de cama18,19 para intentar minimizar las probabilidades de una recidiva y evitar sus posibles complicaciones.
El papel de la Atención Primaria (AP) en esta patología20 debería abarcar la prevención, las recomendaciones dietéticas específicas y la prescripción farmacológica en caso de indicación de tratamiento; bien expulsivo, como la tamsulosina21, o etiológico en pacientes con hiperuricemia13 o pH urinario ácido15.
El objetivo principal de nuestro estudio piloto (EP) fue comparar un seguimiento sistemático (SS) frente al seguimiento habitual (SH) en pacientes con UL en términos de viabilidad metodológica. Secundariamente, realizamos una comparación clínica preliminar de nuestra intervención evaluando seguridad y eficacia.
Material y métodosDiseñoSe realizó un EP externo, multicéntrico, controlado y aleatorizado entre grupos paralelos que se desarrolló en los Centros de Salud de El Coto, La Calzada y Natahoyo, en Gijón, dependiente del Área V de Salud del SESPA. El estudio fue aprobado por el Comité de Ética de la Investigación con Medicamentos del Principado de Asturias y el Comité de Investigación del Área V (Apéndice A).
PacientesLos pacientes fueron reclutados y seguidos entre julio de 2019 y febrero de 2020. Cada paciente recibió y firmó un documento de consentimiento informado (Apéndice B), realizándose un seguimiento de tres meses.
Criterios de inclusión y exclusiónIncluimos pacientes mayores de 18 años con un episodio de cólico renoureteral agudo. Excluimos pacientes en lista de espera quirúrgica por este motivo, portadores de un catéter doble J, en diálisis o con insuficiencia renal grado IV, pacientes con patología genitourinaria previa (malformaciones, secuelas quirúrgicas, cáncer, transplante renal, vejiga neurógena o lesión medular) y poblaciones especiales de alto riesgo de UL (metabolopatías, síndromes malabsortivos o bypass gástrico).
Protocolo de asignaciónLos autores JMC, LGC y GRM se encargaron de asignar los pacientes a cada grupo de seguimiento (SS o SH) en una relación 1:1 según una lista aleatoria generada por ordenador.
Objetivos de viabilidadEl éxito del estudio se basó en alcanzar todos los objetivos de viabilidad22. Definimos dichos objetivos en relación con los procesos que conforman el estudio en términos de: reclutamiento, adherencia al protocolo, finalización y empleo de recursos humanos (tabla 1).
Objetivos de viabilidad
| Variable | Definición de éxito |
|---|---|
| Tasa de reclutamiento | Reclutamiento ≥ 70% de todos los pacientes con criterios de inclusión. Rechazo de la aleatorización en ≤ 5% de los pacientes con criterios de inclusión ≥ 10 pacientes aleatorizados al mes en los tres centros de salud de media |
| Adherencia al seguimiento | Asistencia a todas las revisiones programadas por parte de> 90% de los pacientes incluidos |
| Finalización | Asistencia a la última revisión programada por parte de> 90% de los pacientes incluidos |
| Recursos humanos | El tiempo requerido para realizar las revisiones, la ecografía y la recogida de datos de nuestro protocolo no deberían saturar nuestros recursos humanos |
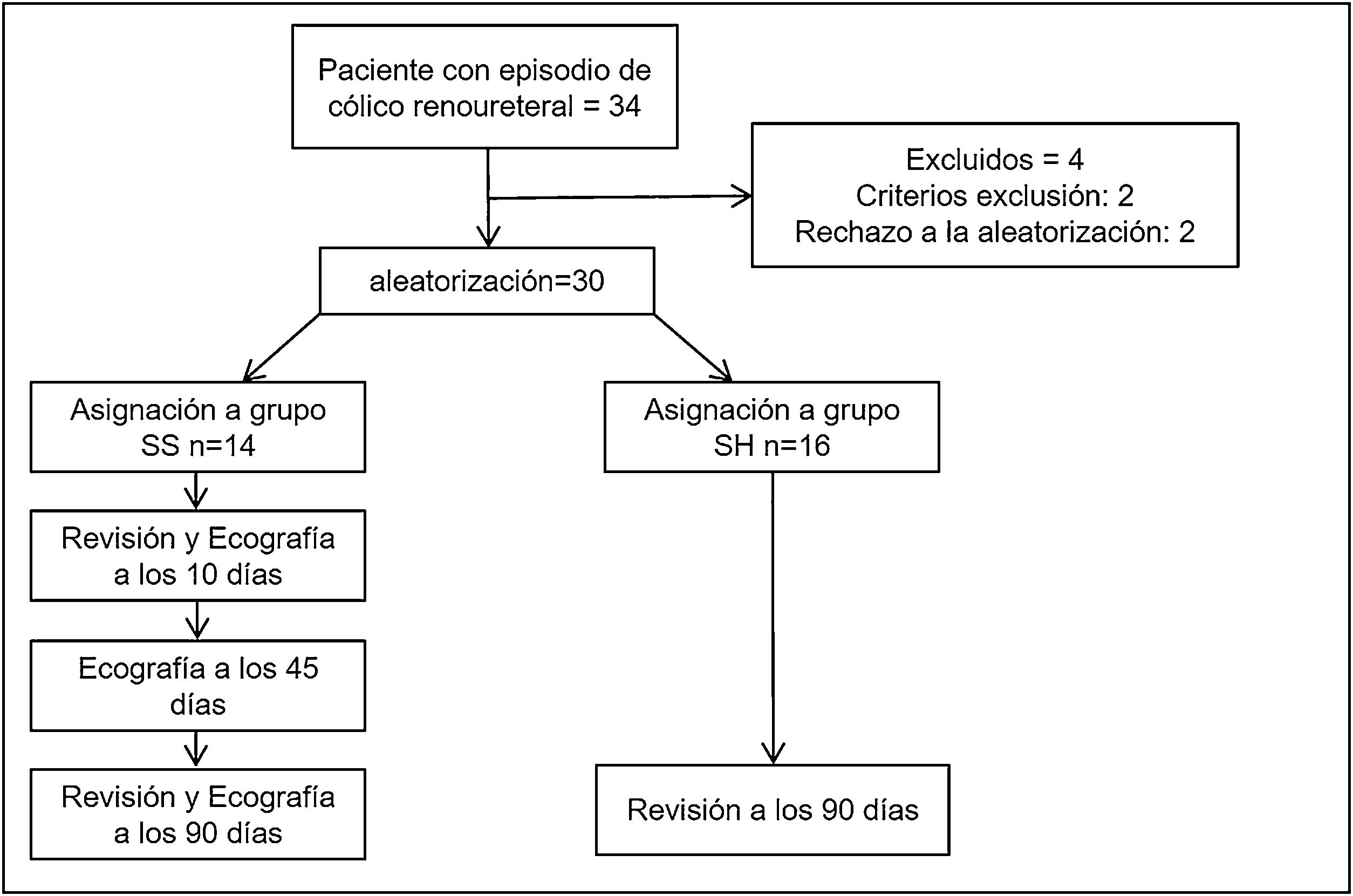
Se programaron dos revisiones médicas (a los 10 y 90 días), dos radiografías simples de abdomen (a los 10 y 90 días) y 3 ecografías de control (a los 10, 45 y 90 días) tras el episodio de cólico (fig. 1). Recogimos posibles factores de riesgo de UL existentes como sobrepeso (IMC), antecedentes familiares de UL o episodios cólicos previos. Registramos variables analíticas en sangre (tasa de filtrado glomerular, ácido úrico y calcio) y orina (leucocitos, hematíes y pH) y una batería de preguntas clínicas. Recogimos el número de visitas al médico de familia por este motivo durante el periodo de seguimiento. Todas las variables están detalladas en la tabla 2. Los autores JMC, LGC y GRM (con la supervisión de PBB y EME, con más de 5 años de experiencia en ecografía clínica) realizaron las ecografías. La dilatación pielocalicial se midió en 4 grados de severidad (normal, leve, moderada y severa) según la clasificación propuesta por Gaspari et al.18.
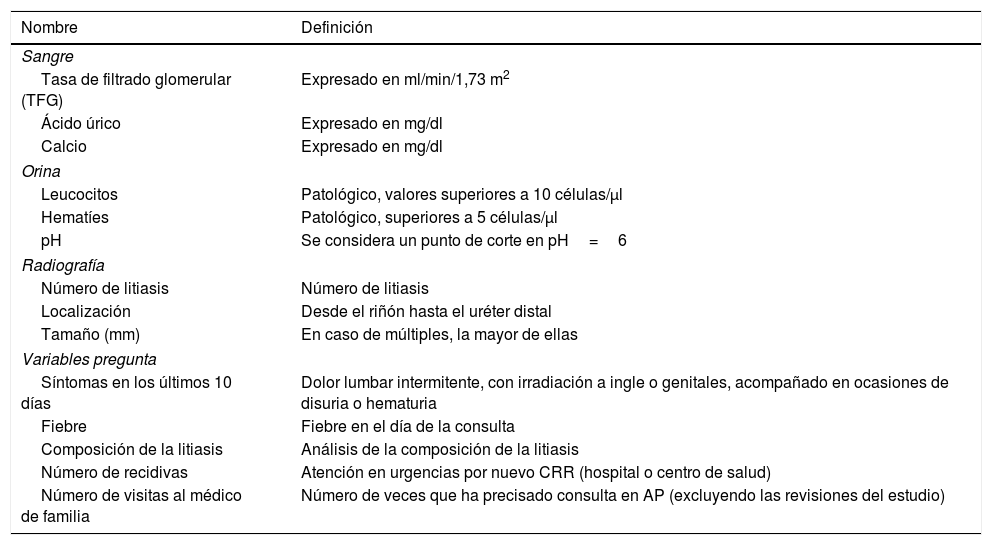
Variables clínicas
| Nombre | Definición |
|---|---|
| Sangre | |
| Tasa de filtrado glomerular (TFG) | Expresado en ml/min/1,73 m2 |
| Ácido úrico | Expresado en mg/dl |
| Calcio | Expresado en mg/dl |
| Orina | |
| Leucocitos | Patológico, valores superiores a 10 células/μl |
| Hematíes | Patológico, superiores a 5 células/μl |
| pH | Se considera un punto de corte en pH=6 |
| Radiografía | |
| Número de litiasis | Número de litiasis |
| Localización | Desde el riñón hasta el uréter distal |
| Tamaño (mm) | En caso de múltiples, la mayor de ellas |
| Variables pregunta | |
| Síntomas en los últimos 10 días | Dolor lumbar intermitente, con irradiación a ingle o genitales, acompañado en ocasiones de disuria o hematuria |
| Fiebre | Fiebre en el día de la consulta |
| Composición de la litiasis | Análisis de la composición de la litiasis |
| Número de recidivas | Atención en urgencias por nuevo CRR (hospital o centro de salud) |
| Número de visitas al médico de familia | Número de veces que ha precisado consulta en AP (excluyendo las revisiones del estudio) |
Variables recogidas en el grupo de seguimiento sistemático en los días 10 y 90 de seguimiento y en el grupo de seguimiento habitual en el día 90.
En la revisión de los 10 días, todos los pacientes recibieron una hoja con recomendaciones dietéticas específicas (Apéndice C) y una hoja con la aclaración de los signos de alarma para acudir a Urgencias (Apéndice D). Se revisó la pauta analgésica instando a disminuir el uso de AINE, se explicaron los factores de riesgo corregibles para un nuevo episodio (con especial hincapié en: sobrepeso, hiperuricemia y baja ingesta hídrica) y se valoró la prescripción farmacológica según la etiología de la UL21 (Apéndice E). En caso de expulsión espontánea instruimos al paciente sobre el modo de aportar el cálculo para el análisis de su composición.
Protocolo para el grupo de seguimiento habitualLos pacientes del grupo de SH actuaron de acuerdo con las indicaciones médicas recibidas el día del episodio de cólico, acudiendo al Centro de Salud en caso de estimarlo necesario. Se realizó una única revisión y una ecografía de control a los tres meses en la que se aplicó el mismo protocolo que en el grupo de SS a los 90 días (tabla 2).
ComplicacionesRecogimos cualquier tipo de complicación o incidencia derivada del manejo en los dos grupos del estudio incluyendo: infecciones de tracto urinario, ingresos hospitalarios, intervenciones quirúrgicas, visitas a Urgencias, bien hospitalarias o en AP, y cualquier efecto adverso a los fármacos administrados.
Estudio estadístico de las variables clínicasSe registró la media, desviación estándar y el rango dependiendo de la variable (SPSS 15.0, Inc., Chicago, IL). Se analizaron los datos empleando la t de Student y la prueba de Fisher (significativos para una p<0,05).
ResultadosObjetivos de viabilidadSe consiguieron satisfactoriamente los objetivos de viabilidad relacionados con la tasa de reclutamiento (94,1%), número de pacientes aleatorizados por mes (10/mes), asistencia a las revisiones (93,1%) y finalización del estudio (90%). No superamos los umbrales de viabilidad (≤ 5%) en la tasa de rechazo a la aleatorización (5,9%). Nuestros recursos humanos no fueron suficientes para la realización de la 2.ª revisión en el plazo estipulado (90 días) realizándose de media a los 98,5 días (rango, 85-112).
Resultados clínicos comparativos preliminaresLas características demográficas de cada grupo están detalladas en la tabla 3.
Características demográficas por grupos
| Sexo | SH (n=16) | SS (n=14) |
|---|---|---|
| Varones | 11 | 9 |
| Mujeres | 5 | 5 |
| Edad media | 45,2 (32-71) | 55,9 (35-75)* |
| IMC | 26,8 (20,8-41,4) | 28,1 (21,9-35-6) |
| Historia previa de CRU | 4 | 6 |
| Historia familiar previa | 11 | 10 |
| Activos laboralmente | 10 | 10 |
La edad media y el IMC se expresaron mediante la media y el rango entre paréntesis.
CRU: cólico renoureteral; IMC: índice de masa corporal; n: número de pacientes por grupo; SH: seguimiento habitual; SS: seguimiento sistemático.
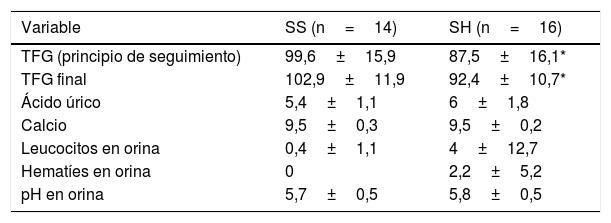
No se observaron diferencias significativas en las variables analíticas estudiadas en sangre ni orina excepto en la TFG tanto al principio como al final del seguimiento (tabla 4). Un paciente en el grupo de SS y 2 en el de SH tuvieron síntomas leves de cólico y no hubo ningún caso de fiebre a los 3 meses. En la revisión de los 10 días, dos pacientes del grupo de SS mostraron en la ecografía una dilatación leve de la unión pielocalicial normalizada al final del seguimiento. En el grupo de SH todas las ecografías fueron normales y no hubo diferencias entre grupos. Ningún paciente recibió tratamiento farmacológico ni aportó la litiasis para su estudio. No hubo diferencias en los días de baja ni visitas al médico de familia relacionadas con el episodio de cólico.
Resultados comparativos de las variables analíticas (sangre y orina) al final del seguimiento
| Variable | SS (n=14) | SH (n=16) |
|---|---|---|
| TFG (principio de seguimiento) | 99,6±15,9 | 87,5±16,1* |
| TFG final | 102,9±11,9 | 92,4±10,7* |
| Ácido úrico | 5,4±1,1 | 6±1,8 |
| Calcio | 9,5±0,3 | 9,5±0,2 |
| Leucocitos en orina | 0,4±1,1 | 4±12,7 |
| Hematíes en orina | 0 | 2,2±5,2 |
| pH en orina | 5,7±0,5 | 5,8±0,5 |
Los valores en cada grupo (SS y SH) se muestran con la media±desviación estándar.
SH: seguimiento habitual, TFG: tasa de filtrado glomerular.
En el grupo de SH hubo una recidiva. No se observaron otras complicaciones en ninguno de los grupos al final del seguimiento.
DiscusiónDistintos factores como la alta prevalencia de cáncer genitourinario23, la repercusión de la pandemia por SARS-CoV-224 y la creciente incidencia de UL2,7 conducen a la necesidad de valorar nuevas estrategias de prevención y tratamiento para estos pacientes en el ámbito de la Atención Primaria. El riesgo de recidiva de los pacientes con UL puede llegar hasta el 50% en presencia de determinados factores de riesgo4. En nuestra opinión, una evaluación sistemática de estos pacientes podría ayudar a identificar factores etiológicos corregibles, mejorando la eficiencia del tratamiento conservador. En los últimos años, el interés por los «programas de seguimiento» ha sido creciente15–17. Estos programas proponen la detección de aquellos pacientes con un mayor riesgo de recidiva proponiendo, para estos casos, un seguimiento más individualizado. De acuerdo con Grases25 los programas de seguimiento deberían incluir: 1) la historia clínica, 2) el estudio del cálculo, 3) parámetros analíticos en sangre y orina y 4) información sobre el estilo de vida del paciente. Jung et al.15, por su parte, proponen que «la evaluación y el manejo médico debe ser personalizado, de acuerdo con el riesgo de recurrencia, la severidad de la UL, la presencia de comorbilidades y la motivación del paciente». No hemos encontrado en la literatura ningún estudio que evalúe la eficacia clínica de un programa de seguimiento en pacientes con UL en el ámbito hospitalario ni en AP.
Al igual que otros autores interesados en el tratamiento conservador de la UL26,27 escogimos un estudio piloto (EP) para valorar la seguridad, eficacia y viabilidad de nuestros métodos. Los EP se han definido como «test a pequeña escala de los métodos y procedimientos que se utilizarán a una escala mayor si el estudio piloto demuestra que dichos métodos y procedimientos pueden funcionar»28. Arain et al.29, por su parte afirmaron que los EP son como «ensayos clínicos en miniatura» destinados a valorar la viabilidad del trabajo pero que también estudian el efecto de la intervención realizada. El tamaño muestral adecuado para este tipo de estudios ha sido ampliamente debatido22,29,30. Lancaster et al.30 afirmaron que 30 casos puede ser una cifra suficiente para satisfacer sus objetivos. Arnold et al.28, por su parte, concluyeron que no existe un consenso claro, encontrando una media de 59,6 participantes (rango 20-120) en los trabajos analizados. Por este motivo, y dentro de las recomendaciones encontradas en la bibliografía, decidimos un tamaño muestral de 30 casos.
Los criterios de viabilidad estudiados (objetivo principal del estudio) se cumplieron mayoritariamente excepto en dos puntos: 1) los recursos humanos disponibles se vieron sobrepasados para realizar el seguimiento en el tiempo estipulado ya que tres investigadores fueron insuficientes para el trabajo de campo. En consecuencia, decidimos aumentar el número de investigadores participantes en la recogida de datos o bien replantear la exhaustividad de nuestras revisiones para un siguiente estudio y 2) en la primera revisión de los pacientes del grupo de SS (día 10) observamos que muchos de ellos tenían una radiografía de abdomen reciente (bien del episodio agudo hecha en el Servicio de Urgencias bien en el contexto de su UL recidivante) con lo que consideramos innecesario someterles a una nueva dosis de radiación y decidimos suprimir esta variable una vez comenzado el estudio. Los resultados clínicos preliminares no mostraron evidencias que pudieran contraindicar o posponer la aplicación de nuestra propuesta de seguimiento en términos de seguridad. No se encontraron diferencias relevantes en las variables clínicas ni se registraron complicaciones en ninguno de los dos grupos más allá de la recidiva registrada en el grupo de SH. A pesar de las explicaciones que proporcionamos a los pacientes, ninguno aportó el cálculo para su estudio con lo que no se prescribió tratamiento específico en el grupo de SS. Para la medida de la función renal escogimos la TFG (mediante la ecuación CKD-EPI) en lugar de la creatinina, por ser la forma de valoración más extendida para la función renal31. También recogimos la dilatación pielocalicial mediante ecografía que aportó un dato de carácter morfológico del parénquima renal18. No hemos encontrado ensayos clínicos que concluyan qué variable es mejor a la hora de monitorizar el daño producido en el tiempo por la UL a nivel renal15,32,33. Es posible que la suma de ambas variables, (funcional y morfológica), sea más precisa que cada una de ellas por separado. Futuros estudios deberán confirmar esta hipótesis.
Encontramos algunas limitaciones reseñables: 1) en el análisis de los parámetros descriptivos se observaron diferencias significativas entre grupos en la TFG a favor del grupo de SS. Probablemente, se debió al limitado número de casos por grupo (14 y 16 en SS y SH, respectivamente). Estos datos limitan la interpretación de los resultados encontrados al final del seguimiento (diferencias estadísticamente significativas a favor del grupo de SS en la TFG) sin invalidar nuestro objetivo principal. Asimismo, las diferencias significativas observadas en la media de edad entre los grupos (45,2 frente a 55,9 en SS y SH, respectivamente) podría cuestionar la validez interna de la diferencia observada en la variable TFG. Sin embargo, la fórmula utilizada para el cálculo de dicho valor (CKD-EPI)31 se ajusta por edad y sexo con lo que las posibles diferencias debidas a este factor quedarían descartadas; 2) un seguimiento de 3 meses es corto y probablemente insuficiente para valorar el potencial daño producido por la UL a nivel renal sin embargo, como se ha expuesto, se trata de una comprobación clínica preliminar; 3) de acuerdo con otros autores15, el grado de motivación de los pacientes es esencial para una buena evolución de la enfermedad y, en este sentido, creemos que los problemas observados para fijar las citas de revisión en el grupo de SS pudieron deberse, en parte, a un seguimiento excesivamente exhaustivo (2 analíticas y 3 ecografías en 3 meses) en pacientes mayoritariamente asintomáticos. En el futuro diseño plantearemos dos analíticas (10 y 90 días) y 3 ecografías (10 y 90 días y 6 meses) para este grupo y 4) por último, las ecografías fueron realizadas por tres médicos residentes pudiendo incurrir en un sesgo por variabilidad interobservador. Sin embargo, todas las ecografías fueron supervisadas por dos especialistas en medicina de familia con amplia experiencia en ecografía clínica. Otros sesgos como la falta de representatividad de la muestra o los abandonos del estudio han sido ampliamente comentados en otros puntos de esta discusión.
ConclusionesEn conclusión, nuestro estudio piloto cumplió con los objetivos de viabilidad necesarios para la realización de un ensayo clínico en pacientes con urolitiasis en atención primaria. No observamos ninguna evidencia que contraindicara su realización en términos de seguridad si bien los resultados clínicos preliminares no mostraron diferencias significativas entre las dos modalidades de seguimiento.
Responsabilidades éticasEl estudio fue aprobado por el Comité de Ética de la Investigación con Medicamentos del Principado de Asturias y el Comité de Investigación del Área V (Apéndice A).
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Agradecemos a la Plataforma de Bioestadística y Epidemiología del Instituto de Investigación Sanitaria del Principado de Asturias (ISPA) su decisiva ayuda con el análisis de datos y sus certeros consejos. Agradecemos al Dr. Álvaro Díaz Álvarez, del Centro de Salud El Natahoyo de Gijón, su asesoramiento en el diseño del estudio.