El papel que los anticonceptivos reversibles de larga duración, como los dispositivos intrauterinos (DIU), pueden tener en la reducción de la tasa de embarazos no deseados, hace que superar las barreras a su uso adquiera especial relevancia. En el presente trabajo se revisan algunas de las barreras más comunes al uso de DIU –incluyendo los liberadores de levonorgestrel (DIU-LNG)–, ofreciendo información de utilidad y sugerencias en aspectos clave antes, durante y después de la inserción de estos dispositivos; para ello, se ha revisado la evidencia científica más actual y se aporta la experiencia de los autores allá donde no exista suficiente evidencia. Entre los aspectos considerados antes de la inserción, se revisa la manera de valorar la elegibilidad de la mujer, cómo informarla adecuadamente, la necesidad de saber cuál es el DIU que mejor se adapta a sus características y necesidades y cuál es el mejor momento para insertarlo. Se revisan los estudios acerca de medidas farmacológicas y no farmacológicas que han demostrado tener un efecto en la reducción del dolor durante la inserción de un DIU. Se cometan también factores predictores del dolor y cómo mejorar la vivencia de la mujer durante la inserción puede ayudar a mitigarlo. La posibilidad de complicaciones como una perforación, aunque baja, requiere conocimiento sobre su manejo e informar adecuadamente a la usuaria sobre signos y síntomas indicativos. La inserción de DIU puede ser especialmente dificultosa en mujeres con estenosis post-conización o que hayan sufrido una cesárea, motivo por el que se revisa. Por último, se comenta la actuación en caso de síndrome vasovagal y aspectos post-inserción, como el dolor o la desaparición de hilos, y cuándo es aconsejable realizar visitas de seguimiento.
The role that long-acting reversible contraceptives, such as intrauterine devices (IUDs) can play in reducing the rate of unwanted pregnancies makes overcoming barriers to their use gain in importance. This paper reviews some of the most common barriers to the wide use of IUDs –including levonorgestrel-releasing intrauterine systems (LNG-IUSs)-, offering useful information and suggestions on key aspects before, during and after placement of these devices. To this end, the most up-to-date scientific evidence has been reviewed and where evidence is insufficient, the authors draw on their experience. Among the aspects to be considered before IUD placement, we examine how to determine a woman's eligibility, how to provide proper information, the need to know which IUD is best suited to her characteristics and needs and when is the best time for placement. Studies on pharmacological and non-pharmacological interventions that have been shown to have an effect on pain relief during IUD placement are discussed. Factors that can predict pain are also discussed, as well as how to help minimize it by improving women's experience during insertion. The risk for complications such as uterine perforation is low. Despite this, healthcare practitioners should be trained on how to manage them and should properly inform users on warning signs and symptoms. IUD placement can be especially difficult in women who present with stenosis after conization or who have undergone a Caesarean section, which we also analyze. Lastly, we examine management of vasovagal syncope and post-placement side-effects, such as pain or lost threads and provide guidelines for follow-up visits.
Los dispositivos intrauterinos (DIU) son métodos anticonceptivos reversibles de larga duración (LARC, long-acting reversible contraception). Están indicados en la mayoría de mujeres, incluidas adolescentes, nulíparas o mujeres que han sufrido un aborto (OMS, 2018). Tienen pocas contraindicaciones (OMS, 2015, NICE, 2019) y la ventaja de que el cumplimiento es independiente de la participación activa de la usuaria. Hoy en día disponemos de dos tipos de DIU, el de cobre (DIU-Cu) y el
liberador de levonorgestrel (DIU-LNG, también denominado sistema liberador intrauterino de LNG, SLI-LNG), que impide la proliferación del endometrio y espesa el moco cervical, lo que dificulta el movimiento del esperma a través del cérvix.
La inserción del DIU-LNG es fácil en más del 80% de las mujeres y exitosa en más del 95% de ellas, independientemente de la paridad, y el riesgo de complicaciones tras la inserción es bajo (Bahamondes et al., 2011, Gemzell-Danielsson et al., 2012, Harvey et al., 2012, Gemzell-Danielsson et al., 2015, Beckert et al., 2020). Pese a ello, el uso de estos dispositivos está poco extendido en España: datos recientes indican que apenas un 8,6% de las mujeres fértiles de nuestro país usa un DIU, de las que la mitad usan un DIU-LNG (SEC, 2018), un porcentaje que apenas ha variado en los últimos años (SEC, 2016). El uso reducido de DIU-LNG en algunos entornos guarda relación con la existencia de barreras hacia los DIU –tanto en el profesional sanitario como en la mujer– originadas por dudas, temores y creencias erróneas, muchas de las cuáles son comunes en ambos (Black et al., 2012, Martínez-Benavides y Gutiérrez-Alés, 2015, Zimmermann et al., 2019). La prescripción del DIU se ve afectada por estas barreras, que desaparecen cuando el profesional sanitario debidamente entrenado gana experiencia en el uso de estos dispositivos (Bahamondes et al., 2014). Dado el relevante papel que podrían tener los DIU en la reducción de la tasa de embarazos no deseados (ACOG, 2009), es fundamental superar estas barreras y aumentar la confianza en la inserción para lograr así un uso más generalizado.
La Sociedad Española de Contracepción (SEC) ha desarrollado recientemente dos protocolos sobre el DIU-Cu y el DIU-LNG que recogen información de utilidad para su uso, como los criterios de elegibilidad de la Organización Mundial de la Salud (OMS, 2015), los modelos comercializados, los beneficios contraceptivos y no contraceptivos, el perfil de seguridad (efectos secundarios, riesgos y complicaciones) y las contraindicaciones. Estos protocolos ofrecen, además, consejos clínicos y recomendaciones para una inserción segura, el seguimiento, el asesoramiento de las mujeres y la retirada del dispositivo (SEC, 2019a, SEC, 2019b). El presente trabajo pretende contribuir a superar algunas de las barreras más comunes a la inserción de DIU entre los profesionales sanitarios –especialmente en lo que se refiere a los DIU-LNG–, ofreciendo información de utilidad y sugerencias en aspectos clave antes, durante y tras la inserción de estos dispositivos, de los que se aporta la evidencia más actual y la experiencia de los autores allá donde no exista suficiente evidencia. Cuando se ha considerado necesario, se refiere a los lectores a los citados protocolos, dado su vigencia e interés para el objetivo del trabajo.
MétodosEl presente trabajo nace de una reunión de expertos llevada a cabo con el objetivo de revisar los aspectos referentes a la inserción de DIU que requiriesen ser actualizados o abordados específicamente con el fin de contribuir a un uso más generalizado de estos dispositivos. Participaron siete ginecólogos con amplia experiencia en el manejo de DIU. Con el objetivo de dar un carácter práctico a la información generada, estos aspectos se dividieron en tres secciones, cada una de las cuales se asignó a un grupo de dos o tres expertos: «Antes de la inserción» (IC e IP), «Durante la inserción» (MA, PL y JQ) y «Después de la inserción» (JG y FM). Cada grupo se encargó de la selección de temas de interés, la búsqueda bibliográfica correspondiente y la presentación de la evidencia. Esta información se compartió y debatió en una reunión virtual que tuvo lugar en junio de 2020. Una vez consensuados los aspectos de interés para ser publicados y cómo abordarlos, cada uno de los expertos se encargó de la redacción de sus secciones correspondientes. Los contenidos se compartieron electrónicamente entre todos los autores hasta aprobarse una versión final. La coordinación de la redacción y la posterior edición de los textos hasta su formato final corrieron a cargo de un redactor médico.
La búsqueda bibliográfica se llevó a cabo en PubMed con base en una selección de tópicos en inglés y español. Estos incluían el dispositivo (DIU, DIU-LNG o SLI-LNG, o su equivalente en inglés: IUD, LNG-IUD o LNG-IUS) y términos relacionados con el aspecto a abordar en cada caso. La búsqueda se acotó a los 10 últimos años, con fecha de cierre a junio de 2020. Los artículos obtenidos fueron revisados manualmente por los autores y seleccionados de acuerdo con la calidad de su evidencia. Esta información se complementó con revisiones y guías de referencia disponibles y la experiencia de los autores.
ResultadosAntes de la inserciónInformación a recopilar antes de la inserción de un DIUEs necesario realizar una historia clínica detallada de la mujer encaminada a indagar su elegibilidad para la inserción de un DIU (OMS, 2015). La historia clínica, junto con la historia sexual, permitirá identificar a las mujeres que presentan factores de riesgo de infecciones de transmisión sexual (ITS), dado que estas pueden ser asintomáticas. Los factores de riesgo de ITS incluyen los siguientes (SEC, 2019a, SEC, 2019b):
- •
Ser sexualmente activa antes de los 25 años
- •
Tener una nueva pareja sexual en los últimos 3 meses
- •
Tener más de una pareja sexual en el último año
- •
Tener una pareja sexual que tiene otras parejas sexuales
- •
Una historia de ITS previa
- •
Haber tenido contacto previo con ITS
- •
El abuso de alcohol u otras sustancias
De entre estos, el mayor factor de riesgo para ITS es la edad, por lo que de forma general se recomienda investigar la posibilidad de ITS en mujeres sexualmente activas menores de 25 años (Faculty of Sexual & Reproductive Healthcare, 2019). La valoración de una posible ITS se complementa con una exploración física con examen pélvico. Se debe ofrecer el despistaje de ITS con exudado vaginal y endocervical a toda mujer asintomática con factores de riesgo de ITS (edad, fundamentalmente) que solicite un DIU.
El embarazo o sospecha del mismo es también una contraindicación. Por ello, es necesario tener una certeza razonable de que la mujer no está embarazada, lo que se logra si no presenta síntomas o signos de embarazo y cumple una serie de criterios (OMS, 2018). Estos criterios se presentan en forma de cuestionario en la tabla 1.
Criterios de exclusión razonada de un embarazo*
| ¿Tuvo relaciones sexuales desde la última menstruación normal?¿Ha utilizado de manera correcta y consistente un método anticonceptivo fiable?¿Se encuentra en los primeros siete días desde el inicio de una menstruación normal?¿Se encuentra en los primeros siete días después de un aborto provocado o espontáneo?¿Todavía no pasó la cuarta semana del puerperio? (en el caso de mujeres que noestán amamantando).¿Está amamantando total o casi totalmente, tiene amenorrea y lleva menos de seis meses de puerperio?a |
Adaptado de OMS, 2018.
Para excluir la posibilidad de embarazo, la mujer tiene que contestar «no» a la pregunta 1 y «sí» a las preguntas 2-6 que procedan.
Sólo si se cumplen estrictamente los criterios del método de amenorrea de la lactancia (MELA) (OMS, 2018).
La realización de una ecografía permite determinar el tamaño de la cavidad uterina y la posición del útero, así como determinar posibles anormalidades que dificulten la inserción o contraindiquen el DIU (p. ej., distorsión de la cavidad uterina) (OMS, 2015). Aunque la realización de una ecografía no es obligatoria en la inserción de un DIU, es altamente recomendable. Su uso rutinario se ve favorecido por la disponibilidad actual de las consultas ginecológicas. La posibilidad de realizar una ecografía será de gran importancia durante el proceso de inserción, como se verá más adelante.
Informar a la mujer acerca de los beneficios y riesgos de los DIUUna vez comprobado que la mujer es candidata a la inserción de un DIU (OMS, 2015), es importante asesorarla acerca de aspectos como las características de estos dispositivos, su mecanismo de acción, sus ventajas (incluida su alta efectividad), los tipos disponibles y cuál se ajustaría más a sus características o necesidades (p. ej., tiempo durante el cual desee evitar un embarazo), el proceso de inserción (incluida la posibilidad de que experimente dolor y qué medidas se usarán para mitigarlo) y las posibles complicaciones, los riesgos (incluidos los signos y síntomas de estos tal y como se describen en las fichas técnicas correspondientes), los posibles efectos adversos y los beneficios no contraceptivos del modelo elegido (tabla 2). Las mujeres deben ser advertidas de que el DIU no protege de las ITS (SEC, 2019a, SEC, 2019b). El objetivo de este asesoramiento no es otro que el proporcionar a la mujer una anticoncepción efectiva como parte fundamental de la atención integral a su salud (Faculty of Sexual & Reproductive Healthcare, 2019). Esta información debe incluirse en el documento de consentimiento informado, que ha de ser debidamente leído y firmado antes de la inserción. También es recomendable ofrecerla en forma de folleto impreso que pueda llevarse consigo o en formato electrónico. Informar adecuadamente a la mujer puede contribuir a disipar sus dudas, reducir su miedo, aumentar la adherencia al método y fomentar su uso (SEC, 2019a, SEC, 2019b).
Contenido del asesoramiento previo a la inserción de un DIU (SEC, 2019a, SEC, 2019b, Ficha técnica Mirena®, Impress, Faculty of Sexual & Reproductive Healthcare, 2019)
| Características y modo de acción | Consultar ficha técnica de cada producto.La elección de un DIU de duración prolongada reduce la exposición a los riesgos asociados a la inserción y tras ésta (ver más abajo). |
| Ventajas | Pocas contraindicaciones (consultar ficha técnica de cada producto).Alta efectividad independientemente de la motivación y la adherencia de la usuaria (Trussell, 2011).Buenas tasas de continuación.Alta satisfacción entre las usuarias.Son reversibles, con un retorno rápido a la fertilidad cuando se retiran.Son altamente coste-efectivos. |
| Proceso de inserción | La inserción es un proceso que dura apenas unos minutos si no hay complicaciones, lo que ocurre con una frecuencia muy baja (ver más abajo).La inserción y la retirada pueden asociarse con la aparición de algo de dolor y sangrado. Informar acerca de las medidas para mitigar el dolor. |
| Complicaciones durante la inserción | Perforación: el riesgo de perforación es mayor durante el posparto y en mujeres que amamantan (Heinemann et al., 2015). También puede ser mayor en mujeres con cérvix estenótico, útero en retroversión o fijo o con distorsiones en la cavidad (Steenland et al., 2013, Aoun et al., 2014). En cualquier caso, la morbilidad asociada a una perforación y la subsecuente extracción del DIU es baja (Barnett et al., 2017). Se comentará con más detalle en esta publicación. |
| Complicaciones post-inserción | Perforación: aunque ocurre con frecuencia durante la inserción, puede detectarse más tarde. Acudir al médico en caso de aparición de sangrado irregular y dolor.Pérdida de hilos de extracción: se comentará con más detalle en esta publicación.Expulsión: El riesgo de expulsión es de cerca de 1 de cada 20, y es más frecuente durante el primer año, especialmente en los tres primeros meses (Faculty of Sexual & Reproductive Healthcare, 2019). El dolor, el sangrado o no notarse los hilos puede ser indicativo de una expulsión parcial o completa del DIU, especialmente en el caso del DIU-LNG, dado que reduce el flujo menstrual. También puede ser asintomática.Aparición de dolor: acudir a consulta cuando aparece dolor persistente y se acompaña de fiebre, leucorrea o dispareunia. De no ser así, puede resolverse la duda telemáticamente. |
| Cambios en el patrón de sangrado | DIU-Cu: Menstruación prolongada y profusa, sangrado irregular y calambres o dolor durante la menstruación, que suelen ser transitorios y desaparecer a los 3-6 meses de uso.DIU-LNG: Puede haber un incremento inicial del manchado durante los primeros meses de empleo durante el proceso de inactivación de la proliferación endometrial. Posteriormente, la potente supresión del endometrio da lugar a una reducción de la duración y cantidad del sangrado menstrual. Un flujo menstrual escaso frecuentemente desemboca en una oligomenorrea o amenorrea, lo que con el DIU-LNG de 52mg ocurre hasta en el 20% de las usuarias*. |
| Efectos adversos | Consultar la ficha técnica.Las reacciones adversas son más frecuentes durante los primeros meses tras la inserción, desapareciendo con el empleo prolongado. Las reacciones adversas muy frecuentes (> 10% de las usuarias) incluyen el sangrado uterino/vaginal (incluido manchado), oligomenorrea y amenorrea y los quistes benignos de ovario. |
| Riesgo ITS | Los DIU no protegen frente a las ITS, por lo que en situaciones de riesgo se recomienda el uso correcto y consistente de preservativos. |
El patrón menstrual resulta de la acción directa del levonorgestrel sobre el endometrio y no refleja el ciclo ovárico. La función ovárica es normal y los niveles de estradiol se mantienen, incluso en usuarias de del DIU-LNG de 52mg amenorreicas. De no producirse menstruación en el plazo de seis semanas tras el comienzo de la menstruación previa, debe considerarse la posibilidad de embarazo. No es necesaria la repetición de la prueba de embarazo en usuarias amenorreicas a no ser que aparezcan otros síntomas de embarazo. Con base en el potente efecto reductor del sangrado menstrual, el DIU-LNG de 52mg está indicado en el tratamiento del sangrado menstrual abundante.
DIU, dispositivo intrauterino; DIU-Cu; DIU de cobre; DIU-LNG, DIU con levonorgestrel; EIP, enfermedad inflamatoria pélvica; ITS, infección de transmisión sexual.
A la hora de elegir entre un DIU-Cu o un DIU-LNG hay que tener en cuenta varios factores relacionados con el dispositivo mismo y con las características de la mujer. Entre las primeras, además de las contraindicaciones propias de cada dispositivo, es importante considerar el tamaño del DIU y el grosor del insertor, dado que se relacionan con la aparición de dolor durante la inserción en mujeres con un cérvix estrecho (p. ej., nulíparas), y la duración. En lo que respecta a las mujeres, hay que considerar el deseo de la mujer de usar anticoncepción hormonal o el tiempo durante el cual desee evitar un embarazo o la presencia de alteraciones como la dismenorrea o sangrado menstrual abundante, en las que el DIU-LNG de 52mg puede aportar beneficios añadidos (Ficha técnica Levosert®, Impress,Ficha técnica Mirena®, Impress). La edad o la paridad no son una contraindicación para el uso de estos anticonceptivos (OMS, 2015).
Elección del momento idóneo para la inserción del DIUSi la mujer no presenta ninguna categoría 3 o 4 en los criterios de elegibilidad (OMS, 2015) y no muestra ninguna contraindicación para la inserción del DIU elegido, idealmente debería de poder procederse a la inserción el mismo día en que se ofrece el asesoramiento anticonceptivo (Whiteman et al., 2013, SEC, 2019b, ACOG, 2015). De esta forma, se evitan retrasos innecesarios –lo cual tiene mayor relevancia si las listas de espera son largas– que podrían incrementar el riesgo de embarazos no deseados. Los DIU pueden insertarse en cualquier momento del ciclo, siempre que se tenga una certeza razonable de que la mujer no está embarazada, por lo que no es necesario esperar a que la mujer esté menstruando (SEC, 2019a, SEC, 2019b). El DIU-LNG puede insertarse inmediatamente después de un aborto (espontáneo o inducido) y del parto (SEC, 2019b).
La presencia de cervicitis purulenta o infección actual por clamidia o gonorrea (ITS más frecuentes) o de síntomas sugerentes de estas (dolor a la movilización cervical o secreción purulenta en el cuello) son contraindicaciones para la inserción de un DIU. En estos casos de ITS con clínica evidente se recomienda retrasar la inserción del DIU hasta que se disponga de los resultados de las pruebas, se haya tratado la infección y se haya resuelto el cuadro clínico (Faculty of Sexual & Reproductive Healthcare, 2019).
En mujeres con factores de riesgo que no presenten síntomas de ITS, puede procederse a la inserción sin profilaxis antibiótica siempre que la mujer sea fácilmente localizable en caso de que el resultado del cultivo sea positivo (Faculty of Sexual & Reproductive Healthcare, 2019). En este caso se debe instaurar el tratamiento antibiótico apropiado, sin que sea necesario retirar el DIU (SEC, 2019b). El riesgo de padecer una enfermedad inflamatoria pélvica (EIP) no es inferior si se espera a tener los resultados antes de la inserción (Sufrin et al., 2012, Faculty of Sexual & Reproductive Healthcare, 2019).
Durante la inserciónEstrategias para prevenir el dolor durante la inserciónEl temor a una inserción dificultosa y/o dolorosa es una de las principales barreras para la prescripción de un DIU y para que la mujer lo elija como opción (Gemzell-Danielsson et al., 2019, Black et al., 2013). Este temor puede estar originado por vivencias ginecológicas dolorosas previas o por comentarios de otras mujeres (Gemzell-Danielsson et al., 2019, Black et al., 2013), aunque tras el procedimiento el grado de satisfacción con la inserción suele ser alto y la mayoría recomendaría este método (Akers et al., 2018, Narayan et al., 2018), lo que pone de manifiesto la importancia de superar esta barrera al uso de DIU en las mujeres.
El dolor durante la inserción puede originarse en el momento de la colocación de la pinza de Pozzi para traccionar el cérvix y rectificar el eje uterino, durante el uso del histerómetro para medir la cavidad uterina, durante la colocación del tubo insertor o durante la inserción misma (Akdemir y Karadeniz, 2019). Abordar el dolor durante la inserción es importante, ya que puede dificultar la inserción por la aparición de espasmos musculares o por movimiento de la mujer. Si el dolor es moderado o intenso, puede además incrementar el riesgo de síncope vasovagal durante la inserción o inmediatamente después de esta (Kass-Wolff y Fisher, 2014).
Factores predictores de dolorEste aspecto es de gran relevancia a la hora de enfocar la estrategia para mitigar el dolor, tanto en el consejo como en intervenciones farmacológicas o no farmacológicas, motivo por el cual ha sido investigado en varias publicaciones. Los factores predictores de un mayor dolor durante el proceso de inserción pueden ser tanto físicos –detectables rutinariamente durante la exploración o a partir de la historia clínica– como psicológicos/socioculturales (Gemzell-Danielsson et al., 2019). Pese a que muchos de ellos podrían considerarse como «no modificables» (paridad, edad, resistencia cervical, etc.), otros, como el tamaño del insertor, la inserción durante la menstruación o no (en nuligrávidas), el que haya pasado mucho tiempo (> 13 meses) desde el último parto o no, entre otros, serían «modificables». Entre estos últimos cabe destacar la anticipación o la expectativa de dolor de la mujer (Allen et al., 2014, Dina et al., 2018, Hunter et al., 2020), que puede estar provocada tanto por el miedo a la inserción del DIU, como por la ansiedad previa a la inserción y, como comentamos anteriormente, por ideas preconcebidas negativas acerca de los DIU, todos ellos aspectos con un fuerte componente emocional (Akdemir y Karadeniz, 2019). Estas potenciales barreras pueden abordarse en el asesoramiento inicial, lo que pone de nuevo de manifiesto la importancia de proveer a la mujer con una información lo más completa posible antes de iniciar el procedimiento.
Históricamente la nuliparidad ha sido una barrera importante para la prescripción de un DIU, dado que se asocia a un canal cervical más estrecho que el de mujeres multíparas, lo que puede dificultar su inserción y causar dolor. Sin embargo, diversos estudios han mostrado que la mayoría de las inserciones pueden hacerse sin dificultad en estas mujeres y que la tasa de fallos es baja (Colomé y De la Viuda-García, 2014), lo que indicaría que en mujeres nulíparas la inserción no se asociaría con un dolor mayor con respecto a mujeres multíparas. En un estudio reciente llevado a cabo en 1.110 mujeres, la mitad de ellas nulíparas, en las que se insertó el DIU-LNG 12, clasificaron el dolor como «ninguno o leve» en el 67,4% de los casos de mujeres nulíparas (Beckert et al., 2020).
Intervenciones farmacológicasVarios estudios han analizado el valor de intervenciones farmacológicas antes, durante y después de la inserción. Estas incluyen el uso de antiinflamatorios no esteroides (AINE), anestésicos locales como la lidocaína, misoprostol u otros durante el momento previo a la inserción o la preparación del cérvix. Estas últimas estrategias han sido adoptadas de procedimientos ginecológicos como el legrado o la histeroscopia (Bahamondes et al., 2014). Los resultados son en muchos casos inconcluyentes. Se han realizado diversas revisiones de la evidencia con el fin de poder extraer conclusiones que sirvan para la toma de decisiones en la práctica clínica diaria. En el presente trabajo presentamos los resultados de los estudios en los que se ha demostrado un efecto positivo sobre el dolor. Se recomienda al lector acudir a las fuentes originales (revisiones) para consultar estudios en los que no se haya logrado demostrar el efecto de las intervenciones farmacológicas comentadas. Nuestra búsqueda hasta junio de 2020 no encontró nuevas intervenciones farmacológicas ni nueva evidencia que refuerce la de estas revisiones.
La última revisión sistemática de la Cochrane Library (Lopez et al., 2015) acerca de intervenciones para el dolor durante la inserción de un DIU, que incluyó 33 ensayos clínicos aleatorizados (ECA) –29 de ellos publicados después de 2010–, en los que participaron 5.710 mujeres, mostró que solo el tramadol o el naproxeno y ciertas formulaciones de lidocaína eran efectivos en la reducción del dolor durante la inserción (valorado mediante la escala visual analógica, EVA) en grupos de mujeres específicos (tabla 3). Sin embargo, la mayoría de esta evidencia proviene de estudios únicos y, globalmente, es de calidad moderada. Una revisión llevada a cabo por Gemzell-Danielsson et al. (2019) actualizó la evidencia disponible hasta septiembre de 2018. Este trabajo identificó 11 ECA más con intervenciones farmacológicas (la mayoría consistentes en la anestesia con lidocaína previa a la inserción, pero también con ketorolaco o misoprostol) que dieron lugar a una reducción de la valoración del dolor vs. placebo o el control (tabla 3).
Evidencia positiva acerca la reducción del dolor mediante intervención farmacológica antes / durante / después de la inserción de un DIU
| Referencia | N | Paridad | Intervención farmacológica | Evaluación / Resultados(puntuación EVA) | DIU | Calidad / Nivel de evidencia* |
|---|---|---|---|---|---|---|
| Revisión sistemática de la Cochrane Library (Lopez et al., 2015) | ||||||
| (Massey et al., 1974) | 50 | 96% nulíparas | Analgesia oral con naproxeno 300mg (4 dosis) o placebo. Todas tenían bloqueo paracervical con lidocaína. | DM (IC 95%) vs. placebo después de la inserción en escala de 5 puntos:1 h post-inserción: -1,04 (-1,67; -0,41)2 h post-inserción: -0,98 (-1,64; -0,32)No se encontraron diferencias durante la inserción ni inmediatamente después. | - | Baja |
| (Karabayirli et al., 2012) | 103 | Multíparas | Analgesia oral con naproxeno 550mg, tramadol 50mg o placebo 1h antes de la inserción. | DM (IC 95%) durante la inserción en EVA 10 cm:Tramadol vs. naproxeno: -0,63 (-0,94; -0,32)Naproxeno vs. placebo: -1,94 (-2,35; -1,53) | - | Moderada |
| (Scavuzzi et al., 2013) | 179 | Nulíparas | Maduración cervical con 400μg de misoprostol o placebo 4 h antes de la inserción. | Reducción del dolor moderado o grave vs. placebo durante la inserción en EVA 10cm (RR 0,56 (32/86 vs. 62/95) [IC 95% 0,41-0,76]; P <0,0001) | - | Baja |
| (Mody et al., 2012) | 50 | - | Bloqueo paracervical con lidocaína al 1% 3min antes de la inserción (10 mL) vs. no intervención. | Mediana de 12 vs. 28 sin intervención durante la colocación del tenáculo (P=0,008) con EVA 100mm. No diferencias en el dolor durante la inserción o post-inserción. | DIU-LNG o DIU-Cu Nova T380 | Baja |
| (Ahmadi-Doulabi et al., 2013) | 92 | - | Anestesia local con 5g de crema de lidocaína 2,5% y prilocaína 2,5% o placebo en cérvix y orificio del cérvix 7min antes de la inserción. | DM (IC 95%) vs. placebo en EVA 10 cm:Al extraer tubo insertor: -1,96 (-3,00; -0,92)Durante colocación tenáculo: -2,78 (-3,66; -1,90) | DIU-Cu Nova T380 | Moderada |
| (Tornblom-Paulander et al., 2015) | 209 | Nulíparas | Anestesia local con gel de lidocaína al 4% o placebo 5min antes de la inserción en superficie del portio, en el canal cervical y en la cavidad uterina (8,5 mL). | DM (IC 95%) vs. placebo post-inserción en EVA 100 mm:A los 10 min: -15,90 (-22,77; -9,03)A los 30 min: -11,10 (-19.05; -3,05) | DIU-LNG o DIU-Cu Nova T380 | Moderada |
| (Aksoy et al., 2016) | 200 | Multíparas | Anestesia local con spray de lidocaína al 10% o placebo (3 pufs en la superficie externa del cérvix y 1 puf hacia el orificio externo del cérvix) aplicado 3min antes de la colocación del tenáculo (40 mg). | Mediana (rango): 1,0 (0-6) vs. 3,0 (0-7) con placebo (P <0,001) en EVA 100mm. | DIU-Cu Nova T380 | Moderada |
| Revisión de Gemzell-Danielsson (Gemzell-Danielsson et al., 2019) | ||||||
| (Crawford et al., 2017) | 72 | Sobre todo paras | Analgesia oral preinserción con 20mg de ketorolaco o placebo 40-60min antes de la inserción. | Puntuación media vs. placebo en EVA 10 cm:Durante la inserción: 4,2 vs. 5,7; P=0,0031Dolor global: 3,6 vs. 4,9; p=0,047A los 10min post-inserción: 1,1 vs. 2,5; P=0,007 | - | 2 |
| (Abdellah et al., 2017) | 140 | Con cesárea previa | Maduración cervical con 2 pastillas de 400μg de misoprostol (total 800μg) o placebo 3 h antes de la inserción. | Puntuación media vs. placebo en EVA 10cm durante la inserción: 2,7±0,6 vs. 4,3±0,8; P=0,001 | DIU-Cu Nova T380 | 2 |
| (Maged et al., 2018) | 120 | Con cesárea previa | Maduración cervical con 600μg de misoprostol o placebo aplicado en la vagina 6 h antes de la inserción. | Puntuación media vs. placebo en EVA 10cm durante la inserción: 5,7±1,4 vs. 6,5±0,9; P <0,001 | - | 2 |
| (Akers et al., 2017) | 95 | Nulíparas | Bloqueo paracervical con lidocaína 1% vs. simulación de bloqueo con aplicador. | Puntuación media (IC 95%) vs. simulación en EVA 100 mm:Durante la inserción: 30,0 (20-58) vs. 71,5 (66,0-82,0); P=0,006De las valoraciones incluidas como objetivos secundarios (basal, espéculo, tenáculo, bloqueo, ecografía uterina, inserción del DIU, retirada de espéculo): 27,7 (16,0-42,0) vs. 53,9 (44,0-57,8); P <0,001 | - | 2 |
| (Mody et al., 2018) | 64 | Nulíparas | Bloqueo paracervical con lidocaína al 1% tamponada antes de la inserción (20 ml) vs. no intervención. | Puntuación media vs. placebo en EVA 100 mm:Durante la inserción: 33 vs. 54; P=0,0025min post-inserción: 12 vs. 27mm, P=0,005)global: 30 vs. 51mm, P=0,015).Administración del bloqueo: 30 vs. 8, P=0,003) | - | - |
| (Abd Ellah et al., 2018) | 48 | Nulíparas y paras | Anestesia local con gel de nueva formulación con lidocaína 2%, pluronic (poliol surfactante no iónico) y/o Gelrite® (polisacárido autogelificante) aplicada por la misma usuaria. | Mediana (RIC) vs. control (gel sin Gelrite®) en EVA 10 cm:Durante la inserción: 3 (2-3,75) vs. 6 (5,5-7); P=0,0001.Durante colocación tenáculo: 2 (1-2) vs. 4 (3-4); P=0,0001.Durante ecografía uterina: 3 (2-3) vs. 5 (4-5); P=0,0001. | - | 2 |
| (Karasu et al., 2017) | 151 | Paras | Anestesia local con spray de lidocaína 10% (40 mg) vs. 2g de crema de lidocaína vs. 10mL de inyección de lidocaína (20 mg/mL) vs. control (no anestesia). | Puntuación media vs. crema y control en EVA 10cm durante la inserción: 2,85±2,5cm vs. 4,0±1,7cm vs. 4,25±1,9, respectivamente).Un mayor porcentaje de mujeres experimentó ausencia de dolor con el spray vs. la crema vs. inyección y control:Durante la inserción: 25,5% vs. 1,9% vs. 2,1% vs. 2,0%, respectivamente, P=0,01Durante colocación tenáculo: 39,2% vs. 7,5% vs. 6,4% vs. 4,1%, respectivamente, P=0,01) | - | 2 |
| (Aksoy et al., 2016) | 200 | Paras | Anestesia local con spray de lidocaína 10% (40 mg) o placebo. | Puntuación media vs. placebo en EVA 10cm durante la inserción: 1,01±1,20 vs. 3,23±1,60; P <0,001.El porcentaje de mujeres con puntuación de dolor ≥ 4 fue significativamente inferior:6% vs. 41%, P <0,001. | - | 2 |
| (Tavakolian et al., 2015) | 92 | Paras | Anestesia local con crema de lidocaína-prilocaína o placebo. | Puntuación media vs. placebo en EVA 10cm durante la inserción: 2,65±2,53 vs. 4,61±2,55; P <0,001. | - | 2 |
| (Abbas et al., 2017) | 120 | Paras | Anestesia local con crema de lidocaína-prilocaína o placebo (2 mL) 7min antes de la inserción en el labio cervical anterior seguido de otra aplicación de 2mL de el canal cervical con un aplicador Q-tip. | Puntuación media vs. placebo en EVA 10 cm:durante la inserción: 3,0 vs. 6,5; P=0,0001.Durante colocación tenáculo: 2,0 vs. 4,0; P=0,0001.Durante la ecografía uterina: 3,0 vs. 6,0; P=0,0001. | DIU-Cu Nova T380 | 2 |
| (Fouda et al., 2016) | 90 | Paras (cesárea y parto vaginal) | Analgesia oral con diclofenaco (2 x 50mg 1 h antes de la inserción)+anestesia local con 3mL de gel de lidocaína 2% en el labio cervical o simulación. | Puntuación media vs. simulación de anestesia en EVA 10 cm:Durante la inserción: 3,14±0,92 vs. 3,94±1,3; P=0,001.Durante colocación tenáculo: 1,66±0,85 vs. 2,33±1,19; P=0,003.Las mujeres que dieron a luz mediante cesárea solo presentaron puntuaciones mayores de dolor vs. las mujeres con parto vaginal: 4,41±1,24 vs. 3,29±1,05; P=0,001. | DIU-Cu Nova T380 | 2 |
| Revisiones sistemáticas | ||||||
| (Samy et al., 2019)Incluye metaanálisis en red. | 38 ECA en 6.314 mujeres | Nulíparas y paras | Crema de lidocaína-prilocaína aplicada en la mucosa genital | DM (IC 95%) en EVA 10 cm:Durante la inserción: -2,78 (-5,42; -0,13) vs. ibuprofeno, -2,76 (-4,61; -0,91) vs. placebo y -3,34 (5,48; -1,21) vs. misoprostol.Durante colocación tenáculo: -2,38 (-4,07; -0,68) vs. placebo y -2,70 (-5,07; -0,32) vs. naproxeno. | - | - |
| Bloqueo paracervical con lidocaína | DM (IC 95%) vs. misoprostol en EVA 10cm durante la inserción: -2,78 (-5,42; -0,13) | |||||
| (Perez-Lopez et al., 2018) | 11 ECA en 1.458 mujeres | Nulíparas y paras | Lidocaína (bloqueo paracervical o anestesia local) | DM (IC 95%) en EVA 10 cm:Durante colocación tenáculo: -0,99 (-1,73; -0,26)Durante la inserción: -1,26 (-2,23; -0,29)Inmediatamente después de la inserción: -1,25 (2,17; -0,33) | ||
| (Anthoulakis et al., 2018) | 9 ECA en 700 mujeres | Nulíparas | Lidocaína (n=140) vs. placebo (n=136) | Puntuación media vs. placebo en EVA 10cm durante la inserción: 4,6±2,1 vs. 5,8±2 (OR 0,12 [IC 95% 0,02-0,91]) | - | - |
Según la publicación original.
EVA, escala visual analógica; DM, diferencia media; IC, intervalo de confianza; OR, odds ratio; RIC, rango intercuartílico; RR, riesgo relativo.
Evidencia de calidad baja/moderada: si el riesgo de sesgo es alto para 2 ítems y los riesgos poco claros=3/ para alguno de los factores analizados o poco claro para dos; en estos casos, la evidencia nueva tendrá muy probablemente/probablemente un impacto importante en la confianza de la estimación del efecto y probablemente cambiará/puede cambiar esta estimación (Lopez et al., 2015).
Nivel de evidencia 2 (Oxford Center for Evidence-Based Medicine levels of evidence): estudio aleatorizado u observacional con efecto patente (Gemzell-Danielsson et al., 2019).
El valor de la lidocaína en este contexto, tanto en forma de bloqueo paracervical como de anestesia local, se analizó también en una revisión sistemática y metanálisis reciente que incluyó 11 ECA en los que participaron 1.458 mujeres. Este trabajo concluyó que el uso de lidocaína se asocia solo a una reducción modesta del dolor durante la colocación de la pinza de Pozzi, durante la inserción y después de ésta (Perez-Lopez et al., 2018) (tabla 3). Una revisión sistemática de 9 ECA solo en mujeres nulíparas en las que se insertó un DIU-LNG (N=700) concluyó que la intervención farmacológica con lidocaína al 4% 5 minutos antes de la inserción, tanto en el canal cervical como en la vagina, podría ser de utilidad para reducir el dolor durante la inserción (Anthoulakis et al., 2018) (tabla 3). Pese al potencial valor del uso de lidocaína para la reducción del dolor en el procedimiento de inserción de un DIU, su beneficio práctico puede verse limitado por el tiempo necesario para que haga efecto (3 minutos para el spray y 7 minutos con el espéculo colocado para la crema con lidocaína y prilocaína), lo que puede contribuir a acrecentar la ansiedad en la mujer. Igualmente, es necesario estandarizar la dosis de estos anestésicos locales, así como las rutas y los modos de aplicación para que a la vez que se optimiza la reducción del dolor, se evite la difusión en el tejido vaginal y se maximice la seguridad (Gemzell-Danielsson et al., 2019, Anthoulakis et al., 2018). Aunque en el bloqueo paracervical la administración de lidocaína puede ser dolorosa, el dolor global percibido durante la inserción del DIU es generalmente más leve (Mody et al., 2018).
La anestesia local con crema de lidocaína y prilocaína aplicada en la mucosa cervical ha despertado mucho interés. Además de la evidencia comentada anteriormente (Gemzell-Danielsson et al., 2019), una revisión sistemática y metanálisis en red de 38 ECA publicados hasta septiembre de 2018 (Samy et al., 2019), en el que participaron 6.314 mujeres, mostró que esta estrategia redujo de forma significativa el dolor durante la colocación de la pinza de Pozzi vs. placebo y naproxeno. La aplicación de esta crema logró también resultados superiores durante la inserción vs. ibuprofeno, placebo o misoprostol. El bloqueo paracervical con lidocaína también redujo el dolor durante la inserción comparado con misoprostol (tabla 3). No se observaron diferencias significativas en las comparaciones de otros tratamientos. Ninguna de las intervenciones farmacológicas fue efectiva en la reducción del dolor 5–20min tras la inserción; solo la crema de lidocaína-prilocaína obtuvo el mayor ranking en la reducción del dolor justo después de la inserción. Sin embargo, se carece de evidencia acerca del valor que podría aportar esta crema en mujeres nulíparas.
En general, no se recomienda la dilatación rutinaria del cuello uterino más allá del diámetro del insertor porque puede generar dolor adicional y aumenta el riesgo de un episodio vasovagal (Bahamondes et al., 2014). Cuando se considere necesaria o cuando la inserción sea difícil puede ofrecerse un anestésico local con inyección paracervical para disminuir el dolor (SEC, 2019b). Dado que la necesidad de dilatación cervical o de intervención farmacológica para mitigar el dolor son difíciles de prever, es recomendable tener a mano el equipamiento necesario (Bahamondes et al., 2014).
Los AINE pueden ofrecerse para disminuir el dolor posterior a la inserción (SEC, 2019b).
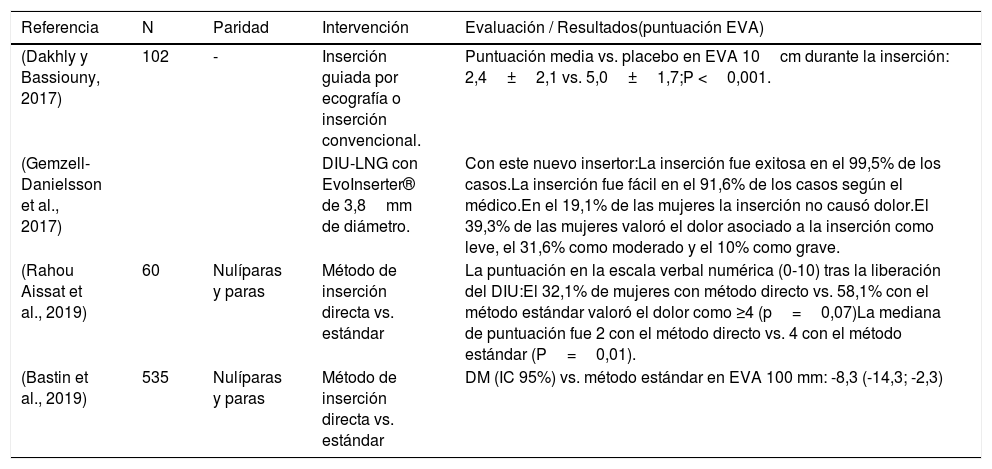
Intervenciones no farmacológicasEntre las intervenciones no farmacológicas durante la inserción, destacan por su novedad algunas relacionadas con el procedimiento como es la aplicación del método de inserción directa, descrito por primera vez en 2005, en contraposición al método estándar recomendado por los fabricantes. Mientras que en este último el insertor pasa a través del orificio cervical interno y llega hasta el fondo uterino, en el método directo el insertor solo se coloca en el orifico y se empuja el dispositivo hacia la cavidad. A pesar de que la evidencia es escasa, los resultados de dos estudios sugieren que el método de inserción directa puede causar menos dolor a la mujer durante la inserción con respecto al método indirecto, con similares tasas de complicaciones durante el procedimiento y efectos adversos (tabla 4) (Bastin et al., 2019, Rahou Aissat et al., 2019).
Evidencia positiva acerca la reducción del dolor antes / durante / después de la inserción de un DIU con intervención no farmacológica
| Referencia | N | Paridad | Intervención | Evaluación / Resultados(puntuación EVA) |
|---|---|---|---|---|
| (Dakhly y Bassiouny, 2017) | 102 | - | Inserción guiada por ecografía o inserción convencional. | Puntuación media vs. placebo en EVA 10cm durante la inserción: 2,4±2,1 vs. 5,0±1,7;P <0,001. |
| (Gemzell-Danielsson et al., 2017) | DIU-LNG con EvoInserter® de 3,8mm de diámetro. | Con este nuevo insertor:La inserción fue exitosa en el 99,5% de los casos.La inserción fue fácil en el 91,6% de los casos según el médico.En el 19,1% de las mujeres la inserción no causó dolor.El 39,3% de las mujeres valoró el dolor asociado a la inserción como leve, el 31,6% como moderado y el 10% como grave. | ||
| (Rahou Aissat et al., 2019) | 60 | Nulíparas y paras | Método de inserción directa vs. estándar | La puntuación en la escala verbal numérica (0-10) tras la liberación del DIU:El 32,1% de mujeres con método directo vs. 58,1% con el método estándar valoró el dolor como ≥4 (p=0,07)La mediana de puntuación fue 2 con el método directo vs. 4 con el método estándar (P=0,01). |
| (Bastin et al., 2019) | 535 | Nulíparas y paras | Método de inserción directa vs. estándar | DM (IC 95%) vs. método estándar en EVA 100 mm: -8,3 (-14,3; -2,3) |
EVA, escala visual analógica; DM, diferencia media; IC, intervalo de confianza;.
En un estudio llevado a cabo en 102 mujeres, la inserción guiada por ecografía no solo redujo el dolor durante la inserción vs. la inserción no guiada, sino que también agilizó la inserción, siendo esta de 33,2±14,8 seg al estar guiada por ecografía vs. 77,7±30,6 seg si no lo estaba (tabla 4) (Dakhly y Bassiouny, 2017). Se observó también que una vejiga urinaria llena, con el fin de cambiar la angulación del útero, podía aumentar el dolor al colocar el espéculo. Además de una gran angulación del útero, el que presente una longitud corta puede asociarse a un mayor dolor durante la inserción (Gemzell-Danielsson et al., 2019). Nuestra experiencia apoya la realización de una ecografía previa a la inserción que permita vislumbrar aspectos anatómicos que puedan dificultar la inserción e incrementar el dolor, o causar una perforación.
El tamaño del DIU (y por tanto del insertor) se ha asociado con el dolor durante la inserción. La disponibilidad de DIU-LNG de diferentes tamaños ha mostrado que aquellos con insertores más finos se asocian con una inserción menos dolorosa: el 72,3% de las mujeres consideraron la inserción del DIU-LNG 13,5mg como «no dolorosa» o que «les produjo dolor leve», frente al 57,9% con el DIU-LNG 52mg (P<0,001) (Gemzell-Danielsson et al., 2012). Un análisis combinado de tres estudios en fase III con DIU-LNG 13,5mg con el dispositivo de inserción EvoInserter®, que presenta un diámetro de tubo de inserción reducido (3,8mm), sugirió que este contribuyó a la facilidad de colocación y que el dolor fue manejable (tabla 4). Análisis exploratorios post hoc indicaron una asociación directa entre la facilidad de inserción/dolor y la edad de la mujer, y entre el dolor y la paridad (Gemzell-Danielsson et al., 2017).
La aplicación de la pinza de Pozzi solo durante unos segundos, haciéndola coincidir con la realización de una maniobra de valsalva de la paciente (por ejemplo toser en el momento de la aplicación) puede facilitar la inserción y contribuir así a reducir el dolor (Faculty of Sexual & Reproductive Healthcare, 2019).
La mejora de la vivencia de la mujerAdemás del asesoramiento previo a la inserción, es fundamental crear un ambiente distendido en la consulta y transmitir confianza, usar estrategias de distracción como la «anestesia verbal» (p. ej., dialogar distendidamente con la mujer) u otras (p. ej., música relajante, elementos multimedia o de distracción con realidad virtual, gráficos interesantes, etc.); sin embargo, la evidencia sobre estas intervenciones es casi inexistente. Un estudio llevado a cabo en 106 mujeres que analizó el efecto de la inhalación de lavanda 30min antes de la inserción mostró que, aunque esta intervención reducía ligeramente la ansiedad antes del procedimiento frente a placebo (P <0,001), no dio lugar a una diferencia significativa en la valoración del dolor (Shahnazi et al., 2012). No obstante, nuestra experiencia apoya el uso de técnicas de distracción durante la inserción.
Ante una sospecha de perforaciónEl riesgo de perforación uterina es muy bajo (2 por cada 1.000 inserciones) (Barnett et al., 2017, Faculty of Sexual & Reproductive Healthcare, 2019). En el estudio europeo prospectivo EURAS, que incluyó a más de 60.000 mujeres usuarias de DIU-Cu o DIU-LNG, hasta un tercio de las perforaciones se detectaron transcurridos los 12 primeros meses tras la inserción (Barnett et al., 2017). El riesgo de perforación fue mayor en mujeres que amamantaban (hasta 6 veces) y durante el posparto (hasta 36 semanas después del parto) (Heinemann et al., 2015), independientemente de cuándo se detectase la perforación (Barnett et al., 2017). En este estudio, el mayor realizado hasta el momento, ninguna de las perforaciones provocó un daño grave a las estructuras pélvicas o intraabdominales. Otros estudios han observado que el riesgo de perforación disminuía al aumentar la paridad y aumentaba conforme lo hacía el número de abortos (Caliskan et al., 2003). Otros autores han descrito factores de riesgo como la poca experiencia del clínico o presentar un cérvix estenótico, un útero inmóvil o en retroversión, así como alteraciones en la distorsión de la cavidad uterina (Steenland et al., 2013, Aoun et al., 2014).
Con el fin de evitar las perforaciones en la medida de lo posible, es recomendable realizar movimientos «delicados y suaves» durante el procedimiento y, en mujeres posparto y lactantes, enderezar cualquier flexión uterina. La inserción guiada por ecografía puede mejorar el éxito y la precisión de la inserción (Elsedeek, 2016). La aplicación de pinzas de Pozzi puede contribuir, además de facilitar la inserción, a reducir el riesgo de perforación (Faculty of Sexual & Reproductive Healthcare, 2019).
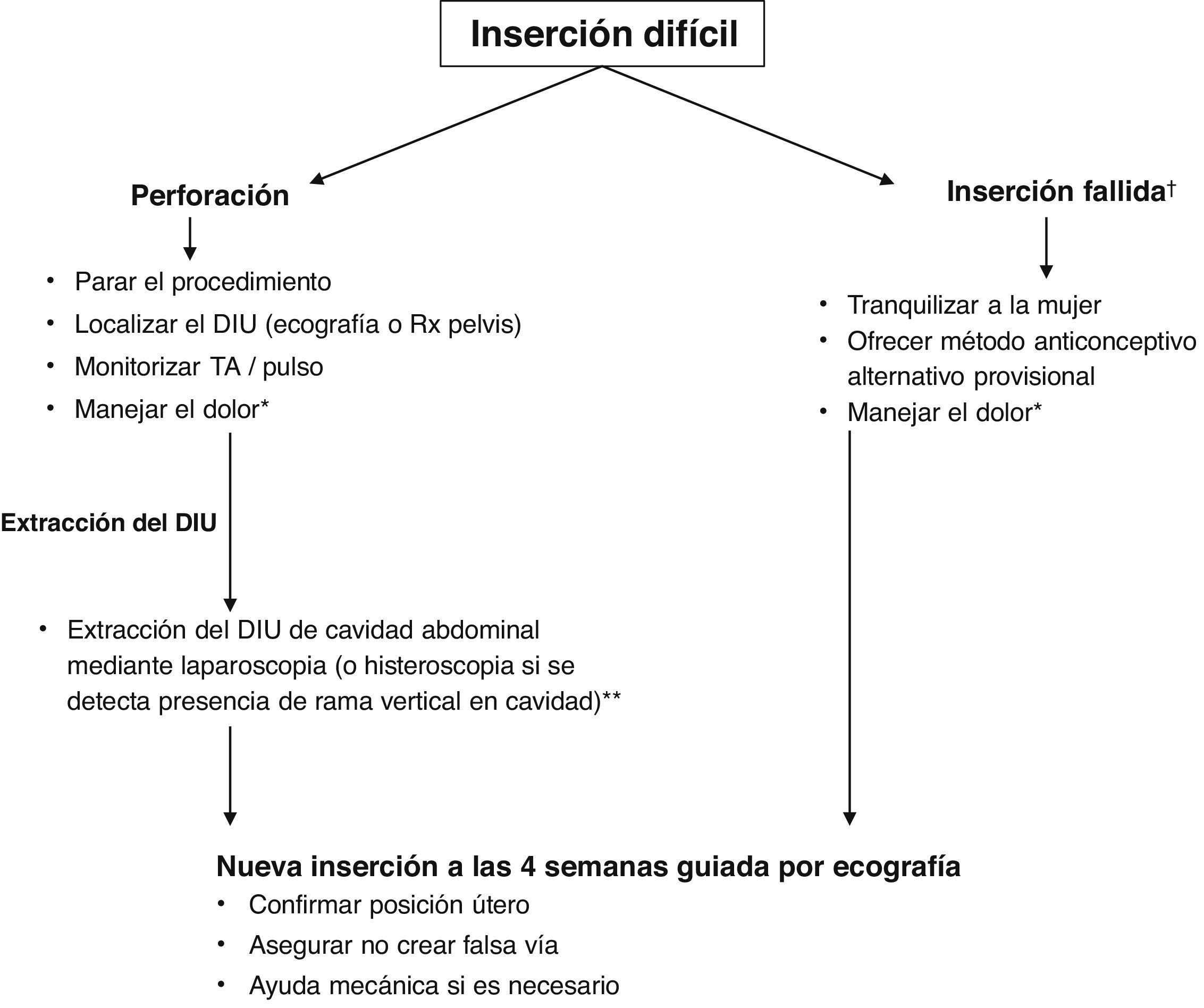
Aunque las perforaciones suelen identificarse en el momento de la inserción, un porcentaje importante se detectan incluso pasado un año (Barnett et al., 2017). Los síntomas que pueden hacer sospechar perforación uterina son sangrado irregular y dolor. Es importante instruir a la mujer en estos signos y resaltar la importancia de que acuda al médico (tabla 1). Igualmente, hay que informarle que la morbilidad asociada a una perforación y la subsecuente extracción del DIU es baja (Barnett et al., 2017). Las acciones a llevar a cabo en caso de sospecharse una perforación se muestran en la figura 1.
Algoritmo de actuación ante una inserción difícil
†Por ejemplo, por dolor intenso
*Ver sección «Estrategias para prevenir el dolor durante la inserción»
**Cuando se diagnostica una perforación, la mayoría de los DIU pueden y deberían de ser extraídos dado el riesgo de inducción de adherencias peritoneales o lesión de órganos vecinos. En la mayoría de los casos la extracción puede llevarse a cabo mediante laparoscopia o histeroscopia, salvo en casos muy poco frecuentes en los que la complicación de la extracción requeriría la realización de una laparotomía. Los riesgos asociados a estas intervenciones hacen que la recomendación de extraer el DIU sea fuente de controversia porque en muchos casos los DIU pueden permanecer en el abdomen sin causar daño durante años. Algunos autores defienden la conveniencia de optar por una actitud expectante en los casos asintomáticos (Rowlands et al., 2016).
DIU, dispositivo intrauterino; Rx, radiografía; TA, tensión arterial.
La malposición del dispositivo en la cavidad uterina es una complicación menos grave que la perforación y ocurre en un 10% de los casos (SEC, 2019b). Otras complicaciones en el momento de la inserción pueden estar relacionadas con la manipulación del DIU previo a la inserción. En algunos dispositivos el manejo simultáneo de la cánula de inserción y el émbolo puede propiciar la caída al suelo. Si ocurre, se debe desechar el dispositivo. Actualmente existen dispositivos integrados como el EvoInserter® que permiten la manipulación con una sola mano, facilitando así la inserción.
Casos con especial dificultadEstenosis post-conizaciónEl tratamiento escisional de lesiones en el cérvix uterino mediante conización quirúrgica es hoy día el tratamiento de elección en mujeres con lesiones cervicales de alto grado (SEGO, 2014, AEPCC, 2015). La estenosis del canal cervical es una de las complicaciones de este procedimiento cuya incidencia varía con la edad y el procedimiento quirúrgico (Houlard et al., 2002). Se define como el estrechamiento del orificio cervical externo que impide introducir una torunda (diámetro menor de 2.5mm).
Si el insertor del DIU no pasa por el canal cervical, debe ajustarse el espéculo de forma que esté completamente alineado con la inclinación del útero y aplicar tracción con la pinza de Pozzi (Prine y Shah, 2018); si es necesario, puede recurrirse a dilatación osmótica (tallos de laminaria) o mecánica. Al igual que para otros procedimientos clínicos como la histeroscopia, las mujeres en las que se identifica una estenosis cervical podrían beneficiarse de una maduración cervical previa con misoprostol (Al-Fozan et al., 2015). Una revisión sistemática y metanálisis llevada a cabo en 2016 analizó la evidencia disponible acerca de la efectividad de diferentes tratamientos para facilitar el procedimiento de inserción: favorecer la inserción, reducir la necesidad de medidas adyuvantes o incrementar el éxito de inserción. De los 15 ECA incluidos, ninguno mostró que la administración de misoprostol, lidocaína intracervical al 2% (inyección o gel tópico±diclofenaco) lograse de forma significativa alguno de estos objetivos vs. placebo (Zapata et al., 2016). Sin embargo, uno de ellos sí demostró una tasa de éxito superior con misoprostol vs. placebo al intentar una segunda inserción (Bahamondes et al., 2015). En este estudio, las mujeres del brazo con tratamiento activo recibieron 200μg de misoprostol aplicado vaginalmente 10h y 4h antes de la inserción. En el 92% de los casos el DIU fue un DIU-LNG. El segundo intento de inserción se llevó a cabo por profesionales sanitarios con amplia experiencia en inserción de DIU. El porcentaje de inserciones exitosas fue de 88% con misoprostol y de 62% con placebo (RR=1,41; IC 95%=8,2; 43,0)
Se carece de evidencia robusta que apoye el uso sistemático de intervenciones farmacológicas para reducir el dolor durante la inserción de un DIU en mujeres con estenosis post-conización. Pueden aplicarse las mismas pautas que las comentadas anteriormente, siendo quizás la anestesia intra o paracervical con lidocaína lo más aconsejado en estos casos (Bahamondes et al., 2014). Las técnicas más habituales para el bloqueo paracervical son la inyección de anestesia en la unión cervicovaginal mediante la aplicación en 4 puntos (a las 2, 4, 8 y 10 de las manecillas de un reloj) o en 2 puntos (sólo a las 4 y 8). Esta última estrategia disminuye el número de punciones, con una eficacia similar a la técnica de 4 puntos. Independientemente del número de puntos de inyección, se aplicarían 10 – 20mL de anestesia (habitualmente lidocaína 1% o cloroprocaína 2%) aproximadamente 10mm dentro del estroma cervical (Vidaeff, 2019).
Si la inserción es imposible pese a estas medidas, hay que interrumpir el procedimiento. Se carece igualmente de evidencia sobre cuál sería el DIU más indicado en estos casos, aunque parece razonable que los DIU de pequeño tamaño puedan facilitar la inserción. Se han publicado dos casos en mujeres con estenosis cervical grave recurrente post-conización en los que la acción antiproliferativa sobre el endometrio del DIU-LNG 52mg usado durante 5 meses redujo complicaciones estenóticas como el hematómetra, la dismenorrea y el sangrado menstrual prolongado. Este DIU redujo también el dolor menstrual, lo que se mantuvo tras la retirada del dispositivo (Motegi et al., 2016).
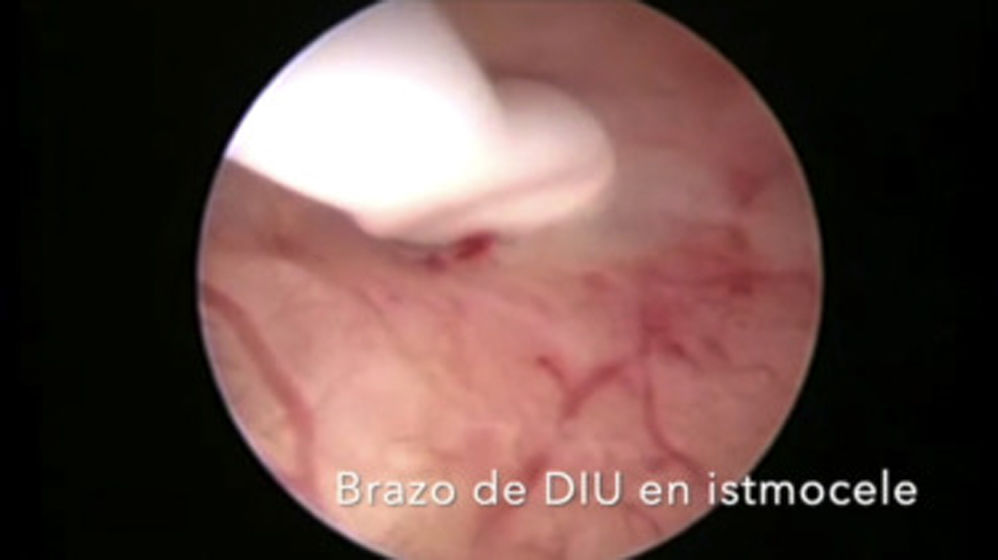
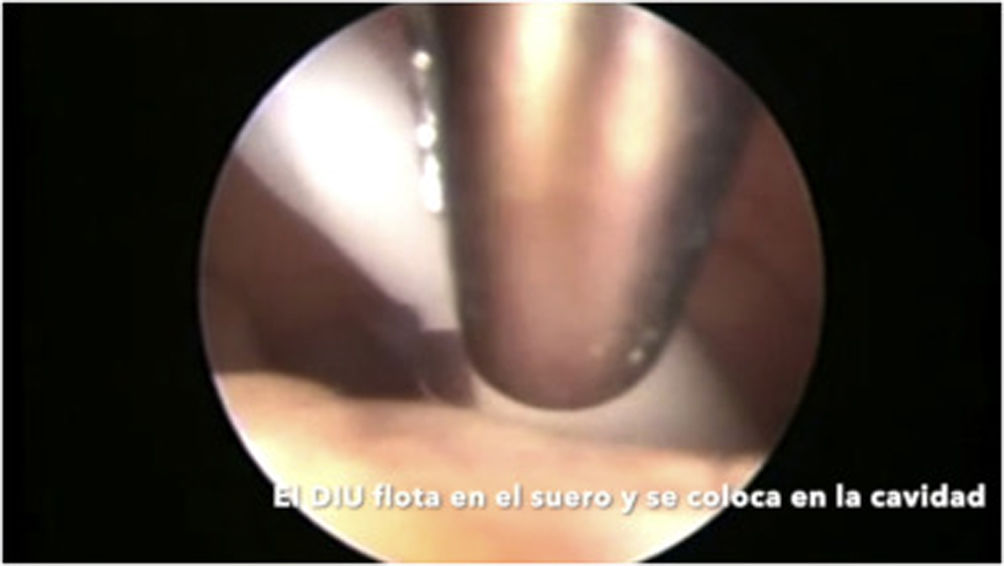
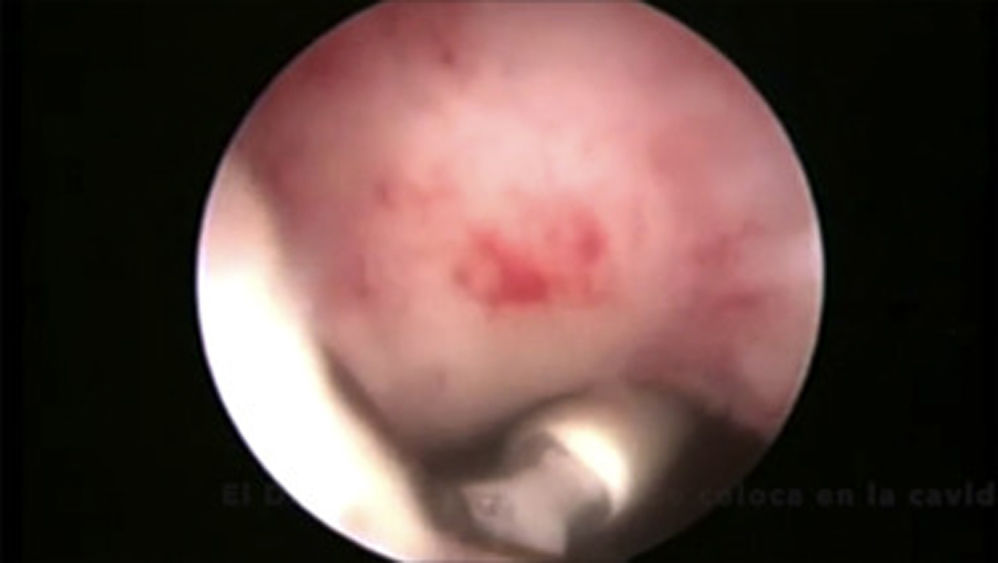
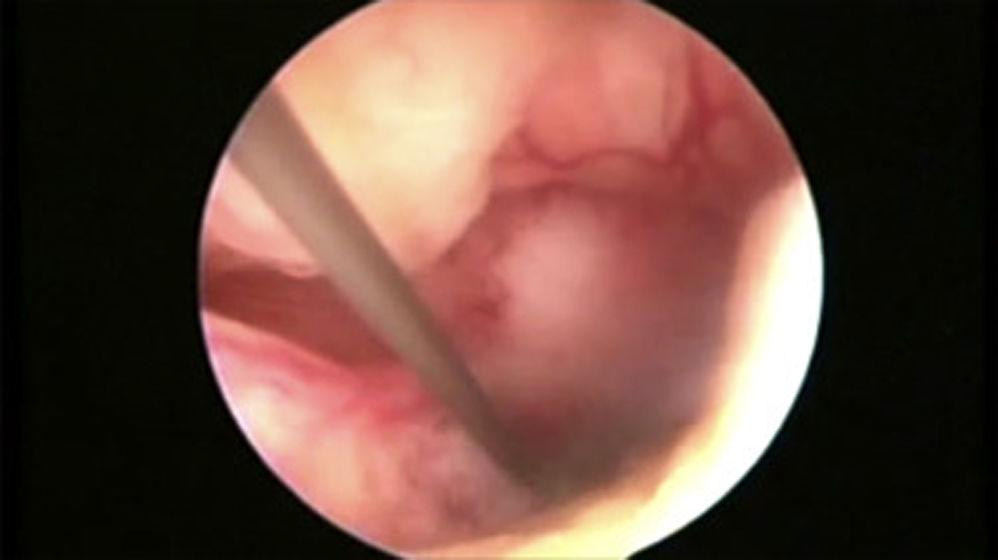
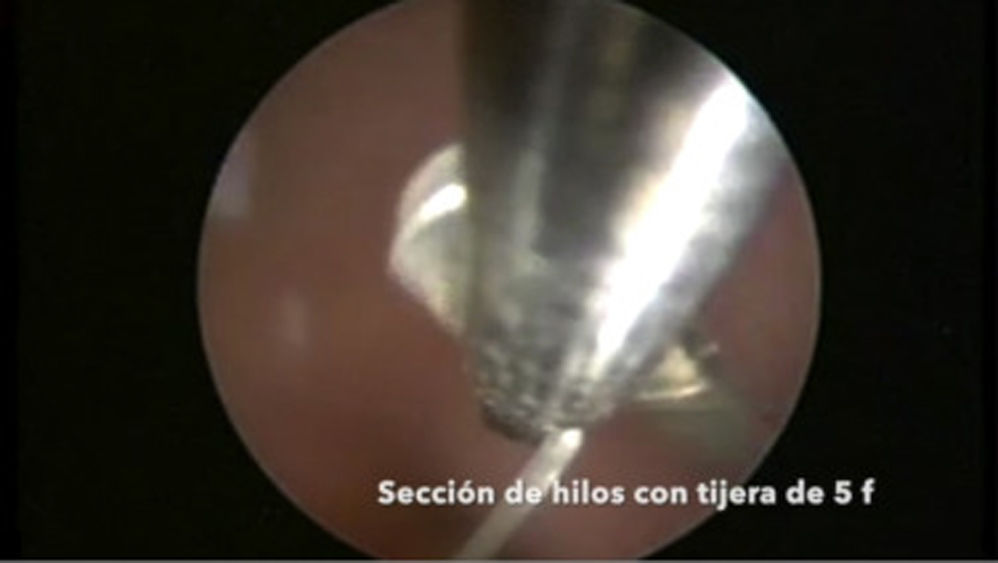
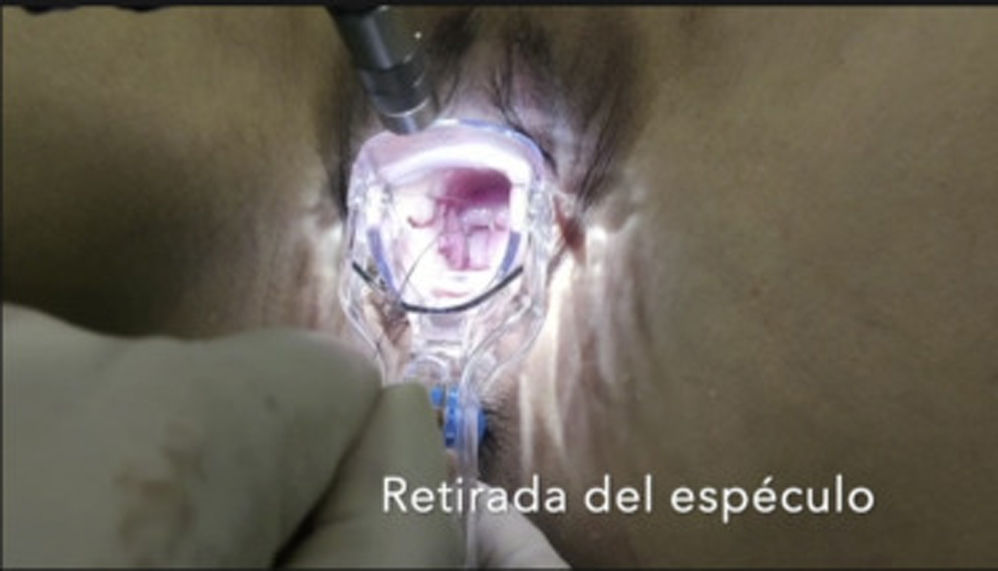
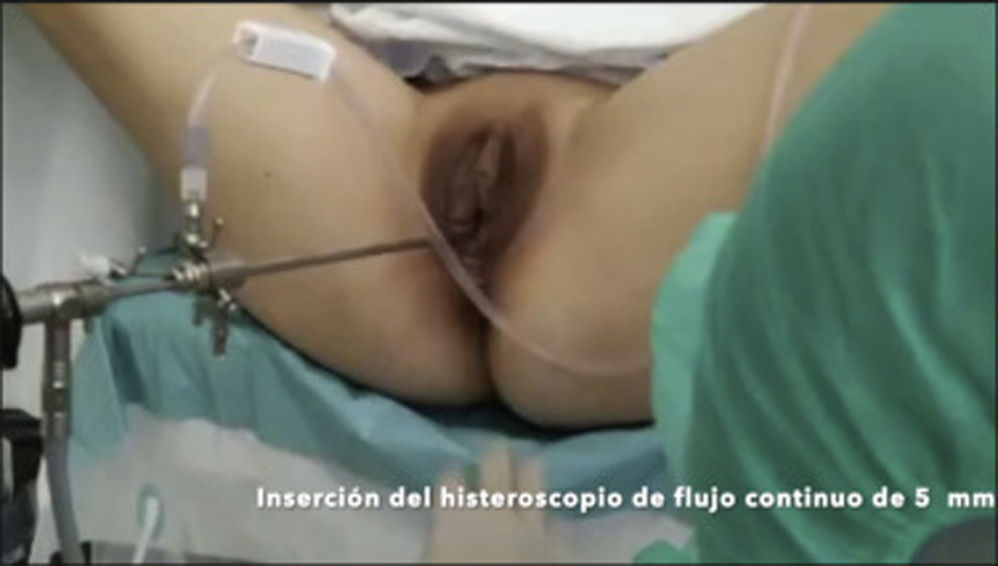
Mujeres con cesárea previaLos DIU pueden insertarse antes de las 48h posteriores al parto por cesárea (OMS, 2018). Estas mujeres, además de ser posiblemente nulíparas, pueden presentar complicaciones de la cicatriz, con aparición de itsmoceles –lo que aumenta la probabilidad de perforación–, y una mayor incidencia de útero en retroversión o más rotado (Bartz y Pocius, 2019). Presentan con frecuencia un cérvix retropúbico y un canal endocervical inicialmente ascendente que tiende posteriormente a la retroflexión (Prine y Shah, 2018). Por estos motivos, previamente a la inserción de un DIU en mujeres que han sido sometidas a cesárea, es fundamental realizar una exploración pélvica bimanual mediante tacto vaginal y una ecografía que permita valorar la posición, la orientación y la movilidad uterina, y medir la cavidad (Faculty of Sexual & Reproductive Healthcare, 2019). Como en el caso de la estenosis cervical, el uso de misoprostol puede ser de utilidad para madurar el cérvix (Faculty of Sexual & Reproductive Healthcare, 2019, SEC, 2019b, Bartz y Pocius, 2019, Bahamondes et al., 2015, Abdellah et al., 2017). El uso de una pinza de Pozzi ayuda a reducir el ángulo de flexión uterino y a estabilizar el cérvix. En caso de itsmocele, puede valorarse la inserción guiada por ecografía, lo que reduce el riesgo de perforación durante la inserción. En casos seleccionados, podría valorarse la inserción guiada por histeroscopia. Aunque la evidencia disponible se centra en la extracción del DIU (Alanis Fuentes y Amoroso Hernandez, 2009) y no en su inserción, en nuestra experiencia, la histeroscopia puede ayudar a que la inserción pueda llevarse a cabo de forma sencilla (ver video).
Después de la inserciónSíncope vasovagalEl síncope vasovagal puede ocurrir durante la inserción o bien inmediatamente después de ella, especialmente en inserciones dificultosas o casos no comunes, y puede verse favorecido por la falta de suficiente experiencia del médico. Dado que es difícil de predecir, es fundamental que el personal implicado en la inserción del DIU esté formado y debidamente actualizado en técnicas de resucitación (aproximación ABCDE, por sus siglas en inglés Airway [vía aérea], Breathing [respiración], Circulation [circulación], Disability [incapacidad, nivel de conciencia] y Exposure [exposición]) (Thim et al., 2012), así como disponer del material y los fármacos necesarios para abordarlo (AINE y atropina 0,5mg subcutánea) (Bahamondes et al., 2014, Faculty of Sexual & Reproductive Healthcare, 2019, SEC, 2019a). Puede ser también útil indagar si la mujer ha sufrido un síncope vasovagal o una crisis epiléptica (en el caso de padecer epilepsia) en otras intervenciones menores, lo que puede orientarnos acerca de una posible predisposición. Ante un síncope vasovagal, la paciente se ha de colocar en posición de Trendelemburg (SEC, 2019a).
Dolor tras la inserciónSe considera como tal a aquel que tiene lugar hasta un día después de la inserción. Es necesario instruir a la mujer para que acuda a consulta o a urgencias si padece dolor intenso o persistente y se acompaña de fiebre, leucorrea o dispareunia (tabla 1). En caso contrario, puede resolverse la consulta telefónicamente. Si se acompaña de algunos de estos signos, pero estos no son sugerentes de infección o no se encuentran causas aparentes que puedan explicar el dolor, habría que valorar la posible desaparición de los hilos (ver más adelante). Tras descartar un posible embarazo, se recomienda realizar una ecografía para valorar la posibilidad de malformación uterina en caso de no disponer de esta información (p. ej., en nuligestas), de desplazamiento o de perforación durante la inserción. En caso de no hallarse una causa aparente, se puede prescribir un analgésico para reducir el dolor y hacer un seguimiento.
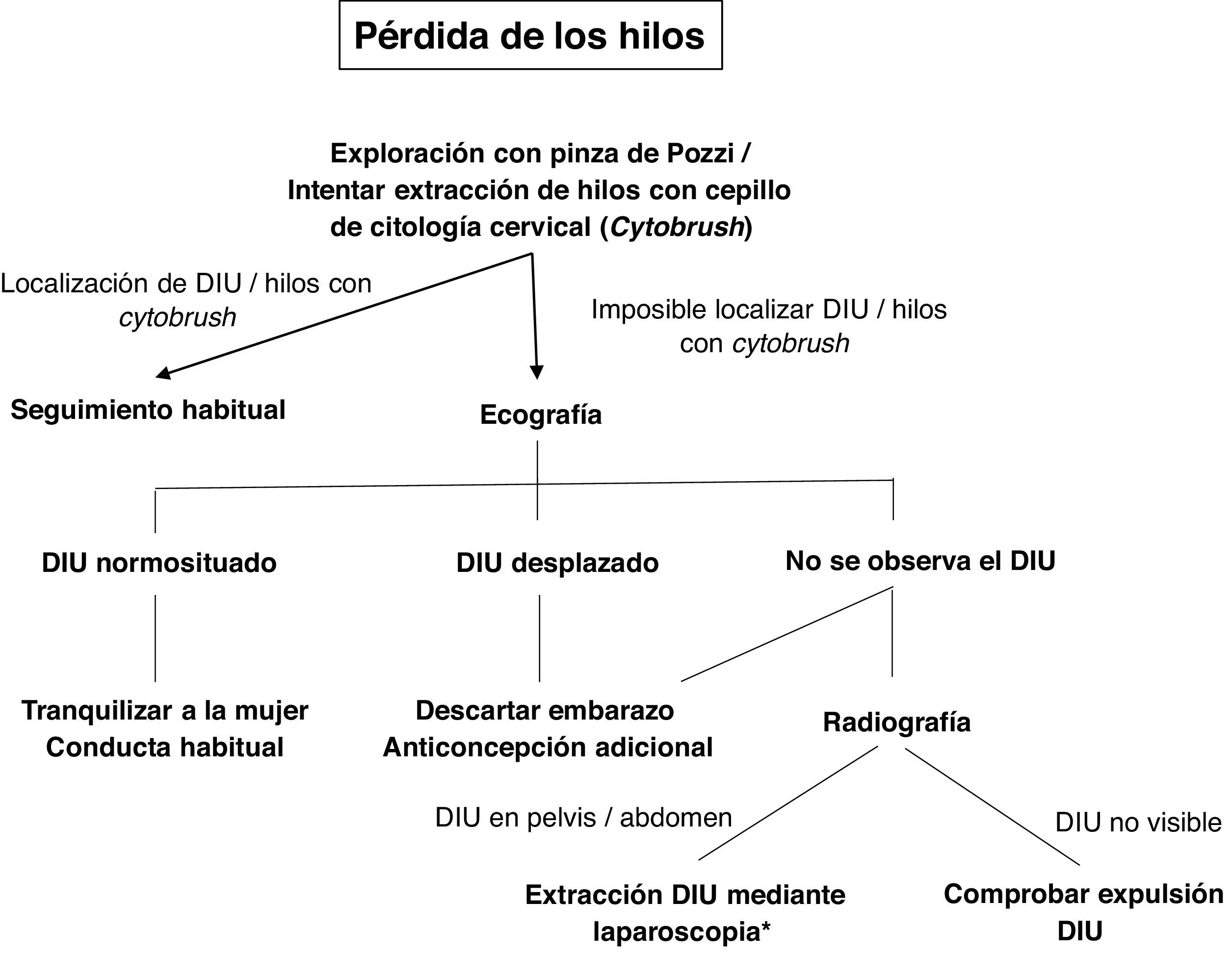
Desaparición de los hilosLa desaparición de los hilos puede detectarse durante una revisión rutinaria o en el momento de la extracción del DIU. Esto puede responder a que, estando el DIU bien colocado, los hilos se hayan retraído hacia el canal endocervical, pero también puede ser indicativa de la expulsión del DIU, de una perforación uterina o de un embarazo (SEC, 2019a, Faculty of Sexual & Reproductive Healthcare, 2019). Los pasos a seguir para averiguar el motivo de la desaparición y las acciones a llevar a cabo se muestran en la figura 2. En caso de sospechar una expulsión, debe valorarse la necesidad de anticoncepción hormonal de urgencia o el uso de métodos barrera (SEC, 2019a).
La exploración regular de la presencia de hilos por la mujer es un tema controvertido. Pese a estar recomendado por algunos expertos, en nuestra opinión es desaconsejable porque puede generar ansiedad en la mujer y aumentar el número de consultas.
Revisiones post-inserciónLas «Recomendaciones sobre prácticas seleccionadas para el uso de anticonceptivos» de la OMS (OMS, 2018) sugieren una única visita tras la primera menstruación o a las 3-6 semanas post-inserción, en las que se comprobará mediante ecografía que el DIU está bien colocado y que no existen signos o síntomas de EIP, especialmente durante los 20 primeros días tras la inserción. Sin embargo, en ocasiones es difícil cumplir esta cita, ya que puede verse afectada por las listas de espera. La mujer debe estar convenientemente informada de los signos de alarma de una posible EIP, una perforación o una expulsión (tabla 1). No es necesaria una exploración vaginal salvo que se sospeche una EIP o la expulsión del dispositivo.
Dada la amplia disponibilidad de ecógrafos en la consulta en nuestros días, puede usarse la ecografía post-inserción inmediata como control de la correcta colocación del DIU, siempre que la inserción no haya sido dificultosa, evitando así la necesidad de una primera revisión a las 3-6 semanas. Esta sería conveniente sólo después de transcurridos 4-6 meses tras la inserción de un DIU-LNG para asegurar que el patrón de sangrado está estabilizado. Es importante instruir a la mujer sobre los cambios durante estos meses (tabla 1). El riesgo de expulsión es muy bajo (menos de 1 de cada 20 mujeres en 5 años) (NICE, 2019), por lo que no se justifica una visita a las 3-6 semanas en ausencia de signos de alarma. Estas consultas pueden tener lugar de forma telemática.
Uso de productos de higiene menstrualEn una revisión llevada a cabo entre 930 mujeres usuarias de DIU, 690 (74,2%) de las cuales usaba tampones y 96 (10,3%) una copa menstrual, no se encontraron diferencias en las tasas de expulsión entre estos dos tipos de usuarias respecto a las usuarias de compresas (resto de mujeres) (Wiebe y Trouton, 2012). Por el contrario, una encuesta reciente llevada a cabo vía on-line en 902 mujeres encontró una asociación positiva entre el uso de la copa menstrual y la expulsión del DIU (OR 2,75 [IC 95% 1,40-5,42], P=0,002), lo que no se observó con el uso de tampones o compresas. Sin embargo, este estudio valoró no sólo el uso actual de DIU, sino el uso anterior, y no todas las expulsiones se asociaron directamente al uso de la copa (Schnyer et al., 2019). La relativa baja experiencia con este producto higiénico y la falta de evidencia robusta acerca de su relación con un mayor riesgo de expulsión dificulta la toma de decisiones a este respecto, pudiéndose únicamente informar a la mujer de los signos y síntomas de una expulsión y hacer seguimiento de los casos.
ConclusionesEl papel que los anticonceptivos de larga duración reversibles como los DIU pueden tener en la reducción de la tasa de embarazos no deseados, hace que superar las barreras a su uso adquiera especial relevancia. Por parte del profesional sanitario, además de una instrucción adecuada y la amplia experiencia, es importante saber cómo superar barreras a su uso tanto de su parte como por parte de la mujer. Saber cómo valorar la elegibilidad de la mujer, cómo informarla adecuadamente, cuál es el DIU que mejor se adapta a sus características y necesidades y cuál es el mejor momento para insertarlo, son aspectos clave a tener en cuenta antes de la inserción que pueden contribuir al éxito del procedimiento. El manejo del dolor mediante medidas farmacológicas o no farmacológicas, incluso la prevención del mismo en la medida de lo posible, son también aspectos fundamentales dado que se trata de una de las principales barreras al uso de DIU. Contribuye a ello el atender a la experiencia de la mujer durante el procedimiento de inserción. La posibilidad de perforación u otras complicaciones es por lo general baja, aunque hay que instruir a la mujer en los síntomas indicativos de estas y saber cómo manejarlas. La inserción de DIU puede ser especialmente dificultosa en mujeres con estenosis post-conización o que hayan sufrido una cesárea; pese a ello, no debería de constituir una barrera para su uso. Por último, entre los aspectos post-inserción que pueden suponer una barrera al uso de DIU, revisamos la actuación en caso de síndrome vasovagal, de dolor o desaparición de hilos, así como el tiempo aconsejable para realizar visitas de seguimiento de acuerdo con las características de nuestro sistema público de salud.
Declaración de autoríaTodos los autores contribuyeron por igual a la elaboración del presente manuscrito.
Conflictos de interesesEl Dr. Lobo Abascal informa los honorarios personales de Bayer y Gedeon Richter, fuera del trabajo presentado.
El Dr. Andeyro reporta honorarios personales de Bayer y Gedeon Richter, fuera del trabajo presentado.
El Dr. Cristóbal reporta honorarios personales de Bayer, fuera del trabajo presentado.
El Dr. Gutiérrez-Ales informa los honorarios personales de Bayer, fuera del trabajo presentado.
El Dr. Martínez informa los honorarios personales de Bayer, fuera del trabajo presentado.
El Dr. Parra Ribes informa los honorarios personales de Bayer y MSD, fuera del trabajo presentado.
El Dr. Quílez reporta honorarios personales de Bayer y Gedeon Richter, fuera del trabajo presentado.
El Dr. Pau Pujol Pineda es empleado de tiempo completo de Bayer Hispania S.L.
Fuentes de financiaciónBayer Hispania financió el servicio de redacción médica, que corrió a cargo de Beatriz Viejo PhD.
Los autores agradecen a Beatriz Viejo, PhD, la asistencia en la redacción y edición del presente manuscrito. Este servicio fue financiado por Bayer Hispania.